祛风安脑口服液质量标准研究
蒋 霞 黄银妹 王小洁 兰丽华 李 梅*
1.广西医科大学第一附属医院药学部,广西 南宁 530021;2.广西医科大学药学院,广西 南宁 530021
祛风安脑口服液质量标准研究
蒋霞1黄银妹2王小洁2兰丽华2李梅1*
1.广西医科大学第一附属医院药学部,广西南宁530021;2.广西医科大学药学院,广西南宁530021
【摘要】目的:建立祛风安脑口服液定性、定量分析方法。 方法:采用TLC对麻黄、黄芩、防风、川芎进行定性鉴别;采用HPLC测定阿魏酸含量,色谱条件:以Inertsil ODS-3(250mm×4.6nm,5μm)为色谱柱,甲醇-1%冰醋酸(30∶70)为流动相,检测波长为321nm,柱温为25℃。结果:薄层色谱斑点清晰,阴性对照无干扰;阿魏酸在1.824~10.940μg线性关系良好(r=0.9998),平均回收率为100.51%,RSD=1.94%。结论:本方法简便易行、结果准确,可作为该产品质量控制的方法。
【关键词】祛风安脑口服液;阿魏酸;HPLC ;TLC
祛风安脑口服液是我院中药制剂,处方源于《备急千金要方》所载的续命汤,由麻黄、红参、黄芩、肉桂、甘草、川芎、苦杏仁、熟附子、防风、干姜、石膏、赤芍、当归这十三味药材加工制成,具有疏通经络、调和营卫、解表祛邪的功效,临床用于中风、身体不能自持、口不能言或拘急不得转侧等症。为保证制剂质量稳定可控,研究采用薄层色谱法(TLC)对该制剂主要成分麻黄、防风、川芎、黄芩进行薄层色谱鉴别,并参考相关文献[1-2],采用高效液相色谱法(HPLC)测定制剂中阿魏酸的含量,为制定祛风安脑口服液的质量标准提供依据。
1仪器与材料
1.1仪器SIL-10AF高效液相(含SPD-15C紫外检测器,岛津国际贸易上海有限公司);XS205DU十万分之一天平(梅特勒-托利多仪器上海有限公司);R-1001N旋转蒸发仪(郑州长城科工贸有限公司);
1.2材料硅胶板(青岛海洋化工分厂);点样毛细管(泰州市北平贸易有限公司);黄芩苷对照品(批号110715-200212,中国药品生物制品鉴定所);阿魏酸对照品(批号110773-201313,中国食品药品检定研究院);甲醇为色谱纯,水为超纯水,其他试剂为分析纯。
2方法与结果
2.1祛风安脑口服液的制备除肉桂、红参外,其他药材加10倍量水,加热煎煮两次,每次1.5h,合并2次煎液,滤过。滤液浓缩,加入乙醇至乙醇浓度为65%,静置24h,滤过,回收乙醇至无醇味。取红参,加10倍水,加热煎煮2次,每次1.5h,滤过,合并2次煎液,浓缩,与上述制得的浓缩液合并,再加入肉桂粉,煮10min,过滤,加入苯甲酸3g,加蒸馏水至900ml,静置24h,滤过,滤液调至总量为1000ml,灌装,即得。
2.2TLC定性鉴定
2.2.1麻黄TLC取样品20ml,加氨水调pH至1~2,用乙醚萃取2次,合并乙醚层,挥干乙醚,加盐酸乙醇(1∶20)10ml,摇匀,水浴蒸干,残渣加甲醇溶解,即为供试品溶液。另取盐酸麻黄碱对照品,加甲醇制成浓度为1mg/ml的溶液,作为对照品溶液。吸取上述溶液各5ml,分别点于硅胶G薄层板上,以正丁醇-冰醋酸-水=8∶2∶1为展开剂[3],展开,晾干,喷以茚三酮试液,105℃烘5min。供试品在与对照品的相应色谱位置上,均显相同紫红色斑点,Rf=0.62。
2.2.2川芎TLC取制剂样品10ml,加乙醚20ml萃取,超声10min,过滤,挥干乙醚,加乙酸乙酯1ml,即为供试品溶液。另取相同制备工艺制成的缺川芎的阴性样品,同法制成阴性对照品溶液。取川芎对照药材1g,加乙醚20ml,超声10min,滤过,挥干,加乙酸乙酯1ml,制成对照液。吸取上述溶液各5μl,分别点于同一硅胶G板,以氯仿-甲醇=8∶1为展开剂[4],展开,取出,晾干,置紫外光灯365nm下检视,供试品色谱中,在与对照药材相应的位置上,显相同颜色的斑点。阴性对照无干扰,Rf=0.857。
2.2.3防风TLC取制剂样品15ml,用乙酸乙酯萃取2次,每次20ml,合并乙酸乙酯层,水浴蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。另取相同制备工艺制成的缺防风的阴性样品,同法制成阴性对照液,取防风对照药材1g,加甲醇10ml,回流30min,滤过,滤液蒸干,加水20ml使溶解,用乙酸乙酯萃取2次,每次15ml,合并乙酸乙酯层,水浴蒸干,残渣加甲醇1ml使溶解作为对照药材溶液。吸取上述溶液各5μl,分别点于同一硅胶G薄层板上,以氯仿-甲醇=4∶1为展开剂[5],展开,取出,晾干。置紫外光灯365nm下检视,供试品色谱中,在与对照药材相应的位置上,显相同颜色的斑点。阴性对照无干扰,Rf=0.758。
2.2.4黄芩TLC取制剂样品10ml,用乙酸乙酯萃取2次,合并乙酸乙酯层,水浴蒸干,加甲醇溶解,作为供试液。另取相同制备工艺制成的缺黄芩的阴性样品,同法制成阴性对照品溶液。另取黄芩苷对照品,加甲醇制成浓度为1mg/ml的溶液,作为对照品溶液。吸取上述溶液各5μl,分别点于硅胶G薄层板上,以乙酸乙酯-甲醇-甲酸-水=7∶2∶0.5∶0.5为展开剂[6],展开,取出,晾干。喷三氯化铁的乙醇溶液,晾干,供试品色谱中,在与对照品相应的位置上,显相同墨绿色的斑点,阴性对照无干扰,Rf=0.756。

2.3HPLC含量测定
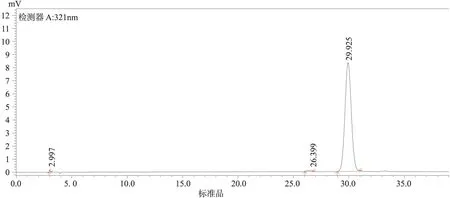
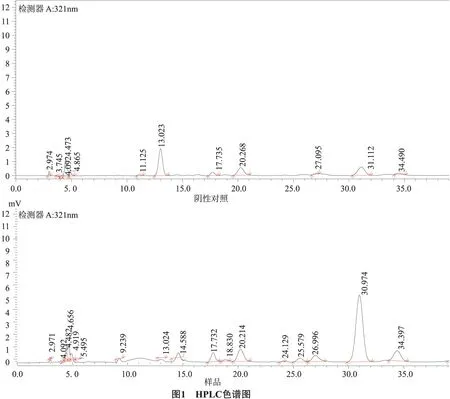
2.3.1色谱条件色谱柱:InertsilODS-3(250mm×4.6nm,5μm);流动相:甲醇-1%冰醋酸(30∶70);检测波长:321nm;柱温:25℃;流速:1ml/min;进样量:10μl。在上述色谱条件下,按阿魏酸峰计算,理论塔板数在4000以上[5];祛风安脑口服液中阿魏酸的色谱峰与其他成分的色谱峰分离良好,且阴性样品溶液无干扰。见图1。2.3.2对照品溶液的制备精密称取阿魏酸4.56mg定容于25ml棕色容量瓶中,加甲醇配成182.40μg/ml对照品储备液,精密量取1ml对照品储备液,定容于10ml的棕色容量瓶中,制成含70%甲醇,浓度为18.24μg/ml的对照品溶液,用0.45μm微孔滤膜滤过,取续滤液,即得。
2.3.3供试品溶液的制备精密称取祛风安脑口服液10ml,用乙醚10ml萃取,萃取3次,挥干乙醚,用甲醇定容于100ml的容量瓶,制成供试品液,摇匀,用0.45μm微孔滤膜滤过,取续滤液,即得。
2.3.4阴性对照品溶液的制备按处方量制成缺当归及川芎的阴性样品,同供试品溶液的制备制成阴性对照液。
2.3.5线性关系考察分别精密吸取对照品溶液(18.24μg/ml)1、2、3、4、5、6ml置于10ml的容量瓶中,加甲醇至刻度,摇匀。按上述色谱条件,测定峰面积。以峰面积为纵坐标(Y),以进样量(μg)为横坐标(X),绘制标准曲线,计算得回归方程Y=58526X+11512,r=
0.9998。结果表明:阿魏酸在1.824~10.940μg范围内呈良好的线性关系。
2.3.6精密度试验吸取对照品溶液10μl,在所选色谱条件下连续进样5次,测定阿魏酸峰面积值,RSD=1.11%。结果表明,仪器的精密度良好。
2.3.7重复性试验精密量取同一批样品5份,按供试品溶液制备方法项下方法操作,共配制5份供试液,各进样10μl,结果测定出的含量RSD为1.67%,表明实验重复性良好。
2.3.8稳定性试验取同一供试品溶液,分别于0、2、4、6、8、10h进样,测定阿魏酸色谱峰面积,比较10h内测得制剂含量RSD值。实验结果显示,RSD为2.00%,表明本供试品溶液在室温下放置10h内稳定。
2.3.9加样回收率试验采用加样回收法,取已知含量同一样品,分别加标0.8倍、1.0倍、1.2倍,每个水平重复3次。按上述的色谱条件进样,计算回收率,结果见表1。
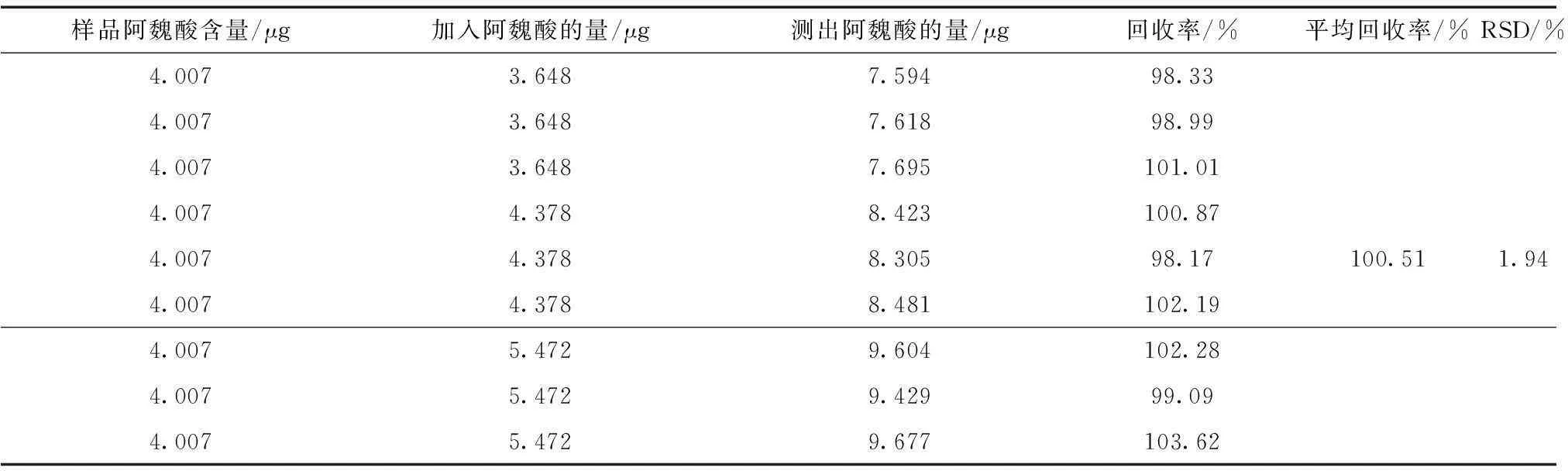
表1 阿魏酸回收率试验结果
2.3.10样品测定精密量取5批祛风安脑口服液,并按“2.3.3”项下制成供试品溶液,分别取10μl,注入高效液相色谱仪,在上述的色谱条件下记录峰面积,计算阿魏酸的含量。结果见表2。
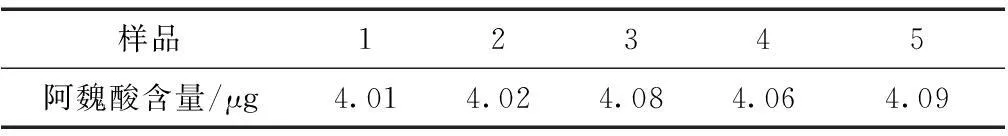
表2 样品阿魏酸测定结果
3讨论
祛风安脑口服液为中药复方制剂,当归和川芎中的共有成分阿魏酸为有效成分之一,故实验选择阿魏酸的含量作为祛风安脑口服液质量控制的参考依据。
由于本品为中药复方制剂,成分复杂,故采用水提后,65%乙醇醇沉,除去水提液中的淀粉、树胶、多糖、粘液质色素等,而乙醇的上清液含有鞣质、生物碱、苷类等[7]。测定阿魏酸含量时,先用乙醚萃取3次,以减少其他成分干扰。报道阿魏酸对光和热不稳定[8],因此稀释后应置于棕色瓶中,于冰箱中保存。
实验结果表明,通过薄层色谱的定性鉴别,各检出成分不受处方中其他成分的干扰,方法简便、快速、专属性强、重复性好。通过阿魏酸的含量测定,可知祛风安脑口服液中阿魏酸在1.824~10.940g/ml范围内线性良好,方法的精密度实验、重复性试验均在合理的范围内,且本供试品溶液在10h内稳定,可见运用本方法测定祛风安脑口服液中阿魏酸的含量可行。
参考文献
[1] 顾民,张亮,张正行.HPLC测定逍遥散及当归中阿魏酸的含量[J].中成药,2000 ,22(5):32.
[2] 王卫锋,康阿龙,汤迎爽,等.HPLC测定妇月康胶囊中阿魏酸的含量[J].中成药,2004 ,26(6):8.
[3] 胡英,刘庆荣.感冒软胶囊中盐酸麻黄碱的薄层色谱鉴别方法探讨[J].中国药事,2006,20(9):573.
[4] 孙菲,丁莹,梁雪,等.川芎、当归的薄层鉴别[J].中国医药学报,2013,41(2):56-57.
[5] 国家药典委员会. 中华人民共和国药典(一部) [S]. 北京:中国医药科技出版社,2010.
[6] 陈菲菲.黄芩苷的提取及结构鉴定[J].天然药物化学实验开题报告,
[7] 王庆.浅谈中药的醇沉工艺及设备[J].中国制药装备,2009,11(11):38.
[8] 孙忠,彭康.HPLC法测定安阳还五汤中阿魏酸的含量研究[J].中医药学刊,2004,22(5) :833.
Quality control of Qu Feng An Nao oral liquid
JIANG Xia1HUANG Yinmei2WANG Xiaojie2LAN Lihua2LI Mei1*
1.Department of Pharmacy, The First Affiliated Hospital of Guangxi Medical Univrsity, Nanning, Guangxi, 530021,China;
2.Pharmacy College, Guangxi Medical University, Nanning, Guangxi, 530021,China
Abstract:Objective To establish Qu Feng An Nao oral liquid qualitative analysis method. Methods Using TLC to ephedra herb, radix scutellariae,radixsileris and rhizoma chuanxiong for qualitative identification, Preparation of ferulaic acid content is determined by HPLC, Inertsil ODS-3 (250mm×4.6nm, 5μm) chromatographic column was used.The mobile phase consisted of methanol and 1% Acetic acid (30∶70); The ultraviolet wavelength was set at 321nm, the colum temperature at 25℃.Results The thin layer plate by TLC spots were clear, Negative control without interference. Ferulaic acid showed a good linear relationship at a range of 1.824-10.940μg(r=0.9998),the average recovery rate was 100.51%, RSD was 1.94%.Conclusions The analysis method is simple feasible and the result is accurate; it can be used for quality control of Qu Feng An Nao oral liquid.
Key words:Qu Feng An Nao oral liquid; ferulaic acid; HPLC; TLC
(收稿日期:2016.01.04)
【中图分类号】R286
【文献标志码】A
【文章编号】1007-8517(2016)06-0019-04
作者简介:蒋霞,副主任药师,硕士,主要从事中药药理学与生药学研究。E-mail:jiangxia771@sina.com通信作者:李梅,主任药师,硕士生导师,主要从事中药学与新药的研究开发。E-mail:326159970@qq.com
基金项目:广西卫生厅中医药科技专项课题(GZYZ 1116)。

