强化混凝对造币废水中镍的去除研究
辛 成,谭 唯,王 群*,柴 彬,李 涛,刘亚淳
(1.四川省地质工程勘察院,四川成都610072; 2.西南交通大学地球科学与环境工程学院,四川成都610031)
强化混凝对造币废水中镍的去除研究
辛 成1,谭 唯2,王 群2*,柴 彬2,李 涛2,刘亚淳2
(1.四川省地质工程勘察院,四川成都610072; 2.西南交通大学地球科学与环境工程学院,四川成都610031)
为了考察不同条件下强化混凝工艺对某造币废水中镍的去除效果,采用预氧化及调节pH值的方法,得到镍去除效果的最佳条件.结果表明:采用氢氧化钠调节pH值对镍的去除效果优于用氢氧化钙调节pH值时镍的去除效果;采用氢氧化钠调节pH=9.5时,可以达到很好的去除效果,其去除率可达99.95%;芬顿试剂预氧化能力要强于次氯酸钠的预氧化能力,当pH=8.5及pH=9.5时,随着芬顿投加量的增加,镍的去除率有所增加,其最佳实验条件是pH=8.5,硫酸亚铁的投加量为78.4 mg/L,过氧化氢投加量为52.8 mg/L,镍去除率可达93.82%;以及pH=9.5时,硫酸亚铁的投加量为58.8 mg/L,过氧化氢投加量为39.6 mg/L,镍去除率可达99.95%.
强化混凝;预氧化;造币废水;镍
造币厂是国家指定的专门从事法定货币生产的特殊企业,造币的独有工艺往往会带来一系列环境问题,其中重金属的污染问题尤为值得关注.造币废水中常见的重金属有铜、锌、镍等.镍是人体必需的生命元素,但过量的镍会对人体造成危害,可引起炎症、癌症、神经衰弱症、系统紊乱、降低生育能力、致畸和致突变等[1].
根据GB8978-1996《综合污水排放标准》中规定,总镍的最高允许排放质量浓度为1.0 mg/L[2].造币废水中的镍以离子态和络合态的形势存在,如果对含镍废水不加处理任意排放,就会对人体和环境带来极大的危害[3-4],其处理主要采用化学沉淀法[5]、电渗析[6]、反渗透[7]及离子交换树脂吸附[8]等方法.当造币废水中含有络合态镍时,镍就很难去除.因此在这种情况下,便要对废水进行预处理措施,在破络后再进行废水中游离镍离子的去除与分离.络合重金属废水的预处理方法常采用调节pH值、氧化还原法、化学置换法等[9].
本研究对比了调节pH值及化学预氧化等方法对造币废水中镍的去除效果,得出最佳实验条件,为造币工业含镍废水处理提供参考和技术支持.
1 实验部分
1.1 实验材料 本实验中采用的药品有聚合氯化铝(PAC);聚丙烯酰胺(PAM);硫酸亚铁(FeSO4);过氧化氢(H2O2),上述药品均为分析纯.芬顿试剂分别由4种不同配比配制:(a)29.4 mg/L硫酸亚铁和19.8 mg/L过氧化氢;(b)39.2 mg/L硫酸亚铁和26.4 mg/L过氧化氢;(c)58.8 mg/L硫酸亚铁和39.6 mg/L过氧化氢;(d)78.4 mg/L硫酸亚铁和52.8 mg/L过氧化氢.
本实验所用含镍的废水来源于某造币工厂,无机废水中镍的初始质量浓度为284.00 mg/L,初始pH值为2.52.
1.2 实验过程 取水样1 L,在不调节pH值和不进行预氧化的条件下,在水样中直接加入50 mg/L聚合氯化铝和5 mg/L聚丙烯酰胺,快速搅拌1 min,慢速搅拌12 min,慢速搅拌时每隔3 min取上清液10 mL,过滤后测定混凝沉淀出水的镍含量.搅拌完成后静沉30 min,每隔5 min取上清液10 mL,过滤后测定混凝沉淀出水的镍含量.
氢氧化钙与氢氧化钠调节pH值除镍实验:取1 L水样,分别采用NaOH和Ca(OH)2调节其pH值至9.0、9.5、10.0、10.5.在上述水样中加入50mg/L聚合氯化铝和5 mg/L聚丙烯酰胺,快速搅拌1 min,慢速搅拌12 min,慢速搅拌时每隔3 min取上清液10 mL,过滤后测定混凝沉淀出水的镍含量.搅拌完成后静沉30 min,每隔5 min取上清液10 mL,过滤后测定混凝沉淀出水的镍含量.
次氯酸钠与芬顿试剂预氧化水样除镍实验:取1 L水样,分别加入0、10、20、30、40和50 mg/L Na-ClO,快速搅拌1 min,加入NaOH将pH值调至9.5;另向水样中分别加入4种不同投加量的芬顿试剂,加入NaOH将水样的pH值分别调至8.5和9.5后,投加50 mg/L聚合氯化铝和5 mg/L聚丙烯酰胺,快速搅拌1 min,慢速搅拌12 min,慢速搅拌时每隔3 min取上清液10 mL,过滤后测定混凝沉淀出水的镍含量,其中快速搅拌的转速为180 r/min,慢速搅拌的转速为60 r/min.实验过程如图1所示.

1.3 测定方法 镍的质量浓度采用日本日立公司生产的日立Z-5000原子吸收分光光度计测定.当测定膜滤后水中镍的质量浓度时,需将处理后的水样上清液经过0.45 μm的滤膜过滤,再通过原子吸收分光光度计测定其镍的质量浓度.镍的原子吸收检出限为0.01 mg/L.水样的酸度采用PHS-4C智能酸度计(成都世纪方舟科技有限公司)测定.
2 实验结果与分析
2.1 不经任何预处理直接添加混凝剂后镍的去除效果 取水样1 L,在不调节pH值和不进行预氧化的条件下,在水样中直接加入50 mg/L聚合氯化铝和5 mg/L聚丙烯酰胺,然后按照实验步骤对每个时间点的水样进行测定,如图2所示.在不调节pH值以及不进行预氧化的情况下,直接加入混凝剂,对水样中的镍的去除率最高为35%.
2.2 氢氧化钠和氢氧化钙分别调节废水水样pH值后镍的去除效果 分别采用氢氧化钠、氢氧化钙调节废水水样pH值至9.5,结果如图3所示.由图3可知,在反应初始阶段,用氢氧化钠调节水样pH值后对镍的去除效果要优于氢氧化钙调节水样pH值后对镍的去除效果.当静沉15 min后,用氢氧化钙和氢氧化钠调节pH值后对镍的去除效果趋于相同,从经济的角度考虑,氢氧化钙的造价成本要低于氢氧化钠,所以实际生产中,可选用氢氧化钙调节水样pH值.
2.3 氢氧化钠调节废水水样pH值后镍的去除效果氢氧化钠调节pH值后镍的剩余质量浓度和去除率随时间的变化情况如图4(a)和4(b)所示.从图4(a)可以看出,随着pH值的增大,镍的质量浓度逐渐在降低,其原因是随着pH值的增加,废水水样中的OH-含量增加,使络合态的镍变成游离态的镍,并使离子态的镍形成了难溶于水的沉淀物,导致废水水样中离子态镍质量浓度减小.当pH值为9.5及以上时,镍的去除已达到很好的效果,去除率均大于99.95%;当不调节pH值时,其镍的去除率达35%左右,而调节 pH值后,其去除率达到99.95%,说明调节pH值后,对络合态的镍有一定的破络作用,且随着搅拌时间增加,形成的沉淀量增大,当不再产生沉淀时,镍已基本完全形成沉淀.当pH值为10.5时,镍的剩余质量浓度快速降低,达到较理想的镍去除效果,当静沉5 min时,去除率可达99.96%.当pH值分别为9.5和10时,随时间变化,镍的剩余质量浓度逐渐降低,当静沉5 min时,镍的去除率分别达到了99.95%和99.96%.从经济的角度看,可选择低成本高效果的方案,则用氢氧化钠调节pH值去除镍时最优pH值为9.5.所以,当实际生产时,可以根据实际情况选择最优方案.
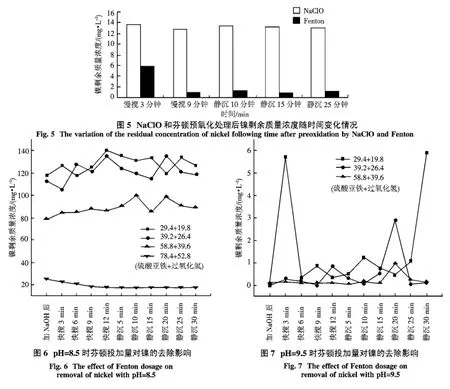
2.4 次氯酸钠和芬顿试剂分别预氧化废水水样后镍的去除效果 由于造币废水中通常含有络合态镍[10],采用预氧化方法可以将其进一步去除.为了便于生产应用,降低运行成本,本文采用预氧化与调节pH值相结合的方式来考察镍的去除效果.将水样调节至pH值为9.5时,投加不同量的次氯酸钠和不同比例的芬顿试剂后,观察镍的剩余质量浓度随时间的变化情况,结果如图5所示.

图5考察了NaClO和芬顿预氧化处理后镍的剩余质量浓度随时间变化情况,从图中可以看出,芬顿预氧化后镍的剩余质量浓度要明显低于次氯酸钠预氧化后镍的剩余质量浓度,其明显强化了镍的去除效果.从(1)~(4)式中可知,在芬顿试剂反应过程中会产生一定量的羟基自由基、铁离子[11-14],芬顿试剂反应如下:


由于羟基自由基和铁的共同作用,使镍的去除效果较好.原因如下:1)羟基自由基氧化作用.反应过程中产生的羟基自由基将有机物氧化,使络合态镍释放到水中,进而被沉淀去除;2)铁絮体的混凝作用.在芬顿反应过程中,铁会在加入碱后形成沉淀,而该沉淀具有很好的混凝、吸附作用,所以将水中镍进一步去除.据江洪龙等[9]的研究表明,芬顿反应过程结束后,向其中加入氢氧化钠,二价铁离子与氢氧根生成黄褐色的沉淀物质,这些物质有很强的絮凝混凝效果,网捕金属镍沉淀物和大分子的络合物沉淀并去除.
从图6和图7可以看出,当pH=8.5时,随着芬顿投加量的增加,镍的去除效果有所提高,当投加量为78.4 mg/L硫酸亚铁和52.8 mg/L过氧化氢时,镍的剩余质量浓度为17.57 mg/L,去除率达到了93.82%;当pH=9.5时,随着芬顿投加量的增加,镍的去除效果均达到了比较好的处理效果,镍的剩余质量浓度为 0.14 mg/L,去除率可达99.95%.原因可能是pH值升高,对水中的络合态镍的破络效果更佳,所以调节pH值在整个反应中起到了控制作用[15-17].因此pH值调节和芬顿试剂的预氧化不论是单独使用还是联合使用,对废水中镍的去除均有可观的效果,并且在实际处理工作中,可根据实际情况(如pH值调节剂与芬顿试剂的价格)选择最佳方案.
3 结论
1)用氢氧化钠调节水样pH值后对镍的去除效果要优于用氢氧化钙调节水样pH值后对镍的去除效果.用氢氧化钠调节废水pH值为9.5及以上时,镍的去除已达到很好的效果,去除率均大于99.95%.
2)芬顿预氧化除镍效果优于次氯酸钠预氧化除镍效果.随着芬顿投加量的增加,镍的去除效果均达到了比较好的处理效果,其最佳实验条件是: (a)pH=8.5,硫酸亚铁的投加量为78.4 mg/L,过氧化氢投加量为 52.8 mg/L,镍去除率可达93.82%;(b)pH=9.5,硫酸亚铁的投加量为58.8 mg/L,过氧化氢投加量为39.6 mg/L,镍去除率可达99.95%.在实际生产过程中可根据实际情况选择最优方案.
[1]陈尔余.天然沸石的改性及处理含镍废水的研究[D].金华:浙江大学,2006.
[2]国家环境保护局,国家技术监督局.污水综合排放标准GB8978-1996[S].[1996-10-04].
[3]郭琳,查红平,廖小刚,等.化学沉淀法处理线路板厂含镍废水[J].环境工程,2011(4):50-53.
[4]吕小梅.结晶沉淀法处理化学镀镍废水的研究[D].哈尔滨:哈尔滨工业大学,2009.
[5]ANKRAH D A,SOSLASHGAARD E G.The applicability of iron and manganese precipitation bacteria in drinking water systems[J].Nanotechnology Perceptions,2009,5(3):209-216.
[6]PANDIAN G,RAMAKRISHNAN K,GANAPATHY S,et al.Oxidized multiwalled carbon nanotubes as adsorbent for the removal of manganese from aqueous solution[J].Environmental Science and Pollution Research,2013,20(2):987-996.
[7]LIM J L,PARK N S,KANG S,et al.Iron and manganese fouling in microfiltration as a pretreatment of seawater reverse osmosis processes[J].Desalination and Water Treatment,2011,33(1/2/3):323-328.
[8]杨勇.湿地系统处理重金属废水的应用研究[D].上海:同济大学,2007.
[9]江洪龙,俞马宏.含有机络合剂的铜镍废水化学处理研究[D].南京:南京理工大学,2013.
[10]李岩.电镀废水处理的新工艺[D].武汉:中南民族大学,2009.
[11]FU F L,WANG Q,TANG B.Fenton and Fenton-like reaction followed by hydroxide precipitation in the removal of Ni(II) from Ni-EDTA wastewater:a comparative study[J].Chem Engineering J,2009,155(3):769-774.
[12]NGAHW S W,HANAFIAH M A K M.Removal of heavy metal ions from wastewater by chemically modified plant wastes as adsorbents:a review[J].Bioresource Technology,2008,99:3935-3948.
[13]NEYENS E,BAEYENS J.A review of classic Fenton’s per oxidation as an advanced oxidation technique[J].J Hazard Mater,2003,98(10):33-50.
[14]袁雪.化学沉淀-铁氧体法处理重金属离子废水的实验研究[D].重庆:重庆大学,2007.
[15]LINDSEY M E,TARR M A.Quantization of hydroxyl radical during Fenton oxidation following a single addition of iron and peroxide[J].Chemosphere,2000,41:409-417.
[16]KANG N,LEE S D,YOON J Y.Kinetic modeling of Fenton oxidation of phenol and monochlorophenols[J].Chemosphere,2002,47:915-924.
[17]LIN S H,LEU H G.Operating characteristics and kinetic studies of surfactant wastewater treatment by Fenton oxidation[J].Water Research,1999,33(7):1735-1741.
Study on Removal of Nickel from Mint Wastewater by Enhanced Coagulation
XIN Cheng1,TAN Wei2,WANG Qun2,CHAI Bin2,LI Tao2,LIU Yachun2
(1.Sichuan Institute of Geological Engineering Investigation,Chengdu 610072,Sichuan; 2.Faculty of Geosciences and Environmental Engineering,Southwest Jiaotong University,Chengdu 610031,Sichuan)
Preoxidation and coagulation sedimentation were used to remove the nickel of the inorganic wastewater from a mint,using calcium hydroxide and sodium hydroxide to adjust pH to select the optimal reaction condition.The results are as follows:the removal of nickel by using sodium hydroxide is better than that by using calcium hydroxide.The removal of nickel is the best when the pH is 9.5 by using the sodium hydroxide and the rate of removal is up to 99.95%.And the preoxidation ability of Fenton reaction is better than that of Sodium hypochlorite,when the pH is 8.5 and 9.5,respectively.The removal rate of nickel is increased with the increasing of Fenton’s quantity,and the removal rate of nickel is up to 93.82%when the pH is 8.5 with the concentration of ferrous sulfate of 78.4 mg/L and the concentration of hydrogen preoxide of 52.8 mg/L.Whst’s more,the removal rate of nickel is up to 99.95%when the pH is 9.5 with the concentration of ferrous sulfate of 58.8 mg/L,and the concentration of hydrogen preoxide of 39.6 mg/L.
enhanced coagulation;pre oxidation;mint wastewater;nickel
X703.1
A
1001-8395(2016)04-0576-05
10.3969/j.issn.1001-8395.2016.046.022
(编辑 李德华)
2015-11-11
国家自然科学基金(51178134)
*通信作者简介:王 群(1980—),男,副教授,主要从事饮用水及污水处理技术的研究,E-mail:wangqun_hit@126.com

