卫生学检查中和剂头孢菌素酶作用范围研究
吴 扬,余 辉,沈祝飞,王丹丹
(杭州北望生物技术有限公司,杭州 310011)
卫生学检查中和剂头孢菌素酶作用范围研究
吴扬,余辉,沈祝飞,王丹丹
(杭州北望生物技术有限公司,杭州 310011)
为给生产厂家选择头孢菌素酶提供参考依据,探讨头孢菌素酶去除各种常见头孢菌素类抗生素抑菌性的能力.采用抑菌圈的方法,对比试验组和空白对照组头孢菌素酶对20种头孢菌素类和3种碳青霉烯类(培南类)药敏纸片去除抑菌性能力的大小,判断头孢菌素酶能否有效地水解各种头孢菌素β-内酰胺环的酰胺键,使其降低或丧失抑菌活性.结果表明,头孢菌素酶对大多数头孢菌素类抗生素均有较强的中和能力,对少部分如头孢曲松等有中和作用,但需要的酶量较大;对碳青霉烯类(培南类)作用很弱.
头孢菌素类抗生素;头孢菌素酶;卫生学检查;抑菌圈
头孢菌素类抗生素属β-内酰胺类抗生素,具有广谱的抗菌性,杀菌力强,对于敏感菌所致的急性扁桃体炎、急性咽炎、中耳炎、肺部感染、尿路感染、皮肤软组织感染等疾病疗效显著.中国药典(2010年版)二部附录ⅪH “无菌检查法”和ⅪJ“微生物限度检查法”中规定了β-内酰胺类抗生素供试品处理方法,要求用β-内酰胺酶来处理供试品,以便消除β-内酰胺类抗生素的抑菌性,排除其对卫生学检查结果的影响,避免造成假阳性的判断[1-2].虽然各生产厂家对使用β-内酰胺酶作为β-内酰胺类抗生素的中和剂已成为共识,但目前大多厂家用户对β-内酰胺酶的适用范围尚不清楚,存在混淆使用的现象[3].本实验选用β-内酰酶中的头孢菌素酶,对市售常见的20种头孢菌素类和3种碳青霉烯类(培南类)产品进行灭活试验,为各生产厂家提供参考依据[4-6].
1 仪器与试药
SW-CJ-1FD单人单面净化工作台(苏州净化设备有限公司),DRP-9052型电热恒温培养箱(上海森信实验仪器有限公司).
抗生素药敏试纸片如表1(购自上海易佰聚贸易有限公司);头孢菌素酶(批号:20130723,杭州北望生物技术有限公司生产,活性>200万单位);营养琼脂平皿培养基(自制);供试菌大肠埃希菌(编号BL21,购自浙江省微生物所).

表1 市售常见头孢类抗生素药敏纸片及其含量
2 方法与结果
2.1供试品配制
取一支头孢菌素酶(>200万单位),用无菌水溶解并稀释至1×105单位∕mL,无菌过滤后在2~8 ℃条件下贮存备用.
2.2培养基制备
照中国药典2010年版附录ⅪH无菌检查法项下培养基制备6营养琼脂培养基制备方法制备.
2.3卫生学检查
试验组:营养琼脂培养基灭菌后,冷却至55~60 ℃.添加头孢菌素酶至琼脂培养基中,每皿添加活性均为105单位.平板上涂布50 μL大肠埃希菌悬液;将药敏纸片贴至平板上,并做好标记.
空白对照组:方法同试验组,但培养基中不加入头孢菌素酶,空白组各药敏纸片均应有抑菌圈.
将上述试验组和空白对照组置培养箱中,(37 ± 1) ℃培养18~24 h后观察结果,以抑菌圈的大小判定供试品是否具有中和抗生素活性的能力.见表2.
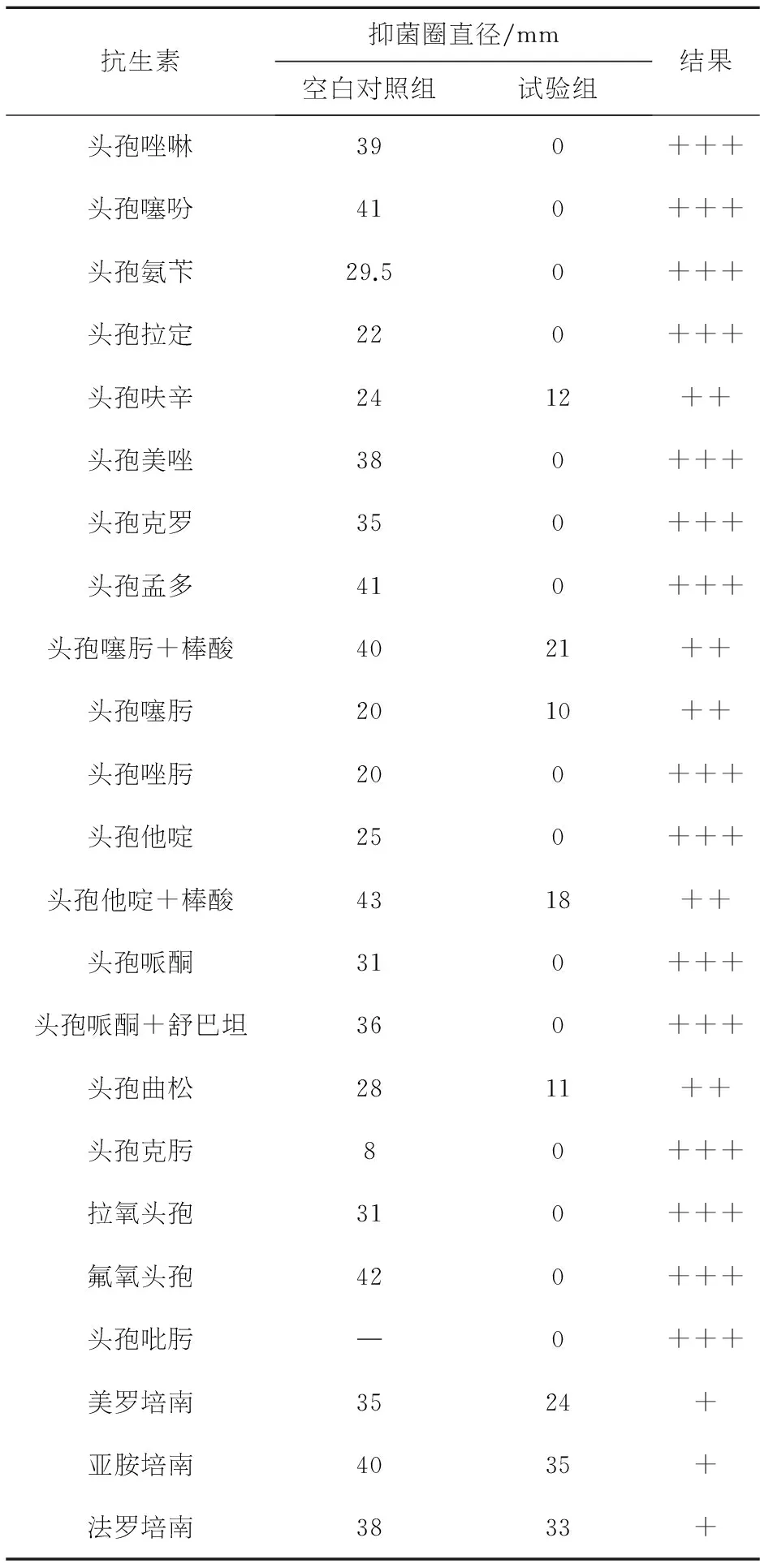
表2 105单位/皿酶量对定量药敏纸片中抗生素的分解效果
-:无分解作用;+:较弱分解作用;++:中等分解作用;+++:较强分解作用;
选出上述2.3试验中有抑菌圈的抗生素,加大平皿中的加酶量,方法同上,观察结果,以抑菌圈的大小判定供试品是否具有中和抗生素活性的能力.见表3.
结果表明:头孢菌素酶对大多数头孢菌素类抗生素均有较强的中和能力,少部分如头孢曲松、头孢呋辛等有中和能力但需要的酶量较大.头孢菌素酶对碳青霉烯类(培南类)中和作用很弱.
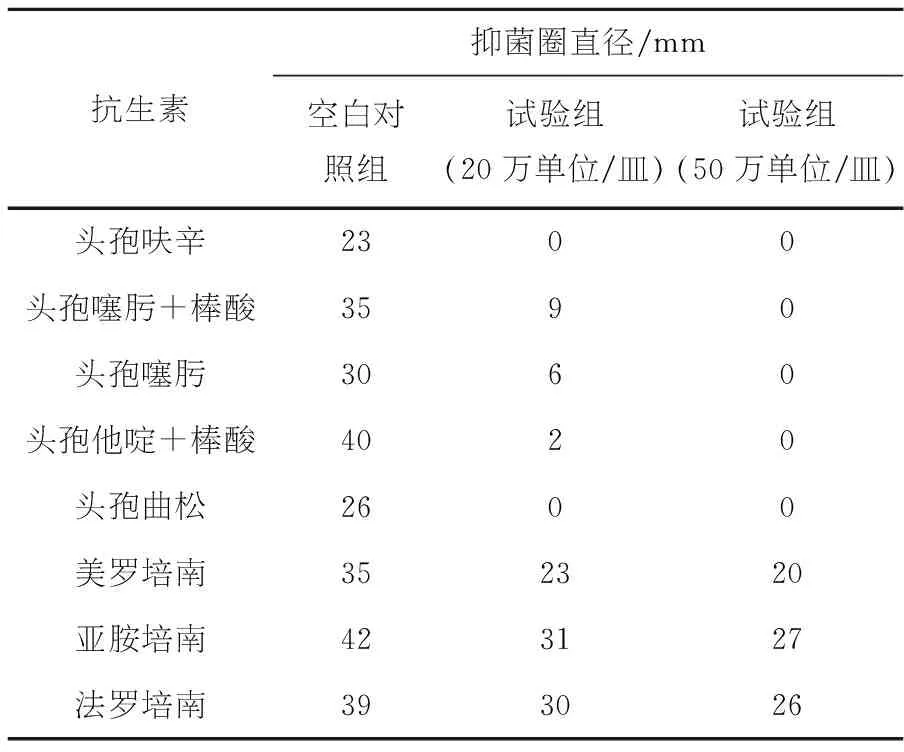
表3 抑菌圈测量
-:无分解作用;+:较弱分解作用;++:中等分解作用;+++:较强分解作用;
3 结 语
原料药和制剂的卫生学检查(无菌检查和微生物限度检查), 是评价药品生产过程中是否受到严重卫生污染的重要依据.但在实际检测工作中, 由于抗生素药品本身的抑菌性,对检查结果的判断产生影响,而选择哪种中和剂需要在检查过程中进行大量的方法学验证,给检验工作带来一定的难度.通过以上研究,可以清楚的了解头孢菌素酶对哪些头孢类抗生素有较好的中和作用,为各头孢菌素类抗生素生产厂家提供了参考依据.
[1]中华人民共和国药典编委会. 中国药典二部(附录)[M]. 北京: 中国医药科技出版社, 2010. 103-107.
[2]中华人民共和国药典编委会. 中国药典二部(附录)[M]. 北京: 中国医药科技出版社, 2010. 107-116.
[3]张峰, 袁菊萍. 不同厂家头孢他啶体外抑菌作用及药物费用分析[J]. 医药导报, 2008, 27(4): 478-479.
[4]李夏林, 覃晓. 注射用头孢呋辛钠无菌检查的方法学验证[J].中国医药科学, 2012, 11(2): 112-113.
[5]佘月坤, 田勇. 头孢菌素类抗生素胶囊剂控制菌检查方法的探讨[J]. 药物分析杂志, 2009, 29(6): 1049-1050.
[6]孙春艳, 张春瑛, 沈佳特, 等. 注射用头孢菌素无菌检查的方法学验证[J]. 医药导报,2007, 26(9): 1089-1091.
Probe into hygiene inspection neutralizer scope of cephalosporins
WU Yang, YU Hui, SHEN Zhu-fei, WANG Dan-dan
(Hangzhou Lion Biotechnology Co., Ltd, Hangzhou 310011, China)
To provide the manufactures reference for choosing cephalosporinase as a neutralizing agent of cephalosporins’ hygiene inspection, the ability of cephalosporinase removing commercial common cephalosporins’ antibacterial abilitiy was investigated. Using cephalosporinase as a neutralizer, the size of inhibiting zone of all kinds of cephalosporin sensitive test paper was observed after neutralization, which can judge the strength of hydrolysis cephalosporins’ beta lactam amide linkage leading to the reduce of antibacterial ability of cephalosporins. Results indicated that cephalosporinase has great effect of neutralization on most kinds of cephalosporin. It also has effect on ceftriaxone, but need more amount of cephalosporinase. The neutralization effect of cephalosporinase on carbapenems(imipenem) is very weak.
cephalosporins; cephalosporinase; hygienic inspection; inhibiting zone
2015-11-10.
吴扬(1976-),男,工程师,研究方向:中药制药.
R927
A
1672-0946(2016)04-0433-02

