HPLC-MS/MS法检测鸡肉中8种镇静剂残留
华萌萌,宫小明,郭礼强,丁葵英,王洪涛,于金玲
(潍坊出入境检验检疫局,山东潍坊261041)
HPLC-MS/MS法检测鸡肉中8种镇静剂残留
华萌萌,宫小明*,郭礼强,丁葵英,王洪涛,于金玲
(潍坊出入境检验检疫局,山东潍坊261041)
建立鸡肉中8种兽药镇静剂(乙酰丙嗪、氯丙嗪、氟哌啶醇、丙酰二甲氨基丙吩噻嗪、甲苯噻嗪、阿扎哌隆、阿扎哌醇和咔唑心安)同时检测的高效液相色谱-串联质谱(HPLC-MS/MS)法。以乙腈-0.1 mol/L盐酸溶液(90/10,体积比)作为提取试剂,混合型阳离子固相萃取柱净化,经AgilentZORBAXRRHDEclipsePlusC18色谱柱(100mm×3.0mm,1.8μm)分离,电喷雾正离子(ESI+)模式电离,多反应监测(MRM)模式进行测定,内标法定量。8种目标物在0.5 μg/L~20.0 μg/L范围内线性关系良好(相关系数r2≥0.998),其检出限(LOD)为0.5 μg/kg,定量限(LOQ)为1.0 μg/kg。在1.0、5.0、10.0 μg/kg加标水平下,平均回收率为85.3%~95.5%,相对标准偏差为0.81%~5.00%。该方法稳定、可靠,能够满足鸡肉中8种镇静剂的检测和确证。
高效液相色谱-串联质谱;鸡肉;镇静剂类;残留
镇静剂类药物对动物中枢神经系统有抑制作用,在畜禽饲养和运输过程中可作为麻醉剂和止痛剂减轻或消除动物狂躁不安、兴奋,达到减少死亡率、增重催肥及缩短出栏时间的目的。此类药物潜伏在动物体内,被人食用后会损害人的中枢神经系统,引起体位性低血压、心悸、运动障碍、肝损害、恶性综合征,甚至诱变致癌[1-2]。因此,许多国家将此类药物列为禁药,并对动物源食品中镇静剂类药物残留量有严格的限量要求。国际食品法典委员会(CAC)规定畜肉中阿扎哌醇、咔唑心安在畜肉中的最高残留限量值分别为肌肉、脂肪中60 μg/kg和5.0 μg/kg,肝脏、肾脏中100 μg/kg和25 μg/kg[3]。我国农业部235号公告已明确规定阿扎哌隆、阿扎哌醇在猪肉、脂肪、肝脏和肾脏中的最高残留限量值分别为60、60、100、100 μg/kg,氯丙嗪只允许治疗使用,不得在动物源食品中检出[4]。
目前,国内外对镇静剂的检测方法有酶联免疫法(ELISA)[5]、高效液相色谱法(HPLC)[6-7]、气相色谱-串联质谱法(GC-MS)[8-9]、高效液相色谱-串联质谱法(HPLC-MS/MS)[1-2,10-11]等。ELISA法检测后需要其他方法验证,高效液相色谱法灵敏度低,气相色谱-串联质谱法虽灵敏度高,但在兽残样品检测时样品需衍生,步骤繁琐且费时长,目前较为常用的为高效液相色谱-串联质谱法[11-14]。本研究选择的目标物为乙酰丙嗪、氯丙嗪、氟哌啶醇等8种镇静剂,利用HPLC-MS/ MS法对鸡肉中8种镇静剂同时检测,以酸化乙腈提取,采用PCX固相萃取柱净化简单快速,与国标GB/T 20763-2006《猪肾和肌肉组织中乙酰丙嗪、氯丙嗪、氟哌啶醇、丙酰二甲氨基丙吩噻嗪、甲苯噻嗪、阿扎哌隆、阿扎哌醇、咔唑心安残留量的测定液相色谱-串联质谱法》、行标SN/T 2113-2008《进出口动物源食品中镇静剂类药物残留量的检测方法液相色谱-质谱/质谱法》、孙雷等[1,10,12-13]报道使用的叔丁基甲醚提取、调pH值酶解及液液萃取的前处理方法[15]相比毒性小、耗时短、操作简单,采用内标法(氯丙嗪-D6)定量,具有良好的准确度和精密度能够满足要求,检出限为0.5 μg/kg,定量下限为1.0 μg/kg,可为动物源食品中镇静剂类药物残留检测提供有力帮助。
1试验部分
1.1仪器、试剂与材料
Agilent 1290-6460液相色谱-串联质谱仪:Agilent公司;Mettler AE163万分之一天平:Mettler公司;IKA TA25均质器、IKA MSI振荡器:IKA公司;Eppendorf 5810R高速冷冻离心机:Eppendorf公司;Supelco固相萃取装置:Supelco公司;N-EVAP-111氮吹仪:美国Organomation公司。
甲苯噻嗪标准品:Sigma-Aldrich公司;氟哌啶醇:上海安谱公司;乙酰丙嗪、丙酰二甲氨基丙吩噻嗪、阿扎哌醇、氯丙嗪、咔唑心安、阿扎哌隆标准品:Dr.Ehrenstorfer公司;氯丙嗪-D6:TRC公司;乙腈、甲醇、甲酸(色谱纯):Merk公司;水为Milli-Q纯水机得到的超纯水;混合型阳离子固相萃取柱(PCX固相萃取柱,60 mg,3 mL):Angel公司;中性固相萃取柱(HLB固相萃取柱,60 mg,3 mL):Waters公司。
1.2标准溶液的配制
准确称取8种标准品10 mg,用甲醇溶解,定容至100 mL,得到质量浓度为100 μg/mL的单标准储备液;将1 mg包装的内标氯丙嗪-D6,用甲醇溶解,定容至100 mL,得到质量浓度为10 μg/mL的单标准储备液;将上述储备液稀释成100 μg/L中间液,避光于4℃下保存。为避免分析物分解,应采用棕色器容量瓶保存。用初始流动相(见1.4.1)分别配制浓度为0.5、1.0、2.0、5.0、10.0、20.0 μg/L的标准溶液(内标氯丙嗪-D6的浓度为5.0 μg/L),用于质谱检测分析,现用现配。
1.3样品处理
1.3.1样品提取
准确称取2.0 g样品,置于50 mL塑料带盖离心管中,加入10 mL乙腈-0.1 mol/L盐酸(90/10,体积比)提取溶液,于均质机上高速均质2 min,于10 000 r/min下离心10 min,用塑料小漏斗、脱脂棉过滤上清液,待净化。
1.3.2样品净化
采用混合型阳离子PCX固相萃取柱净化,经过3 mL甲醇、3 mL水活化;将上述样品提取液(约10 mL)全部过柱,弃去流出液;再用3 mL水、3 mL甲醇淋洗除去杂质和脂肪,抽真空后,用5 mL 5%氨水-甲醇溶液洗脱,收集洗脱液,氮气吹干,用初始流动相(见1.4.1)定容至1 mL,0.22 μm膜过滤待质谱检测。
1.4HPLC-MS/MS条件
1.4.1HPLC条件
色谱柱:Agilent ZORBAX RRHD Eclipse Plus C18column(100 mm×3.0 mm,1.8 μm);柱温:40℃;进样量:10 μL;流动相:A相为0.1%甲酸水溶液,B相为乙腈;梯度洗脱顺序:0~2 min,20%B;2 min~4 min,20%~30%B;4 min~8 min,30%~60%B;8 min~8.2 min,60%~20%B;8.2min~10min,20%B。流速:0.4mL/min。
1.4.2MS/MS条件
电离源:电喷雾离子源(ESI+);扫描方式:多反应监测(MRM)模式;离子源温度:350℃;干燥气流速9 L/min;喷雾针压力:40 psi(1 psi=6.895 kPa);电子倍增器电压:4 000 V;碰撞气:高纯氮(纯度为99.999%);8种镇静剂的质谱参数见表1。
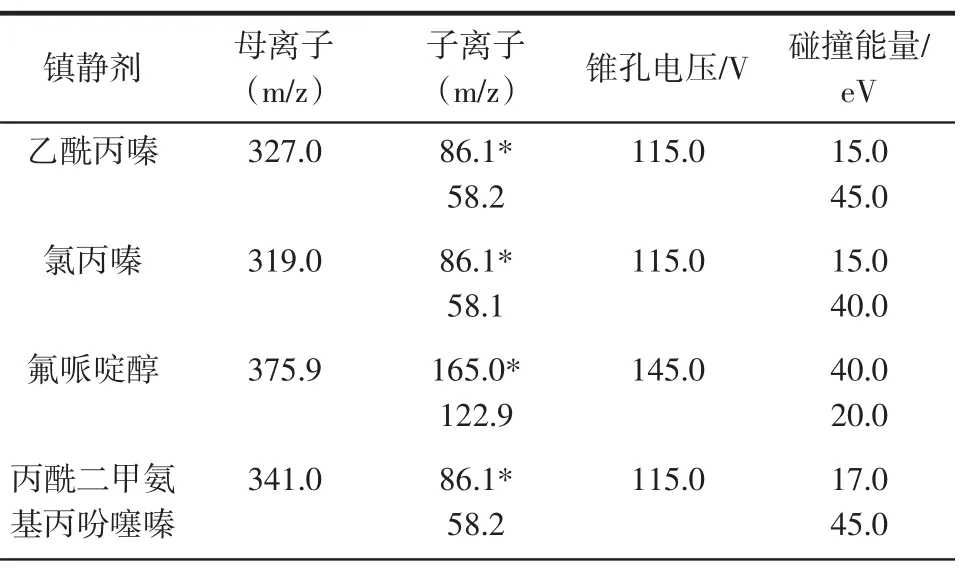
表1 8种镇静剂的质谱检测参数Table 1MS parameters of the 8 sedatives

续表18种镇静剂的质谱检测参数Continue table 1MS parameters of the 8 sedatives
2结果与讨论
2.1色谱条件的优化
本研究考察不同流动相对8种镇静剂的HPLCMS/MS检测的影响,分别就有机相选择甲醇或乙腈及0.1%甲酸-水溶液是否加入乙酸铵进行分析。图1 a、b、c中峰1~8分别代表8种镇静剂在不同流动相中的定量离子色谱图(如图1注释),其中x轴为峰保留时间,y轴为峰面积响应值。如图1 a、b所示8种镇静剂在乙腈-甲酸水系统和甲醇-甲酸水系统中的出峰时间段分别在1.5 min~7.4 min和4.5 min~9.5 min,并且氯丙嗪(8峰)、乙酰丙嗪(5峰)在甲醇-甲酸水系统中峰面积响应值明显降低。图1 a、c所示8种镇静剂在0.1%甲酸水溶液中加入10 mmol/L乙酸铵与不加乙酸铵出峰时间段分别为3.2 min~7.5 min和1.5 min~7.4 min,各目标物峰面积响应值没有影响。由于8种镇静剂的化学性质不同,不同流动相系统中出峰顺序也有所不同。综上所述,本研究选择出峰时间早、响应值高的乙腈和0.1%甲酸-水溶液作为流动相。
2.2样品前处理条件的优化
2.2.1固相萃取柱的选择
已知8种目标物为弱碱性化合物,在前处理过程中应选择中性或阳离子固相萃取柱进行样品净化。
本研究选择中性HLB和混合型阳离子PCX两种固相萃取柱,就它们对8种目标物回收率的影响进行如下试验。将8种镇静剂1.0 μg/L的混合标准液分别经上述两种小柱,分别收集每步流出液,氮吹后经质谱检测,结果表明经HLB固相萃取柱在上样和淋洗过程中都有检测到目标物,洗脱过程中得到8种目标物回收率为50%~60%;而经PCX固相萃取柱的回收率90%以上,其他过程均未检测到目标物。说明PCX固相萃取柱更能有效的结合目标物,保证在去除样品中的脂肪、蛋白等杂质的过程中目标物不损失,达到净化目的。
2.2.2提取试剂的优化
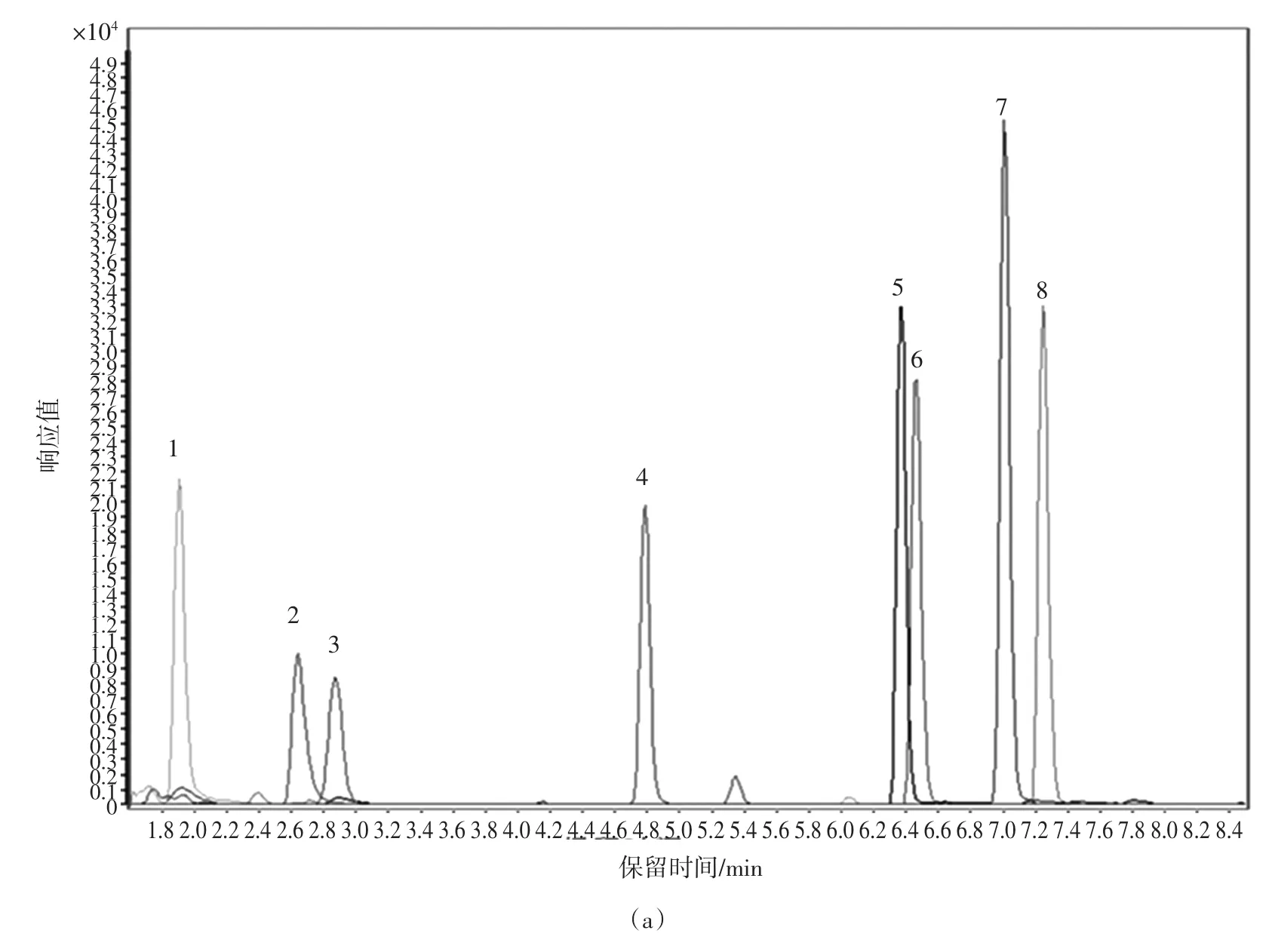

图1 不同流动相中8种镇静剂添加水平1.0 μg/L的鸡肉样品定量离子叠加色谱图Fig.1Quantitative ion overlap chromatograms of the blank chicken sample spiked with 8 sedatives at 1.0 μg/kg in different mobile phases
本研究考察两种不同pH值提取试剂,分别为提取液a:乙腈-0.1 mol/L盐酸溶液(90/10,体积比,pH为3左右);提取液b:乙腈-甲酸溶液(98/2,体积比,pH为4左右)。在空白鸡肉样品中添加1.0 μg/kg水平下,比较二者在经PCX固相萃取柱净化后的回收率。检测结果表明8种目标物经提取液a的回收率在80%以上,提取液b的回收率仅为50%左右,说明不同提取试剂的pH值对8种目标物经PCX固相萃取柱的净化有影响,故本试验选择乙腈-0.1 mol/L盐酸溶液作为提取试剂。
2.3线性关系、检出限和定量下限
本研究采用内标法定量,按照“1.3”配制一系列不同质量浓度的8种镇静剂混合标准溶液(内标氯丙嗪-D6的浓度为5.0 μg/L)作标准曲线进行分析,各目标物的线性范围及回归方程见表2,相关系数(r2)均≥0.998 0。以3倍信噪比(S/N)对应的加标水平为检出限(LOD),10倍信噪比(S/N)对应的加标水平为定量下限(LOQ)。结果得出,8种目标物的检出限为0.5 μg/kg,定量下限为1.0 μg/kg(见表2)。
2.4准确度和精密度
对空白样品中进行加标回收试验。以回收率结果表示检测方法的准确度,回收率的相对标准偏差(RSD)表示方法的精密度。在空白鸡肉样品中添加1.0、5.0、10.0 μg/kg3个水平回收,每个水平平行测定6个样品,测定结果见表3。

表3 8种镇静剂的回收率和相对标准偏差Table 3The recoveries and relative standard deviations(RSDs)of 8 sedatives
8种镇静剂在3个加标水平的平均回收率在85.3%~96.7%,相对标准偏差(RSD)为0.81%~5.00%。
2.5实际样品的检测
利用本方法对采购于本地区农贸市场和超市的10份鸡肉样品进行分析,未发现有镇静剂残留。
3结论
本研究建立了8种镇静剂的高效液相色谱-串联质谱的多残留同时检测方法,采用内标法定量,准确性强、灵敏度高。本研究前处理方法简单快速、可操作性强,重现性强,各项指标均能满足兽药残留检测分析的要求,可用于鸡肉中镇静剂类药物多残留检测,可为动物源食品中镇静剂的常规检测提供有力帮助。
[1]苏海滨,李百舸,吴鹏飞,等.牛奶和奶粉中八种镇定剂残留量的液相色谱-串联质谱测定[J].齐齐哈尔医学院学报,2011,32(4):514-518
[2]张烁,周爽,陈达炜,等.畜肉中10种镇静剂残留的超高效液相色谱-串联质谱测定方法[J].分析测试学报,2014,33(11):1213-1218
[3]Codex Alimentarius Commission(CAC).Codex Alimentarius Commission Maximum Residue Limits for Veterinary Drugs in Foods Updated as at the 35th Session of the Codex Alimentarius Commission[EB/OL].(2012-7-2)[2015-6-6].http://www.docin.com/p-84540694.html
[4]农业部.中华人民共和国农业部公告第235号[EB/OL].(2002-10-24)[2015-6-6].http://www.docin.com/p-595344430.html
[5]Peng C,Duan X,Song S,et al.Parts per trillion detection of 7-aminonitrazepam by nano-enhanced ELISA[J].Int J of Mol Sci,2013,14(10):19474-19483
[6]Mercolini L,Mandrioli R,Iannello C,et al.Simultaneous analysis of diazepam and its metabolites in rat plasma and brain tissue by HPLC-UV and SPE[J].Talanta,2009,80(1):279-285
[7]Li P,Han H,Zhai H,et al.Determination of trace vitamin C by ionpair HPLC with UV detection in calcium gluconate and vitamin C compound oral solution[J].J of Chromatogr Sci,2012,50(2):108-113
[8]Kumazawa T,Hasegawa C,Uchigasaki S,et al.Quantitative determination of phenothiazine derivatives in human plasma using monolithic silica solid-phase extraction tips and gas chromatographymass spectrometry[J].J of Chromatogr Sci,2011,1218(18):2521-2527
[9]Meyer G M J,Maurer H H.Qualitative metabolism assessment and toxicological detection of xylazine,a veterinary tranquilizer and drug of abuse,in rat and human urine using GC-MS,LC-MSn,and LCHR-MSn[J].Anal Bioanal Chem,2013,405(30):9779-9789
[10]孙雷,张骊,徐倩,等.超高效液相色谱-串联质谱法检测猪肉和猪肾中残留的10种镇静剂类药物[J].色谱,2010,28(1):38-42
[11]高洁,苗虹.兽药残留检测技术研究进展[J].食品安全质量检测学报,2013,4(1):11-18
[12]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 20763-2006猪肾和肌肉组织中乙酰丙嗪、氯丙嗪、氟哌啶醇、丙酰二甲氨基丙吩噻嗪、甲苯噻嗪、阿扎哌隆、阿扎哌醇、咔唑心安残留量的测定液相色谱-串联质谱法[S].北京:中国标准出版社,2006:1-9
[13]中华人民共和国国家质量监督检验检疫总局.SN/T 2113-2008进出口动物源食品中镇静剂类药物残留量的检测方法液相色谱-质谱/质谱法[S].北京:中国标准出版社,2008:1-7
[14]张力群,吴平谷,金铨,等.镇静剂残留分析的色谱检测技术研究进展[J].中国卫生检验杂志,2013,26(6):1634-1638
[15]汪丽萍,邱月明,赵海香,等.镇静剂残留分析的样品前处理技术研究进展[J].药物检测,2004,21(4):28-29
Determination of Eight Sedative Residues in Chicken by HPLC-MS/MS
HUA Meng-meng,GONG Xiao-ming*,GUO Li-qiang,DING Kui-ying,WANG Hong-tao,YU Jin-ling
(Weifang Entry-Exit Inspection and Quarantine Bureau,Weifang 261041,Shandong,China)
A method for the determination of 8 sedative(acetopromaizine,chlorpromazine,haloperidol,propionylpromazine,xylazine,azaperone,azaperol and carazolol)residues in chicken by high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS)had been developed.The sample was extracted with acetonitrile-0.1 mol/L HCl(90/10,volume ratio)and cleaned up with Angel PCX SPE colum.The targeted compounds were loaded onto an Agilent ZORBAX RRHD Eclipse Plus C18column(100 mm×3.0 mm,1.8 μm). The electrospray was operated in the positive mode and the samples were monitored by the multiple reaction monitoring(MRM)mode,and an internal standard method was used for quantitative analysis of 8 sedatives.The calibration curves of the 8 sedatives showed good linearity in the range of 0.5 μg/L-20.0 μg/L(correlation coefficients r2≥0.998).The limits of detection of the 8 sedatives were 0.5 μg/kg,and the limit of quantification was 1.0 μg/kg.The average recoveries and the relative standard deviations ranged from 85.3%-95.5%and from 0.81%-5.00%at the spiked levels of 1.0,5.0,10.0 μg/kg for the 8 sedatives in chicken matrix.This method is reliable,and suitable for the determination of 8 sedative residues in chicken.
HPLC-MS/MS;chicken;sedatives;residue
10.3969/j.issn.1005-6521.2016.19.031
2015-09-28
山东检验检疫局科研基金项目(SK201216);潍坊市2015年科学技术发展计划(2015ZJ1101)
华萌萌(1986—),女(汉),中级工程师,硕士,研究方向:农兽药残留及添加剂分析。
宫小明,高级工程师,硕士。

