盐酸拉贝洛尔时控缓释微丸的研制
高捷 朱淼 沃联群 王文喜
1.浙江医药高等专科学校实验实训中心,浙江宁波315100;2.浙江工业大学药学院,浙江杭州310014
盐酸拉贝洛尔时控缓释微丸的研制
高捷1朱淼2沃联群1王文喜2
1.浙江医药高等专科学校实验实训中心,浙江宁波315100;2.浙江工业大学药学院,浙江杭州310014
目的研究制备盐酸拉贝洛尔时控缓释微丸。方法采用挤出滚圆法制备载药丸芯,通过流化床包衣法分别覆上交联羧甲基纤维素钠作为溶胀层、乙基纤维素和羟丙甲纤维素作为控释层制备时控缓释微丸,通过单因素考察筛选溶胀层、控释层的处方组成对体外释药性能的影响。结果以微晶纤维素、羧甲基淀粉钠和乳糖为添加剂可制得性能良好的高载药微丸。随着溶胀层厚度的增加,药物释放时滞变短,速率显著增加;随着控释层包衣厚度的增加,时滞延长,释药减慢;控释层中羟丙甲纤维素用量增加,时滞缩短;控释层中增塑剂用量增加,时滞延长。结论所得包衣微丸具有良好的释药性能,有广阔的应用前景。
盐酸拉贝洛尔;时控缓释微丸;溶胀层;控释层
盐酸拉贝洛尔(1abeta1o1hydroch1oride)是兼具α、β受体阻断作用的抗高血压药物,临床用于治疗各种类型的高血压[1-4]。高血压的发生具有明显的时辰节律性,市售盐酸拉贝洛尔制剂多为注射液、片剂和胶囊等普通制剂,需一日多次给药且不能满足夜间治疗的要求[5-6]。本研究针对其发作的时间特殊性,制备具有3 h时滞的时控缓释微丸,使其达到晚间睡前服药,发病高峰期维持治疗疗效的血药浓度。微丸是多单元释药体系,可以避免个别单元因制造缺陷或不寻常的胃刺激引起的药物解体失效的弊端,具有更好的重现性[7-9]。本研究采用挤出滚圆法制备载药丸芯,以高溶胀性能的交联羧甲基纤维素钠CC-Na作溶胀层,以羟丙甲纤维素(HPMC)和乙基纤维素(EC)混合物为控释层,通过单因素考察筛选溶胀层、控释层的处方组成,并对其体外释药性能和释药机制进行初步考察。
1 仪器与试剂
Mini DPL 0.2多功能制粒/包衣机(重庆精工制药机械有限责任公司);Mini-250低温挤出滚圆机(深圳信宜特科技有限公司);ZRS-8G型智能溶出仪(天大天发科技有限责任公司);FA2004B型电子天平(上海佑科仪器仪表有限公司);He1iosλ紫外可见分光光度计(美国热电公司);FT-2000型脆碎度仪(天津大学精密仪器厂)。
盐酸拉贝洛尔(南京爱里凯德化工有限公司);微晶纤维素(MCC)、羧甲基淀粉钠(CMS-Na)、交联羧甲基纤维素钠(CC-Na)、羟丙基甲基纤维素(HPMC)、柠檬酸三乙酯(TEC)、蓖麻油均由安徽山河药用辅料股份有限公司惠赠;乙基纤维素(EC)(卡乐康公司),其他试剂皆为分析纯。
2 方法与结果
2.1 载药丸芯的制备
采用挤出滚圆法制备载药丸芯,称取处方用量的盐酸拉贝洛尔、MCC、CMS-Na和乳糖,混合均匀后,加适量纯化水制软材,经挤出滚圆机制成载药微丸[10]。挤出速率为25 r/min,滚圆转速为1200 r/min,滚圆时间为4min,40℃烘干过夜,过筛,取18~24目微丸,备用。
2.2 盐酸拉贝洛尔含量测定方法学研究
2.2.1 吸收波长的选择将盐酸拉贝洛尔溶于0.1 mo1/L的盐酸中,配制成适宜浓度的溶液,另取相同处方用量的空白辅料于盐酸中,过滤,取续滤液,在200~400 nm波长范围内扫描测定其紫外吸收行为。结果见图1。从图中可看出,盐酸拉贝洛尔在此波长范围内有三个吸收峰,而辅料仅在200 nm附近有末端吸收,考虑到方法的专属性,故选定300 nm作为盐酸拉贝洛尔的检测波长。

图1 盐酸拉贝洛尔和辅料溶液的紫外吸收图谱
2.2.2 标准曲线的建立精密称定盐酸拉贝洛尔标准品适量,配成1000μg/mL的储备液,分别稀释成10、20、40、60、80、100、120μg/mL浓度,以溶出介质作空白对照,在300 nm处测其吸光度,以吸光度(A)对浓度(C)(μg/mL)作线性回归,得回归方程为A= 0.007 13C+0.004 29,相关系数r=0.9998。表明在10~120μg/mL范围内,盐酸拉贝洛尔的吸光度(A)和浓度(C)线性关系良好。
2.2.3 回收率试验精密称取盐酸拉贝洛尔80、100、120 mg各三份,置于100 mL容量瓶内,分别按处方比例加入其他辅料,加入0.1mo1/L盐酸溶解,超声30min,加入盐酸至刻度,摇匀,过滤,弃初滤液,稀释,制备成80、100、120μg/mL的溶液,在波长300 nm处,测吸光度,计算回收率结果见表1。三个浓度的平均回收率是102.80%、101.87%、99.55%,RSD是0.62%、 0.70%、0.28%,结果符合要求。

表1 回收率试验(n=3)
2.2.4 精密度试验精密称取盐酸拉贝洛尔适量,溶解稀释配制成80、100、120μg/m L的三种浓度,用紫外分光光度法分别在同日内不同时间和不同日内测其吸光度,考察精密度。结果见表2。

表2 精密度试验(n=3)
2.3 载药丸芯的质量评价
2.3.1 外观及圆整度测定采用测定微丸的长短径比作为圆整度的评价指标。取微丸200粒以上,均匀分散在背景板上,控制微丸间的间隙,拍照后使用Image Pro p1us软件处理,先剔除连在一起的微丸,再测长短径之比[11]。结果发现,当盐酸拉贝洛尔的药物含量超过60%时制备的丸芯成球性能较差,加入乳糖可提高圆整度,最佳处方的长短径比为1.26。
2.3.2 脆碎度精密称取6.5 g左右的微丸,加入10粒直径为3 mm的玻璃珠,一起置于脆碎度检测仪中旋转8min,收集微丸并精密称定其重量,计算失重百分率。结果发现,加入降低药物含量,提高乳糖用量可降低脆碎度,最佳处方的脆碎度为0.26%。
2.3.3 溶出度测定精密称取微丸适量,照《中国药典》2015年版四部溶出度与释放度测定法第二法装置测定,以900mLpH值6.8磷酸缓冲液为介质,转速75 r/min。在预定时间取样5mL(同时补充同温等量纯化水),经0.45μm微孔滤膜过滤,取续滤液适当稀释,在300 nm波长处测定吸光度,计算各时间点的累积释药百分率。
结果发现,当丸芯内无CMS-Na时,药物释放不完全,加入10%的CMS-Na可以提高释药速率。综合考虑丸芯的脆碎度、圆整度和体外溶出度,最终选择的处方为:m(盐酸拉贝洛尔):m(MCC):m(CMS-Na):m(乳糖)=50:35:10:5,其在1 h内即能释药完全。其溶出度曲线见图2。

图2 丸芯处方溶出曲线
2.4 溶胀层的确定
HPMC E5加水溶解,加入处方量的CC-Na,搅拌过夜,制成均匀分散体系。取载药丸芯50 g,采用流化床底喷包衣法对载药微丸进行包衣。工艺参数为:风机频率25 Hz,进风温度45℃,物料温度35℃,进液速率1.3~1.4mL/min,雾化压力0.175 MPa。
在没有控释层存在的情况下,先考察溶胀层增重45%对药物释放的影响,从图中可看出,在没有控释层时,溶胀层增重对于丸芯药物的释放几乎没有影响,1 h内的药物释放均超过80%。结果见图3。
再按“2.5”项下对包有溶胀层的微丸进行控释层包衣,控制控释层增重14%,考察溶胀层增重对释药行为的影响,随着溶胀层厚度增加,时滞变短,释药速率显著加快。结果见图4。
2.5 控释层考察
将HPMC加入95%乙醇中溶解,依次加入处方量的TEC、EC和滑石粉,搅拌过夜,制备成均匀分散体系。取丸芯50 g,采用流化床底喷包衣法对微丸进行包衣。工艺参数为:风机频率25 Hz,进风温度45℃,物料温度35℃,进液速率1.6~1.8 mL/min,雾化压力0.175MPa。
2.5.1 HPMC的比例对释药行为的影响按照“2.3”项下的包衣操作,控制溶胀层增重为45%,调整控释层包衣中EC与HPMC的比例分别为2:1和4:1,考察EC与HPMC的比例对体外释放的影响,从图中可看出,随着控释层处方中HPMC比例的增加,时滞变短,药物释放速率变快。但是EC与HPMC的比例为2:1时,药物释放时滞较短,且释放较快,不符合时滞后缓释的目的,故选用EC与HPMC的比例为4:1做进一步考察。结果见图5。
2.5.2 增塑剂对释药行为的影响根据“2.4”和“2.5”项下的包衣操作,控制溶胀层增重45%,在控释层14%水平下考察控释层中增塑剂TEC及蓖麻油对体外释放的影响,从图中可看出,增塑剂TEC对时滞有明显的影响,不含增塑剂的微丸具有很短的时滞,但加入增塑剂蓖麻油后,药物无释放,因此选用TEC作为最优处方增塑剂。结果见图6。
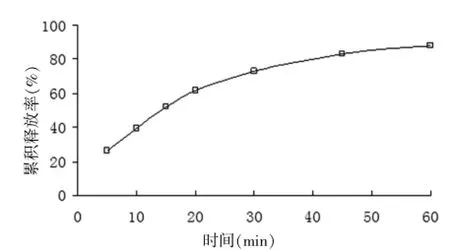
图3 溶胀层厚度对无控释层载药微丸释放度的影响

图4 溶胀层厚度对药物释放的影响(控释层增重14%)

图5 EC和HPMC E5的比例对药物释放的影响
2.5.3 控释层的厚度对释药行为的影响选用溶胀层增重45%的微丸,按照“2.5”项下的包衣操作,得到控释层增重7%、14%、21%的小丸三批,考察控释层厚度对释药行为的影响,随着控释层厚度的增加,释放的时滞变长,药物释放速率变慢。结果见图7。

图6 增塑剂对药物释放的影响

图7 控释层厚度对药物释放的影响

图8 释放介质对释放行为的影响
2.6 释放介质考察
取最优处方时控缓释微丸,分别以水、pH值1.2的盐酸、PBS以及先2 h盐酸后转入PBS为介质测定其释药行为,考察释放介质对最终产品药物释放的影响,释放介质对药物的释放无明显影响。结果见图8。
2.7 包衣膜爆破考察
取微丸适量于溶出杯中,按“2.3.3”项下条件操作,分别于每小时取出微丸,用数字显微镜观察微丸的外观变化,微丸的外观变化和体外释放曲线基本吻合。前3 h微丸的膜表面完整,没有明显的破裂,在这段时间内药物基本无释放,而当4 h时,微丸的膜已经破裂,药物大量释放出来。这说明药物的时控缓释释放是由于微丸膜的破裂。结果见图9。
3 讨论
载药丸芯的制备主要有空白丸芯上药法、离心造粒法和挤出滚圆法等[12-14]。其中挤出滚圆法由于具有载药量高、粒径分布窄、圆整度好、机械性能强等优点,已成为应用最广泛的技术之一[15-16]。本研究选用MCC为成丸骨架材料,制得含药量高达50%的载药丸芯,进一步提高药物含量,则不能得到球状微丸。研究中发现,不含CMS-Na的处方药物释放不完全,加入CMS-Na可促进药物释放完全,但圆整度略有降低,加入少量乳糖可提高微丸的圆整度和机械性能。

图9 溶出过程中微丸外观变化
脉冲控释微丸的释药原理主要有渗透压控制型、溶蚀型和溶胀爆破型等[17-19]。溶胀爆破型是由于溶胀层吸水膨胀后使控释膜破裂导致药物脉冲释放,因此溶胀层的厚度对释药时滞有非常重要的影响。从结果中可看出,随着溶胀层厚度的增加时滞明显缩短,随着溶胀层厚度的增加,其吸水产生的溶胀力更大,故能在更短时间内胀破外膜,所以时滞变短。
控释层的处方也是脉冲释药系统的关键,EC为最常用的控释膜材之一,但单独使用时透水性太差,常需加入适量致孔剂来调节水分的渗入[20]。本研究采用HPMC作为致孔剂考察其用量对释药性能的影响,增加HPMC用量可以提高吸水速率,同时会降低膜的刺穿强度,因此,会缩短时滞,提高药物释放速率。控释层中增塑剂TEC的加入会增加膜的韧性,从而提高控释膜耐受胀破的能力,故加入增塑剂可延长药物的释放时滞[21]。
[1]秦玲.盐酸拉贝洛尔对重度妊娠高血压综合征的治疗效果观察[J].中国医药导刊,2011,13(7):1202-1203.
[2]周琼.盐酸拉贝洛尔联合酚妥拉明及硫酸镁治疗妊娠期高血压的疗效分析[J].中国医学工程,2014,22(2):43-44.
[3]胡俊.盐酸拉贝洛尔联合综合干预模式对妊娠高血压患者妊娠结局的影响[J].中国处方药,2015,13(9):108-109.
[4]董嗣庆.盐酸拉贝洛尔注射液在高血压急症临床应用的效果探讨[J].中外医疗,2015,34(7):132-133.
[5]孙建国,王广基,杨海涛,等.盐酸拉贝洛尔缓释片在犬体内的药代动力学研究[J].中国药科大学学报,2003,34(6):529-533.
[6]冯年平,屠锡德.盐酸拉贝洛尔缓释片及其药动学研究[J].中国药科大学学报,1996,27(1):13-15.
[7]Dashevsky A,Mohamad A.Deve1opmentof pu1sati1emu1ti-p1articu1ate drug de1ivery system coated with aqueous dispersion Aquacoat(R)ECD[J].Internationa1 journa1of pharmaceutics,2006,318(1-2):124-131.
[8]李娇,王扣存,宗莉.扎来普隆脉冲释放微丸的制备及体外释放[J].中国现代应用药学,2012,29(10):924-930.
[9]Jagda1e SC,Chede SM,Gu1wady R,et a1.Pu1sati1e Mu1tiparticu1ate Drug De1ivery System for Metopro1o1Succinate. Archives of Pharmaca1Research[J].2011,34(3):369-376.
[10]陈洪轩,陈寅生,马莉,等.复方盐酸奈福泮萘普生钠缓释胶囊的制备和工艺考察[J].中国药学杂志,2011,46(8):605-609.
[11]王文喜,章哲文,李佳萍,等.庆大霉素普鲁卡因胃漂浮缓释微丸的制备及质量评价[J].浙江工业大学学报,2013,41(3):265-269.
[12]陈智伟,刘志承,丘晓清.硫酸沙丁胺醇脉冲释药微丸的制备及其体外释药研究[J].中国医药导报,2013,10(19):124-126.
[13]常乃丹,于辉,彭海生,等.葛根素微丸制备及含量测定方法[J].中国医药导报,2011,8(30):60-62.
[14]王立,马维阳,张文君,等.离心造粒法制备奥美拉唑速释微丸[J].中国医药工业杂志,2016,47(2):183-187.
[15]陈宴,郎朗天,操锋,等.微丸制备工艺研究进展[J].药学进展,2012,36(8):362-369.
[16]刘耀,刘松青.挤出-滚圆法制备微丸的研究进展[J].中国药学杂志,2008,43(6):401-405.
[17]Hung SF,Hsieh CM,Chen YC,et a1.Formu1ation and process optimization of mu1tiparticu1ate pu1sati1e system de1ivered by osmotic pressure-activated rupturab1e membrane[J].Internationa1 journa1 of pharmaceutics,2015,480(1-2):15-26.
[18]Chaudhary SS,Pate1HK,ParejiyaPB,eta1.Chronomodu1ated drug de1ivery system of urapidi1 for the treatment of hypertension[J].Int J Pharm Investig,2015,5(2):107-113.
[19]Yadav D,Survase S,Kumar N.Dua1 coating of swe11ab1e and rupturab1e po1ymers on G1ipizide 1oaded MCC pe11ets for pu1sati1e de1ivery:Formu1ation design and in vitroeva1uation[J].Internationa1Journa1ofPharmaceutics,2011,419(1-2):121-130.
[20]Sungthongjeen S,Puttipipatkhachorn S,Paerataku1 O,et a1.Deve1opment of pu1sati1e re1ease tab1ets with swe11ing and rupturab1e 1ayers[J].Journa1of contro11ed re1ease,2004,95(2):147-159.
[21]Bussemer T,BodmeierR.Formu1ation parametersaffecting the performance of coated ge1atin capsu1es with pu1sati1e re1ease profi1es[J].Internationa1Journa1of Pharmaceutics,2003,267(1-2):59-68.
Preparation of tim e-controlled of labetalol hyd rochloride sustained-release pellets
GAO Jie1ZHU Miao2WO Lianqun1WANGWenxi2
1.Experimenta1 and Training Center,Zhejiang Pharmaceutica1Co11ege,Zhejiang Province,Ningbo 315100,China;
2.Co11ege of Pharmaceutica1Science,Zhejiang University of Techno1ogy,Zhejiang Province,Hangzhou 310014,China
Objective To deve1op a nove1 time-contro11ed pe11ets for 1abeta1o1 hydroch1oride with sustained-re1ease behavior.M ethods The 1abeta1o1-1oaded pe11ets cores were prepared by extrusion-spheronization,then were coated with croscarme11ose sodium as swe11ing 1ayer,fo11owed by themixture of ethy1 ce11u1ose and hydroxypropy1methy1ce1-1u1ose as contro11ed re1ease 1ayer via the f1uid bed coating equipment.The effects of swe11ing 1ayer and contro11ed re-1ease membrane on the profi1e of drug re1ease in vitro were investigated by sing1e factor test.Resu lts The high 1abeta1o1-1oaded pe11et coresmade ofm icroce11u1ose,sodium carboxymethy1 starch and 1actose showed satisfactory characters.With the thickness of the swe11ing 1ayer increasing,the 1ag time of drug re1ease was pro1onged and the re1ease rate increased.With the increase of HPMC ratio in the contro11ed re1ease 1ayer,the 1ag time increased.The 1ag time was a1so pro1onged with the addition of p1asticizer.Con lusion The obtained pe11ets disp1ay good drug re1ease behavior,which suggests a great potentia1 in c1inic app1ication.
Labeta1o1hydroch1oride;Sustained-re1ease pe11ets of time-contro11ed;Swe11ing 1ayer;Contro11ed-re1ease 1ayer
R943
A
1673-7210(2016)07(a)-0026-05
2016-02-18本文编辑:赵鲁枫)
浙江省药品监督管理局计划项目(2014012)。
高捷(1976-),女,高级实验师,主要从事药物制剂研究。
王文喜(1977-),男,博士,副教授,硕士生导师,主要从事药物新剂型与新技术研究。

