基于GSH-CdTe的荧光检测法用于水溶液中氟离子浓度的检测
王逸飞+陈晓琴+范红松
摘 要 饮用水中氟离子浓度与人类健康息息相关,氟离子浓度过高或过低都会引发不同的健康问题,因此准确检测水中氟离子浓度使其保持在一定范围内至关重要。本文以谷胱甘肽为稳定剂合成了具有优异荧光性质的量子点(GSH-CdTe),在加入不同浓度的氟离子后,通过检测量子点的荧光强度变化从而得到氟离子浓度与荧光强度的拟合相关曲线,其检出限为20nmoL/L,通过对照实验发现其他阴离子的存在并不会干扰氟离子浓度的检测,此方法操作简单,检出限比传统的方法更低且更灵敏。
关键词 荧光强度;氟离子;GSH-CdTe;团聚
中图分类号 O6-3 文献标识码 A 文章编号 1674-6708(2016)172-0251-05
氟离子与人类健康有着密切的关系,一方面氟是人体必需的微量元素之一,适量的氟能维持机体正常代谢,有利于钙和磷的利用以及在骨骼中沉积,加速骨骼的形成,增加骨骼的硬度。机体中氟摄入不足会严重的影响牙齿和骨骼的健康,导致龋齿与骨质疏松等疾病。另一方面,人体摄入氟过量会造成氟中毒[ 1 ],引发尿石病[ 2 ],肾功能衰竭[3],癌症甚至导致死亡等[4]。因此精确而又快速的检测饮用水中氟离子的浓度,使其保持在最佳范围至关重要[ 5 ]。
目前,科学家已研究出多种方法用于氟离子浓度的检测。如离子选择性电极法[ 6 ],色谱分析法[ 7 ],荧光分光光度法[8],动态光散射法[ 9 ]。尽管每种方法都有自己的优点和缺点,但基于荧光的氟离子检测法却以其低成本,高灵敏度及高选择性等优点引起了科研工作者的广泛关注。多种不同的纳米材料比如Au[10],C量子点[ 1 1 ],Si纳米线[ 1 2 ],量子点[13,14]都已被作为荧光探针用于氟离子的检测。其中量子点由于其独特的大小,优异的电学和光学性质等优势在用作氟离子荧光探针的检测中具有广泛的应用前景。但通常采用有机相合成的量子点反应条件苛刻,毒性高,水溶性差。因此,研究开发出具有优异光学性质的低毒性水溶性量子点用于检测水溶液中氟离子浓度具有较大的应用前景。谷胱甘肽(GSH)是一种含巯基的生物寡肽,以GSH为稳定剂,通过巯基与Cd2+之间的络合配位作用可以包裹在Cd2+的周围,合成谷胱甘肽包裹的量子点。由于谷胱甘肽含有大量的羧基和氨基,因此能更好地提高量子点的水溶性及化学稳定性。此外,根据我们之前的研究报道[ 1 5 ]以谷胱甘肽为稳定剂合成的量子点具有更为优异生物安全性,因此在实际应用中更为安全环保。
本文以谷胱甘肽(GSH)为表面活性剂,合成了具有优异的荧光性质以及低毒性的水溶性CdTe量子点,并将其用于水溶液中氟离子的检测,实验结果表明,以GSH-CdTe为荧光探针,在检测水溶液中氟离子浓度时具有较高的选择性及敏感性,其检出限低至0.1mg/L。本文中研究出的这种方法操作简单,成本低廉,环保无毒,具有较强的离子选择性,能做到特异性检测,具有非常好的应用前景。
1 实验与方法
1.1 仪器与试剂
碲粉(99.9%,分析纯)购于天津光伏精细化工研究所,氯化镉(99%,分析纯)、NaBH4(99%,分析纯)购于上海阿拉丁有限公司,谷胱甘肽(95%,Sigma,美国)。其它试剂如无特殊说明均为分析纯,购自成都科龙试剂有限公司,实验用水均为超纯水(电阻率为18.2 MQ-cm)。
1.2 GSH-CdTe量子点的合成
GSH-QD的制备方法参考此前的研究报道[ 1 5 ]。首先将95毫升的超纯水加入四口瓶中,然后加入1mmol还原性谷胱甘肽和4ml氯化镉(0.1mol/L)溶液,形成Cd2+-GSH络合物,用NaOH和HCL(1mol/L)将溶液的pH调到9,对溶液进行加热同时向溶液中通入N2以去除体系中的氧气等成分使体系保持在无氧状态,当温度上升至90℃时,在剧烈搅拌下迅速注入1ml新鲜制备的NaHTe水溶液(0.1mol/L),各反应物的摩尔比为Cd2+:Te:GSH=4:1:10,在氮气保护下冷却回流,待1小时后终止反应,待其冷却后按1:1的比例加入异丙醇混合均匀后进行离心洗涤(15 000rmp,10分钟),以除去过量的未反应物质,反复3次后将纯化后的量子点溶于超纯水中并避光保存在4℃备用。
1.3 量子点的表征
在室温条件下,分别通过紫外分光光度计(PerkinElemer,Lambda 650)、荧光分光光度计(HITACHI,F-7000)对不同回流时间合成的量子点的光学性能进行表征,通过马尔文粒度测试仪对合成的量子点的粒径大小和表面电荷进行表征。通过高分辨透射电子显微镜(HRTEM,TECNAI G2,F20 S-TWIN,FEI)对量子点的形貌尺寸及晶格结构进行表征。
1.4 水溶液中氟离子浓度检测
在一定浓度的GSH-CdTe量子点溶液中分别加入不同浓度(0.25mg/L~50mg/L)的氟离子溶液。将混合样放入摇床中震荡孵育(100r/min),震荡20min后取出,利用荧光分光光度计检测混合液的荧光发射波长及其荧光强度,激发波长统一为400nm,电压600v,测定温度为25℃。利用原始数据绘制得到(F-浓度)/(增加的荧光强度)的标准曲线,通过校准数据3σ/k得到氟离子的检测极限(LOD),其中σ是空白样的标准偏差,k是标准曲线的斜率。
为了评估在有其它相关离子存在干扰的情况下,利用GSH-QD的荧光测定F-离子浓度是否有选择性,实验
同时设置了Cl-,Br-,I-,S-,SO4-,SO3-,HCO3-,HPO4-,CH3COOH-,H2PO4-等离子对GSH-QD荧光强度的影响,离子浓度为50mg/L。
2 结果与讨论
2.1 荧光探针的表针
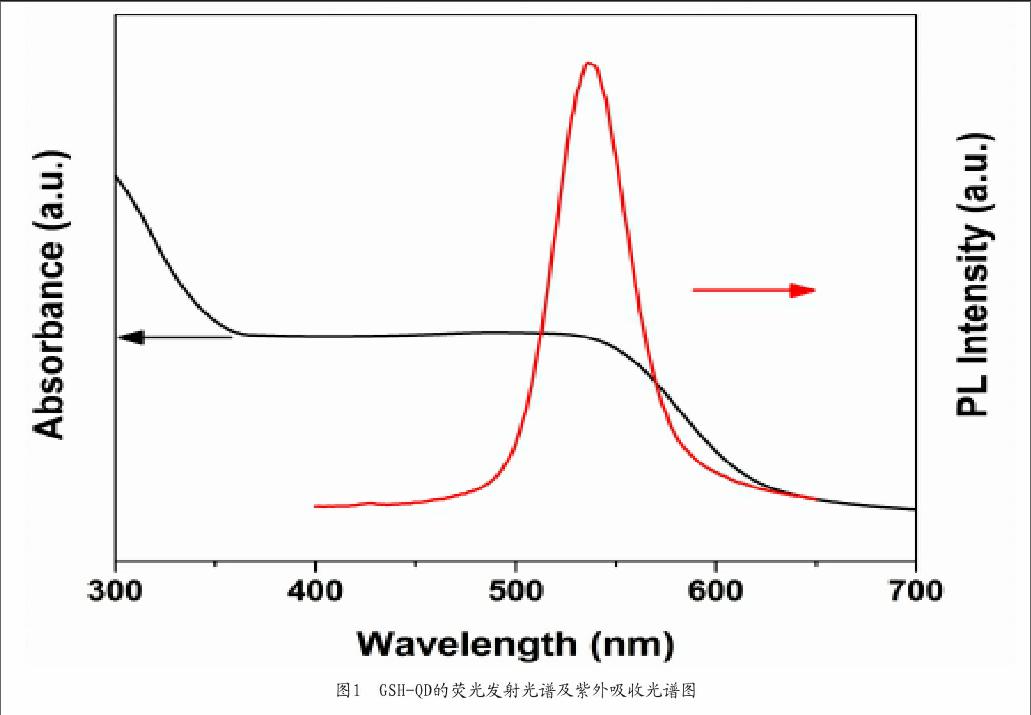
本文以还原性谷胱甘肽(GSH)为稳定剂,利用简单快速的水相法制备了水溶性GSH-CdTe量子点,由于谷胱甘肽含有大量的羧基和氨基基团,因此以其为稳定剂制备的量子点极易溶于水溶液。产物在水溶液中的紫外-可见吸收光谱如图1所示,吸收光谱显示GSH-CdTe量子点有很宽的吸收范围,曲线平滑,没有单独的吸收峰,由此可见,GSH-CdTe量子点可以被多种不同的激发波长所激发,而普通的有机荧光染料只能通过特定的波长进行激发,这个优势使得GSH-CdTe量子点在检测氟离子浓度时,对仪器的要求不那么苛刻,多数仪器都能检测。图1同时显示了GSH-CdTe量子点的荧光发射光谱图,由图中可以看出,本文合成的GSH-CdTe量子点具有完全对称的发射光谱,发射波长为538nm,其半峰宽(FWHM)较窄约为38nm,显示本文中合成的量子点质量较好,尺寸分布较窄,具有优异的荧光性能可作为荧光探针使用。
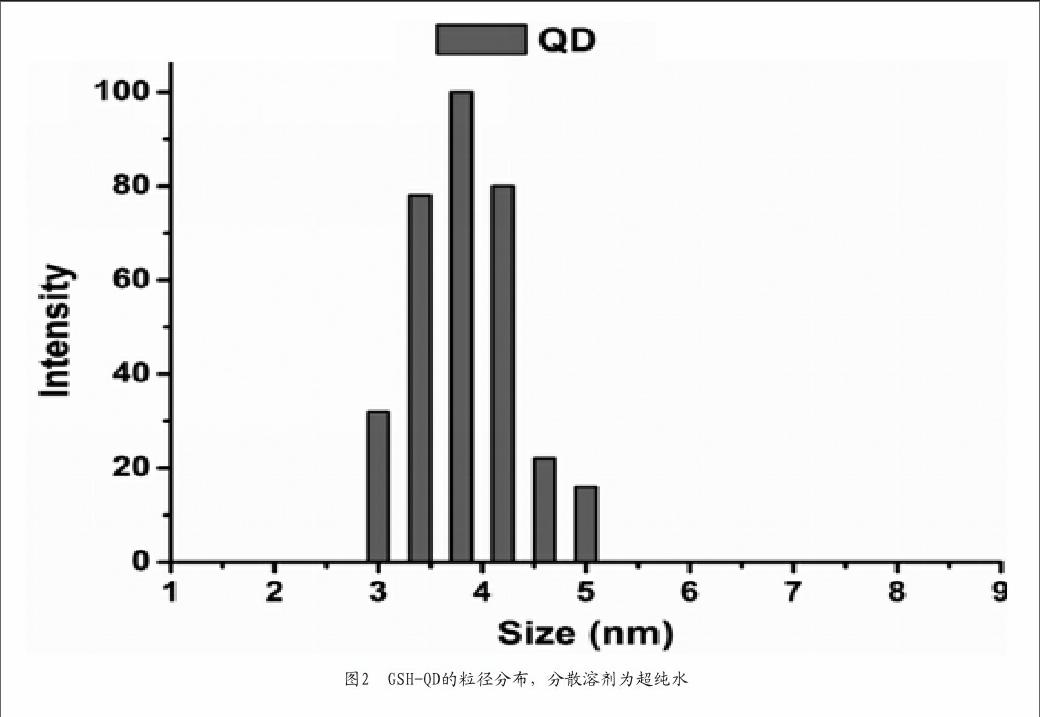
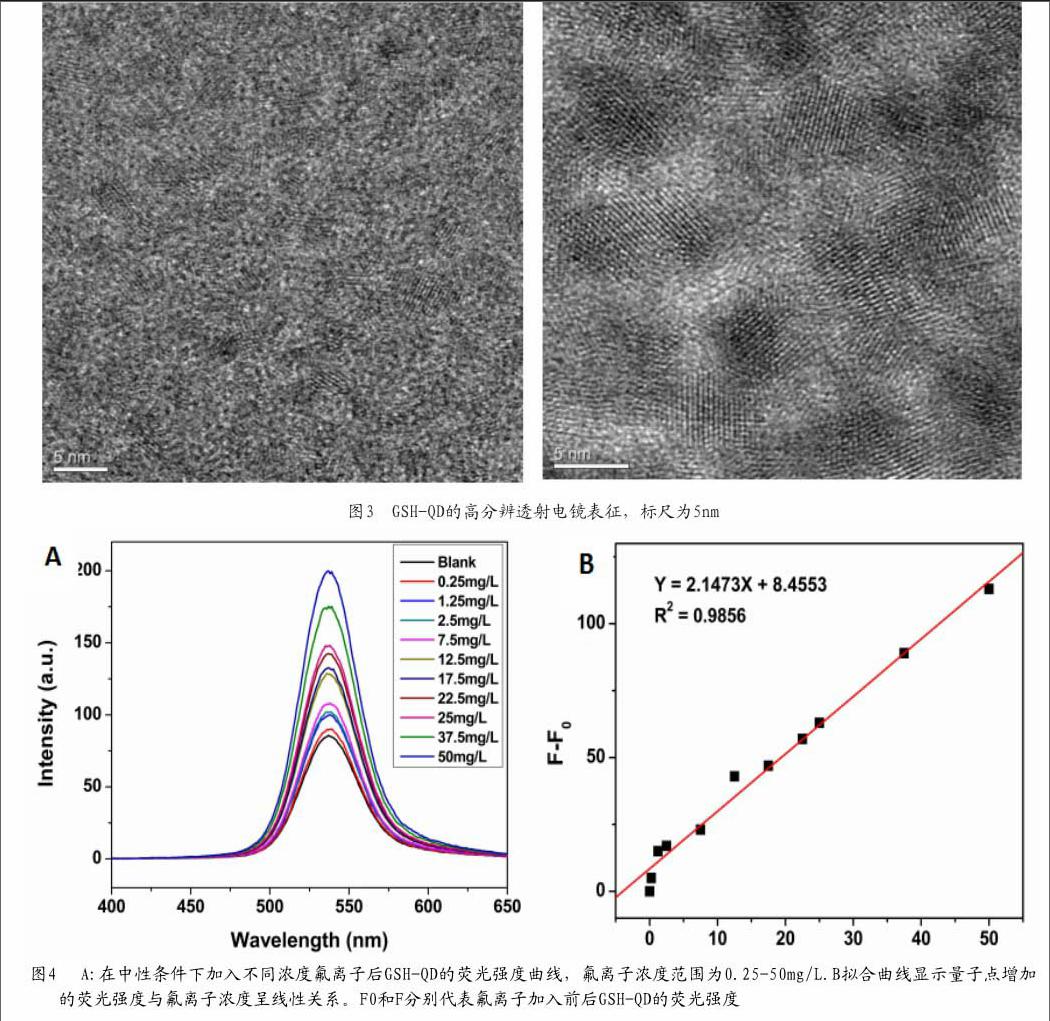
图2表征了制备的GSH-CdTe量子点的粒径,结果显示本文中合成的量子点具有良好的水溶性与单分散性,粒径比较均匀,尺寸较小,在3nm~5nm之间。图3高分辨透射电镜显示合成的量子点晶面清晰可见,具有优异的晶体结构,粒径尺寸约为3nm~5nm,与测出的量子点粒径吻合。
2.2 氟离子浓度检测
本文通过荧光法考察了不同浓度的氟离子对谷胱甘肽包裹的量子点(GSH-CdTe)荧光发射强度的影响,此法方便快捷,且具有选择性和特异性。量子点在合成过程中用谷胱甘肽做稳定剂及包裹剂,使得其表面存在了大量的基团,对量子点纯化后再加入相应浓度的氟离子,通过荧光分光光度计检测不同浓度的氟离子对量子点荧光强度影响。
2.2.1 氟离子浓度检测标准曲线
图4显示了在中性条件下不同浓度的F-(0.25mg/ L~50mg/L)与GSH-QD共孵育后溶液的荧光发射图谱。结果显示随着F-离子浓度的增加,量子点的荧光发射强度逐渐增大,在一定范围内,荧光强度的增加与F-浓度呈较好的线性关系(R2=0.9856),通过校准数据3σ/k可算出GSH-QD荧光检测法检测F-离子浓度的极限(LOD)约为0.1mg/L,与离子选择电极法相比具有一定的优势。
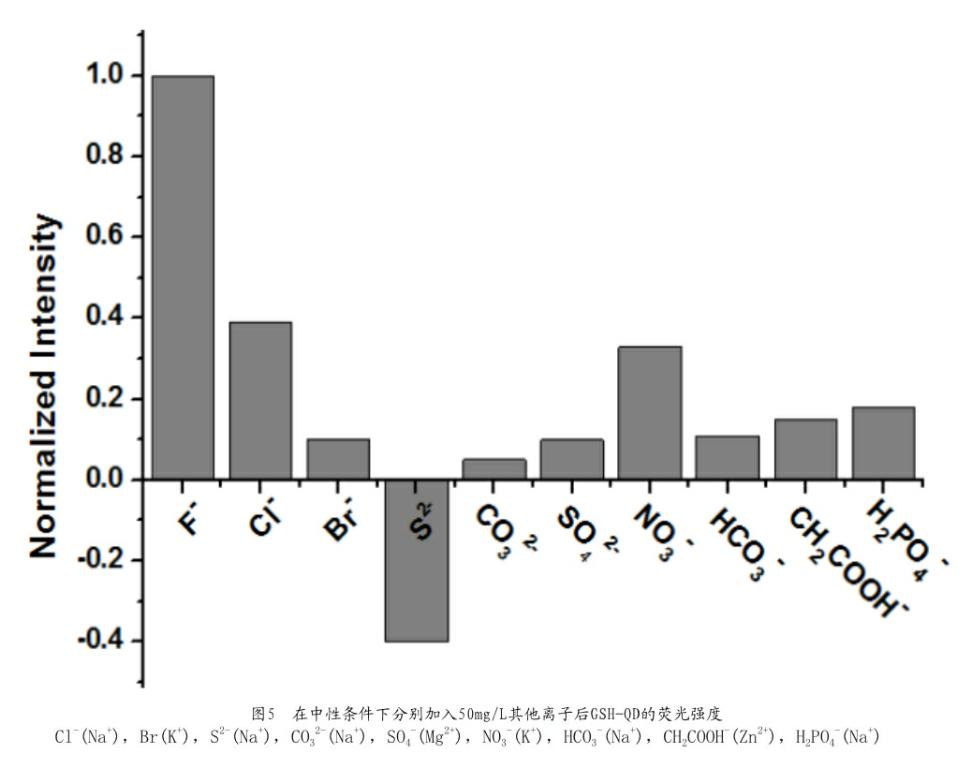
2.2.2 特异性分析,离子选择性分析
为了考察GSH-QD荧光探针检测氟离子浓度的选择性和特异性,以及是否会受其它背景离子的干扰影响,本文继续验证了其它常见离子对GSHQD荧光强度的影响。文中分别选用了50mg/L的Cl-(Na+),Br(K+),S2-(Na+),CO32-(Na+),SO4-(Mg2+),NO3-(K+),HCO3-(Na+),CH2COOH-(Zn2+),H2PO4-(Na+)做了对比实验,这些都是较可能存在于饮用水中的干扰离子。图5显示这些离子对GSH-QD荧光探针的强度和灵敏度没有明显的影响,证明即使在有其它背景离子存在的情况下,GSH-QD荧光探针依然可以选择性的检测氟离子浓度,具有较好的特异性。
2.2.3 机理探讨
谷胱甘肽量子点表面带有大量的羧基,氨基基团,在中性环境下,GSH-CdTe由于颗粒之间形成NH-N键,颗粒间的电荷排斥力减小,在水溶液中比较容易自发团聚和非特异性吸附,引起荧光强度的降低。加入氟离子后,氟离子可与氨基形成更强的NH—F氢键并取代NH—N氢键,诱导团聚的GSH-QD颗粒重新分散,荧光强度得到恢复[ 1 6 ]。后面加入Cl-、NO3-、H2PO4-可使量子点团聚体略有分散;加入Br、CO32-、HCO3-、SO4-离子对量子点团聚体基本无影响也是由于电性强度不同;而加入S离子反而加剧了颗粒的团聚,我们猜想是因为S离子可能与重金属离子镉和碲形成络合物因而导致团聚更厉害,荧光因此淬灭,因此,可根据量子点荧光强度的变化实现对氟离子的特异性检测.
3 结论
本文基于GSH-CdTe的荧光强度变化,成功研究出了可方便快捷检测水溶液中氟离子浓度的荧光探针,文中合成的量子点荧光探针尺寸在3nm~5nm之间,具有较好的荧光强度。在加入不同浓度的氟离子后,量子点探针的荧光强度得到了显著的提高,并具有较好的线性关系。校准曲线显示本文研发的荧光探针最低可以检测0.1mg/L的氟离子浓度。通过与其它离子对比研究发现,荧光探针的灵敏度并不会受到氟离子以外的其它离子的干扰,证明利用GSH-QD荧光探针检测水溶液中氟离子浓度具有选择性和特异性。本文提出的氟离子浓度检测法操作简单,价格低廉,检测灵敏度高且具有选择特异性,可用于检测饮用水,生物环境中氟离子浓度的检测。
参考文献
[1] S. Ayooba, A. K. Guptaa, Fluoride in Drinking Water: A Review on the Status and Stress Effects,Crit. Rev. Env. Sci. Tech. 2006, 36, 4330487.
[2] Singh, P. P.; Barjatiya, M. K.; Dhing, S.; Bhatnagar, R.; Kothari, S.; Dhar, V. Evidence Suggesting that High Intake of FLuoride Provokes Nephrolithiasis in Tribal Population. Urol. Res. 2001, 29, 2380244.
[3] Cittanova, M.L.; Lelongt, B.; Verpont, M.C. Fluoride Ion Toxicity in Human Kidney Collecting Duct Cells. Anesthesiology 1996, 84, 428–435.
[4] Bassin, E. B.; Wypij, D.; Davis, R.B. AgeSpecific Fluoride Exposure in Drinking Water and Osteosarcoma (United States). Cancer Cause. Control 2006, 17(4), 421–428.
[5] Gilles, D; Loehr, R. Waste Generation and Minimization in Semiconductor Industry. J. Environ. Eng., 1994, 120:1(72), 72-86.
[6]. Frant, M. S.; Ross, J. W. Electrode for Sensing Fluoride Ion Activity in Solution. Science 1966,154, 155301555.
[7] Stefan, R. I.; van Staden, J. F.; Aboul0Enein,H. Y. Determination of Fluoride in Toothpaste,Effluents Streams and Natural and Borehole Water Using a Flow Injection System with a Fluoride Selective Membrane Electrode. Pharm. Acta Helv. 1999, 73, 307–310.
[8]Culik, B. Microdiffusion and Spectrophotometric Determination of Fluoride in Biological Samples. Anal. Chim. Acta 1986, 189, 3290337.
[9]WANG Qing,YANG Li—Yan,LIU Jian—Bo,YANG Xiao—Hai,WANG Ke—Min,JI Hai—Ning,LIU Yan.Chem.Dynamic Light Scattering for Fluoride Ions Detection. J.Chinese Universities [J],2012,33(10):2195—2198.
[10]Watanabe, S.; Seguchi, H.; Yoshida, K.; Kifune, K. Colorimetric Detection of Fluoride Ion in an Aqueous Solution using a ThioglucoseCapped Gold Nanoparticle. Tetrahedron Lett. 2005, 46, 8827 – 8829.
[11]Basu, A.; Suryawanshi, A.; Kumawat, B.; Dandi,A.; Guin, D.; Ogale, S. B. Starch (Tapioca) to Carbon Dots: an Efficient Green Approach to an On–Off–On Photoluminescence Probe for Fluoride Ion Sensing. Analyst 2015, 140, 1837 – 1841.
[12]Wang, H.; Fan, P.0H.; Tong, B.; Dong,Y.0P.; Ou, X.0M.; Li, F.; Zhang, X.0H. Hydrogen-Terminated Si Nanowires as Label0Free Colorimetric Sensors in the Ultrasensitive and Highly Selective Detection of Fluoride Anions in Pure Water Phase. Adv. Funct. Mater. 2015, 25,1506 – 1510.
[13]Mulrooney, R. C.; Singh, N.; Kaur, N.; Callan,J. F. An “Off–On” Sensor for Fluoride using Luminescent CdSe/ZnS Quantum Dots. Chem. Commun. 2009, 686 – 688.
[14]Jianbo Liu, Xiaohai Yang, Kemin Wang, Ronghua Yang, Haining Ji, Liyan Yang, Chunlei Wu. A switchable fluorescent quantum dot probe based on aggregation/disaggregation mechanism. Chem. Commun., 2011,47, 935-937.
[15]Xiaoqin Chen , Yajun Tang , Bing Cai and Hongsong Fan. ‘One-pot synthesis of multifunctional GSH–CdTe quantum dots for targeted drug Delivery. Nanotechnology, 2014,25, 235101.
[16]Jianbo Liu, Xiaohai Yang, Kemin Wang,* Ronghua Yang, Haining Ji, Liyan Yang and Chunlei Wu,A switchable fluorescent quantum dot probe based on aggregation/disaggregation mechanism, Chem. Commun, 2011, 47, 935–937.