不同剩余污泥发酵液对NOx-还原的影响
何岳兰,王淑莹,李夕耀,马 斌,郭思宇 (北京工业大学,北京市污水脱氮除磷处理与过程控制工程技术研究中心,北京市水质科学与水环境恢复工程重点实验室,北京 100124)
不同剩余污泥发酵液对NOx-还原的影响
何岳兰,王淑莹*,李夕耀,马 斌,郭思宇 (北京工业大学,北京市污水脱氮除磷处理与过程控制工程技术研究中心,北京市水质科学与水环境恢复工程重点实验室,北京 100124)
在(35±1)℃,且pH值分别为酸性(pH=4.0, 5.0, 6.0)和碱性(pH=8.0, 9.0, 10.0)条件下进行剩余污泥厌氧发酵,批次试验研究了相同体积的不同污泥发酵液对N Ox-还原过程的影响.结果表明:当pH=8.0产生的发酵液做碳源时反应速率最高,NO3-和NO2-的比还原速率分别为16.28mg/(gVSS·h)和17.51mg/(gVSS·h).酸性条件产生的发酵液做碳源时NO2-还原过程较NO3-还原过程快;而碱性条件产生的发酵液做碳源时NO3-还原速率高,且产生了反硝化过程中亚硝酸盐积累现象,其中pH=10.0产生的发酵液做碳源时反硝化过程亚硝积累率高达82.5%.
污泥发酵液;反硝化;碳源;碳氮比
生物脱氮技术被污水处理厂广泛采用[1-4],而生物脱氮往往需要充足的碳源,目前我国大多数污水处理厂存在碳源不足的问题[5-6].甲醇是近年来常被污水处理厂采用的反硝化碳源,但是甲醇价格昂贵,其投资费用占污水处理厂操作和维护费用的70%以上[7].因此,经济且高效的碳源开发成为研究的热点[8-12].
污泥厌氧发酵可使污泥减量,溶出的挥发性脂肪酸(VFAs)可以作为生物脱氮过程中一种既经济又高效的碳源代替甲醇[13].一些研究者将污泥厌氧发酵液加入到生物强化除磷工艺[14]、生物脱氮工艺[4]、反硝化除磷工艺[15]等,发现利用污泥发酵液做脱氮除磷碳源有利于实现短程硝化反硝化[16],同时氮磷去除效率高于普通碳源[4,14].在氮氧化物(NOx--N)还原过程中,反硝化菌可利用的碳源种类较多,黄惠珺等[17]发现碳源不同活性污泥储存的内碳源不同.因此,反硝化速率与碳源类型密切相关.而厌氧发酵产酸过程可以在pH值为3.0~12.0进行,且不同的pH值条件产生的酸化产物种类和含量不同[18-19].因此,利用不同的pH值条件产生的污泥发酵液做反硝化碳源,对反硝化过程的影响差别较大.
剩余污泥厌氧发酵过程中产甲烷菌适宜生长的pH值为7.0±0.5,在此pH值范围内污泥厌氧发酵过程为产甲烷型过程,产酸量极低[20].因此,pH=7.0±0.5条件下产生的污泥发酵液不适宜做反硝化碳源.本研究在(35±1)℃条件下,调节不同pH值(4.0, 5.0, 6.0, 8.0, 9.0, 10.0)进行剩余污泥厌氧发酵长期培养,批次试验考察等体积的酸性(pH=4.0, 5.0, 6.0)和碱性(pH=8.0, 9.0, 10.0)条件下产生的剩余污泥发酵液做碳源对反硝化性能的影响,并从发酵液特性来分析讨论其影响效果.通过本研究,对比不同pH值条件下产生的污泥发酵液特性及其做碳源时反硝化性能,可为反硝化替代碳源的选择提供理论支持.
1 材料与方法
1.1 试验污泥
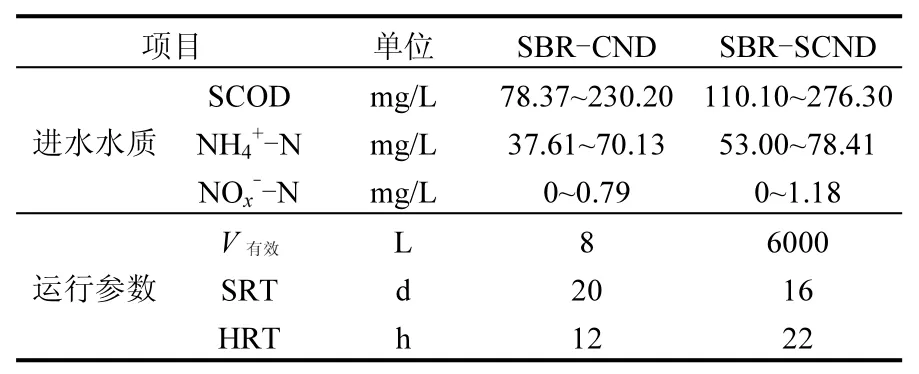
表1 两套生物脱氮反应器水质及运行参数Table 1 Wastewater quality and operating parameter of nitrification systems
根据试验需求,试验污泥分为3类:硝酸盐(NO3-)还原污泥、亚硝酸盐(NO2-)还原污泥和污泥发酵所用的剩余污泥.3类污泥分别取自于北京市某实验室处理实际生活污水的序批式全程硝化反硝化反应器(SBR-CND)的曝气结束污泥、序批式短程硝化反硝化反应器(SBR-SCND)的曝气结束污泥及SBR-SCND的剩余污泥.表1为两套生物脱氮反应器进水水质及运行参数,试验期间运行稳定,平均总氮去除率大于95%;表2为3类试验污泥的基本特征.

表2 试验污泥的基本特征Table 2 Characteristic of sludge used in this study
1.2 污泥发酵液来源
试验装置采用密闭的SBR(图1).将上述实验室SBR-SCND的剩余污泥投加至图1的污泥厌氧发酵系统,分别在酸性(pH=4.0, 5.0, 6.0)和碱性(pH=8.0, 9.0, 10.0)条件下进行连续搅拌中温[(35 ±1)℃]厌氧发酵,调节pH值时采用5mol/L的HCl和1mol/L的NaOH,各系统HRT和SRT均为16d,挥发性悬浮固体(MLVSS)为15g/L左右.运行稳定后,取各系统污泥发酵液上清液做NOx-还原过程碳源,表3反映了试验中所用污泥发酵液的有机物含量和比例.
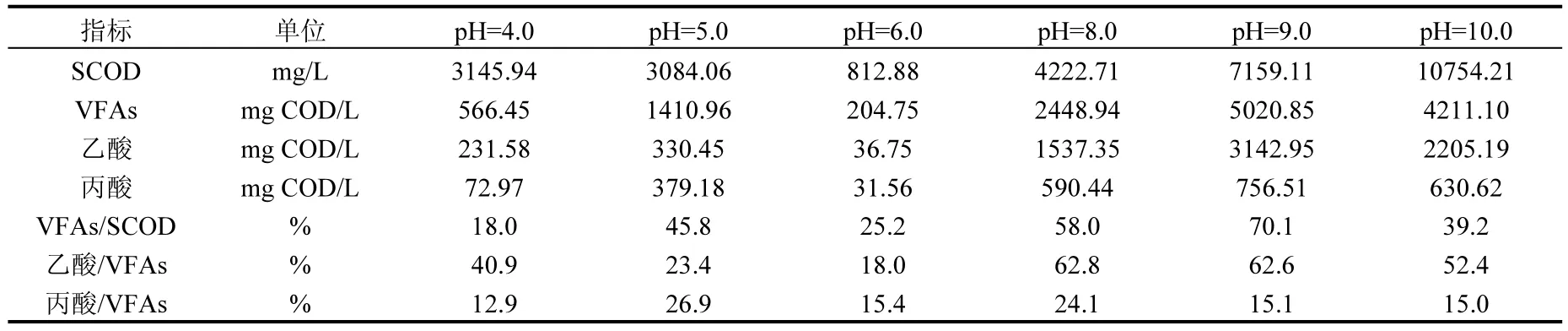
表3 试验中所用不同pH值条件产生的污泥发酵液的有机物含量和比例Table 3 Organic matter content and proportion of sludge fermentation liquid used in this study
1.3 批次试验
将上述实验室的NO3-还原污泥和NO2-还原污泥的混合液分批次接种0.9L到图1试验装置的NOx-还原系统中,混合液以氮气去除其中的溶解氧后分别投加上述pH值为酸性和碱性条件下厌氧发酵产生的污泥发酵上清液0.1L作为碳源.试验过程中不控制pH值,试验温度维持在(25± 0.5)℃,MLSS均控制在2500mg/L左右.每组试验均平行做3次,反应时间为2h.
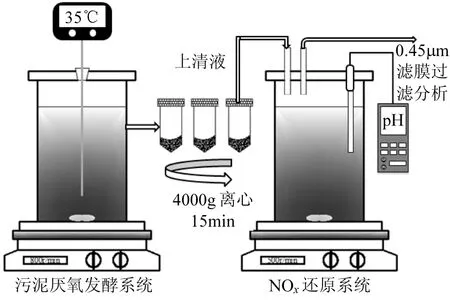
图1 试验装置Fig.1 Schematic diagram of experimental system
1.4 分析项目与方法
试验过程中pH值采用德国WTWpH3310仪在线监测;MLSS和MLVSS采用质量法;试验样品经0.45µm的微孔纤维滤膜过滤后,滤液用于指标分析.SCOD采用5B-3(B)型COD快速测定仪检测;NH4+-N, NOx--N, PO43--P采用流动注射分析仪(Lachat Quik-Chem8500, LachatⅠnstrument, USA)检测;蛋白质采用改良型Bradford法蛋白质浓度测定试剂盒测定(生工SK3041);多糖采用苯酚-硫酸法测定;VFAs采用气相色谱法测定[19].
2 试验结果
2.1 酸性发酵液做碳源对NOx-还原的影响
连续搅拌中温[(35±1)℃]厌氧发酵系统在酸性条件(pH=4.0, 5.0, 6.0)下产生的污泥发酵液做碳源对NOx-还原过程的影响如图2所示.从图2可以看出:不同pH值条件下产生的污泥发酵液做反硝化碳源,NOx-还原速率差异较大.而且在相同反应时间内,不同电子受体对同一发酵液的利用程度也存在差别.

图2 酸性发酵液做碳源NOx-还原情况Fig.2 Reduction of NOx-when used acidic fermentation liquid as carbon source
在NO3-还原过程中[图2(a)],pH=4.0产生的发酵液做碳源时,经过2h的反应NO3--N浓度从20.51mg/L降至10.80mg/L,比NO3-还原速率(SNaRR)为2.08mg/(gVSS·h); pH=5.0产生的发酵液做碳源时,NO3-在1.5h内还原完全,在反应初始0.5h内系统SNaRR为2.38mg/(gVSS·h),同上述pH=4.0时反应速率相当,但在0.5~1.5h内反应速率迅速增加,SNaRR达到7.93mg/(gVSS·h),增加了3.3倍;而在整个反应时间内,pH=6.0产生的发酵液做碳源时,NO3--N浓度仅减少了1.13mg/L.
在NO2-还原过程中[图2(b)],pH=4.0产生的发酵液做碳源时,反应2h时NO2--N浓度降至3.33mg/L,减少了25.13mg/L,比NO2-还原速率(SNiRR)为对应SNaRR的2.5倍;而当pH=5.0产生的发酵液做碳源时,NO2--N浓度成线性减少,SNiRR始终为7.82mg/(gVSS·h),这与NO3-还原过程不同;当pH=6.0产生的发酵液做碳源时,反应2h后NO2--N浓度降低了4.36mg/L,与NO3-还原相比,反应速率提高了70.0%.
研究发现反硝化过程中适宜的pH值范围为6.5~9.0[21].当pH=4.0产生的发酵液做碳源时,各反应初始的pH值在5.25±0.3范围内,反应pH值条件不适宜,尽管有可利用的碳源,NOx-还原速率仍偏低.反应2h后NO3-还原过程pH值仅升高了0.7,NO2-还原过程pH值升高了2.2. NO2-还原需要的碳源明显低于NO3-还原[16],在投加相同碳源时NO2-利用速率高,产生碱度快,迅速达到了反硝化适宜pH值范围,因此pH值为酸性条件下产生的发酵液做碳源时,SNiRR均高于对应的SNaRR;当pH=5.0产生的发酵液做碳源时各反应初始pH值在5.87±0.3范围内,NO3-还原过程初始阶段反应缓慢,随着反应的进行pH值升高到反硝化适宜范围时,系统内仍存在充足的碳源,因此SNaRR快速增加;当pH=6.0时,污泥发酵产酸量降低,乙酸仅有36.75mgCOD/L(表3),这与Emine等[13]研究一致.因此,当pH=6.0产生的发酵液做碳源时,可利用碳源较少,碳源不足导致反应停滞.
2.2 碱性发酵液做碳源对NOx-还原的影响
污泥厌氧发酵过程中产甲烷菌适宜的pH值为6.6~7.5,当pH>8.0时产甲烷菌就会受到抑制,导致产酸增加[20].因此,碱性发酵液产酸量高,是可供选择的替代碳源[4,16].图3为碱性条件产生的污泥发酵液做碳源时NOx-还原情况,而图4具体显示了碱性发酵液做碳源时NO3-还原过程中NOx--N的转化情况.
由图3可知,pH=8.0产生的发酵液做碳源时,NO3-和NO2-还原过程均在45min时反应彻底,反应速率高于其他两组pH值条件产生的发酵液做碳源时的反应速率,分别为16.28mg/(gVSS·h)和17.51mg/(gVSS·h).这是由于pH=8.0产生的发酵液乙酸和丙酸占VFAs的比例高(表3),而研究发现微生物对VFAs利用有一定的偏好,较易利用乙酸,其次为丙酸[7,22];pH=9.0产生的发酵液做碳源时,NO3-还原过程的SNaRR明显高于NO2-还原过程SNiRR,这是因为反应系统中碳源充足,NO2-还原过程碳源消耗速率较快,反应pH值迅速升高,超出了反应的最适范围;而pH=10.0产生的发酵液做碳源时,NO3-和NO2-还原过程系统初始pH值均超出反硝化适宜范围,尽管反应系统中存在大量的可利用碳源,但反应速率仍较低.然而,值得注意的是pH=10.0产生的发酵液做碳源时,NO3-还原过程中,NO3--N浓度降低了13.55mg/L,但从图4可以看出,这部分NO3--N中82.5%转化成了NO2--N.也就是说,当利用pH=10.0产生的污泥发酵液做碳源时,NO3-还原过程实现了反硝化过程的NO2--N积累,亚硝积累率(NAR)达到82.5%.
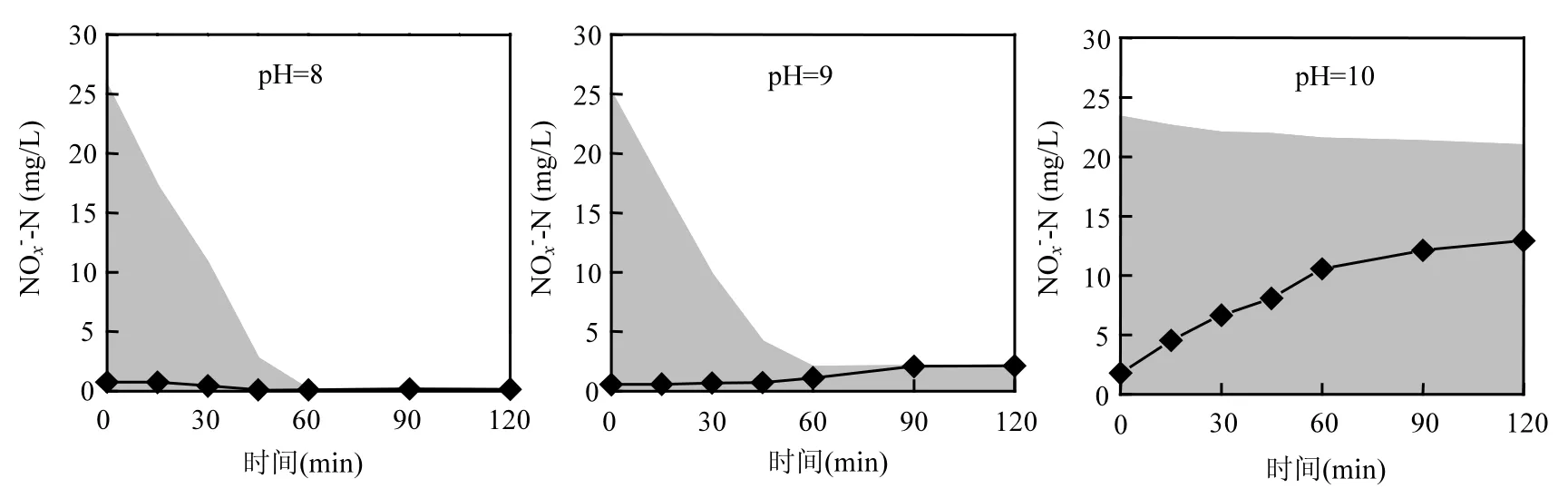
图4 碱性发酵液做碳源时NO3-还原过程中NOx--N转化情况Fig.4 The NOx--N conversion during NO3-reduction process when used alkaline fermentation liquid as carbon source
因此,在反硝化适宜的pH值范围内,利用碱性发酵液做碳源可以完成氮的彻底去除,且反应速率较高,这与大多数文献研究结果一致.Tong等[23]将碱性发酵液投加至生物脱氮系统中,其总氮(TN)去除率由44.0%升高到92.9%.Ji等[16]研究了剩余污泥碱性发酵液做碳源与乙酸做碳源生活污水短程硝化反硝化效果,结果发现反应系统TN去除率分别为97.6%和73.4%.
3 讨论与分析
3.1 不同pH值条件下产生的污泥发酵液特性及其做碳源效果分析
剩余污泥厌氧发酵过程实现污泥减量的同时产生丰富的VFAs,作为碳源可以强化生物脱氮除磷效果[4,11].然而,pH值对污泥厌氧发酵过程产酸量影响较大[13,24],近年来已有一些研究证明碱性发酵产酸量最高[19,23,25].本研究中不同pH值条件剩余污泥中温[(35±1)℃]厌氧发酵产生的发酵液其SCOD各组分含量及C/N如图5所示,其中SCOD各组分包括溶解性碳水化合物(SC),溶解性蛋白质(SP),其他溶解性有机物及VFAs(表3).
从产生有机物角度可以看出,碱性条件发酵溶出的有机物含量远远高于酸性条件溶出的有机物.SP和VFAs均是碱性条件含量远大于酸性条件,SC含量却相差不大;其他溶解性有机物含量则在偏中性时最低,并随着pH值的增大或减小其含量逐渐增大.碱性条件抑制了厌氧发酵过程中产甲烷菌的活性[22,26],从而导致水解产酸效率提高,有机物溶出增加,本研究中在pH=9.0时产酸量达到最高,与Zhang等[27]研究结果一致.从NH4+-N溶出角度可以看出,pH=4.0时溶出量最小,而pH值分别为5.0, 9.0, 10.0时NH4+-N溶出量较大,在560.00mg/L左右波动.因此,不同pH值条件下产生的污泥发酵液SCOD/N差异较大,pH=6.0时最小为2.35,随着pH值的减小和增大SCOD/N均增加,pH=10.0时高达19.22;而生物脱氮易利用有机物VFAs与溶解的NH4+-N之比碱性条件远高于酸性条件,pH=9.0时VFAs/N最大为8.97.

图5 不同pH值条件产生的污泥发酵液性能Fig.5 The performance of sludge fermented liquid produced in different pH conditions
3.2 不同pH值条件产生的污泥发酵液做碳源时反硝化性能
剩余污泥发酵液作为碳源反硝化虽然已经被大量研究[4,14-16,23],但大多数研究仅单一的研究某一种发酵液,尤其是pH=10产生的碱性发酵液.
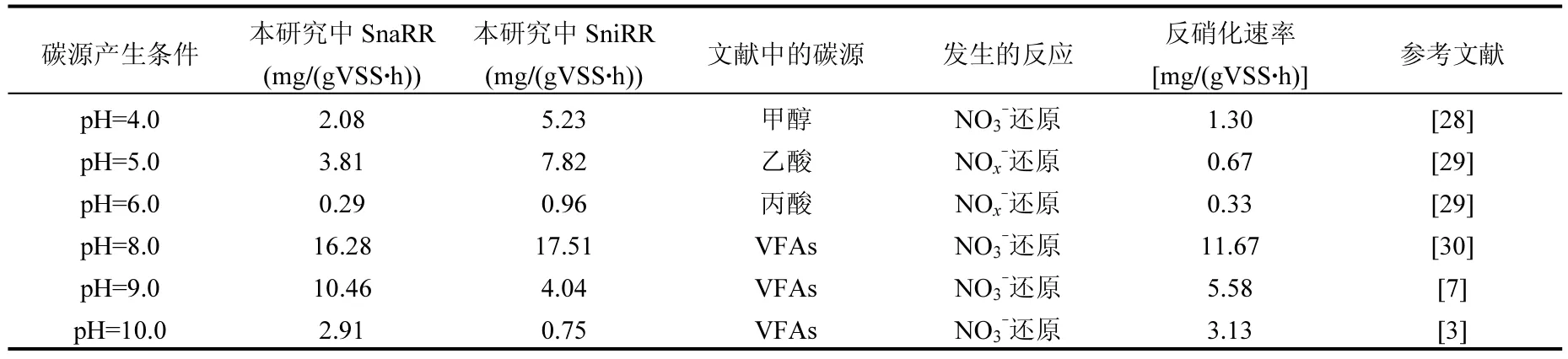
表4 不同pH值条件下产生的污泥发酵液做碳源NOx-还原过程反应速率Table 4 The reaction rate of NOx-reduction process used different sludge fermented liquid as carbon source

图6 不同pH值条件下产生的污泥发酵液做碳源NOx-还原过程碳源消耗速率Fig.6 Carbon consumption rates during NOx-reduction process used different sludge fermented liquid as carbon source
表4将本研究中不同pH值条件下产生的剩余污泥发酵液做碳源反应速率与文献进行了比较,可以发现污泥发酵液是一种高效的可供选择的替代碳源,其做碳源反硝化速率基本上均高于乙酸和甲醇,这与Gao等[25]研究结果相同.而且,等体积的不同类型污泥发酵液做碳源,其反硝化速率差异较大,一方面是由于发酵液pH值不同导致反硝化初始pH值不同,另一方面是由于不同pH值条件发酵过程中产甲烷菌的受抑制程度不同,致使产酸量差异较大[22,26].本研究中,等体积的不同类型污泥发酵液做碳源时,酸性条件下产生的发酵液做碳源其反应速率均低于碱性条件下产生的发酵液做碳源时反应速率;pH=8.0产生的发酵液做碳源时反硝化速率最高,尽管pH值为9.0和10.0时产生的污泥发酵液VFAs含量较高(表3),但是随着反应的进行其pH值超出了反硝化过程的适宜范围,特别是pH=10.0时产生的发酵液做碳源.而且,高pH值产生较高的操作费用和较高的出水pH值,不利于后续处理[24].
研究发现反硝化完成实际需要的COD常常高于理论值的5~10mgCOD/mgN[31],因此在反应适宜的pH值范围内,系统初始的C/N比至关重要.图6表征了不同类型发酵液做碳源NOx-还原过程初始VFAs,C/N及碳源消耗速率(kc),其中C以可快速利用碳源VFAs计.可以看出不同pH值条件下产生的污泥发酵液做碳源,加入等体积的发酵液,反应初始VFAs含量差异较大,反应过程初始VFAs-C/N相差很大,同发酵液本身VFAs含量成正相关.同时,在反硝化适宜pH值范围内,初始VFAs-C/N越高,反应过程kc越大,且NO2-还原过程kc偏高.也就是说,初始碳源含量对反应kc有很大的影响,Elefsiniotis等[3]研究证明在特定的温度下kc与初始碳源含量是存在函数关系的.
3.3 不同pH值条件产生的污泥发酵液做碳源等初始反应pH值时反硝化效率
表5给出了不同pH值条件下产生的剩余污泥发酵液做碳源,将反应初始pH值均调节为7.5时,NOx-还原过程的比反应速率SNaRR和SNiRR.可以看出,当调节NOx-还原反应初始pH值为7.5时,其反应速率与发酵液中的VFAs/N呈正相关(VFAs/N见图5),VFAs/N越高,反应速率越大. pH=9.0产生的发酵液做碳源时,调节反应初始pH值为7.5后,反应SNaRR和SNiRR达到不调节反应初始pH值时反应速率的4.1和10.9倍,而pH=8.0产生的发酵液做碳源时两种情况反应速率却几乎相同.而且,调节反应初始pH值为7.5后,pH=9.0产生的发酵液做碳源反应速率达到pH=8.0产生的发酵液做碳源反应速率的2.5倍.
然而,从表5中不同pH值条件下产生的发酵液做碳源时,NOx-还原反应的初始pH值可以发现,若调节NOx-还原反应初始pH值为7.5,pH=9.0产生的发酵液做碳源时,虽然反应速率增加,但其调节pH值所投加的碱量远高于pH=8.0产生的发酵液做碳源,且其产生发酵液时调节pH值所需碱量也高于pH=8.0,其总投加碱量远超pH= 8.0的总投加碱量.

表5 不同pH值条件下产生的发酵液做碳源时NOx-还原反应初始pH值及等初始pH值时NOx-还原速率Table 5 Beginning pH of NOx-reduction process used sludge fermented liquid produced in different pH conditions as carbon source and NOx-reduction rate of identical beginning pH
4 结论
4.1 在反硝化适宜的pH值范围内,碱性条件下产生的发酵液做碳源时反应速率高于酸性条件下,pH=8.0产生的发酵液做碳源时反应速率最高,SNaRR和SNiRR分别为16.28mg/(gVSS·h)和17.51mg/(gVSS·h).
4.2 酸性条件产生的发酵液做碳源时,NO2-还原系统SNiRR高于对应的NO3-还原系统SNaRR;而碱性条件产生的发酵液做碳源时,NO3-还原系统SNaRR较高,并且可以实现反硝化过程中的NO2--N积累.
4.3 在反硝化适宜的pH值范围内,初始C/N比越高,反应速率越快,反应过程kc越大.
4.4 不同的pH值条件对剩余污泥中温厌氧发酵过程中有机物及NH4+-N的溶出影响较大,其SCOD/N和VFAs/N均是碱性条件远高于酸性条件,pH=9.0时产生的污泥发酵液VFAs/N最大;若调节NOx-还原反应初始pH值为7.5后,当以不同pH值条件产生的发酵液做碳源时,反应速率与发酵液VFAs/N呈正相关.
[1] Francis G S, Trimmer L A, Tregurtha C S, et al. Winter nitrate leaching losses from three land uses in the Pukekohe area of New Zealand [J]. New Zealand Journal of Agricultural Research,2003,46(3):215-224.
[2] Wakida F T, Lerner D N. Non-agricultural sources of groundwater nitrate: A review and case study [J]. Water Research,2005,39(1):3-16.
[3] Elefsiniotis P, Li D. The effect of temperature and carbon source on denitrification using volatile fatty acids [J]. Biochemical Engineering Journal, 2006,28(2):148-155.
[4] Zheng X O, Chen Y G, Liu C C. Waste activated sludge alkaline fermentation liquid as carbon source for biological nutrients removal in anaerobic followed by alternating aerobic-anoxic sequencing batch reactors [J]. Chinese Journal of Chemical Engineering, 2010,18(3):478-485.
[5] 张树军,韩晓宇,张 亮,等.污泥发酵同步消化液旁侧脱氮 [J].中国环境科学, 2011,31(1):19-24.
[6] 邢立群,彭永臻,金宝丹,等.盐度强化剩余污泥碱性发酵产酸[J]. 中国环境科学, 2015,35(6):1771-1779.
[7] Elefsiniotis P, Wareham D G. Utilization patterns of volatile fatty acids in the denitrification reaction [J]. Enzyme and Microbial Technology, 2007,41(1/2):92-97.
[8] Sun S P, Nacher C P Ⅰ, Merkey B, et al. Effective biological nitrogen removal treatment processes for domestic wastewaters with low C/N ratios: A review [J]. Environmental Engineering Science, 2010,27(2):111-126.
[9] Peng Y Z, Ma Y, Wang S Y. Denitrification potential enhancement by addition of external carbon sources in a pre-denitrification process [J]. Journal of Environmental Sciences-China, 2007,19(3):284-289.
[10] 李梦露,蒋建国,张昊巍.餐厨垃圾水解酸化液作碳源的脱氮效果研究 [J]. 中国环境科学, 2014,34(4):917-923.
[11] Kampas P, Parsons S A, Pearce P, et al. Mechanical sludge disintegration for the production of carbon source for biological nutrient removal [J]. Water Research, 2007,41(8):1734-1742.
[12] Elefsiniotis P, Wareham D G, Smith M O. Use of volatile fatty acids from an acid-phase digester for denitrification [J]. Journal of Biotechnology, 2004,114(3):289-297.
[13] Cokgor E U, Oktay S, Tas D O, et al. Ⅰnfluence of pH and temperature on soluble substrate generation with primary sludge fermentation [J]. Bioresource Technology, 2009,100(1):380-386.
[14] Guerrero J, Guisasola A, Baeza J A. The nature of the carbon source rules the competition between PAO and denitrifiers in systems for simultaneous biological nitrogen and phosphorus removal [J]. Water Research, 2011,45(16):4793-4802.
[15] Wang Y Y, Geng J J, Guo G, et al. N2O production in anaerobic/ anoxic denitrifying phosphorus removal process: The effects of carbon sources shock [J]. Chemical Engineering Journal, 2011,172(2/3):999-1007.
[16] Ji Z Y, Chen Y G. Using sludge fermentation liquid to improve wastewater short-cut nitrification-denitrification and denitrifying phosphorus removal via nitrite [J]. Environmental Science & Technology, 2010,44(23):8957-8963.
[17] 黄惠珺,王淑莹,王中玮,等.不同碳源类型对活性污泥PHA贮存及转化的影响 [J]. 化工学报, 2010,161(16):1510-1517.
[18] 任南琪,王爱杰,马 放.产酸发酵微生物生理生态学 [M]. 北京:科学出版社, 2005.
[19] Yu G H, He P J, Shao L M, et al. Toward understanding the mechanism of improving the production of volatile fatty acids from activated sludge at pH 10.0 [J]. Water Research, 2008,42(18):4637-4644..
[20] 胡纪萃.废水厌氧生物处理理论与技术 [M]. 北京:中国建筑工业出版社, 2002.
[21] 杨莎莎,宋英豪,赵宗升,等.pH和碳氮比对亚硝酸型反硝化影响的研究 [J]. 环境工程学报, 2007,12(1):15-19.
[22] Mokhayeri Y, Riffat R, Murthy S, et al. Balancing yield, kinetics and cost for three external carbon sources used for suspended growth post-denitrification [J]. Water Science and Technology,2009,60(10):2485-2491.
[23] Tong J, Chen Y G. Recovery of nitrogen and phosphorus from alkaline fermentation liquid of waste activated sludge and application of the fermentation liquid to promote biological municipal wastewater treatment [J]. Water Research, 2009,43(12):2969-2976.
[24] Ahn Y H, Speece R E. Elutriated acid fermentation of municipal primary sludge [J]. Water Research, 2006,40(11):2210-2220.
[25] Gao Y Q, Peng Y Z, Zhang J Y, et al. Biological sludge reduction and enhanced nutrient removal in a pilot-scale system with 2-step sludge alkaline fermentation and A(2)O process [J]. Bioresource Technology, 2011,102(5):4091-4097.
[26] Wu H Y, Yang D H, Zhou Q, et al. The effect of pH on anaerobic fermentation of primary sludge at room temperature [J]. Journal of Hazardous Materials, 2009,172(1):196-201.
[27] Zhang P, Chen Y G, Zhou Q, et al. Understanding short-chain fatty acids accumulation enhanced in waste activated sludge alkaline fermentation: kinetics and microbiology [J]. Environmental Science & Technology, 2010,44(24):9343-9348.
[28] Hagman M, Nielsen J L, Nielsen P H, et al. Mixed carbon sources for nitrate reduction in activated sludge-identification of bacteria and process activity studies [J]. Water Research, 2008,42(6/7):1539-1546.
[29] Li D. Denitrification using volatile fatty acids (VFAs): The effects of nitrate concentrations, types of VFAs, C/N ratio and temperature [D]. M.E. Thesis, University of Auckland, Auckland,New Zealand, 2001.
[30] Chae S R, Lee S H, Kim J O, et al. Simultaneous removal of organic and strong nitrogen from sewage in a pilot-scale BNR process supplemented with food waste [J]. Water Science and Technology, 2004,49(5/6):257-264.
[31] Bernat K, Wojnowska-Baryla Ⅰ, Dobrzynska A. Denitrification with endogenous carbon source at low C/N and its effect on P(3HB) accumulation [J]. Bioresource Technology, 2008,99(7): 2410-2418.
Effect of different waste activated sludge fermentation supernatants on NOx-reduction process.
HE Yue-lan, WANG Shu-ying*, LI Xi-yao, MA Bin, GUO Si-yu (Engineering Research Center of Beijing, Key Laboratory of Beijing for Water Quality Science and Water Environment Recovery Engineering, Beijing University of Technology, Beijing 100124, PR China). China Environmental Science, 2016,36(10):2964~2971
This research adopted the (35±1)℃ temperature and pH were acidity (pH=4.0, 5.0, 6.0) and alkaline (pH=8.0,9.0, 10.0) conditions to conduct waste activated sludge anaerobic fermentation, using an equal volume of different fermentation liquid as carbon source researched its effect on NOx-reduction process.The results showed that: when the fermentation liquid produced in pH=8.0 condition as carbon source, the highest reaction rate appeared, NO3-and NO2-reduction rate respectively were 16.28mg/(gVSS·h) and 17.51mg/(gVSS·h). The NO2-reduction process was faster than the NO3-reduction process while the fermentation liquid as carbon source produced by acidic condition, but the NO3-reduction rate was higher when the fermentation liquid as carbon source produced by alkaline condition. Meanwhile,which produced the nitrite accumulation phenomenon among the denitrification process, the accumulation rate of nitrite during denitrification process reached 82.5% when the fermentation liquid as carbon source produced in pH=10.0condition.
sludge fermentation liquid;denitrification;carbon source;C/N
X703.1
A
1000-6923(2016)10-2964-08
何岳兰(1990-),女,甘肃庆阳人,主要从事污泥厌氧发酵减量及发酵液利用研究.发表论文1篇.
2016-02-18
住建部2014年科学技术项目计划(2014-k7-022);北京工业大学第13届研究生科技基金项目(ykj-2014-10898)
* 责任作者, 教授, wsy@bjut.edu.cn

