番红花红T检测羟自由基方法的探讨
樊琛++闫雪梅++王会++曾庆华++李燕

摘要:采用全波长分析方法,从12种染料中选出番红花红T检测羟自由基,番红花红T溶液在Fenton试剂体系中,在550~560 nm吸光度变化明显,从而用分光光度法检测Fenton反应产生的羟自由基(·OH)。通过对反应体系FeSO4溶液、H2O2溶液、温度以及时间4个影响条件的单因素试验以及正交试验,得出最佳反应条件为FeSO4溶液1.0 mL、H2O2溶液0.6 mL、温度25 ℃、时间35 min,在此最佳反应条件下,随着抗坏血酸溶液浓度的增大,羟自由基的清除率增大,得出所选最佳反应条件适合进行检测羟自由基试验。验证试验证明,乙醇溶液对Fenton体系有明显清除羟自由基的作用,抗氧化性能良好,溶度较小时抗氧化性能仍然很好;番红花红T检测羟自由基的体系在酸性环境pH 2~6.4范围内稳定。
关键词:番红花红T;Fenton反应;羟自由基
中图分类号:S567.23+9;R927.1 文献标识码:A 文章编号:0439-8114(2017)01-0132-05
DOI:10.14088/j.cnki.issn0439-8114.2017.01.034
Study on Detection of Hydroxyl Free Radical by Safranine T Method
FAN Chen, YAN Xue-mei, WANG Hui, ZENG Qing-hua, LI Yan, SUN Xiao-fan, ZHENG Huan-qin
(Agricultural College of Liaocheng University, Liaocheng 252059,Shandong,China)
Abstract:Through the full wave analysis method,the Safranine T from 12 kinds of dye were selected for the detection of hydroxyl free radical,in the Fenton reagent system,the absorbance of safranine T solution changed apparently between 550~560 nm,then using spectrophotometry to detect hydroxyl free radical(·OH) produced by Fenton reaction.By single factor experiment and orthogonal test,4 influence factors in reaction system as FeSO4 solution,H2O2 solution,temperature and time were obtained, the optimum reaction conditions were FeSO4 solution 1.0 mL,H2O2 solution 0.6 mL,temperature 25 ℃,time 35 min,i.e. the best combination was A1B2C2D2. Under the optimum reaction conditions,with the increase of concentration of ascorbic acid, the scavenging rate of hydroxyl free radical increased,it concluded that the optimum reaction conditions were suitable for test detection of hydroxyl free radical. The verification experiment showed that,ethanol solution had obvious scavenging effect on Fenton system,with excellent oxidation resistance even in low solubility. The detection system of hydroxyl free radical by safranine T was stable at pH 2~6.4 in the acidic environment.
羟自由基可造成生物组织脂质过氧化、核酸断裂、蛋白质和多糖分解。羟自由基的反应活性大,寿命短,存在浓度低,所以在有关羟自由基的研究中,其分析检验方法对于羟自由基的作用研究有重要的意义,特别是在测定及筛选抗羟自由基物质方面具有重要价值[1,2]。近年来国内外文献报道了检测羟自由基的一些重要方法,有电子自旋共振法、高效液相色谱法、化学发光法、荧光法、分光光度法等。电子自旋共振法和高效液相色谱法操作复杂,仪器昂贵;化学发光法虽然操作简便,测定快速,但仪器普及不广[3-9]。
本试验采用番红花红T作为显色剂,用分光光度法测定Fenton反应产生的·OH,具有操作简便,费用低,易于广泛使用的优点。
1 材料與方法
1.1 材料与试剂
番红花红T,甲基橙,次甲基兰,溴酚蓝,甲基红,铬黑T,溴甲酚紫,溴百里香酚蓝,靛红,结晶紫,甲基蓝,考马斯亮蓝,硫酸亚铁,30%的过氧化氢溶液,无水乙醇,氢氧化钠,蒸馏水。
1.2 仪器与设备
UV-1700型全波长自动分光光度仪(日本岛津公司);UV-1800型紫外分光光度仪(上海美谱达仪器有限公司);SB-2000型水浴锅(上海爱朗仪器有限公司);T-214型电子天平(北京赛多利斯仪器系统有限公司)。
1.3 方法
1.3.1 染料筛选 准确称取固体染料,加入溶剂20.0 mL溶解,摇匀,待用。取4支比色管,分别标号①、②、③和空白,放入30 ℃水浴中,恒温30 min后,取出。①号管中加入FeSO4溶液(浓度0.18 mmoL/L[10],以下均使用该浓度溶液)2.0 mL,染料溶液2.0 mL,H2O2溶液(浓度0.3%,以下均使用该浓度溶液)2.0 mL,蒸馏水补足体积至8.0 mL,其中H2O2溶液最后加入;②号管中加入FeSO4溶液2.0 mL,染料溶液2.0 mL,蒸馏水补足体积至8.0 mL;③号管中加入染料溶液2.0 mL,调节pH溶液(与该硫酸亚铁溶液的pH一致)2.0 mL,H2O2溶液2.0 mL,蒸馏水补足体积至8.0 mL,其中H2O2溶液最后加入;空白管中加入染料溶液2.0 mL,蒸馏水补足体积至8.0 mL。
观察4支比色管的颜色变化,使用全波长分光光度仪逐一测定各比色管的全波长图谱,比较各波段的图谱[11-13],筛选适合的染料。
1.3.2 单因素试验[14]
1)FeSO4溶液用量。分别加入FeSO4溶液0、0.5、1.0、1.5、2.0、3.0、4.0、5.0 mL[15,16],番红花红T溶液1.0 mL,H2O2溶液2.0 mL,蒸馏水补足体积至8.0 mL;空白对照为番红花红T溶液1.0 mL,蒸馏水补足体积至8.0 mL。放入30 ℃水浴中30 min后取出,于554 nm处测定吸光度。以吸光度变化△A判定羟自由基的含量,计算公式如下:
△A=A0-A1
式中,A0为空白对照吸光度;A1为试验组吸光度。
2)H2O2溶液用量。分别加入H2O2溶液的量0、0.5、1.0、1.5、2.0、2.5、3.0、4.0、5.0 mL[15],番红花红T溶液1.0 mL,FeSO4溶液1.0 mL,蒸馏水补足体积至8.0 mL;空白对照为番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。放入30 ℃水浴中30 min后取出,于554 nm处测定吸光度。以吸光度变化△A判定羟自由基的含量,计算公式如下:
△A=A0-A1
式中,A0为空白对照吸光度;A1为试验组吸光度。
3)温度。分别加入FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液2.0 mL,蒸馏水补足体积至8.0 mL;空白对照组为番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。水浴温度分别为2、10、15、20、25、30、35、40 ℃,恒温30 min后,取出,于554 nm处测定吸光度。以吸光度变化△A判定羟自由基的含量,计算公式如下:
△A=A0-A1
式中,A0为空白对照组吸光度;A1为试验组吸光度。
4)时间。分别加入FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液2.0 mL,蒸馏水补足体积至8.0 mL;空白对照组为番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。放入25 ℃水浴中,恒温时間分别为0、5、10、15、20、25、30、35、40、45、50 min后取出,于554 nm测定吸光度。以吸光度变化△A判定羟自由基的含量。计算公式如下:
△A=A0-A1
式中,A0为空白对照组吸光度;A1为试验组吸光度。
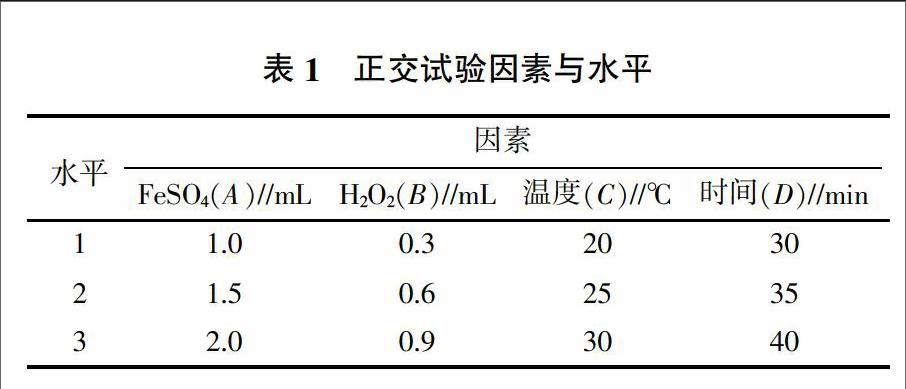
1.3.3 正交试验 通过单因素试验,确定各个影响因素的优化范围,进行正交试验,采用四因素三水平的正交试验,选取的因素分别为FeSO4溶液、H2O2溶液、水浴温度、反应时间。
1.3.4 验证试验 根据正交试验结果,FeSO4溶液的量、H2O2溶液的量、水浴温度和反应时间均按照正交试验,选择最优体系方案,进行验证试验。
1)乙醇的影响。分别加入30%、10%、5%、1%、0%的乙醇溶液1.0 mL,FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液0.6 mL,蒸馏水补足体积至8.0 mL;空白对照组分别加入30%、10%、5%、1%、0%的乙醇溶液1.0 mL,番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。放入25 ℃水浴中,恒温35 min后,取出,于空白对照组测定波长处测定吸光度,计算公式如下:
△A=A0-A1
式中,A0为空白对照组吸光度;A1为试验组吸光度。
2)pH的影响。分别加入pH调节溶液2.0 mL,FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液0.6 mL,蒸馏水补足体积至8.0 mL;空白对照组分别加入pH调节溶液2.0 mL,番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。放入25 ℃水浴中,恒温35 min后,取出,于空白对照组测定波长处测定吸光度。以吸光度变化△A判定反应体系适宜的酸碱范围,计算公式如下:
△A=A0-A1
式中,A0为空白对照组吸光度;A1为试验组吸光度。
3)抗坏血酸清除羟自由基的作用。分别加入5×10-1、1×10-1、5×10-2、1×10-2、1×10-3 mmoL/mL的抗坏血酸溶液2.0 mL,FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液0.6 mL,蒸馏水补足体积至8.0 mL;空白试验为FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液0.6 mL,蒸馏水补足体积至8.0 mL;空白对照为番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。放入25 ℃水浴中,恒温35 min后,取出,于554 nm测定吸光度,计算出羟自由基清除率D[17]。以羟自由基清除率D判定抗坏血酸溶液的抗氧化能力。羟自由基清除率计算公式如下:
D=[(A2-A1)/(A0-A1)]×100%
式中,A0为空白对照吸光度;A1为空白试验吸光度;A2为试验组吸光度。
2 结果与分析
2.1 染料筛选试验结果
根据对各种染料的全波长图谱的分析,番红花红T的4支比色管得出的图谱相比较,Fenton反应体系在300~350 nm间吸光度明显升高,在560 nm左右处吸光度明显降低;与FeSO4溶液、H2O2溶液单独使用时,无明显变化。其他染料不受羟自由基影响或与FeSO4溶液、H2O2溶液单独使用时发生变化(图1)。如图1所示,番红花红T-·OH反应体系吸光度在550~560 nm明显降低,经检测波峰处为554 nm。选择番红花红T染料做单因素试验。
2.2 单因素试验结果
2.2.1 FeSO4溶液用量分析 各试验组出现明显的颜色变化,随着FeSO4溶液加入量的增加,△A急剧上升,FeSO4溶液1.0 mL时△A达到最高,随后,FeSO4溶液1.5~5.0 mL,△A缓慢减小,即△A随FeSO4溶液加入量增加先增大后减小(图2)。故选择FeSO4溶液的量为1.0 mL进行以下试验。
2.2.2 H2O2溶液用量分析 各试验组出现明显的颜色变化,随着H2O2溶液加入量的增加,各试验组颜色变浅,由粉红色变为浅黄色至无色。H2O2溶液加入量0~0.5 mL时,△A急剧上升;随着H2O2溶液加入量的增加,在0.5~5.0 mL,△A随H2O2溶液加入量增加变化不明显(图3)。H2O2溶液加入量2.0 mL时,反应体系在554 nm处△A较稳定,选择H2O2溶液的量为2.0 mL进行以下试验。
2.2.3 温度对反应体系的影响 随着水浴温度的增加,各管颜色逐渐变浅,由浅橙黄色变为浅黄色;空白管呈粉红色。温度为2~25 ℃,△A上升明显;在温度25 ℃时,△A达到峰值,随后下降。即△A随水浴温度增加先增大后减小(图4)。故选择温度为25 ℃进行以下试验。
2.2.4 时间对反应体系的影响 随着反应时间的增加,颜色由浅橙黄色变为浅黄色;反应时间0~5 min,△A几乎不变;5~35 min,△A逐渐上升;35~50 min,△A变化不显著,即△A随时间增加先增大,而后基本持平(图5)。故选择反应时间为35 min。
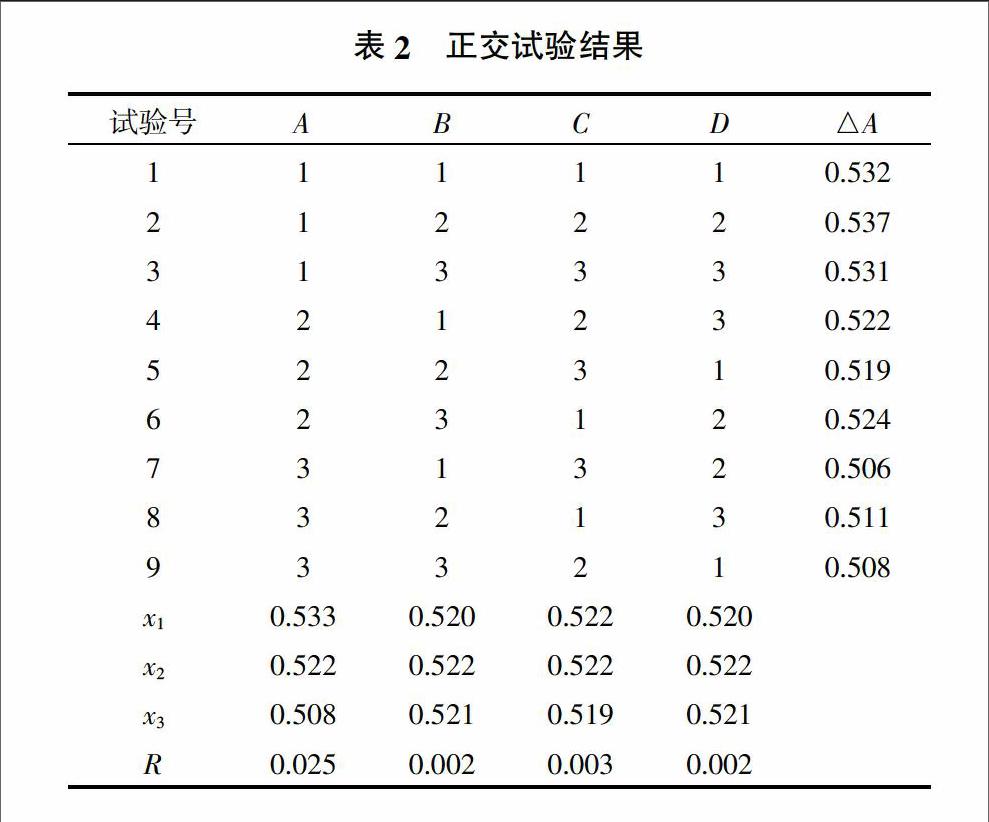
2.3 正交试验结果
根据表1正交试验设计,对试验进行测定,试验组与空白组番红花红T溶液均为1.0 mL,结果见表2。由表2可见,各因素影响由大到小为FeSO4溶液、温度、H2O2溶液、时间;最主要的影响因素为FeSO4溶液,其余3个因素在既定的水平下影响较小。最佳组合为A1B2C2D2即FeSO4 1.0 mL、H2O2 0.6 mL、温度25 ℃、时间35 min。
2.4 验证试验结果
选用A1B2C2D2组合,即FeSO4溶液的量为1.0 mL,H2O2溶液的量为0.6 mL,水浴温度为25 ℃,保温时间为35 min,番红花红T溶液的加入量为1.0 mL,△A=0.539。
2.4.1 乙醇的影响 分别加入30%、10%、5%、1%的乙醇溶液1.0 mL,FeSO4溶液1.0 mL,番红花红T溶液1.0 mL,H2O2溶液0.6 mL,蒸馏水补足体积至8.0 mL;对照组分别加入30%、10%、5%、1%的乙醇溶液1.0 mL,番红花红T溶液的量1.0 mL,蒸餾水补足体积至8.0 mL。放入25 ℃水浴中,恒温35 min。结果显示,番红花红T检测羟自由基的体系中,加入不同体积分数的乙醇溶液,峰值处波长不变,为554 nm。对照组颜色均呈现粉红色,试验组中呈现橙红色。于554 nm处测定吸光度,△A随乙醇体积分数的减小而增大(表3)。由表3可见,乙醇对Fenton体系影响较大,即使少量乙醇也可对Fenton体系的产生明显影响。乙醇与番红花红T混合颜色为粉红色,试验组中呈现橙红色,推测乙醇具有清除/阻碍羟自由基的能力或阻碍自由基与番红花红T反应的能力。因此,相关试验中应注意避免混入含有乙醇的物质。
2.4.2 pH的影响 pH调节溶液2.0 mL,FeS04溶液1.0 mL,番红花红溶液1.0 mL,H202溶液0.6 mL,蒸馏水补足体积至8.0 mL;空白对照组分别加入pH调节溶液2.0 mL,番红花红T溶液的量1.0 mL,蒸馏水补足体积至8.0 mL。放入25 ℃水浴中,恒温35 min。结果显示,在碱性环境下,有沉淀生成;在酸性环境下,不同pH溶液各管颜色相近,均为淡黄;空白对照组均为粉红色(表4)。由表4可见,番红花红T检测羟自由基的体系在酸性环境pH 2~6.4保持稳定。
2.4.3 抗坏血酸清除羟自由基的作用 在番红花红T检测羟自由基的体系中,加入不同浓度的抗坏血酸溶液后,各试验管颜色变化明显(表5)。由表5可见,随抗坏血酸溶液浓度增大,羟自由基的清除率增大,抗坏血酸溶液的浓度较低时,有助氧化作用。表明,此番红花红T检测羟自由基的体系适合抗氧化物质清除羟自由基能力的检测。
3 结论
反应体系中最主要的影响因素为FeSO4溶液,最佳组合为FeSO4溶液1.0 mL、H2O2溶液0.6 mL、温度25 ℃、反应时间35 min,测定波长为554 nm。
乙醇溶液对此反应体系影响较大,此反应体系适于检测水浸提物或去除乙醇后再进行检测;体系在酸性环境pH 2~6.4稳定,碱性浸提物不适合该反应体系。
参考文献:
[1] 韩鹤友,何治柯,曾云鹗.羟自由基的分析研究进展[J].分析科学学报,2001,17(1):84-86.
[2] 王仕良,张 曾,黄干强.羟基自由基的产生与测定[J].造纸科学与技术,2003,22(6):45-47.
[3] 高迎新,张 昱,杨 敏,等.Fe3+或Fe2+均相催化H2O2生成羟基自由基的规律[J].环境科学,2006,27(2):305-309.
[4] STOKES N J,TABNER B J,HEWITT C N. Determination of hydroxyl radical concentration in environmental chambers using electron spin resonance[J].Chemosphere,1994,28(5):999-1008.
[5] STEINER M G,BABBS C F. Quantitation of the hydroxyl radical by reaction with dimethyl sulfoxide[J].Arch Biochem Biophys,1990,278(2):478-481.
[6] 徐向荣,王文华,李华斌.比色法测定Fenton反应产生的羟自由基及其应用[J].生物化学与生物物理进展,1999,26(1):67-69.
[7] 朱琳娜,何争光,吴 超.NR光度法测定Fenton试剂所生成的羟基自由基[J].福建分析测试,2006,15(3):10-12.
[8] 方光荣,刘 洁,刘丽虹.分光光度法测定中药对羟自由基的清除率[J].湖北大学学报(自然科学版),2004,26(2):151-154.
[9] 刘立明,刘丽虹,宋功武,等.分光光度法测定Fenton反应产生的羟自由基[J].湖北大学学报(自然科学版),2002,24(4):326-328.
[10] 颜 军,苟小军,邹全付,等.分光光度法测定Fenton反应产生的羟基自由基[J].成都大学学报(自然科学版),2009,28(2):91-93.
[11] 王金刚,王西奎,国伟林,等.亚甲蓝光度法测定羟自由基[J].理化检验:化学分册,2007,43(6):495-497.
[12] 王祥洪,杨季冬,刘江涛.番红花红分光光度法测定硫酸皮肤素[J].化学试剂,2008,30(11):853-855.
[13] 张爱梅,李林尉,宁晓东,等.番红花红O-Mn2+-H2O2光度法測定茶叶的抗氧化性[J].分析科学学报,2006,22(1):90-92.
[14] 管荷兰,王永顺,林国华.水杨酸在羟基自由基检测中的应用[J].理化检验:化学分册,2010,46(3):333-335.
[15] 李铭芳,王慧琴,李淑芳,等.亚甲基蓝光度法检测Fenton试剂所生成的羟自由基[J].江西农业大学学报,2003,25(5):794-796.
[16] 刘 骏.结晶紫分光光度法测定Fenton反应产生的羟自由基[J].武汉工业学院学报,2005,24(2):53-55.
[17] 焦士蓉,郑贵菊.柚皮黄酮类物质的微波辅助提取及其抗氧化活性研究[J].科学研发,2007,23(1):73-75.
Key words: safranine T; Fenton reaction; hydroxyl free radical

