锂离子电池用三维氧化锡/石墨烯水凝胶负极材料
白雪君 侯 敏 刘 婵 王 彪 曹 辉,3 王 东,3
(1上海航天电源技术有限责任公司,上海 201615;2东华大学材料科学与工程学院,上海 201620;3上海空间电源研究所,上海 200245)
锂离子电池用三维氧化锡/石墨烯水凝胶负极材料
白雪君1,*侯 敏1刘 婵1王 彪2曹 辉1,3王 东1,3
(1上海航天电源技术有限责任公司,上海 201615;2东华大学材料科学与工程学院,上海 201620;3上海空间电源研究所,上海 200245)
通过溶液水解反应在氧化石墨烯表面引入氧化锡(SnO2)纳米颗粒,再经过自组装作用形成具有三维结构的氧化锡/石墨烯水凝胶(SnO2-GH)负极材料。其中三维多孔的石墨烯水凝胶为碳质缓冲基体,SnO2纳米颗粒为活性物质,其颗粒尺寸为 2-3 nm,均匀分布在石墨烯层上,担载量可以达到 54%(w,质量分数)。直接将该材料用作锂离子电池负极时,在 5000 mA·g-1的大电流密度下循环 60 次容量稳定在 500 mAh·g-1,电流减小到 50 mA·g-1循环 80 次后容量仍高达 865 mAh·g-1。这些优异的循环稳定性和大电流充放电性能主要得益于三维石墨烯水凝胶的疏松、多孔结构和良好的导电性。石墨烯水凝胶能够提高电极比表面积,保证电解液对电极的浸润程度;内部空隙能够为锂离子的传输提供快速通道,缩短离子传输距离和时间。同时丰富的内部空间能够有效避免SnO2纳米颗粒团聚,缓冲SnO2巨大体积膨胀,维持电极结构的稳定性,是一种非常适于大电流充放电的锂离子电池负极材料。
石墨烯水凝胶;氧化锡;锂离子电池;负极;三维
1 引言
锂离子电池由于具有比能量高、应用温度范围宽、自放电率低、循环寿命长、环境友好等优势,自成功开发以来,其应用范围越来越广泛1-4。商业化锂离子电池负极一般为石墨类材料。虽然碳材料作为锂离子二次电池负极具有较好的循环性能,但已基本达到其理论极限容量(石墨理论比容量为 372 mAh·g-1)5,6,限制了石墨类负极材料在高能量密度化学电源中的应用。另外石墨电极的性能容易受制备工艺的影响,这也直接制约了锂离子电池的进一步发展7。
氧化锡作为锂离子电池的负极材料有比容量高(781 mAh·g-1)、安全性好的优势,受到了研究人员的广泛关注8,9。但是氧化锡与锂发生反应时会产生巨大的体积膨胀(~200%),造成电极粉化甚至脱落,电接触变差而失效,导致电池循环性能迅速下降10。针对这个问题,研究者提出了两种解决方法:一是制备具有特殊结构的氧化锡材料,如纳 米 颗 粒11,12、 纳 米 管13、 纳 米 线14、 介 孔 结 构15、中空微球等16-18;二是将纳米氧化锡嵌入具有缓冲作用的基体材料中,如石墨烯19,20、无定形碳21、碳纳米管22、过渡金属等23-25。其中石墨烯具有良好的导电性和柔韧性,丰富的微/介孔结构,能够有效缓冲氧化锡的体积膨胀效应26。在传统二维石墨烯膜的基础上,将二维结构转变为三维的多孔石墨烯材料,可以有效地阻止石墨烯层的堆叠,提高材料比表面积以及离子的快速传输通道。目前MoS2/GH、 Fe2O3/GH、 TiO2/GH、 Si/GH 等 三 维 电极材料已经成功制备,并最终用在锂离子电池中27-30。
本文通过水解反应在氧化石墨烯表面均匀沉积 SnO2纳米颗粒,然后以抗坏血酸(VC)为还原剂和交联剂,以一种温和的方式低温制备氧化锡/石墨烯水凝胶(SnO2-GH)复合材料,并将此复合物直接用于锂离子电池自支撑负极材料。希望通过这种三维多孔结构能够有效提高负极材料的比表面积、保证电解液的浸润性、提供丰富的电子和离子传输路径、有效缓解SnO2体积膨胀等。
2 实验部分
2.1 石墨烯水凝胶的制备
采 用 改 性 Hummers 法31制 备 氧 化 石 墨 烯(GO),得到浓度为 0.5%(w)的 GO 水溶液。将一定量的抗坏血酸(99%,Sigma Aldrich)加入 5 mL 上述GO水溶液中,超声分散使VC完全溶解。将反应液置于 10 mL 密封玻璃瓶中,加热至 80 °C 静置反应一段时间后得到黑色块状水凝胶。多次水洗去除水凝胶内部残余杂质,再冷冻干燥得到石墨烯水凝胶(GH),具体实验参数如表1所示。
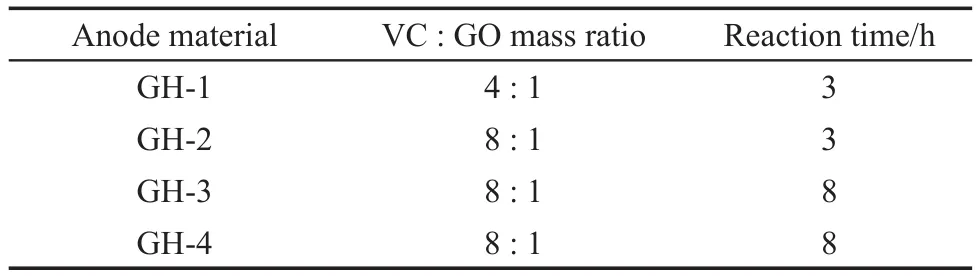
表1 水相体系中制备石墨烯水凝胶(GH)的实验参数Table 1 Experiment parameters of graphene hydrogel (GH)in aqueous solution

表2 水相体系中制备SnO2-GH 负极材料的实验参数Table 2 Experiment parameters of SnO2-GH anode materials in aqueous solution
2.2 氧化锡/石墨烯水凝胶的制备
为了 在 GH 中 引 入 氧 化 锡 颗 粒 , 将 18 mL 的SnCl4水溶液(SnCl4,99.995%,Sigma Aldrich)缓慢加入到 2 mL 上述 GO 水溶液中(0.5%(w)),超声分散均匀。在强烈搅拌下,以 30 mL·h-1的速率缓慢滴加 NaOH 水溶液(11.4 mmol·L-1),具体反应物加入量如表 2所示。强烈搅拌反应 2 h 后,将反应液进行离心分离得到棕色沉淀物,并多次水洗直至中性。然后加入 2 mL 去离子水和 80 mg VC,超声分散直至 VC 溶解。将此反应液至于 10 mL 密封玻璃瓶中,加热至 80 °C 静置反应 24 h 后得到黑色块状水凝胶。然后多次水洗去除水凝胶内部残余杂质,再冷冻干燥得到氧化锡/石墨烯水凝胶。制备过程中材料结构变化示意图见图1。

图1 SnO2-GH负极材料制备过程中结构变化流程图Fig.1 Schematic illustration of structure change in the process of preparation of SnO2-GH anode materials
2.3 性能测试
采 用 X 射 线 衍 射 仪 (XRD, Rigaku D/max 2550V,Cu-Kα,λ=0.154056 nm,日本)对材料物相 进 行 分 析 。 采 用 拉 曼 光 谱 仪 (Raman, Horiba T64000,λ=514.5 nm,日本)和 X 射线光电子能谱(XPS, Thermo Scientific ESCALAB 250Xi, Al Kα,1486.6e,美国)对材料的组分进行分析。利用热重分析仪(TGA,Netzsh TG 209 F1,德国)对样品 的 组 分 含 量 进 行 分 析 , 空 气 气 氛 (20 mL · min-1), 升温速率为 15 °C·min-1,温度 范围 25-800 °C。 采 用 场 发 射 扫 描 电 镜 (FESEM, Hitachi SU8030,日本)对材料表面形貌进行观察,同时利用附件能量色散谱(EDS)对样品表面成分进行分析。电池循环测试之后的电极在氩气气氛手套箱中用碳酸二甲酯冲洗干净并自然干燥后再进行FESEM 测 试 。 采 用 透 射 电 镜 (TEM, JEOL JEM-2100F,日本)对样品微观结构进行研究。将少量样品分散在乙醇溶液中,超声分散 10 min,然后滴加在TEM铜网上,常温干燥。
负极材料的电化学性质通过组装成CR2032型扣式半电池进行测试。将制备得到的负极材料直接裁剪成直径为 5 mm,厚度 2 mm 的圆片作为工作电极,锂片为对电极,Celgard2400 为隔膜,碳酸乙烯酯/碳酸二甲酯(EC/DMC,1:1(V/V))-LiPF6(1 mol·L-1)为 电 解 液 (BASF Corporation, 德 国)进行组装。整个组装过程是在氩气气氛手套箱中进行,其中水、氧含量均在 10 × 10-6g·mL-1以下。采用电池测试系统(Arbin BT2000,美国)对电池的循环充放电容量、稳定性等进行测试。测试电压为 2.0-0.01 V(vs Li/Li+),测试时活性物质质量为SnO2-GH 材料的质量。采用电化学工作站(Autolab PGSTAT128N,瑞士)对电池循环伏安曲线(CV)和电化学交流阻抗谱(EIS)进行测试。CV 测试电压为2.0-0.01 V(vs Li/Li+), 电 压 扫 描 速 率 为 0.1 mV· s-1。EIS 测试电压为 0.6 V,电压幅度为 10 mV,频率为106-10-2Hz。

图2 水相溶液中不同合成条件下制备的GH的X射线光电子能谱(XPS)高分辩 C 1s谱图Fig.2 X-ray photoelectron spectroscopy(XPS)high resolution C 1s spectra of GH with different experiment parameters in aqueous solution
3 结果与讨论
本文通过改变加入还原剂VC的量以及反应时间,以求能够得到一种还原程度高、结构稳定的 GH 制备方法。制备过程中发现 GH-1、GH-2、GH-3、GH-4四个样品均由棕色的液体变成黑色凝胶状固体,表明GO已经被部分还原。采用XPS对四种GH中的碳/氧比和碳元素存在形式进行进一步研究,分析GO被还原的程度。如图2所示,四种 GH 的 C 峰可被分成三个:284.7、286.3、288.2 eV,分别对应于C―C、O―C―O/C―O、C=O三种基团。随着VC加入量的增加和反应时间的延长,GH中的C―C峰强度逐渐增强,且O元素含量逐渐降低。说明在恒定反应温度下(80 °C),GH的还原程度随着上述两个反应条件的增加而增加。
由GH-1、GH-2、GH-3、GH-4的 FESEM 图像(图 3)可知,提高还原剂用量、延长反应时间并没有对GH的微观结构产生明显的影响。GH中的石墨烯呈现立体三维结构,层与层之间没有形成紧密堆垛。材料内部有均匀、丰富、相互贯穿的微孔结构,微孔尺寸为 2-10 μm。石墨烯层出现褶皱、扭曲,这样的结构更有利于其他物质稳定附着 。 图 3(c)内 图 显 示 GH 能够 承受 一定 的 外 力 作用,具有一定的抗压能力,在作为负极材料时,有利于维持电极微观结构的稳定性。综合考虑不同条件下制备的GH的还原程度及微观结构,本文采用GH-4作为锂离子电池负极材料的碳质基体。

图3 水溶液中不同合成条件下制备的 GH 的场发射扫描电镜(FESEM)照片Fig.3 Field emission scanning electron microscopy(FESEM)images of GH with different experiment parameters in aqueous solution

图4 SnO2-GH-1 和 GH-4 负极材料的(a)X射线衍射(XRD)图和(b)拉曼图谱Fig.4 (a)X-ray diffraction(XRD)patterns and(b)Raman spectra of SnO2-GH-1 and GH-4 anode materials
经 过 SnCl4水 解 反 应 、GO 还 原 、 成 型 过 程后,成功的在GH中引入不同含量的锡元素。图4 (a)为 SnO2-GH-1 负 极 材 料 的 XRD 图,图中 SnO2-GH-1 的特征峰与四方晶型的 SnO2(JCPDS No.41-1445)标准卡片的峰对应。且在 25°左右的宽峰与GH-4的峰对应,说明该方法能够把GO有效还原成石墨烯。图 4(b)中,SnO2-GH-1 的 D、G 两峰强度相当,且与 GH-4 的曲线类似,说明在SnO2-GH-1中有序石墨化结构和无序碳结构的含量相当,SnO2颗粒的引入并没有对石墨烯的还原产生影响 。 图 中 400-800 cm-1处 的 小 峰 是 由 SnO2引 起的。通过 XPS 测试可 以进一步研究 SnO2-GH 负极材料中的元素组成及价态。如图 5(a)所示,该负极材料主要包含Sn、C、O三种元素,没有其他杂质的存在。从图 5(b)高分辨 C 1s谱图中可以看出,该负极材料的碳峰可被分为三个峰:284.7、286.3、288.2 eV, 它 们 分 别 对 应 C―C、 O―C―O/C―O/ C―N、C=O三种基团。C―C基团对应的峰强度最高,为主峰,另外两个峰的强度明显较弱。说明经过VC还原后,GO中绝大部分含氧基团消失,达到很高的还原程度。图 5(c)为高分辨 Sn 3d谱 图 , 曲 线 可 被 分 为 两 个 特 征 峰 (495.8 和 487.3 eV),分 别 对应 SnO2的 3d3/2峰和 3d5/2峰 , 且两 峰之间的位置差为 8.5 eV。

图5 SnO2-GH-1 负极材料的 XPS 图谱Fig.5 XPS spectra of SnO2-GH-1 anode materials
作为锂离子电池复合负极材料,各组分之间的比例对材料的性能具有很大影响。如图6所示,在空气气氛中,温度升至 800 °C 后,所有的GH-4与氧气反应以气体形式排出,剩余质量仅为 1.4% (w),而 SnO2作为一个稳定结构的金属氧化物则保持质量恒定。因此,可以通过空气气氛中的负极材料剩余质量来计算SnO2的含量。经过计算可知负 极 材 料 SnO2-GH-1、 SnO2-GH-2、 SnO2-GH-3、SnO2-GH-4 中 SnO2含量分 别 为 54%、44%、32%、22%(w)。
图7 为 SnO2-GH 负极材料的 FESEM 图。与图 3 (d)中 GH-4 的微观结构相比,引入不同含量的 SnO2颗粒对GH的成型过程及微观结构并没有明显的影响。SnO2-GH 负极材料也是呈多孔的三维结构,孔与孔保持连通且微孔尺寸与GH一致。这种三维结构的负极材料能够在很大程度上保证电解液的浸润性、提高材料有效反应比表面积。当放大 SnO2-GH的局部结构后发现,石墨烯的表面并不平滑,而是存在许多褶皱和扭曲结构,同时SnO2颗粒的尺寸非常小,通过FESEM很难辨认,但是颗粒的分散比较均匀,没有出现明显的团聚或二次颗粒等。
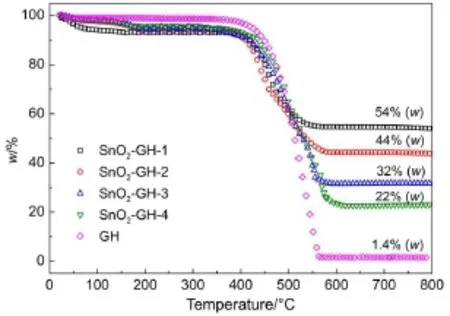
图6 SnO2-GH 和 GH-4 负极材料的热失重分析(TGA)曲线Fig.6 Thermogravimetic analysis(TGA)curves of SnO2-GH and GH-4 anode materials
本文通过TEM进一步研究SnO2颗粒的分布情况及尺寸大小。图 8(a,b)为 SnO2-GH-1 的 TEM 图像,其中 SnO2的含量为 54%(w)。即使在这么高的含量下,SnO2纳米颗粒依旧没有发生明显团聚现象,证明该方法制备的SnO2纳米颗粒以GO上丰富的官能团为依托,均匀分布在GO单片层的表面,颗 粒 大小约 为 2-3 nm。而 且 在一 定 范围 内 提高Sn4+离子溶液的浓度,对 SnO2颗粒大小没有产生明显影响。随着 Sn4+离子溶液的浓度的降低,SnO2的含量逐渐降低,且 SnO2颗粒的分布越来越稀疏。图 8(f)高分辨 TEM 图像中显示颗粒的晶面间距为0.335 nm,验证了图中所示的纳米颗粒为 SnO2。
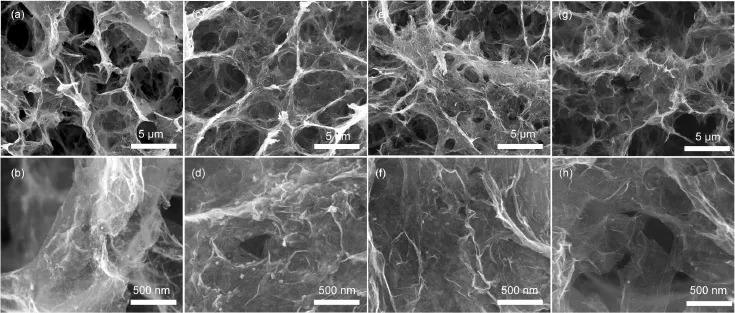
图7 不同 SnO2-GH 负极材料的 FESEM 照片Fig.7 FESEM images of various SnO2-GH anode materials
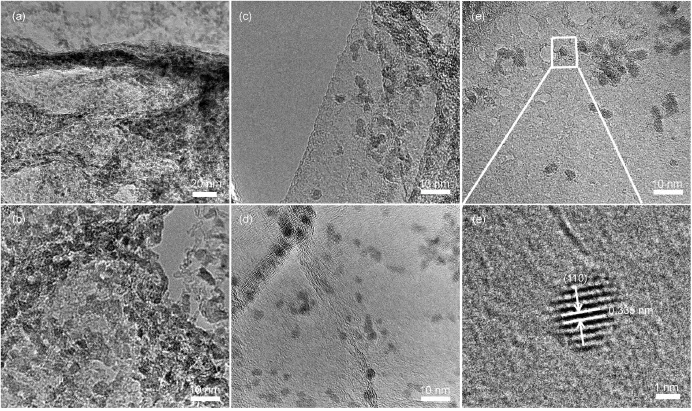
图8 不同SnO2-GH 负极材料的透射电子显微镜(TEM)照片Fig.8 Transmission electron microscope(TEM)images of various SnO2-GH anode materials
图9 为 SnO2-GH-1 负极材料在 2.0-0.01 V 电压下的循环伏安曲线,用来研究该负极材料在电池充放电过程中发生的电化学反应。首次循环在0.7-1.5 V 之间的宽还原 峰 与 负 极 材 料 表 面的 SEI的形成以及 SnO2与 Li+发生反应形成 Sn 和 Li2O 的反应有关。该宽峰在后续的循环中宽度缩小、强度减弱、且位移至 0.9 V,表明 SEI膜的反应只发生在首次,在后续循环中存在的是 SnO2与 Li+发生的还原反应。相对应的,1.3 V 处的氧化峰为部分 Sn氧化形成 SnO2的反应。0.2 及 0.01 V 的两个还原峰分 别 对应 Sn 和 GH 的嵌 锂 反应 ; 相对应 的 0.6 和0.1 V 两处氧化峰为 Sn 和 GH 的脱锂反应。

图9 SnO2-GH-1负极材料的循环伏安(CV)曲线Fig.9 Cyclic voltammetry(CV)curves of SnO2-GH-1 anode materials

图10 (a)GH-4 负极材料在 100 mA·g-1电流密度下的电池循环性能,(b)SnO2-GH负极材料的电池倍率循环性能,(c)SnO2-GH-1负极材料的恒流充放电剖面图Fig.10 (a)Cycle capacity of GH-4 anode materials at 100 mA·g-1,(b)rate capacity of SnO2-GH anode materials,and (c)galvanostatic charge-discharge profiles of SnO2-GH-1 anode materials
从图 10(a)可以看出 GH-4 在 100 mA·g-1的电流密度下,首次可逆容量为 290 mAh·g-1,库仑效率为 40.4%,较低的首次库仑效率是由于 GH-4 的高比表面积导致过多的SEI膜反应的。经过100次循环后容量为 279 mAh·g-1,库仑效率为 99.5%,与首次相比容量保持率为 96.2%。表明 GH 作为锂离子电池负极材料基体具有优越的电化学稳定性。图 10(b)为 SnO2-GH-1、-2、-3、-4 负极材料在不同电流密度下的倍率循环性能。从图中可以看出,四个负极材料的循环稳定性基本保持一致,区别只在于容量大小。四种材料的容量与SnO2的含量呈 正 比 。 以 SnO2-GH-1 为 例 , 依 次 在 50、100、200、500、1000、2000、5000 mA·g-1电流密度下充放电 10 个循环后,在 5000 mA·g-1的超大电流下循环充放电 60 个循环,之后再恢复到 50 mA·g-1的小电流密度,循环充放电80个循环。不同电流密度 下 对 应 的 可 逆 容 量 分 别 稳 定 在 1000、870、800、710、645、560、500、865 mAh·g-1,对比前10个循环的平均可逆容量,该负极材料在倍率循环 200 次之后的容量保持率高达 86.5%。这样优越的倍率循环稳定性能主要来源于GH基体的连通多孔三维结构。GH的多孔结构可以提高电解液的浸润率,同时缩短离子在负极材料内部的传输距离,有利于大电流下材料的快速嵌/脱锂反应。GH内部具有丰富、充足的空间,能够有效缓冲SnO2充放电过程中的体积变化,保持微观结构的稳定。再者,GH中石墨烯层表面的褶皱能够保证与SnO2颗粒的紧密结合,也可以避免在重复充放电过程中活性物质脱落、失活、团聚等现象。图10 (c)为 SnO2-GH-1 在 不 同 电 流 密 度 下 (50、 100、200、500、1000、2000、5000 mA·g-1)的恒流充放电剖面图。随着电流密度的增加,充放电曲线的形状并没有发生明显变化,证明该负极材料所发生的充放电反应没有发生变化,而可逆容量随着电流密度的增加而减小。50 mA·g-1电流密度下的材料的库仑效率仅为85%,其他电流密度下的库仑效率都保持在95%以上,说明该负极材料的不可逆变化主要集中在前10个循环。图11为倍率循环测试之后 SnO2-GH-1 负极极片的 FESEM 图像 ,循环后电极依旧保持三维网络结构和丰富均匀的微孔结构,放大后电极表明没有看到明显的裂痕和团聚等现象,证明石墨烯水凝胶这种三维结构能够在大电流充放电之后保持原有的微观结构。经过EDS分析可以看出材料的元素组成也未发生明显变化。
为 了 进 一 步 考 察 SnO2-GH-1、 SnO2-GH-2、SnO2-GH-3、SnO2-GH-4 负 极 材 料 的 电化 学 特性 ,在倍率循环之后对电池进行交流阻抗测试,如图12 所示。可以看出 Nyquist曲线分为三个部分,高频区和中频区的半圆,另外是后面跟随的低频区的斜线。其中,高频区半圆部分主要与电池内部接触电阻、SEI膜电阻有关,中频区半圆主要与电池内部电荷转移阻抗有关,而低频区斜线主要与锂离子在电极固相内的扩散过程有关。通过Zview软件对四条 Nyquist曲线进行模拟得到一个合适的等效电路,如图12插图所示。等效电路实际上是把电池的每个部分分成了一个个单独的电阻元件。其中 Rs代表电池内部接触电阻、RSEI代表界面膜阻抗、Rct代表电荷转移阻抗、Wo代表锂离子在固相内扩散的 Warburg 阻抗。模拟得到的具体数值见表 3。四种负极材料的 Rs和 RSEI随着 SnO2含量的降低而 减 小 , 而 Rct却没有明显变化 。 由 于 SnO2的导电性比GH差,因此SnO2含量降低时,电池的Rs相应减小。SEI是在GH和SnO2纳米颗粒表面生成的一种不可逆膜,因此,随着 SnO2含量降低,生成的 SEI会越少,从而使得 RSEI阻抗减小。根据上文提到的四种负极材料的微观结构几乎一致,Rct与其结构具有密切联系,因此这四种负极材料的Rct值变化不明显。这也与上述倍率循环稳定性结果相一致。

图11 SnO2-GH-1负极材料倍率循环后负极极片的 FESEM 照片Fig.11 FESEM images of SnO2-GH-1 anode materials after rate cycling test
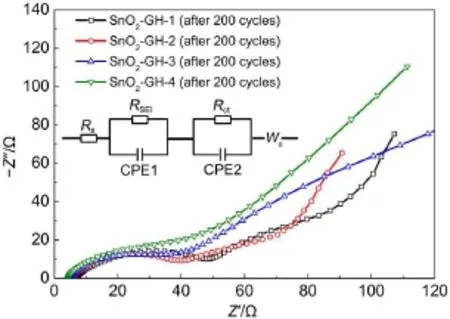
图12 SnO2-GH 负极材料循环后的电化学交流阻抗谱图Fig.12 EIS spectra of SnO2-GH anode materials post-cycles

表3 SnO2-GH负极材料电化学交流阻抗谱(EIS)拟合数据Table 3 Electrochemical impedance spectroscopy(EIS) fitting results of SnO2-GH anode materials
4 结论
本文采用三维多孔的石墨烯水凝胶为导电碳质基体,通过溶液水解反应在石墨烯水凝胶中引入 SnO2纳米颗粒,得到不同 SnO2含量的三维 SnO2-GH 负极材料。2-3 nm 的 SnO2均匀分布在石墨烯表面,没有明显团聚现象,且SnO2颗粒的担载量可以达到 54%(w)。随着三维 SnO2-GH 负极材料中SnO2含量增加,材料始终保持极高的循环稳定性能。在 5000 mA·g-1的大电流密度下循环 60 次容量稳定在 500 mAh·g-1,电流减小到 50 mA·g-1循环80 次后容量仍高达 865 mAh·g-1。SnO2-GH 具有相互贯通的多孔结构,这赋予了材料极高的比表面积,保证了电解液对材料的浸润性,并有效缩短了离子的传输距离。同时丰富的内部空间还能够有效避免 SnO2颗粒团聚,缓冲其巨大体积膨胀 ,维持电极结构的稳定性,是一种适于大电流充放电的锂离子电池负极材料基体。
(1)Goodenough,J.B.;Kim,Y.Chem.Mater.2010,22,587. doi:10.1021/cm901452z
(2)Dunn,B.;Kamath,H.;Tarascon,J.M.Science2011,334,928. doi:10.1126/science.1212741
(3)Li,H.;Wang,Z.;Chen,L.;Huang,X.Adv.Mater.2009,21, 4593.doi:10.1002/adma.200901710
(4)Wang,J.T.;Wang,Y.;Huang,B.;Yang,Y.J.;Tan,X.;Lu,S.G.Acta Phys.-Chim.Sin.2014,30,305.[王建涛,王 耀,黄 斌,杨娟玉,谭 翱,卢世刚.物理化学学报,2014,30,305.] doi:10.3866/PKU.WHXB201312022
(5)Huang,J.J.;Dong,Z.J.;Zhang,X.;Yuan,G.M.;Cong,Y.; Cui,Z.W.;Li,X.K.Acta Phys.-Chim.Sin.2016,32,1699. [黄家骏,董志军,张 旭,袁观明,丛 野,崔正威,李轩科.物理化学学报,2016,32,1699.]doi:10.3866/PKU. WHXB201604011
(6)Tarascon,J.M.;Armand,M.Nature2001,414,359. doi:10.1038/35104644
(7)Eom,K.S.;Jung,J.;Lee,J.T.;Lair,V.;Joshi,T.;Lee,S.W.; Lin,Z.;Fuller,T.F.Nano Energy2015,12,314.doi:10.1016/j. nanoen.2014.12.041
(8)Yang,Z.;Zhang,W.;Shen,Y.;Yuan,L.X.;Huang,Y.H.Acta Phys.-Chim.Sin.2016,32,1062.[杨 泽,张 旺,沈 越,袁利霞,黄云辉 .物理化学学报,2016,32,1062.]doi:10.3866/ PKU.WHXB201603231
(9)Bai,X.J.;Wang,B.;Cheng,X.;Jiang,J.M.J.Donghua Univ. (Eng.Ed.)2015,32,379.
(10)Zhong,Y.;Li,X.;Zhang,Y.;Li,R.;Cai,M.;Sun,X.Appl.Surf. Sci.2015,332,192.doi:10.1016/j.apsusc.2015.01.099
(11)Wang,M.S.;Lei,M.;Wang,Z.Q.;Zhao,X.;Xu,J.;Yang,W.; Huang,Y.;Li,X.J.Power Sources2016,309,238.doi:10.1016/ j.jpowsour.2015.11.074
(12)Guo,W.;Li,F.;Duan,X.;Ma,J.Mater.Lett.2016,166,210. doi:10.1016/j.matlet.2015.12.081
(13)Shao,Q.G.;Chen,W.M.;Wang,Z.H.;Qie,L.;Yuan,L.X.; Zhang,W.X.;Hu,X.L.;Huang,Y.H.Electrochem.Commun.2011,13,1431.doi:10.1016/j.elecom.2011.09.014
(14)Kim,J.G.;Nam,S.H.;Lee,S.H.;Choi,S.M.;Kim,W.B.ACS Appl.Mater.Interf.2011,3,828.doi:10.1021/am101169k
(15)Yu,Y.;Chen,C.H.;Shi,Y.Adv.Mater.2007,19,993. doi:10.1002/adma.200601667
(16)Lou,X.W.;Li,C.M.;Archer,L.A.Adv.Mater.2009,21,2536. doi:10.1002/adma.200803439
(17)Han,Y.;Wu,X.;Ma,Y.;Gong,L.;Qu,F.;Fan,H.CrystEngComm2011,13,3506.doi:10.1039/c1ce05171g
(18)Lei,D.;Zhang,M.;Hao,Q.;Chen,L.;Li,Q.;Zhang,E.;Wang, T.Mater.Lett.2011,65,1154.doi:10.1016/j.matlet.2011.01.012
(19)Zhou,X.;Zou,Y.;Yang,J.J.Power Sources2014,253,287. doi:10.1016/j.jpowsour.2013.12.034
(20)Wang,R.H.;Xu,C.H.;Sun,J.;Gao,L.;Yao,H.L.ACS Appl. Mater.Interf.2014,6,3427.doi:10.1021/am405557c
(21)Billaud,D.;Balan,L.;Schneider,R.;Willmann,P.Carbon2006,44,2508.doi:10.1016/j.carbon.2006.05.023
(22)Du,G.;Zhong,C.;Zhang,P.;Guo,Z.;Chen,Z.;Liu,H.Electrochem.Acta2010,55,2582.doi:10.1016/j. electacta.2009.12.031
(23)Hassoun,J.;Panero,S.;Mulas,G.;Scrosati,B.J.Power Sources2007,171,928.doi:10.1016/j.jpowsour.2007.06.067
(24)Lee,W.J.;Park,M.H.;Wang,Y.;Lee,J.Y.;Cho,J.Chem. Commun.2010,46,622.doi:10.1039/b916483a
(25)Park,J.;Eom,J.;Kwon,H.Electrochem.Commun.2009,11, 596.doi:10.1016/j.elecom.2008.12.022
(26)Yang,Q.H.Acta Phys.-Chim.Sin.2016,32,1051.[杨全红 .物理化学学报,2016,32,1051.]doi:10.3866/PKU. WHXB201603301
(27)Gong,Y.;Yang,S.;Zhan,L.;Ma,L.;Vajtai,R.;Ajayan,P.M.Adv.Funct.Mater.2014,24,125.doi:10.1002/adfm.201300844
(28)Xiao,L.;Wu,D.;Han,S.;Huang,Y.;Li,S.;He,M.;Zhang,F.; Feng,X.ACS Appl.Mater.Interf.2013,5,3764.doi:10.1021/ am400387t
(29)Zhang,Z.;Xiao,F.;Guo,Y.;Wang,S.;Liu,Y.ACS Appl.Mater. Interf.2013,5,2227.doi:10.1021/am303299r
(30)Bai,X.;Yu,Y.;Kung,H.H.;Wang,B.;Jiang,J.M.J.Power Sources2016,306,42.doi:10.1016/j.jpowsour.2015.11.102
(31)Zhao,X.;Hayner,C.M.;Kung,M.C.;Kung,H.H.Adv.Energy Mater.2011,1,1079.doi:10.1002/aenm.201100426
3D SnO2/Graphene Hydrogel Anode Material for Lithium-Ion Battery
BAI Xue-Jun1,*HOU Min1LIU Chan1WANG Biao2CAO Hui1,3WANG Dong1,3
(1Shanghai Aerospace Power Technology LTD,Shanghai 201615,P.R.China;2College of Material Science and Engineering, Donghua University,Shanghai 201620,P.R.China;3Shanghai Institute of Space Power Source,Shanghai 200245,P.R.China)
With the widespread use of mobile electronic devices and increasing demand for electric energy storage in the transportation and energy sectors,lithium-ion batteries(LIBs)have become a major research and development focus in recent years.The current generation of LIBs use graphite as the anode material,which has a theoretical capacity of 372 mAh·g-1.Tin-based materials are considered promising anode materials for next-generation LIBs because of their favorable working voltage and unsurpassed theoretical specific capacity. However,overcoming the rapid storage capacity degradation of tin caused by its large volumetric changes (> 200%)during cycling remains a major challenge to the successful implementation of such materials.In this paper,SnO2nanoparticles with a diameter of 2-3 nm were used as active materials in LIB anodes and a threedimensional(3D)graphene hydrogel(GH)was used as a buffer to decrease the volumetric change.Typically, SnCl4aqueous solution(18 mL,6.4 mmol·L-1)and graphene oxide(GO)suspension(0.5%(w,mass fraction), 2 mL)were mixed together via sonication.NaOH aqueous solution(11.4 mmol·L-1,40 mL)was slowly added and then the mixture was stirred for 2 h to obtain a stable suspension.Vitamin C(VC,80 mg)was then added as a reductant.The mixture was kept at 80 °C for 24 h to reduce and self-assemble.The resulting black block was washed repeatedly with distilled deionized water and freeze-dried to obtain SnO2-GH.In this composite, GH provides large specific surface area for efficient loading(54%(w))and uniform distribution of nanoparticles. SnO2-GH delivered a capacity of 500 mAh·g-1at 5000 mA·g-1and 865 mAh·g-1at 50 mA·g-1after rate cycling.This outstanding electrochemical performance is attributed to the 3D structure of GH,which provides large internal space to accommodate volumetric changes,an electrically conducting structural porous network,a large amount of lithium-ion diffusion channels,fast electron transport kinetics,and excellent penetration of electrolyte solution.This study demonstrates that 3D GH is a potential carbon matrix for LIBs.
Graphene hydrogel;SnO2;Lithium-ion battery;Anode;Three-dimension
O646
10.3866/PKU.WHXB201610272
Received:September 26,2016;Revised:October 26,2016;Published online:October 27,2016.
*Corresponding author.Email:renee1125@163.com;Tel:+86-21-67756490-8709.
The project was supported by the Shanghai Science and Technology Innovation Plan,China(15DZ1201001,16111106001).
上海市科技创新行动计划(15DZ1201001,16111106001)资助© Editorial office of Acta Physico-Chimica Sinica

