微波辅助稀酸降解玉米芯的工艺优化及其效果研究
朱李妍 - 杨晓瑞 - 王 伟 梁金花 - 朱建良 -
(南京工业大学生物与制药工程学院,江苏 南京 211800)
玉米、水稻等是中国主要粮食,产量大,但利用率却不高。木质纤维素是农作物的主要成分,可以通过一定的方法将其转化为可发酵糖等各种化合物[1-2],如糖、醇、酸等广泛应用于食品、医药、化工等各大领域[3]。木质纤维素由纤维素、半纤维素和木质素形成致密的网状结构,具有较高的结晶度,难以降解。预处理可以改变纤维素生物质的结构使它更容易被酶所接受;同时也可以降低纤维素的聚合度和结晶度;此外,还可以有选择性地从木质纤维素基质中去除半纤维素和木质素[4]。
目前预处理的方法有很多,如蒸汽爆破法[5-6]、热水法[7-8]、生物法和酸碱法[9-10]等。不同的方法都有一定的优缺点,蒸汽爆破法无污染,但半纤维素的损失较大;热水法时间较长,能耗大;酸碱法存在污染回收等问题;生物法对酶的要求比较高,且成本较高。近年来,人们成功地利用了新颖的微波法[11]、微波酸法[12-13]和超声波法[14]对木质纤维素材料的糖化进行了更好的预处理。微波法具有操作简单、清洁、高效等特点,微波法大大缩短了反应时间,微波辅助稀酸提高了半纤维素的降解率,与其他方法相比,其还原糖得率也明显较高。为了充分有效地利用生物质材料,提高其木质纤维素的转化率,本试验以稀酸为催化剂,利用微波辐射加热的方法对木质纤维素进行水解,通过调节时间、微波功率、玉米芯与催化剂量的比例及颗粒大小优化水解工艺条件,并对其最优条件进行表征,以期为实际工业中的应用提供参考。
1 材料与方法
1.1 材料与仪器
玉米芯:取自河南濮阳,自然风干后用粉碎机将其粉碎、过不同目数的筛网后保存备用;
硫酸:分析纯,江苏太平洋化学工业公司;
高速多功能粉碎机:JP-300B型,温岭市林大机械有限公司;
紫外可见分光光度计:752型,上海光学仪器有限公司;
高效液相色谱(HPLC):岛津-20A型,日本岛津有限公司;
微波反应器:WBFY-201型,巩义予华仪器有限公司;
扫描电子显微镜:JSM-6510型,日本电子公司;
傅里叶变换红外光谱仪:Nicolet380型,美国Thermo公司;
比表面及孔径分析仪:JW-BK122W型,北京精微高博有限公司。
1.2 试验方法
1.2.1 试验步骤 称取5 g一定大小的玉米芯放入250 mL烧瓶中,按照一定的固液比加入一定浓度的稀硫酸,搅拌均匀后,放入密闭的微波反应器中反应,设定微波功率和辐射时间后进行水解反应,观察反应现象,反应结束后冷却过滤,所得澄清液用NaOH溶液中和至中性,然后用高效液相色谱仪测木糖、葡萄糖和阿拉伯糖的含量,用DNS法测总还原糖含量。
1.2.2 单因素试验设计
(1) 硫酸浓度对玉米芯降解性能的影响:设定固液比为1∶10 (g/mL),功率为195 W,微波辐射时间为10 min,玉米芯颗粒大小为20~40目,分别控制硫酸浓度(质量分数)为0%,2%,5%,7%,10%,13%,15%,18%,20%,降解玉米芯,考察硫酸浓度对玉米芯降解产糖的影响。
(2) 颗粒大小对玉米芯降解性能的影响:设定固液比为1∶10 (g/mL),功率为195 W,微波辐射时间为10 min,稀硫酸浓度为10%,分别控制颗粒大小为20~40,40~60,60~80,80~100,100目以上,降解玉米芯,考察颗粒大小对降解玉米芯产糖的影响。
标准筛目数对应尺寸:20目(孔径0.900 mm)、40目(孔径0.450 mm)、60目(孔径0.250 mm)、80目(孔径0.180 mm)、100目(孔径0.154 mm)。
(3) 微波辐射时间对玉米芯降解性能的影响:设定固液比为1∶10 (g/mL),功率为195 W,硫酸浓度为10%,玉米芯颗粒大小为60~80目,分别控制微波辐射时间为5,10,15,20,25 min,降解玉米芯,考察微波辐射时间对玉米芯降解产糖的影响。
(4) 固液比对玉米芯降解性能的影响:设定功率为195 W,硫酸浓度为10%,玉米芯颗粒大小为60~80目,微波辐射时间为20 min,分别控制固液比为1∶6,1∶8,1∶10,1∶12,1∶14 (g/mL),降解玉米芯,考察固液比对玉米芯降解产糖的影响。
(5) 微波辐射功率对玉米芯降解性能的影响:设定功率为195 W,硫酸浓度为10%,玉米芯颗粒大小为60~80目,微波辐射时间为20 min,固液比为1∶8 (g/mL),分别控制微波辐射功率为65,130,195,260,325 W,降解玉米芯,考察微波辐射功率对玉米芯降解的影响。
1.2.3 正交试验设计 基于单因素试验结果,确立正交试验考察4个因素的3个水平,并按照L9(34)进行试验设计,每个因素水平进行3次平行试验,优化降解玉米芯的最佳工艺条件。并在该最佳工艺条件下,对微波辐射稀酸催化玉米芯水解进行3次平行验证实验。
1.3 分析与测定方法
1.3.1 糖含量测定 采用液相色谱仪测定小分子糖液浓度,检测器为RID-10A示差折光,色谱柱为bio-rad Aminex HPX-87H 糖分析柱。以0.005 moL的硫酸为流动相,柱温55 ℃,流速0.6 mL/min,进样体积10 μL。待反应结束,将过滤后的糖液过0.45 μm的水系滤膜,经HPLC分析得到的糖主要有木糖、葡萄糖和阿拉伯糖,采用DNS比色法[15]测定还原糖,利用外标法计算还原糖得率、原料的转化率及半纤维纤维素转化率,计算公式见式(1)~(4)。
(1)
(2)
(3)
(4)
式中:
h——糖得率,%;
a1——原料转化率,%;
a2——半纤维素转化率,%;
a3——纤维素转化率,%;
c——还原糖的浓度,g/L;
cxyl——木糖浓度,g/L;
cara——阿拉伯糖浓度,g/L;
cglu——葡萄糖浓度,g/L;
v——糖液的体积,mL;
n——稀释的倍数;
m——水解前玉米芯干重,g;
m1——水解后残余物干重,g;
10-3——换算系数。
1.3.2 成分分析 利用NREL法[16]测定微波水、微波酸以及酸3种条件下反应后残余物的成分,比较并分析纤维素、半纤维素和木质素含量。
1.3.3 比表面积测定 采用液氮吸附法(Brunauer Emmett Teller,BET)[17]测定原料、3种不同降解方法反应后残渣的比表面积。样品在105 ℃下抽真空脱气2 h除去其中的水分,然后进行BET测定,BET比表面积测定方法遵循多层吸附理论。
1.3.4 扫描电镜(SEM)测定 采用JSM-6510型扫描电子显微镜(SEM)对原料和3种不同处理方法的残渣进行表征,观察残渣处理前后的表面形貌变化。
1.3.5 红外光谱分析(FT-IR) 采用傅立叶变换红外光谱仪对原料及3种不用方法处理后的玉米芯进行红外分析,使用KBr压片,在波数为400~4 000 cm-1范围内进行扫描,采集数据。

2 结果与讨论
2.1 微波辅助稀酸降解玉米芯产糖的条件优化
2.1.1 硫酸浓度对玉米芯降解性能的影响 由图1可知,在没有催化剂(稀硫酸)时,玉米芯降解所得总还原糖得率为3.94%,原料转化率为12.8%;当加入稀硫酸时,总还原糖得率及原料转化率都发生了巨大的变化。硫酸浓度从2%增加到10%时,总还原糖得率和原料转化率都迅速增加,当硫酸浓度为10%时,所产生的总还原糖得率为62.04%,是酸浓度为2%时的6倍,此时半纤维素与纤维素的转化率分别为75.24%,4.43%;继续增大硫酸浓度,总还原糖得率出现了下降的趋势。这是由于在酸性介质中,H+与水生成的H3O+使大分子中糖苷键的氧原子质子化,形成共轭酸减弱糖苷键的键能使其断裂,末端的正碳离子与水反应生成单糖[18],酸浓度继续增加时,在微波加热下,玉米芯及其产生的糖易发生碳化结焦现象,且低聚糖易与H+产生甲酸、乙酸等副产物,说明稀酸超过一定值对玉米芯降解效率的提高意义不大,所以选择稀硫酸浓度为10%。

图1 硫酸浓度对玉米芯降解的影响Figure 1 Effect of sulfuric acid concentration on the degradation of corncob
2.1.2 颗粒大小对玉米芯降解性能的影响 由图2可知,颗粒大小对玉米芯降解的还原糖得率和原料转化率有一定的影响。随着玉米芯颗粒的减小,还原糖得率及半纤维素转化率出现先增大后减小的趋势,原料转化率和纤维素转化率的变化趋势较小,当玉米芯颗粒大小为60~80目时总还原糖得率达到最高为64.63%,此时原料转化率为47%,半纤维素及纤维素的转化率分别为79.52%,7.07%。当颗粒较大时,比表面积较小,纤维素、半纤维素与木质素之间的结构被破坏得不够充分;当颗粒较小时,具有较大的比表面积,由于大分子木聚糖转化成小分子糖,易继续反应转化成相应的副产物,从而出现还原糖得率及半纤维素转化率减少的趋势。因此微波酸化降解玉米芯产糖的最适颗粒大小为60~80目。
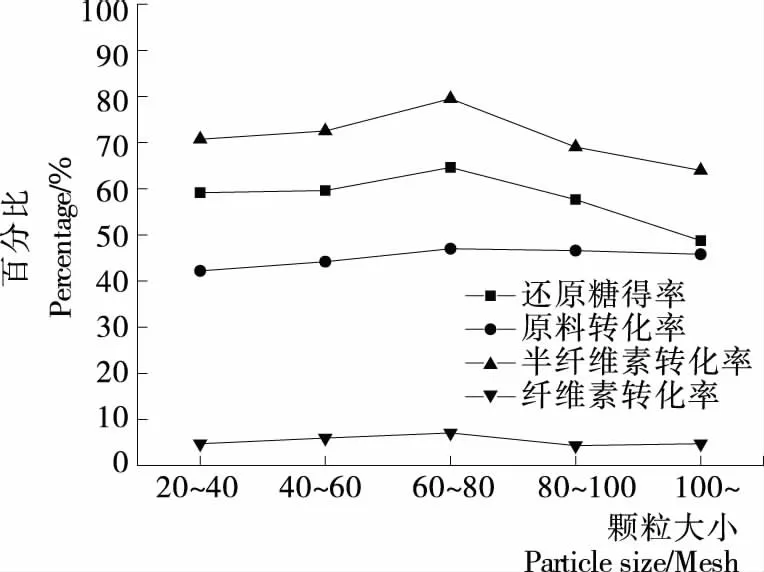
图2 颗粒大小对玉米芯降解的影响Figure 2 Effect of particle size on the degradation of corncob
2.1.3 微波辐射时间对玉米芯降解性能的影响 由图3可知,微波辐射时间对玉米芯降解的效果具有显著影响。在一定功率和固液比的条件下,辐射时间由5 min增加到10 min,玉米芯还原糖得率、原料转化率及半纤维素转化率都出现大幅度的增加,10~20 min时三者增加的幅度相对缓慢,当辐射时间为20 min时,总还原糖得率达到最大为73.88%,半纤维素转化率最大为90.76%,此时原料转化率最高为54.2%,继续延长辐射时间,还原糖得率及原料转化率开始下降。由于玉米芯催化降解的过程是木质纤维素降解产还原糖的过程,继续反应使还原糖被分解生成副产物。当反应时间较短时,稀酸不能充分溶解玉米芯,还原糖得率及原料转化率都较低;辐射10~20 min时,糖得率增加缓慢,因为半纤维素的减少与糖浓度的增加使物质之间产生抑制作用[19];当反应达到某种平衡后,继续延长辐射时间,会破坏反应平衡,使降解生成的部分糖液发生二次反应,分解为甲酸、乙酸、糠醛和5HMF等副产物,导致糖浓度较低。所以,选择辐射时间为20 min较宜。
2.1.4 固液比对玉米芯降解性能的影响 由图4可知,随着固液比中溶剂量的增大,总还原糖得率、半纤维素及纤维素转化率都出现先缓慢增加后减小的趋势,原料转化率的变化不大。当固液比为1∶8 (g/mL)时,还原糖得率最高为63.8%,比固液比为1∶6 (g/mL)时的高4.77%,半纤维素及纤维素转化率也达到最高分别为89.05%,7.15%,此时原料转化率为48.4%。由于溶剂量过小,玉米芯与硫酸不能充分接触,降解不完全;随着溶剂量的增多,木质纤维素与酸接触充分,降解效果好,还原糖得率及半纤维素、纤维素转化率较高;继续增加溶剂,料液过多,秸秆易团聚一起,水解反应效果差。由此可得,玉米芯降解产糖过程中的最适固液比为1∶8 (g/mL)。
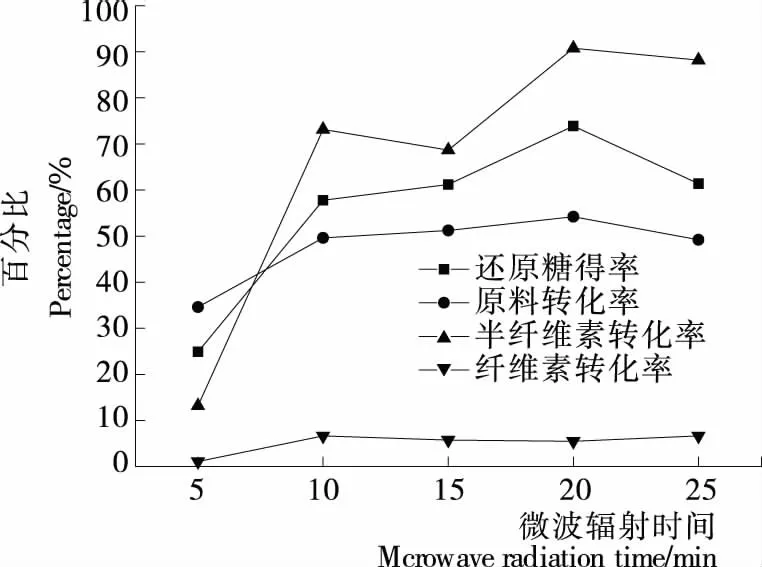
图3 微波辐射时间对玉米芯降解的影响Figure 3 Effect of microwave radiation time on degradation of corncob

图4 固液比对玉米芯降解的影响Figure 4 Effect of solid-liquid ratio on the d degradation of corncob
2.1.5 微波辐射功率对玉米芯降解性能的影响 由图5可知,微波辐射功率对秸秆降解的影响较大。65~130 W时,还原糖得率、原料转化率及半纤维素转化率都出现较大的浮动,还原糖得率从8.6%升到72.64%,半纤维素转化率从4.16% 升到90.87%,原料转化率也从15.2%增加到52.7%。130~325 W时,还原糖得率及半纤维素转化率都出现下降的趋势,而原料转化率在不断增加。这主要是微波辐射功率小达不到反应所需要的温度,反应效果差;增大微波功率,能促进H+对木质纤维素的破坏作用,从而提高还原糖得率及原料转化率;微波功率越大,反应器内的温度越高,硫酸越容易将秸秆及降解所产生的糖碳化,使原料转化率增高,还原糖得率及半纤维素转化反而减少。由此可得,玉米芯降解过程中适宜的微波功率为130 W。

图5 微波辐射功率对玉米芯降解的影响Figure 5 Effect of microwave power on the degradation of corncob
2.2 正交试验结果与分析
基于单因素试验的结果,选取硫酸浓度、微波辐射时间、固液比、微波辐射功率4个因素3个水平进行L9(34)正交试验,试验因素与水平设计情况见表1,正交试验结果与分析见表2。

表1 正交因素试验水平

表2 正交试验结果
由表2可知,微波辐射稀酸催化玉米芯水解的最佳工艺条件为A3B2C2D2,即硫酸浓度为13%,微波辐射时间为20 min,固液比为1∶8 (g/mL),微波辐射功率为130 W。各因素对还原糖得率的影响次序为微波功率>硫酸浓度>微波辐射时间>固液比。
2.3 验证实验
2.3.1 正交试验结果的验证 基于正交试验的结果,采用最佳工艺条件,即硫酸浓度13%,微波辐射时间20 min,固液比1∶8 (g/mL),微波辐射功率130 W、颗粒大小60~80目时,对微波辐射稀酸催化水解玉米芯进行3次平行验证实验,还原糖得率分别为65.83%,67.46%,65.94%,所得还原糖平均得率为66.41%,大于正交试验表中所有因素水平组合的试验结果,表明本试验优化参数较为可靠,达到了微波辐射稀酸催化水解玉米芯的工艺目的。
2.3.2 不同降解方法的比较 按照正交试验确定的最佳工艺条件水解玉米芯,与微波水法、稀硫酸法水解玉米芯比较,结果见表3。
由表3可知,微波酸法与其他2种方法相比,还原糖得率、原料转化率与半纤维素转化率都有较好的结果。加热是热量通过对流从材料表面传到内部区域的一种方式。在传统的加热过程中,能量转移是热梯度的结果[18],而微波能直接加热被电磁波辐射的物质,在辐射的影响下,一方面是电磁波内部加热使极性分子高频振动,平均动能增加,导致温度升高;另一方面是离子化物质在电磁场中因摩擦而产生热效应[20]。因此,微波加热比常规加热更直接更快且均匀,故选择微波酸法进行降解。

表3 不同处理方法的比较
2.4 秸秆反应前后成分含量及比表面积的变化
玉米芯的主要成分见表4,采用NREL法对反应前及不同方法反应后的材料进行测定,分析秸秆中半纤维素、纤维素和木质素的成分含量变化,利用比表面积分析仪测定反应前玉米芯与不同方法反应后秸秆的比表面积,比较结果见表5。

表4 玉米芯的主要成分
表5反应前后玉米芯中成分含量及比表面积的变化
Table 5 The changes of component content and surface properties of corncob before and after treated

处理方式半纤维素含量/%纤维素含量/%木质素含量/%比表面积/(m2·g-1)反应前28.1036.9215.002.233微波水27.8236.8615.332.250微波酸3.1358.7818.792.810酸 15.7843.7119.352.498
由表5可知,玉米芯在微波酸的方法下反应效果最好,半纤维素降解的较为彻底,由原来的28.1%降到3.13%,纤维素与木质素的含量增加,这是由于微波辅助酸对木质素没有影响,半纤维素含量减少,使得纤维素与木质素含量相对增加。不同的水解方法反应后玉米芯的比表面积都有所增大,而微波酸法增加的最多,这是由于微波辅助酸降解了大部分的半纤维素,降低了纤维素的结晶度,打破了木质纤维素之间的紧密结构,使结构变得疏松,孔隙增多,从而使秸秆的比表面积增大。
2.5 反应前后秸秆的SEM图比较
用扫描电子显微镜对玉米芯原料、微波水、微波酸、及酸处理后的玉米芯进行表征,观察原料及不同方法处理后玉米芯表面的形态和微观结构变化。玉米芯扫描电镜图见图6。
由图6可知,反应前玉米芯表面结构致密,可以清楚地看到纤维束表面平整光滑;微波水效果较差,物料表面的孔较少;酸法中玉米芯表面的孔增多且密集程度增大;微波酸法中玉米芯表面疏松、凹凸不平,反应后秸秆的立体结构受到破坏,表面产生很多空隙,平整的表面消失、断裂。这是由于微波辐射导致秸秆中的水分子吸收能量而产热,使细胞内温度上升,液态水汽化产生的压力将细胞膜和细胞壁冲破,形成小孔,继续加热,细胞内的水分减少,细胞收缩,表面出现孔洞和裂纹[21]。微波辅助酸降解玉米芯时,玉米芯的紧密结构遭到破坏,半纤维素几乎完全降解,纤维素则部分降解,同时纤维素内部的氢键被打开,有效降低了其结晶度,这些对后续玉米芯的充分利用具有重要的影响。

图6 反应前后玉米芯的SEM图Figure 6 The SEM spectrum of corncob before and after treated
2.6 FT-IR红外光谱分析
为表征微波辐射稀酸催化玉米芯的水解程度,对原料及3种不同方法处理后的残渣进行傅里叶红外光谱表征分析,结果见图7。
由图7可知,在3 700~3 300 cm-1处的吸收峰属于O—H键的伸缩振动,1 500~1 300 cm-1处的吸收峰属于C—H键的弯曲振动;1 200~1 000 cm-1处的吸收峰属于C═C键和C—O—C键的伸缩振动,经过分析与原样相比不同的处理方法相差很大,其中微波酸的效果最好。经微波酸处理后,1 316~1 210 cm-1处的峰消失,此处主要为半纤维素木聚糖中的乙酰基CH3C═O基团的特征峰,表明秸秆半纤维素基本完全加氢降解;在3 354 cm-1左右存在一个很强的吸收峰,此处为纤维素中OH的重叠峰,说明纤维素微晶结构没有受到破坏。2 345~1 971 cm-1处的吸收峰,说明分子之间的结构遭到严重的破坏。而在2 898 cm-1处的特征峰偏移到2 855 cm-1,表明反应过程中分子内氢键断裂。此外1 081~1 041 cm-1处的纤维素特征峰也有所减弱,说明纤维素部分降解。图7中1 728 cm-1处为木质素中的共轭碳基,可以明显地看出此处红外吸收强度减少,说明木质素的结构受到了一定的影响。此外,在1 000~400 cm-1指纹区,吸收峰发生了明显变化,表明在降解过程中秸秆的分子结构发生了改变。

图7 原料及水解残渣红外光谱Figure 7 Raw material and the residues of infrared spectrum
3 结论
采用微波辐射稀酸催化水解玉米芯,利用单因素试验考察了硫酸浓度、微波辐射时间、固液比、颗粒大小及功率对还原糖得率与原料转化率的影响,正交优化试验得到最佳反应条件:功率130 W,硫酸浓度13%,固液比1∶8 (g/mL),反应时间20 min,秸秆目数60~80目,此时产糖率最高为66.41%,降解率为52.70%,半纤维素及纤维素转化率分别为63.36%,4.31%。在最适条件下对反应后的残渣进行了表征分析,结果表明,微波辐射酸法破坏了秸秆的内部结构,降低了纤维素的结晶度,但纤维素的转化率还有待进一步提高。
[1] XIAO Jun, SHEN Lai-hong, ZHANG Yan-nan, et al. Integra-ted analysis of energy, economic, and environmental perform-ance of biomethanol from rice straw in China[J]. Industrial and Engineering Chemistry Research, 2009, 48(22): 9 999-10 007.
[2] AKHTAR Junaid, IDRIS Ani, RAMLAN Abd Aziz. Recent advances in production of succinic acid from lignocellulosic biomassa[J]. Applied Microbiol and Biotechnology, 2014, 98(3): 987-1 000.
[3] BALAT Mustafa. Production of bioethanol from lignocellulosic materials via the biochemical pathway: a review[J]. Energy Conversion and Management, 2011, 52(2): 858-875.
[4] REZENDE Camila Alves, DE LIMA Marisa Aparecida, MAZIERO Priscila, et al. Chemical and morphological characterization of sugarcane bagasse submitted to a delignification process for enhanced enzymatic digestibility[J]. Biotechnology For Biofuels, 2011, 4: 1-18.
[5] BALAT Mustafa, BALAT Havva, OZ Cahide. Progress in bioethanol processing[J]. Progress in Energy and Combustion Science, 2008, 34(5): 551-573.
[6] SUN Ye, CHENG Jia-yang. Hydrolysis of lignocellulosic materials for ethanol production: a review[J]. Bioresource Technology, 2002, 83(1): 1-11.
[7] NLEWEM Kingsle C, THRASH Marvin E. Comparison of different pretreatment methods based on residual lignin effect on the enzymatic hydrolysis of switchgrass[J]. Bioresource Technology, 2010, 101(14): 5 426-5 430.
[8] KIM Kyoung Heon, HONG Juan. Supercritical CO2pretreat-ment of lignocellulose enhances enzymatic cellulose hydrolysis[J]. Bioresource Technology, 2001, 77(2): 139-144.
[9] CANILHA Larissa, SANTOS Victor T O, ROCHA George J M, et al. A study on the pretreatment of a sugarcane bagasse sample with dilute sulfuric acid[J]. Journal of Industrial Microbiology, 2011, 38(9): 1 467-1 475.
[10] XU Ning, ZHANG Wei, REN Shuang-feng, et al. Hemicelluloses negatively affect lignocellulose crystallinity for high biomass digestibility under NaOH and H2SO4pretreatments in miscanthus[J]. Biotechnology for Biofuels, 2012, 5: 1-12.
[11] LI Hong-qiang, QU Yang-qing, CHANG Sen-lin, et al. Microwave irradiation-a green and efficient way to pretreat biomass[J]. Bioresource Technology, 2016, 199: 34-41.
[12] AKHTAR Nadeem, JAIN Alok Kumar, GOYAL Dinesh, et al. Surfactant-assisted microwaveacid pretreatment of leaf litter biomass for enhanced enzymatic release of sugars[J]. Cellulose Chemistry and Technology, 2016, 50(1): 127-137.
[13] BINOD Parameswaran, SATYANAGALAKSHMIA Karri, SINDHU Raveendran, et al. Short duration microwave assisted pretreatment enhances the enzymatic saccharification and fermentable sugar yield from sugarcane bagasse[J]. Renewble Energy, 2012, 37(1): 109-116.
[14] SINDHU Raveendran, KUTTIRAJA Mathiyazhakan, PREETI Varghese Elizabeth, et al. A novel surfactant-assisted ultrasou-nd pretreatment of sugarcane tops for improved enzymatic release of sugars[J]. Bioresource Technology, 2013, 135: 67-72.
[15] 李朝英, 郑路. 基于DNS比色法的土壤蔗糖酶检测条件选择[J]. 中国农学通报, 2016, 27(32): 171-176.
[16] 张红漫, 郑荣平, 陈敬文, 等. NREL法测定木质纤维素原料组分的含量[J]. 分析实验室, 2010, 29(11): 15-18.
[17] 刘淑瑞, 张建然. 蔗渣浆比表面积的测定及其对纸浆性能影响的研究[J]. 广东造纸, 1993(2): 5-9.
[18] 金强, 张洪漫, 严立石, 黄和. 生物质半纤维素稀酸水解反应[J]. 化学进展, 2010, 22(4): 654-662.
[19] 何北海, 林鹿, 孙润仓, 孙勇. 木质纤维素化学水解产生可发酵糖研究[J]. 化学进展, 2007, 19(8): 1 141-1 146.
[20] 马梅芳, 李洁. 微波炮制中药研究进展[J]. 江西中医药杂质, 2008, 39(4): 74-77.
[21] 邹安, 沈春银, 赵玲, 等. 玉米秸秆中半纤维的微波-减预处理提取工艺[J]. 华东理工大学学报: 自然科学版, 2010, 36(4): 469-474.

