新型锂离子超级电容器用聚合物电解质研究
张一凡,袁 平,杨佩瑜,田文生,马晓华,李 敏
(1.复旦大学 材料科学系,上海 200433; 2.上海空间电源研究所,上海200245)
新型锂离子超级电容器用聚合物电解质研究
张一凡1,袁 平1,杨佩瑜1,田文生2,马晓华2,李 敏1
(1.复旦大学 材料科学系,上海 200433; 2.上海空间电源研究所,上海200245)
对新型锂离子超级电容器的含硼聚合物电解质的制备与性能进行了研究。以甲基丙烯酸缩水甘油酯(GMA)和聚乙二醇甲醚甲基丙烯酸酯(OEGMA)为单体,经自由基聚合法共聚得到P(GMA-co-OEGMA),并进一步添加苯硼酸酐改性,产物为含硼聚合物电解质P(GMA-co-OEGMA)-B。理化表征和电化学测试的结果表明:P(GMA-co-OEGMA)-B有良好的机械性能和耐热性能,电位窗口较大,变温条件下离子电导率佳,其中常温下的离子电导率最高可达1.62×10-3S/cm。与传统液态电解质和全固态电解质相比,合成的含硼聚合物电解质在应用中可避免漏液、易燃、易爆等安全性问题,且室温电导率较高,能满足锂离子超级电容器应用的要求。此外,该含硼聚合物电解质的安全性,宽电位窗口,较高的低温电导率在航天领域亦具备一定的应用前景。
含硼聚合物电解质; 离子电导率; 甲基丙烯酸缩水甘油酯; 聚乙二醇甲醚甲基丙烯酸酯; 苯硼酸酐; 自由基聚合; 高倍率充放电; 锂离子超级电容器
0 引言
快速充放电电池等储能器件在航天及军事领域中的应用广泛。在太空飞行器中,理想的快速充放电电池不仅要有传统意义上的高比能量、高比功率,而且需具稳定性佳、安全性好、任意改变形状,将太阳能或其他能量进行存储与快速释放等性能。这就对快速充放电电池,尤其是其中的电解质提出了很高的要求。在过去的20年中,传统的基于液态电解质的锂离子技术虽有极大的优点,如室温下电导率大于10-3S/cm,电位窗口宽等,但由于液态电解质本身固有的不稳定性易造成严重的安全问题,如液态电解质的漏液、溶剂的挥发导致高温下分解,以及燃烧甚至爆炸等。使用聚合物电解质不仅可有效解决上述安全问题,而且便于加工微型化,提高能量密度,因此成为了研究重点[1-3]。
近年来,有关高性能聚合物电解质的研究取得了很大进展,主要研究的内容有新型聚合物合成、聚合物及聚合物电解质物理特性、电荷传输的理论模型建立,以及聚电解质/电极界面物理、化学特性等。研究者通过分子设计合成梳型、星型、交联、超枝化,以及嵌段等聚合物,改变其微观结构以提供离子快速传输的通道从而提高低温电导率等电化学性能[4-8]。此外,通过正、负离子的络合,能进一步提高离子电导率等电化学性能,即通过增强无机盐中正负离子的解离度提高离子电导率。方法有两种:一是通过络合、解络合离子实现;二是通过添加一种缺电子体络合无机盐中负离子,使正离子可快速传输。文献[9]报道了一种基于聚乙二醇(PEG)-硼酸酯的三臂凝胶聚合物电解质,研究发现:在硼酸酯的聚合物电解质中,PEG-硼酸酯既作增塑剂,又作Lewis酸,可与无机盐中的负离子相互作用,提高盐的离解程度。硼酸酯与负离子的络合程度越高,离子电导率相应就越高。文献[10]报道了PEG-硼酸酯对聚合物电解质的影响,作为一种Lewis酸,PEG-硼酸酯可产生稳定的循环性能并保持足够高的室温电导率(约10-4S/cm)。但作为航天应用中的超级电容器要求具高倍率充放电、宽电势窗口,以及高效的循环稳定性能、高比容量、高能量密度等特性,目前报道的研究成果仍难以满足上述要求。
对此,本文对一种新型含硼聚合物电解质合成进行了研究,通过调整聚合物微观结构以提供离子传输通道,利用缺电子有机质硼络合负离子促进锂盐解离提高锂离子的迁移数,使其在高低温下能保持高离子电导率、高离子迁移数和高能量密度,以便用于锂离子超级电容器。
1 实验部分
1.1 实验试剂与仪器
本文实验中所用主要试剂为:甲基丙烯酸缩水甘油酯,阿拉丁试剂有限公司(AR级);聚乙二醇甲醚甲基丙烯酸酯,阿拉丁试剂有限公司(MW 950);过氧化二苯甲酰,上海化学试剂有限公司(AR级);苯硼酸酐,萨恩化学技术(上海)有限公司(AR级);二氧化硅,国药集团化学试剂有限公司(粒径约15 nm);N’-N-二甲基甲酰胺,上海强顺化学试剂有限公司(AR级);高氯酸锂,上海中锂实业有限公司(电池级)。
本文实验及测试中所用主要仪器为:FA1104电子天平,上海天平仪器厂;81-2控温磁力搅拌器,上海司乐仪器厂;DHZ-6090真空干燥箱,上海医普晗精密设备有限公司;DHG-9036A恒温鼓风干燥箱,上海精宏实验设备有限公司;769YP-24B压片机,天津市科器高新技术公司;CHI660E电化学工作站,上海辰华仪器有限公司。
1.2 含硼聚合物电解质P(GMA-co-OEGMA)-B制备
所有实验均在温度(20±5) ℃、相对湿度小于2%的干燥环境中进行。以聚合物薄膜具备一定的力学性能又不会过硬以致电导率不佳(拉伸强度约5~20 MPa)为标准,反应条件定为单体/溶剂体积比=2∶3、投料摩尔比n(GMA)/n(OEGMA)=5∶1、引发剂过氧化二苯甲酰(BPO)用量为质量分数1%[11]。
制备具体步骤如下:将单体GMA(约1.43 g)和OEGMA(约1.92 g)、溶剂2MDMF-LiClO4(2 mol/L的N’-N二甲基甲酰胺-高氯酸锂溶液)2 mL加入容量瓶中,置于磁力搅拌器上搅拌30 min;分别投入质量分数3%,5%,10%的苯硼酸酐继续搅拌至其全部溶解并均匀分散在体系中;最后加入质量分数1%的BPO混合均匀后浇铸于PTFE模具中。将PTFE模具放入恒温干燥箱中于85 ℃、氮气保护的条件下分别反应2.5,3.0,3.5 h。最终得到含硼聚合物电解质薄膜,薄膜厚度为1~1.3 mm。反应机理如图1所示。

图1 P(GMA-co-OEGMA)聚合反应化学方程式Fig.1 Chemical equation of P(GMA-co-OEGMA) polymerization
1.3 红外光谱分析
实验仪器:用Nicolet 6700型傅里叶红外光谱仪对样品P(GMA-co-OEGMA)-B进行红外光谱测试,分辨率2 cm-1,频率范围为中红外400~4 000 cm-1。
1.4 形貌表征
采用扫描电子显微镜(SEM)对样品形貌进行观测,分辨率3.5 nm,放大倍数500~5 000。
1.5 热稳定性表征
用美国TA公司Q500型热重分析仪对样品的热稳定性进行测试。气氛条件为氮气,温度范围25~500 ℃,升温速率20 ℃/s。
1.6 恒、变温电导率测试
聚合物电解质电导率的测定采用三明治夹心结构模型,即将不同组分的含硼聚合物电解质膜P(GMA-co-OEGMA)-B置于两个不锈钢阻塞电极间,形成不锈钢电极/P(GMA-co-OEGMA)-B/不锈钢电极结构,用电化学工作站进行交流阻抗(EIS)测试,频率范围为1~1×106Hz,温度范围10~80 ℃,电压振幅10 mV/s。
1.7 循环伏安法测试(CV)
以还原氧化石墨烯为两电极材料,P(GMA-co-OEGMA)-B为聚合物电解质,组装成对称型超级电容器,测试其电化学性能。其中电极材料的制备过程为:活性物质(还原氧化石墨烯),粘结剂(聚偏氟乙烯PVDF),导电剂(乙炔黑)按质量比8∶1∶1混合,滴加溶剂N-甲基吡咯烷酮(NMP),室温下搅拌2~3 h使其分散均匀。采用市售泡沫镍作为集流体,将制备的混合液涂覆在直径1.6 cm的泡沫镍上,温度120 ℃下真空干燥24 h。然后将干燥的电极材料用红外压片机于3.0 MPa下压片得到还原氧化石墨烯电极材料。对称型超级电容器的组装:按正极/聚合物电解质/负极的顺序将制备的电极材料与聚合物电解质组装在2032型纽扣电池中。超级电容器循环伏安测试:扫描速率20 m V/s,电势窗口0~2.5 V。
1.8 长循环测试
对装配成的对称型超级电容器作3 000次的恒电流充放电长循环测试,扫描速率1 A/s,电势窗口0~2.0 V。
2 结果与讨论
2.1 宏观观察
图2是制备得到的含5%苯硼酸酐P(GMA-co-OEGMA)聚合物电解质膜如图2所示。由图2可知:该聚合物膜具有一定的透明度、柔韧性和可弯曲性能,厚度为1.6~2.0 mm。

图2 5%苯硼酸酐P(GMA-co-OEGMA)聚合物电解质膜Fig.2 Gel polymer electrolyte membrane of P(GMA-co-OEGMA) with 5% triphenylboroxin
2.2 红外光谱分析
苯硼酸酐,P(GMA-co-OEGMA)和含硼5%聚合物电解质P(GMA-co-OEGMA)-5% B的红外光谱如图3所示。由图3可知:在1 727 cm-1,1 251 cm-1和1 090~1 100 cm-1附近的3个峰表明了P(GMA-co-OEGMA)共聚物的存在;在1 601,1 441,701 cm-1的峰则与苯硼酸酐的红外峰相对应,加上位于1 386 cm-1处的峰应为-B-O-硼氧键特征峰,证明了产物中含有苯硼酸酐。此外,P(GMA-co-OEGMA)-5% B中有1个位于1 700 cm-1处的强峰,应为溶剂DMF的羰基峰。

图3 苯硼酸酐,P(GMA-co-OEGMA)和P(GMA-co-OEGMA)-5% B的FT-IR图Fig.3 Infrared spectra of triphenylboroxin, P(GMA-co-OEGMA) and P(GMA-co-OEGMA)-5% B
2.3 形貌分析
P(GMA-co-OEGMA)和含5%硼聚合物电解质P(GMA-co-OEGMA)聚合物电解质放大5 000倍的SEM图如图4所示。由图4可知:P(GMA-co-OEGMA)膜在数微米的尺寸下表面较平滑;加入苯硼酸酐后,聚合物链段表面即使在数微米的尺寸下也表现出凹凸不平的粗糙结构,推测这是由苯硼酸酐颗粒附着在聚合物链段上所致。这些微观表面上的粗糙结构使电解质膜的表面积大幅上升,对离子的吸附和传输有良好的贡献,从而大幅提升了离子电导率。

图4 P(GMA-co-OEGMA)和含5%硼聚合物电解质P(GMA-co-OEGMA)-5% B的SEM图Fig.4 SEM images of P(GMA-co-OEGMA) and P(GMA-co-OEGMA)-5% B
P(GMA-co-OEGMA)-5% B和P(GMA-co-OEGMA)-10% B的SEM图如图5所示。由图5可知:在相同放大倍率下,加入5%苯硼酸酐的聚合物电解质膜显得非常粗糙,还可见孔洞的存在,推测该螺旋型的孔洞是由于P(GMA-co-OEGMA)中GMA和OEGMA链间的诱导力使其互相吸引围绕成螺旋状的结构。但在苯硼酸酐的投料比增至10%后,粗糙孔洞的结构消失,分析可能是由于苯硼酸酐的投料量过多时,作为颗粒会发生团聚现象。

图5 P(GMA-co-OEGMA)-5% B和P(GMA-co-OEGMA)-10% B的SEM图Fig.5 SEM images of P(GMA-co-OEGMA)-5% B and P(GMA-co-OEGMA)-10% B
2.4 热稳定性分析
P(GMA-co-OEGMA)和P(GMA-co-OEGMA)-5% B的TGA图如图6所示。由图6可知:两条曲线的基本趋势相似,可见在200 ℃前P(GMA-co-OEGMA),P(GMA-co-OEGMA)-5% B均有25%~30%的失重,这是由于聚合物电解质中存有的少量溶剂挥发,也可能是聚合物中小分子的分解所致;在200~300 ℃,有一稳定的平台,表示在300 ℃前P(GMA-co-OEGMA)聚合物电解质膜相对较稳定;在约310 ℃处,失重率随温度的上升急剧增加,这是由温度过高而导致的聚合物分解、挥发所致。

图6 P(GMA-co-OEGMA)和P(GMA-co-OEGMA)-5% B的TGA图Fig.6 TGA images of P(GMA-co-OEGMA) and P(GMA-co-OEGMA)-5% B
比较两者可知:在加入苯硼酸酐后,升温过程中质量的损失均略高于未添加的P(GMA-co-OEGMA)聚合物电解质膜,推测原因可能为以下两点:一是苯硼酸酐小分子的分解损失;另一可能是由于苯硼酸酐的加入,分散在聚合物链结构中的小分子使P(GMA-co-OEGMA)的结构变得更松散,故在受热后较容易分解。尽管如此,P(GMA-co-OEGMA)-5% B发生剧烈分解并大量失重的温度亦在300 ℃以上,该结果表明本实验所制备的含硼聚合物电解质膜的热稳定性可高达300 ℃左右。
2.5 含硼聚合物电解质膜P(GMA-co-OEGMA)-B电化学测试
2.5.1 室温电导率
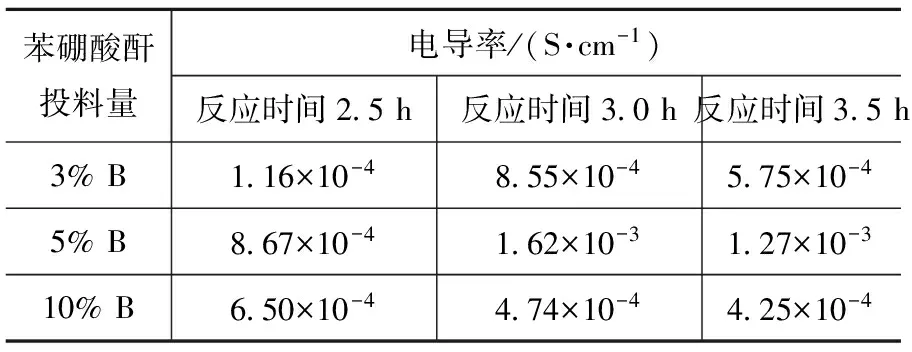
不同苯硼酸酐投料量与反应时间所得产物的室温电导率见表1。
表1 不同苯硼酸酐投料量与反应时间对产物的室温电导率
Tab.1 Electrical conductivity at room temperature with different amount of triphenylboroxin and reaction time
苯硼酸酐投料量电导率/(S·cm-1)反应时间2 5h反应时间3 0h反应时间3 5h3%B1 16×10-48 55×10-45 75×10-45%B8 67×10-41 62×10-31 27×10-310%B6 50×10-44 74×10-44 25×10-4
由表1可知:当反应时间为2.5 h时,加入3%的苯硼酸酐对电导率的提升略大于5%的苯硼酸酐,但在反应时间为3.0 h时含5%苯硼酸酐的聚合物膜的电导率却是含量为3%的两倍。这是因为随着苯硼酸酐加入量的增大,越来越多的苯硼酸酐小分子充填在反应体系中,在共聚物的聚合过程中使结构更为无序、松散,所以短的反应时间会影响体系的反应程度,反应程度不足会导致成膜性能不好,同时影响了电导率。
比较不同的反应时间,可发现加入5%苯硼酸酐的产物随反应时间的增加出现先增后减的趋势,这说明了当反应时间提高至3.0 h时,体系的反应程度最合适,电导率可高达1.62×10-3S/cm;若再升至3.5 h,则体系内反应程度过高,导致形成的产物近似于全固态的聚合物电解质,离子在其中的运动能力下降,从而电导率有所下降。又相较于含3%苯硼酸酐的试样,5%的即使在较高的反应程度下仍保有较高的电导率,可认为对这个体系,5%是苯硼酸酐最适合的投料量。
当加入10%的苯硼酸酐时,由表1可知电导率在各反应时间下电导率均是下降的,这可能是由于过多的苯硼酸酐小分子充填在聚合物结构中,加上其自身可能发生团聚,这就显著阻碍了离子在体系内的吸附迁移,最终结果显示电导率有所下降。
2.5.2 变温电导率测试
以电导率最佳的试样(苯硼酸酐含量5%、反应3.0 h)进行变温电导率测试并与PGMA,P(GMA-co-OEGMA)比较,结果如图7所示。由图7可知:加入苯硼酸酐后电导率大幅上升,与未添加苯硼酸酐的P(GMA-co-OEGMA)相比普遍提升约60%。此外,值得一提的是虽然聚合物电解质膜的电导率随温度降低而大幅减小,但在加入苯硼酸酐后电解质膜的低温电导率由5.52×10-4S/cm提升至1.09×10-3S/cm,提升了将近1倍,在低温条件下依然表现出优良的电导率性能。

图7 含硼聚合物电解质膜P(GMA-co-OEGMA)-5% B电解质膜的变温电导率Fig.7 Thermal conductivity test of gel electrolyte membrane P(GMA-co-OEGMA)-5% B
2.5.3 含硼聚合物电解质膜P(GMA-co-OEGMA)在超级电容器中的循环伏安表现
将制得的含硼聚合物电解质膜P(GMA-co-OEGMA)-5% B与石墨烯电极组装成超级电容器,在控制扫描速率20 mV/s下测试其在不同电位窗口下的C-V曲线,结果如图8所示。由图8可知:充放电的对称性较好,且在电位窗口达到近2.1 V时还保持相对稳定的状态,表明本文制备的聚合物电解质膜可在最高2 V左右的电压下稳定工作。

图8 P(GMA-co-OEGMA)-5% B组装成超级电容器的C-V图Fig.8 C-V curve of P(GMA-co-OEGMA)-5% B assembled into supercapacitor
2.5.4 含硼聚合物电解质膜P(GMA-co-OEGMA)在超级电容器中的长循环表现
将制得的含硼聚合物电解质膜P(GMA-co-OEGMA)-5% B与石墨烯电极组装成超级电容器后,用恒电流充放电法,在控制充放电速率1 A/s下测试其在2 V电位窗口下的3 000次长循环比电容保持率,结果如图9所示。其中:每隔60次循环取1个点计算其比电容保持率,结果发现在第一次的比电容为10.1 F/g下,前240次循环比容出现了一定的衰减,降至9.2 F/g,保持率为91.1%,而此后的衰减较稳定,循环3 000次时比电容降至8.4 F/g,保持率为83.2%。开始测试阶段出现较大衰减的原因可能是由于聚合物电解质膜中的电解液离子在较大电流的作用下与电极发生了界面反应,增大了接触电阻,另外电极片上部分结合不甚稳固的活性物质亦有可能因此脱落。

图9 P(GMA-co-OEGMA)-5% B组装成超级电容器的长循环Fig.9 Long cycle curve of P(GMA-co-OEGMA)-5% B assembled into supercapacitor
3 结束语
[1] FENTON D E, PARKER J M, WRIGHT P V. Complexes of alkali metal ions with poly (ethylene Polymer)[J]. Polymer, 1973(14): 589-591.
[2] QUARTARONE E, MUSTARELLI P. Electrolytes for solid-state lithium rechargeable batteries: recent advances and perspectives[J]. Chemical Society Reviews, 2011, 40(5): 2525-2540.
[3] AHMAD S. Polymer electrolytes: characteristics and peculiarities[J]. Ionics, 2009, 15(3): 309-321.
[4] BLOCH E, PHAN T, BERTIN D, et al. Direct synthesis of mesoporous silica presenting large and tunable pores using BAB triblock copolymers: influence of each copolymer block on the porous structure[J]. Microporous and Mesoporous Materials, 2008, 112(1-3): 612-620.
[5] ITOH T, GOTOH S, UNO T, et al. Properties of the cross-linked composite polymer electrolytes using hyperbranched polymer with terminal acryloyl groups[J]. Journal of Power Sources, 2007, 174(2): 1167-1171.
[6] IKEDA Y, MASUI H, SYOJI S, et al. Comb-shaped high molecular weight polyether consisting of oxyethylene units for polymer solid electrolyte[J]. Polymer International, 1997, 43(3): 269-273.
[7] ISHIKAWA M, MORITA M, IHARA M, et al. Electric double-layer capacitor composed of activated carbon fiber cloth electrodes and solid polymer electrolytes containing alkylammonium salts[J]. Journal of the Electrochemical Society, 1994, 141(7): 1730-1734.
[8] MOON S, LEE C, JIN B, et al. Ionic conductivities of cross-linked polymer electrolytes prepared from oligo (ethylene glycol) dimethacrylates[J]. Journal of Power Sources, 2000, 87(1): 223-225.
[9] KATO Y, YOKOYAMA S, YABE T, et al. Ionic conductivity and transport number of lithium ion in polymer electrolytes containing PEG-borate ester[J]. Electrochimica Acta, 2004, 50(2-3): 281-284.
[10] JIN Z, XIE K, HONG X, et al. Capacity fading mechanism in lithium sulfur cells using poly (ethylene glycol)-borate ester as plasticizer for polymer electrolytes[J]. Journal of Power Sources, 2013, 242: 478-485.
[11] APPECTECCHI G B, CROCE F, SCROSATI B. Kinetics and stability of the lithium electrode in poly (methyl methacrylate)-based gel electrolythes[J]. Electrochimica Acta, 1995, 40: 991.
Study on Polymer Electrolyte for Lithium Ion Supercapacitor
ZHANG Yi-fan1, YUAN Ping1, YANG Pei-yu1, TIAN Wen-sheng2, MA Xiao-hua2, LI Min1
(1. Department of Materials Science, Fudan University, Shanghai 200433, China; 2. Shanghai Institute of Spaceflight Power, Shanghai 200245, China)
The production and performances of boron-dopedpolymer electrolyte for lithium ion supercapactior were researched in this paper. With GMA and OEGMA as monomers, a polymer electrolyte (GMA-co-OEGMA) was produced by free radical polymerization. Furthermore, triphenylborox was added in for modification and P(GMA-co-OEGMA)-B was prepared. Properties of the P(GMA-co-OEGMA)-B were analyzed and results showed that P(GMA-co-OEGMA)-B expressed superior mechanical and thermal properties and wide potential window. Meanwhile, with great performances in thermal conductivity test, the maximum ionic conductivity value reached 1.62×10-3S/cm at room temperature. Compared with the traditional liquid electrolyte and solid electrolyte, the boron polymer electrolyte is able to avoid leakage, flammable, explosive and other security issues, as well as intimate high conductivity at room temperature, which meets the need of lithium ion super capacitor. In addition, with high safety, wide potential window, good conductivity at low temperature, the boron polymer electrolyte also has a certain application prospect in the aerospace field.
gel polymer electrolyte; ionic conductivity; glycidyl methacrylate (GMA); poly (ethylene glycol) methyl enther methacrylate (OEGMA); triphenylboroxin; free radical polymerization; high rate charge-discharge; lithium ion super capacitor
1006-1630(2017)03-0148-07
2016-12-06;
2017-01-25
上海航天科技创新基金资助(SAST2016110)
张一凡(1994—),男,硕士生,主要研究方向为锂离子电池与超级电容器,
TM53
A
10.19328/j.cnki.1006-1630.2017.03.020

