视安利胶囊的制备及其含量测定
★ 张婷彭红金鑫 肖飞 许军 邹文清 李佳君
视疲劳作为眼科中常见的疾病,是眼或者全身器质性因素与精神因素相互交织所引起的一组疲劳综合征, 患者的症状多种多样,常见为用眼后出现眼部不适、眼及眼眶周围疼痛、眼睛干涩、流泪、视物模糊、视觉障碍及头晕、恶心等全身症状[1-3]。如果这种视疲劳状态长期得不到调整和治疗,就会出现睫状肌痉挛,从而挤压眼内毛细血管,导致微循环障碍、视力下降而成为近视眼[4-5]。近年来,我国佩戴眼镜的人数呈现逐年增长趋势。因此保护视力、改善视疲劳已成为刻不容缓的问题。
视安利胶囊是以中医药理论为基础,并结合了现代药理学研究成果,以药效为主导研究开发的一种新复方制剂,用于缓解视疲劳和防治近视。其主要成分是莲子壳提取物原花青素及叶黄素,原花青素具有抗氧化性,能防止细胞被自由基破坏,保护和改善眼底微循环从而有效舒缓视疲劳[6]。而叶黄素是一种广泛存在于鲜花、水果、蔬菜等植物中的天然物质,属于“类胡萝卜素”物质。叶黄素是眼睛组织中的重要营养元素, 其本身是一种抗氧化物,能够有效促进眼部微循环, 并可以吸收蓝光等有害光线从而缓解眼睛干涩及视疲劳症状[7]。胶囊剂不仅能够掩盖药物不适的苦味,使其整洁美观便于吞服,而且能提高药物的稳定性,便于运输和保存[8],本文参考有关文献[9-11],将该复方制剂制成了便于患者服用的胶囊剂。现就视安利胶囊成型工艺及含量测定进行了如下探讨。
1 材料
Aglient1260高效液相色谱仪;HZT-A1000电子天平(上海嘉展仪器有限公司);GZX-9146MBE电热鼓风干燥箱(苏州豫通自动化电热设备有限公司);KQ-250E超声波清洗器(深圳超声仪器有限公司)。
原花青素对照品(樊克生物有限公司,纯度>95%,批号:20140628);叶黄素对照品(上海同田生物科技有限公司,纯度≧98%,批号:20140703);莲子壳提取物(实验室自制,原花青素含量为28.7%,批号:20140613);无水乙醇(辽宁东源药业有限公司);淀粉(辽宁东源药业有限公司);微晶纤维素、糊精(曲阜市药用辅料有限公司);二氧化硅(山西红日股份有限公司);硬脂酸镁(西安辅料股份有限公司);明胶空心胶囊(河南省商水县富源明胶有限公司);甲醇 (固安县华阳化工销售有限公司);乙腈 (天津盛通化工有限公司);纯化水为实验室自制三蒸水。
2 方法与结果
2.1 处方与工艺研究
2.1.1 辅料种类及用量的选择 选用淀粉、微晶纤维素、糊精、硬脂酸镁、二氧化硅作为辅料,均需过100目筛,组成不同处方考察流动性和吸湿性。
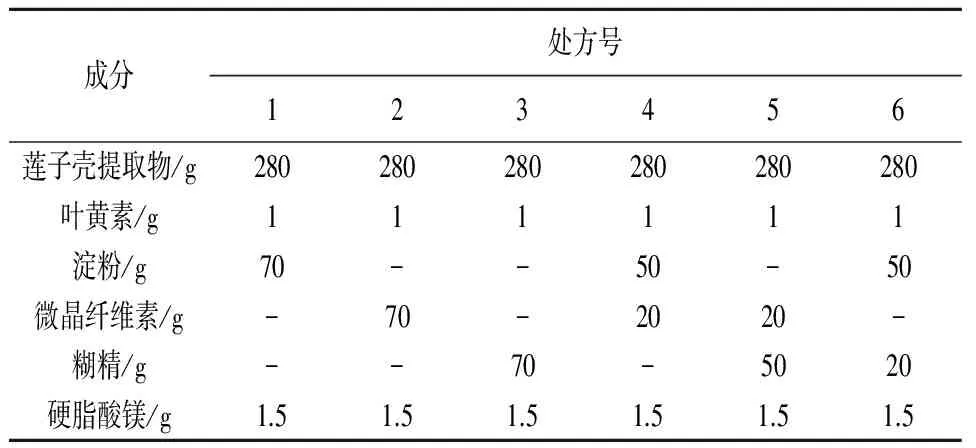
表1 不同辅料的配伍处方
2.1.1.1 不同处方休止角测定 采用固定漏斗法,将3只漏斗串联并固定最低端于距水平放置的坐标纸上1cm处,小心将按不同辅料制成的药粉沿漏斗壁倒入最上的漏斗中,直到坐标纸上形成的药粉圆锥体尖端接触到漏斗下口为止。由坐标纸测出圆锥体底部的直径2R(反复测定3次),己知圆锥体高H,计算休止角:tga=H/R,不同处方的休止角结果见表2。由表可知,6组处方的流动性均符合要求,但处方4,处方5的流动性较好。

表2 不同处方休止角的测定
2.1.1.2 不同处方吸湿率测定 将底部盛有氯化钠过饱和溶液的玻璃干燥器于25℃条件下恒温24h,此时干燥器内的相对湿度为75%。在己恒重的扁形称量瓶底部放入厚约2mm的药粉,精密称定,置于25℃,相对湿度为75%的恒温恒湿的玻璃干燥器内(称量瓶盖打开),分别于6、12、24、48h精密称定药粉重量,计算吸湿率,结果见表3,处方2,处方4的吸湿率较小,且结合表2的实验结果,说明处方4的流动性较好,吸湿率较低,因此确定处方为莲子壳提取物280g,叶黄素1g,淀粉50g,微晶纤维素20g,硬脂酸镁1.5g,二氧化硅2g,共制成1000粒。

表3 不同处方吸湿百分率的测定 %
2.1.2 润湿剂的选择 分别选择了40%、50%、60%和80%的乙醇作为润湿剂进行制粒工艺考察。试验过程中发现40%的乙醇与药粉混合后,药粉容易结成硬块,无法制粒;80%乙醇粘度太小,颗粒无法成型;60%乙醇,可以制粒,但细粉较多;50%乙醇可以满足制粒要求,因此,本实验采用50%乙醇, 并按30%比例加入到药粉中,制成软材后用24目筛制粒,45℃干燥3h后整粒。过65目筛除去细粉,即得粒度为24~65目的颗粒。
2.1.3 颗粒干燥时间的确定 在45℃下,分别干燥1、2、3、4、5h后,按照药典规定,测定颗粒中水分含量和原花青素的含量。结果见表4,结果表明,当颗粒的干燥时间超过3h后,颗粒的含水量已无明显变化,结合原花青素含量测定结果,选用3h为干燥时间。
2.1.4 颗粒干燥温度的确定 分别在25℃、35℃、45℃、55℃、65℃条件下,干燥3h,按照药典规定,测定颗粒中水分含量和原花青素含量。结果见表5,结果表明,当颗粒的干燥温度超过45℃后,颗粒的含水量已无明显变化,结合原花青素含量测定结果,选用45℃为干燥温度。
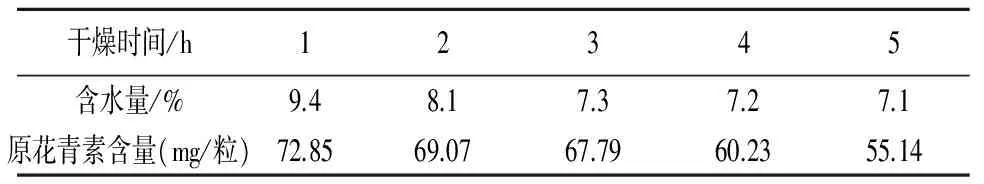
表4 不同干燥时间的试验结果(n=3)
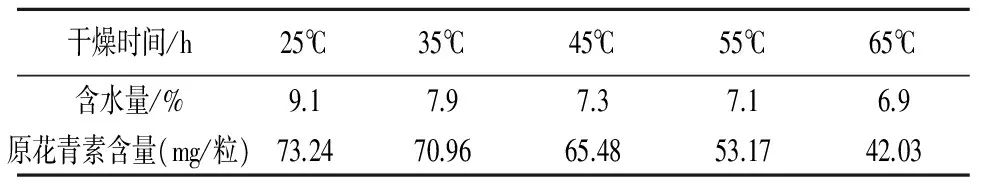
表5 不同干燥温度的试验结果(n=3)
2.1.5 颗粒休止角的测定 按2.1.1.1项下方法操作,测定颗粒的休止角,反复测定3次,计算休止角,结果颗粒的休止角为21.8°(<30°),表明经过制粒,颗粒的流动性更为良好。
2.1.6 颗粒吸湿率的测定 按照2.1.1.2项下方法操作,分别测定6、12、24、48、72h后颗粒的吸湿率,结果见表6。

表6 颗粒的吸湿率(n=3)
2.1.7 颗粒临界相对湿度的测定 取已干燥至恒重的颗粒1g,精密称定,置己恒重的扁形称量瓶中,分别置于盛有7种不同浓度硫酸和不同盐的过饱和溶液的干燥器内(称量瓶盖打开),于25℃恒温条件下保持48h后称量颗粒吸湿重量,计算不同相对湿度下的吸湿率,以相对湿度为横坐标,吸湿率为纵坐标,绘制吸湿曲线,结果见表7。由图可知,视轻松颗粒的临界相对湿度为75.0%。

表7 不同相对湿度下颗粒的吸湿百分率
2.1.8 颗粒堆密度的确定 取颗粒适量,精密称定,置10mL量筒内,将量筒上下振动5次,测定颗粒体积。己知颗粒质量m和体积V,根据公式P=m/V计算,颗粒的堆密度为0.64g/mL,物料容积0.55mL,可选择1号胶囊进行填充。
2.1.9 处方 根据预实验结果,确定处方为:莲子壳提取物280g,叶黄素1g,淀粉50g,微晶纤维素20g,硬脂酸镁2g,二氧化硅1.5g。
2.1.10 视安利胶囊的制备 按上述处方量将莲子壳提取物、叶黄素、淀粉、微晶纤维素、硬脂酸镁、二氧化硅采用等量递增法混匀,加入30%药粉量的50%的乙醇,约106mL制备成软材。将所制软材通过2号筛,挤压制粒,将颗粒在45℃干燥3h,用2号筛整粒,装1号胶囊,即得。
2.2 含量测定
2.2.1 原花青素的含量测定
2.2.1.1 色谱条件 色谱柱为Diamonsil C18柱(4.6 mm×250 mm, 5μm),DAD检测器;流动相为水∶甲醇∶异丙醇∶甲酸(65∶15∶10∶10 V/V);流速为1.0 mL/min;检测波长为525 nm,进样量20μL。
2.2.1.2 对照品溶液的制备 称取原花青素对照品约15mg,精密称定,置于10mL棕色瓶中,加甲醇溶解至刻度,摇匀,即得对照品储备液,从中精密量取1.0mL置于10mL棕色量瓶中,加甲醇溶液至刻度,摇匀,即得对照品溶液。
2.2.1.3 供试品溶液的制备 取本品内容物,用研钵研细,精密称定约0.2g内容物置于具塞锥形瓶中,精密加入25mL甲醇溶液,密塞后称重,超声(功率250W,频率40kHz)处理30min,取出后放冷,再次称重,用甲醇补足减失重量。摇匀,滤过,精密量取续滤液1mL置10mL容量瓶中,加甲醇至刻度,摇匀,即得。
2.2.1.4 阴性对照品溶液的制备 取按制剂“2.1.9”项下处方比例及“2.1.10”项下制备工艺除去莲子壳提取物的阴性样品,按“2.2.1.3”项下制备供试品的方法制备成阴性对照品溶液。
2.2.1.5 系统适应性实验 按“2.2.1.1”项下色谱条件进行HPLC分析,色谱图见图1。
2.2.1.6 标准曲线的制备 分别精密量取“2.2.1.2”项下的原花青素对照品储备液0.1,0.25,0.5,1.0,1.5,2.0 mL置10 mL棕色容量瓶中,加甲醇至刻度,混匀后按“2.2.1.1”项下色谱条件进行试验,分析数据,得标准曲线方程:Y=1.54X-17.02,r=0.9993(X为浓度,Y为峰面积)。结果表明,在浓度15.03~302.42μg/mL范围内线性关系良好。
2.2.1.7 精密度实验 取“2.2.1.2”项下对照品溶液,重复进样6次,记录其峰面积。计算RSD为0.45%,表明仪器精密度良好。
2.2.1.8 重复性实验 取本品内容物6份,按“2.2.1.1”项下色谱条件进行试验,结果表明原花青素的平均含量分别为标示量的100.48%,RSD为0.76% (n=6),表明该方法的重复性较好。
2.2.1.9 稳定性考察 取同一供试品溶液,室温放置,分别于0、4、8、12、18、24 h测定,记录原花青素的峰面积。原花青素的峰面积的RSD%为1.36% (n=5)。表明供试品溶液在24h内稳定性较好。

a.供试品;b.对照品;c.空白样品
2.2.1.10 加样回收率实验 取本品内容物6份,各约0.1g,精密称定,分别置具塞锥形瓶中,精密加入25 mL甲醇溶液,称定重量,超声(功率250W,频率40kHZ)处理30min,取出,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液1 mL,置10 mL量瓶中,分别加入对照品储备液0.5 mL,并加甲醇至刻度,摇匀,按“2.2.1.1” 项下色谱条件进行试验,测得平均回收率为100.5%。RSD为1.15%,表明方法的准确度良好。
2.2.1.11 样品含量测定 取10批不同视安利胶囊样品(标示装量为0.35g/粒),按“2.2.1.3”项下制备样品溶液的方法制备视安利胶囊样品溶液,按“2.2.1.1”项下色谱条件进行试验,用外标法计算含量。结果见表8。
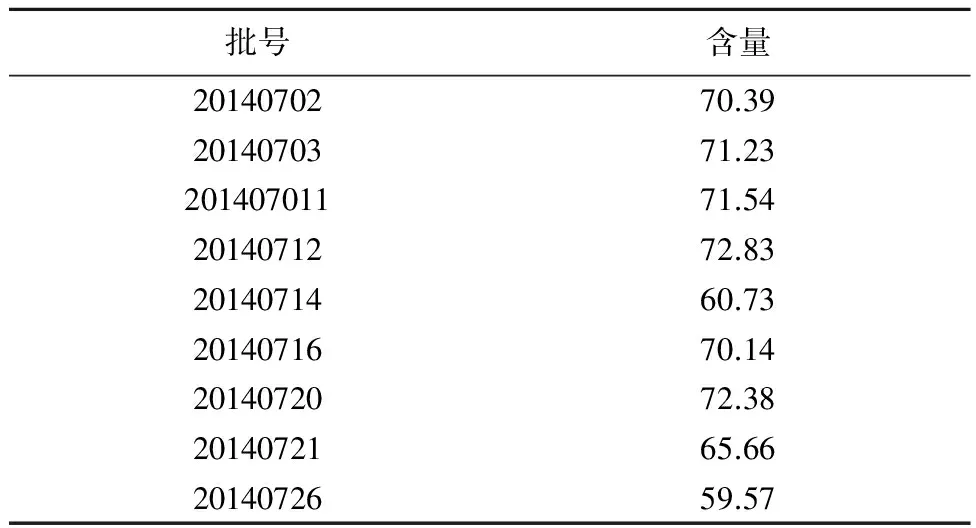
表8 样品中原花青素的测定结果(n=10) mg/粒
2.2.2 叶黄素的含量测定
2.2.2.1 色谱条件 色谱柱为Diamonsil C18柱(4.6mm×250mm,5μm),DAD检测器;流动相为甲醇∶水∶乙腈(15∶5∶80);流速:1.0 mL/min;检测波长:447 nm;进样量:20μL。
2.2.2.2 对照品溶液的制备 精密称取适量经P2O5干燥的叶黄素对照品,加流动相溶解后定量制成每1mL含24 μg的叶黄素对照品溶液,即得。
2.2.2.3 供试品溶液的制备 取本品内容物,研细,精密称定约0.2g,置具塞锥形瓶中,精密加入流动相25mL后密塞,称重,超声20min,放冷,再次称重,用流动相补足减失的重量,摇匀,滤过,即得。
2.2.2.4 阴性对照品溶液的制备 取按制剂“2.1.9”项下处方比例及“2.1.10”项下制备工艺,除去叶黄素的阴性样品,按“2.3.2.3”项下制备供试品的方法制备成阴性对照品溶液。
2.2.2.5 系统适应性实验 按“2.2.2.1”项下色谱条件进行HPLC分析,色谱图见图3。结果表明叶黄素的峰形良好,R值均大于1.5,n均大于7500,无拖尾现象。
2.2.2.6 标准曲线 分别精密吸取“2.2.2.2”项下对照品溶液0.5, 1.0, 2.0, 3.0, 4.0, 5.0mL 置10mL 棕色量瓶中, 加流动相稀释至刻度,摇匀,按“2.2.2.1”项下色谱条件测定叶黄素的峰面积,以峰面积积分值为纵坐标(Y),对照品浓度为横坐标(X),绘制叶黄素对照品的标准曲线,其回归方程为Y=80.45X+1.83,r=0.9997。结果表明, 叶黄素在浓度 5.23~49.76μg/mL范围内呈良好的线性关系。
2.2.2.7 精密度实验 取“2.2.2.2”项下叶黄素对照品溶液,按“2.2.2.1” 项下色谱条件连续进样6次,记录叶黄素峰面积,测得RSD%为0.71%,表明方法的精密度良好。
2.2.2.8 重复性实验 取同一批号的供试品,按“2.2.2.3”项下制备供试品溶液的方法平行制备5份供试品溶液,按“2.2.2.1”项下色谱条件下进行分析测定,记录叶黄素的峰面积。结果测得叶黄素的平均含量为标示量的99.7%,叶黄素峰面积的RSD%为2.2%,表明方法重复性良好。
2.2.2.9 稳定性实验 取同一供试品溶液,室温放置,分别于0、4、8、12、18、24 h测定,记录叶黄素的峰面积。测得RSD%为1.05%。表明供试品溶液在24h内稳定。
2.2.2.10 加样回收率实验 精密称取已知含量的样品(2.98mg/g)约0.1g,共6份,分别精密加入0.5mL叶黄素对照品溶液(0.6024mg/mL),然后按“2.2.2.3”项下方法制备供试品溶液,按“2.2.2.1”项下色谱条件测定叶黄素的含量,计算回收率。测得平均回收率为100.8%。RSD为0.73%,表明方法的准确度良好。

a.叶黄素对照品溶液 b.样品溶液 c.阴性对照溶液
2.2.2.11 样品含量的测定 取10批视安利胶囊样品,按“2.2.2.3”项下制备方法制备供试品溶液,经高效液相色谱分析,用外标法计算含量。测得三批样品中叶黄素含量见表9。故拟定视安利胶囊按干燥品计算,含叶黄素不得少于2.6mg/g。

表9 视安利胶囊中叶黄素的含量结果(n=10) mg/g
3 讨论
视安利胶囊是以莲子壳提取物原花青素及叶黄素为主要原料制备而成,用于缓解各种因素所引起的视疲劳症状。本文对视安利胶囊的制备工艺及其主药的含量进行了测定,为视安利胶囊的研究开发提供了科学、合理的药学研究资料。同时,也为缓解和调理眼部疲劳提供了一种新的制剂研究方法与思路。
本课题的研究仍有不足之处,原花青素为不同聚合度的聚合物,我们所得到是原花青素不同聚合度的混合物。而莲子壳提取物生物活性的高低与原花青素低聚物的含量有关,如何获得纯度较高的原花青素低聚物需要进一步研究。
[1]Kommerell G, Kromeier M, Scharff F, et al. Asthenopia,Associated Phoria, and Self-Selected Prism[J].Strabismus,2015,23(2):51.
[2]M A Riva, C Arpa and M Gioco. Dante and asthenopia: a modern visual problem described during the Middle Ages[J]. Eye,2014,28(4):498.
[3]Samuel O. Wajuihian. Frequency of asthenopia and its association with refractive errors[J]. African Vision and Eye Health,2015,74(1):1 001.
[4]张玉,杨先,姜丽萍,等. BMP-2在C57BL/6小鼠形觉剥夺性近视眼巩膜中表达的变化[J].国际眼科杂志,2016,16(3):423.
[5]林巧雅,周罕英,李学喜.近视与眼相对调节力的相关性研究[J].国际眼科杂志,2015,15(7):1 234.
[6]张慧文,张玉,马超美. 原花青素的研究进展[J].食品科学,2015(5):296.
[7]曹广美,赵桂森,贺艳丽. 叶黄素的视力保护作用及提取工艺[J].食品与药品,2012,14(5):199.
[8]张良,王燕斐,刘宏生,等.天然植物高分子药用胶囊的研究与发展[J].高分子学报,2013(1):1-10.
[9]刘莉,刘强.小儿热清按摩凝胶的制备及质量控制[J].中华中医药杂志,2010,25(3):431-433.
[10]李小万,陈文,周俊,等.葡萄籽多酚泡腾颗粒制备工艺及含量测定[J].中成药,2016,38(4):937-940.
[11]刘奇,张玲,郎玉麟,等. 郎氏扶正颗粒的制备及质量标准研究[J]. 中华中医药学刊,2014,32(1):196-199.

