利伐沙班的合成研究进展
李 杰,潘辛梅,赖永莉
(1. 四川卫生康复职业学院 药学系,四川 自贡 643000;2. 陆军军医大学第一附属医院 药学部,重庆 400038)
利伐沙班(拜瑞妥,Rivaroxaban),化学名5-氯-N- ( { ( 5S) -2-氧代-3-[4-( 3-氧代-4-吗啉基)苯基]-1,3-噁唑烷-5-基}甲基) -2-噻吩羧酰胺,是由德国拜耳公司和美国强生公司共同研制开发的一种新型口服抗凝血药物,属于Xa因子竞争性抑制剂类[1]。该药于2008年首次在加拿大和欧盟上市销售,次年进入中国市场,并在2011年7月正式被FDA批准用于患者膝和髋关节置换术后静脉血栓栓塞症的预防[2-3]。其主要作用机制为通过直接抑制Xa因子,中断凝血瀑布内源性及外源性途径,从而发挥抗凝血作用[4]。该药具有择性高,生物利用度好,副作用小和患者使用后出血风险低的优点,一经上市就获得临床上广泛的应用[5]。由于该药的应用前景较好,因此其合成工艺的生产研究也备受市场的广泛关注。本文根据合成原料及研制工艺的不同综述了利伐沙班(化合物1)及其两个重要中间体4-( 4-氨基苯基) -3-吗啉酮(2)和4-{4-[(5S)-5-(氨基甲基) -2-氧代-1,3-噁唑烷-3-基]苯基}吗啉-3-酮(3)的合成方法,并对其可能的工业化生产路线进行了总结。
1 4-( 4-氨基苯基) -3-吗啉酮(2)的合成
4-( 4-氨基苯基) -3-吗啉酮(2)的合成见图。
1.1 路线A
以4为原料,首先在碘化亚铜的催化下与2-氨基乙醇反应得到8,接着再与氯乙酰氯反应得到10,然后在氢氧化钠作用下完成环合得到15,再与硫酸/硝酸反应得到16,最后再经过催化氢化得到目标化合物2[6]。该方法原料易得,实验条件温和,但后处理繁琐,收率较低(32%),不利于工业化生产。
1.2 路线B
以4为原料,先在硫酸/硝酸条件下进行苯环上硝化反应得到5,然后以碘化亚铜作催化剂,与2-氨基乙醇反应得到9,接着再与氯乙酰氯完成酰化反应得到11,再在氢氧化钠作用下完成环合得到16,最后用雷尼镍或H2-Pd/C还原硝基得到目标化合物2[7]。该方法与前述路线A较为类似,虽然将苯环上的硝化反应放在前面进行,简化了后处理操作,且收率有一定提高(42%),但该方法重复性不强,先上硝基导致后面成环困难,因此不适合大规模工业化应用。
1.3 路线C
以4为原料制得9,经H2-Pd/C还原硝基后得到6,然后在三乙胺催化下与氯甲酸叔丁酯反应保护氨基得到7,在与氯乙酰氯反应后,在氢氧化钠作用下得到14,随后再脱掉叔丁氧羰基得到目标化合物2[8]。该方法反应简单,条件温和,具有一定的应用价值。
1.4 路线D
以4为原料制得9,与过量的氯乙酰氯反应后得到12,再经H2-Pd/C还原硝基得到13,最后在氢氧化钠作用下得到目标化合物2[9]。该方法与前述路线C类似,但减少了氨基保护和脱保护两步反应,使其更加适合工业化应用。
1.5 路线E
以17为原料,与环氧乙烷反应得到18,再在叔丁醇钾的作用下与氯乙酸乙酯反应得到15,然后再按照路线B所述方法得到目标化合物2[10]。15也可经17与1,4-二噁烷-2-酮在高温高压下直接反应制得[11],但该操作危险性较大,不建议采用。总的来说,该路线原料廉价易得,但苯胺毒性较大且遇明火高度可燃,不适宜于工业化应用。
1.6 路线F
以19为原料,在乙腈做溶剂的条件下与吗啉反应得到20,然后再经高锰酸钾氧化吗啉环得到16,最后经催化氢化得到目标化合物2[12-13]。19也可直接在钠氢和N-甲基吡咯烷酮(NMP)的作用下与3-吗啉酮反应得到16[14]。但前种方法在进行高锰酸钾氧化时,所产生的副产物较多,分离纯化难度较大,导致收率降低,而后种方法虽然简化了反应步骤但所用试剂相对较贵且用到了反应活性较高的钠氢,在工业生产上具有一定的危险性,因此该方法整体上也不适合工业化应用。
1.7 路线G
以21为原料,与5-氯-2,3-二氢-1,4-二氧杂环己二烯或2-( 2-氯乙氧基)乙酰氯反应得到22,然后在碳酸钾作用下完成环合得到16,最后经催化氢化得到目标化合物2[15-16]。该反应虽然反应步骤较短,但所用试剂价格昂贵,不易制备,尤其是5-氯-2,3-二氢-1,4-二氧杂环己二烯的制备更为复杂,难以大量获得,因而限制了其工业化应用。
1.8 路线H
以23为原料,在碘化亚铜催化下,以N, N -二甲基己二胺为溶剂,直接与3-吗啉酮反应得到目标化合物2[17]。该路线是合成化合物2所有路线中最短的一条,但其所用试剂价格昂贵,原料难以获得,后处理工艺复杂繁琐,收率不高,限制了其工业化应用。
2 4-{4-[(5S)-5-(氨基甲基) -2-氧代-1,3-噁唑烷-3-基〗苯基}吗啉-3-酮(3)的合成
4-{4-[(5S)-5-(氨基甲基) -2-氧代-1,3-噁唑烷-3-基]苯基}吗啉-3-酮(3)的合成见图2。
2.1 路线1
2与28在乙醇的作用下反应得到24,然后以4-二甲氨基吡啶(DMAP)做催化剂,与N'N-羰基二咪唑(CDI)反应构建噁唑环得到25,再在氢氧化钠碱性条件下水解酯键得到26,随后与对甲苯磺酰氯反应得到27,再与邻苯二甲酰亚胺反应得到31,最后与甲胺反应得到目标化合物3[18-19]。该路线反应步骤繁琐,试剂应用复杂,虽然每一步收率较高,但总收率偏低,工业化应用前景不大。
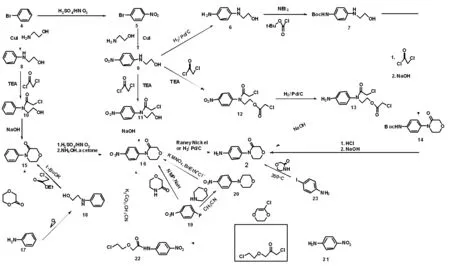
图1 中间体2的合成路线Fig.1 Synthetic methods of compound 2
2.2 路线2
2与29在乙醇的作用下反应得到30,后再经DMAP和CDI作用构建噁唑环得到31,最后与甲胺反应得到目标化合物3[20-24]。该反应虽步骤简短,但其所用试剂N-环氧丙基邻苯二甲酰亚胺(29)在工业上制备困难,价格昂贵,因此限制了本方法在工业上的应用。
2.3 路线3
2与(S)-环氧氯丙烷(46)在甲醇的作用下反应得到32,随后在CDI作用下得到33,再以DMF作溶剂与邻苯二甲酰亚胺钾盐反应得到31,最后再与甲胺反应得到目标化合物3[25]。32也可先与邻苯二甲酰亚胺钾盐反应得到34后再与CDI反应构建噁唑环得到31[25]。该路线反应条件温和,原料价廉易得,操作简单,无论是先成环还是后成环都有较高的收率,具有大规模工业化应用价值。
2.4 路线4
2与三光气反应得到35,随后在四氢呋喃(THF)溶液中与碘化镁反应得到化合物36,接着与叠氮化钠反应后再用氢气钯碳还原叠氮基得到目标化合物3[26]。该路线反应步骤简单,但所用试剂均价格昂贵,叠氮化钠与三光气均属于易爆物品,工业应用危险性较大,因此使本路线仅适用于实验室合成,而不适合工业化生产。
2.5 路线5
2经酰化反应后得到酰胺化合物37,随后与38在甲醇锂或叔丁醇锂的作用下得到39,最后用盐酸水解亚胺得到目标化合物3[27-28]。该路线虽然反应步骤简短,但其所用的醇锂试剂化学性质十分活泼,易挥发、易燃烧,毒性较大,且反应要求较高,反应条件苛刻,具有一定危险性,不适合工业化应用。
2.6 路线6
2与氯甲酸苄酯(40)反应得到41,在THF作溶剂的条件下与(S)-3-氯-1,2-丙二醇(42)反应得到43,最后再用乙醇作溶剂,与羟胺反应得到目标化合物3[29-32]。该路线步骤较短,但所用试剂同样存在毒性大,价格昂贵等缺点,也不适合工业化应用。

图2 中间体3的合成路线Fig.2 Synthetic methods of compound 3
2.7 路线7
2与(S)-2,3-环氧-1-丙醇(44)反应得到45,随后在二碳酸二叔丁酯与甲醇钠的作用下得到43,再按上述2.6方法得到目标化合物3[29,33]。该方法反应条件温和,试剂应用简单,但后处理较复杂,收率不高,经过工艺优化以后可能有助于工业化应用。
2.8 路线8
46与叠氮化钠和氯化铵在甲醇溶液中反应得到47,随后与碳酸钾溶液反应得到叠氮环氧化合物48,在异丙醇的作用下与2反应得到49,再与CDI反应成环得到50,最后经催化氢化得到目标化合物3[34]。该反应步骤繁琐,反应过程中也涉及叠氮化合物的应用与处理,操作危险性较大,难以实现大规模生产。
2.9 路线9
36与碘化钠反应得到碘代化合物51,随后与乌洛托品反应得到52,最后在酸性条件下水解得到目标化合物3[35]。该反应所用原料须经多步反应制得,价格昂贵,虽然步骤简短,但增加了生产成本,不适合工业化生产。
2.10 路线10
2-氨基乙醇(53)与丙酸乙酯(54)在钠氢的作用下得到吗啉酮(55),然后在碘化亚铜和1, 2-环己二胺(57)的作用下与溴苯(56)反应得到58,再经N-溴代丁二酰亚胺(NBS)溴代得到59;(S)-环氧氯丙烷(46)与氰酸钠反应得到60,再与邻苯二甲酰亚胺钾盐在DMF中反应得到61,然后61与59在碘化亚铜和57作用下得到31,最后与甲胺反应得到目标化合物3[36]。该路线试剂应用复杂,反应条件苛刻,步骤较多,收率偏低,需进一步工艺优化以后再考虑是否适合大规模生产。
3 利伐沙班(化合物1)的合成
利伐沙班(化合物1)的合成见图3。
3.1 方法A
2与(S)-环氧氯丙烷(46)在异丙醇作用下得到63,再与N,N-二异丙基乙胺和氯化苄(66)反应得到67,,随后与叠氮化钠反应得到64,再经磷酸和三苯基膦还原叠氮基得到65,与5-氯噻吩-2-甲酰氯(69)反应后得到68,最后用三光气脱去苄基得到终产物1[37]。该方法反应步骤较多,所用试剂较昂贵且反应危险性较高,特别是氯化苄,与空气接触后易形成爆炸性混合物,此外该试剂还具有潜在致癌性和致突变性,毒性较大,因此极大地限制了该方法的工业化应用。
3.2 方法B
2与70在高氯酸锂的作用下得到71,再经CDI成环得到终产物1[38-40]。该方法所使用的高氯酸锂价格昂贵,易制爆,属于管制化学品,且该方法收率不高,因而也难以进行大批量生产。
3.3 方法C
2与氯甲酸甲酯(72)反应得到73,在钠氢和DMF的作用下与46反应得到74,最后与5-氯噻吩-2-甲酰胺(75)在氯化锂和叔丁醇钾的作用下得到终产物1[41]。该方法反应步骤虽短,但其后两步反应条件较苛刻,后处理难度较大,成本较高,难以实现大规模工业化应用。
3.4 方法D
以乙腈作溶剂,76与氯甲酸乙酯反应得到77,再与5-氯噻吩-2-甲酰氯反应得到78,最后在乙醇和乙腈的作用下得到终产物1[42]。该方法所用原料并非是现有工业原料,是由多步反应制备所得且制备成本较大,使该方法仅限于实验室研究,不具备工业化价值。
3.5 方法E
69与(R)-3-氨基-1,2-丙二醇盐酸盐(79)反应得到80,随后与溴化氢反应得到81,再与2反应得到82,最后经光气和CDI成环得到终产物1[31,43-44]。该方法反应条件温和,所用试剂价廉易得,收率较高,唯一的缺点是用到了毒性剧烈且具有强腐蚀性的光气,因而限制了其进一步工业化应用。
3.6 方法F
69与3-氨基丙烯(83)在吡啶和THF的作用下反应得到84,随后在二氯甲烷(DCM)中与间氯过氧苯甲酸(m-CPBA)反应得到85,再与2反应得到82,最后经3.5所述得到终产物1[45]。该方法除用到光气以外还用到了另一个高度危险的3-氨基丙烯,其不仅毒性剧烈且极易燃烧,此外所需反应条件也较苛刻,几乎不具备大规模工业化生产价值。
3.7 方法G
由中间体3与5-氯噻吩-2-甲酰氯(69)直接反应得到终产物1[20-30]。该方法是目前工业化生产的主流方法,其反应条件简单,收率较高,但要制得中间体3则需多步反应,制备工艺也相当复杂多样,因此完成此反应的关键是要找到制备中间体3的最优方法。
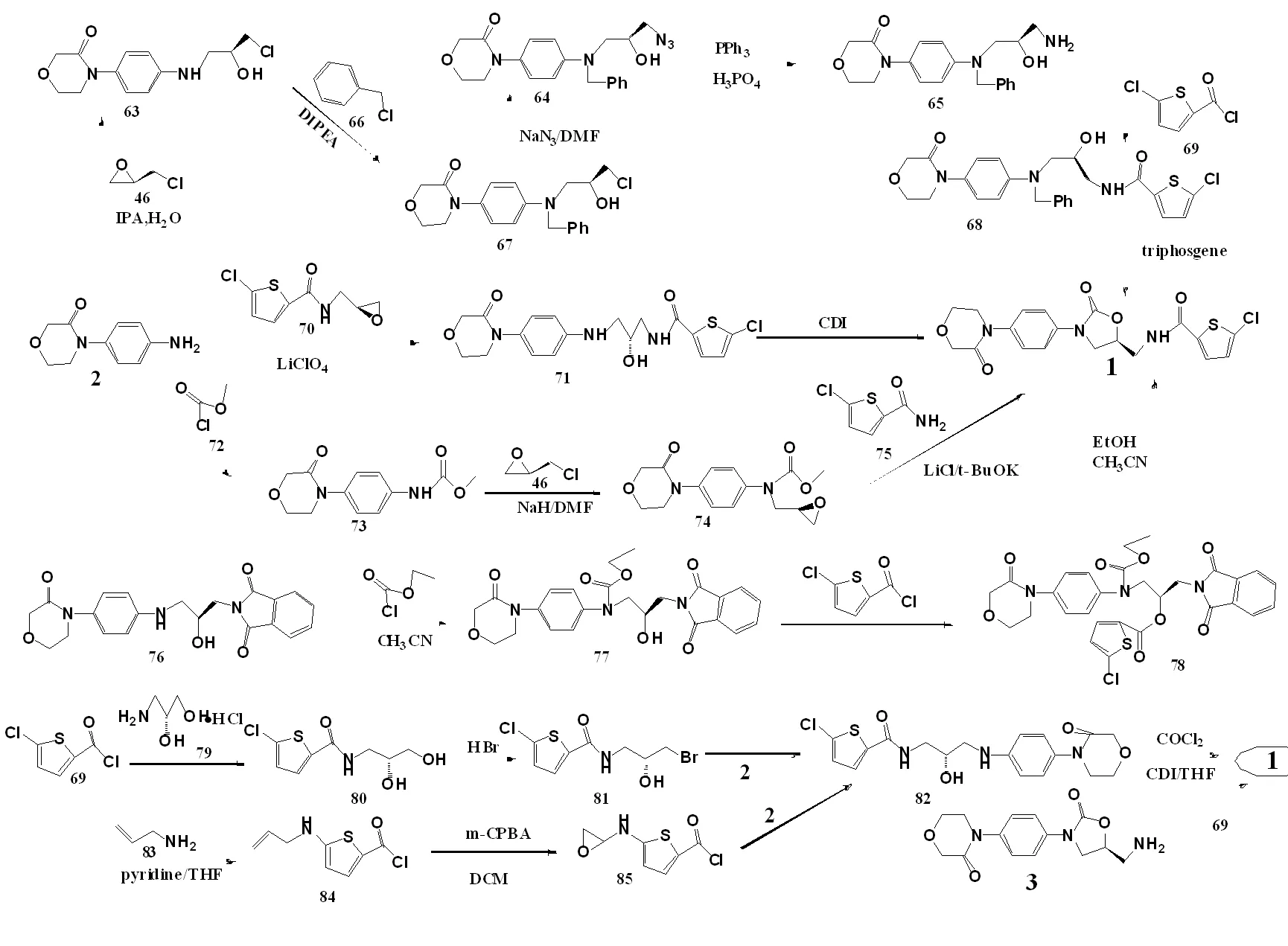
图3 利伐沙班的合成路线Fig.3 Synthetic methods of Rivaroxaban
4 结语
综上所述,目前报道的新型口服抗凝血药利伐沙班的各合成方法均有不足之处,按照1.3或1.4所述制备中间体2,再按2.3所述制备中间体3,最后按3.7所述制备终产物利伐沙班(1)的方法可能具有大规模工业化应用前景。但该路线依然存在反应步骤较多,试剂应用复杂,实验过程难以控制等问题,因此,该工艺仍然需要进一步改进和优化。
[1] 刘 薇,董金华.利伐沙班(rivaroxaban)[J].中国药物化学杂志,2011,(06):508,510.
[2] 杨礼庆,王 程,沈 涛,等. 口服利伐沙班预防人工全髋关节置换术后深静脉血栓的临床研究[J]. 中国临床药理学杂志,2013(04):260-262.
[3] 庞家莲,蒙光义. 利伐沙班临床研究与应用进展[J].内科,2012(04):389-391.
[4] 冯 冰.利伐沙班在我国血栓高风险患者中群体药代动力学及药效动力学研究[D].北京:北京协和医学院, 2015.
[5] 周 健,刘忠达,林伟龙.髋关节置换术后利伐沙班预防下肢深静脉血栓的疗效与安全性[J]. 中国临床药理学杂志,2015(12):1106-1108.
[6] 王国华.抗凝血新药利伐沙班中间体4-(4-氨基苯基)-3-吗啉酮合成工艺研究[D]. 广州:广东药学院,2009.
[7] 罗玲艳,申东升,周宗洲,等.4-(4-氨基苯基)-3-吗啉酮的合成[J]. 中国医药工业杂志,2011(02):93-95.
[8] 宋明熙,徐 斌,张飞飞,等.一种4-(4-氨基苯基)-3-吗啉酮的合成方法:CN,105111163 A[P].2015-12-02.
[9] 戴 川,赵圣轩,陈宇瑛.4-(4-氨基苯基)-3-吗琳酮的合成[J]. 华西药学杂志,2015(06):642-644.
[10] 张 胜.一种利伐沙班中间体4-(4-氨基苯基)-3-吗啉酮的制备方法:CN,104829551A[P].2015-08-12.
[11] GLICKMAN S A,EASTON,SCHULTZ H S,et al.Preparation of N-substituted-3-morpholones:US,3092630[P].1963-06-04.
[12] DIETER D,WERNER M,CHRISTOST,et al.Phenyl derivatives:WO,2002057236[P].2002-07-25.
[13] MASSE C E. Substituted oxazolidione derivatives:WO,2009023233[P].2009-02-19.
[14] STRAUB A,LAMPE T,POHLMANN J,et al.Substituted oxazolidinones and their use in the field of blood coagulation:WO,0147919[P].2001-07-05.
[15] 袁 静,黄长江,张俊伟,等.利伐沙班的合成[J].中国新药杂志,2010,19(23):1385-1387.
[16] Mederski W W K R,Cezanne B,van Amsterdam C,et al.Chlorothiophenecarboxamides as P1 surrogates of inhibitors of blood coagulation factor Xa[J].Bioorganic & medicinal chemistry letters,2004,14(23):5817-5822.
[17] SONG Y H,ZHU B Y,WANG S M,et al.Use as factor Xa inhibitors:WO,2006063113[P].2006-06 -15.
[18] DWIVEDI SHRIPRAKASH DHAR,PRASAD ASHOK,PAL DAYA RAM,et al.Processes and intermediates for preparing rivaroxaban:US,2014378682[P].2014-12-25.
[19] DWIVEDI SHRIPRAKASH DHAR,PRASAD ASHOK,PAL DAYA RAM,et al.Processes and intermediates for preparing rivaroxaban:WO,2013098833[P].2013-07-04.
[20] STRAUB ALEXANDER,LAMPE THOMAS,POHLMANN JENS,et al.Substituted oxazolidinones and their in the field of blood coagulation: US, 2003153610[P].2003-08-14.
[21] BERWE MATHIAS,THOMAS CHRISTIAN,REHSE JOACHIM,et al.Preparation process:US,2005182055[P].2005-08-18.
[22] MATHAD VIJAYAVITTHAL THIPPANNACHAR,PATIL NILESH SUDHIR NILESH,NIPHADE NAVNATH CHINTAMAN NAVNATH,et al.A process for preparation of rivaroxaban and intermediates thereof:WO,2013121436[P].2013-08-22.
[23] FERRARI MASSIMO,GHEZZI EMANUELE,GHEZZI MARCELLO.Process for the synthesis of rivaroxaban and intermediate for the production thereof:WO,2015198259[P].2015-12-30.
[24] RAO DHARMARAJ RAMACHANDRA,MALHOTRA GEENA,PULLELA VENKATA SRINIVAS,et al.Process for the preparation of rivaroxaban:WO,2016030669 [P].2016-03-03.
[25] MOHAN RAO DODDA,KRISHNA REDDY PINGILI,ANNA REDDY AMBATI,et al.Processes for the preparation of 4-{4-[5(s)-(aminomethyl)-2-oxo-1,3-oxazolidin-3-yl]phenyl} morpholin-3-one:WO,2012032533[P].2012-03-15.
[26] Li C,Liu Y,Zhang Y,et al.An approach to the anticoagulant agent rivaroxaban via an isocyanate-oxirane cycloaddition promoted by MgI2.etherate[J].Journal of Chemical Research,2011,35(7):400-401.
[27] BERZOSA RODRíGUEZ XAVIER,MARQUILLAS OLONDRIZ FRANCISCO,LLEBARIA SOLDEVILLA AMADEO,et al.Process for obtaining rivaroxaban and intermediate thereof:US,201412860[P].2014-05-08.
[28] BERZOSA RODRíGUEZ XAVIER,MARQUILLAS OLONDRIZ FRANCISCO,LLEBARIA SOLDEVILLA AMADEO,et al.Process for obtaining rivaroxaban and intermediate thereof:WO,2012159992[P].2012-11-29.
[29] MOHAN RAO DODDA, VENKAT REDDY BUTHUKURI.Processes for the preparation of 5-chloro-n-({(5s)-2-oxo-3-[4-(3-oxo-4-morpholinyl)phenyl] -1,3-oxazolidin-5-yl}methyl)-2-thiophene-carboxamide and intermediates thereof:WO,2013105100[P]. 2013-07-18.
[30] MOHAN RAO DODDA,KRISHNA REDDY PINGILI, VENKAT REDDY BUTHUKURI.Processes for the preparation of 5-chloro-n-({(5s)-2-oxo-3-[4-(3-oxo-4-morpholinyl) phenyl] -1,3-oxazolidin-5-yl} methyl)-2-thiophene-carboxamide and intermediates thereof:WO,2013046211[P].2013-04-04.
[31] SANDOZ A G.Method for the preparation of rivaroxaban:EP,2354128[P].2011-08-10 .
[32] STURM HUBERT,DE SOUZA DOMINIC,KNEPPER KERSTIN,et al.Method for the preparation of rivaroxaban:WO,2011098501[P].2011-08-18.
[33] 徐在春,杜成铭,王明林,等.一种利伐沙班中间体的制备方法:中国,105566310[P].2016-05-11.
[34] BHEMIREDDY SATYANARAYANA REDDY,PAIDIMARLA V VARA PRASADA REDDY,YARAPATHI VENKAT REDDY.Process for preparation of oxazolidinone derivatives:WO,2014170908[P].2014-10-23.
[35] STURM HUBERT,KNEPPER KERSTIN. Method for the preparation of substituted oxazolidinones:WO,2012140061[P].2012-10-18.
[36] 侯俊凯,王乐会,李 华.一种利伐沙班的制备方法:中国,105801572[P].2016-07-27.
[37] KUMAR AGARWAL VIRENDRA,RAMESHCHANDRA UPADHYAY ASHISH,MANSUKHLAL THUMAR NILESH,et al.A process for the preparation of rivaroxaban:WO,2015026761[P].2015-02-26.
[38] HIRPARA KETAN,SINGH PANKAJ KUMAR,JESUNADH KDV,et al.Process for the preparation of rivaroxaban:WO,2015011617[P].2015-01-29.
[39] SINGH PANKAJ KUMAR,HASHMI MOHAMMED SALMAN,SACHDEVA YOGINDER PAL,et al.Process for the preparation of rivaroxaban and intermediates thereof:WO,2013156936[P].2013-10-24.
[40] ROEHRIG SUSANNE,POHLMANN JENS,PERZBORN ELISABETH,et al.Imino-oxazolidines and use thereof:US,2010048548[P].2010-02-25.
[41] BODHURI PRABHUDAS,WEERATUNGA GAMINI.Processes for the preparation of rivaroxaban and intermediates thereof:US,7816355[P].2010-10-19.
[42] BODHURI PRABHUDAS,WEERATUNGA GAMINI.Processes for the preparation of rivaroxaban and intermediates thereof:WO,2012051692[P].2012-04-26.
[43] ISHIBUCHI MASATAKE,HIKAWA HIDEMASA,TARAO AKIKO,et al.Pharmaceutical composition containing new amide derivative:JP,2011246461[P].2011-12-08.
[44] 张爱华,宋兴昌,刘小红,等.一种利伐沙班的制备方法:中国,103951661[P].2014-07-30.
[45] 肖柑媛,李 岩,邓 勇,等.N-环氧丙基-N-酰基苯胺类化合物其制备方法和用途:中国,104860904[P].2015-08-26.

