单向免疫扩散测定四价流感病毒裂解疫苗中两种B型血凝素含量
帅旗 余军 杨文彬 吴富强 吴建华 蒋正东 杨宪普 赵越 赵静 付建林225300泰州,江苏金迪克生物技术有限公司
四价流感病毒裂解疫苗包括两种A型病毒株(H1N1和H3N2)和两个谱系的B型(B/Victoria和B/Yamagata)株。根据 2001—2002年到 2010—2011年11个流感季节中原使用三价流感疫苗中根据流行预估选择一个谱系的B型病毒株制备该流行季疫苗,仅6次预估正确[1-4],世界卫生组织在2012年2月提出了一项关于四价流感疫苗应包括两种B型谱系毒株的建议。江苏金迪克生物技术有限公司于同年完成四价流感病毒裂解疫苗的实验室研究,通过优化生产工艺,建立了成熟、稳定、可靠的生产程序,制备四价流感病毒裂解疫苗[3],并完成了Ⅲ期临床试验。该公司制备的四价流感病毒裂解疫苗由生产的H1N1、H3N2、B1和B2四种病毒型别单价原液,其效力指标是准确测定各种血凝素抗原含量,每株血凝素含量约为33μg/ml,合格产品每1 ml中各型流感病毒株血凝素含量应为配制量的80%~120%。
本研究旨在探究使用传统的单价参考品抗原,SRID是否能准确反映四价疫苗中两种谱系的B型血凝素抗原含量;两种谱系血凝素抗原是否有交叉;在原三价疫苗中的血凝素成分对新增加的B型病毒血凝素抗原浓度检测是否有影响。
1 材料与方法
1.1 材料
1.1.1 流感病毒株:本试验中所使用的流感病毒株是:A1(A/California/7/2009,NYMCX-179A)、A3(A/Hong Kong/4801/2014,NYMCX-263B)、B1(B/Brisbane/60/2008,NYMC BX-35)、B2(B/Phuket/3073/2013,B/Phuket),均从英国国家生物标准与控制研究所(NIBSC)引进。
1.1.2 标准品:标准抗原:A1(A/California/7/2009,H1N1pdm,NYMCX-179 A)批号为 13/164、A3(A/Hong Kong/4801/2014,NYMCX-263B)批号为15/230、B1(B/Brisbane/60/2008)批号为 13/234、B2(B/Phuket/3073/2013)批号为14/252;标准抗血清:A1(A/California/7/2009)批号为14/310、A3(A/Hong Kong/4801/2014)批号为 16/100、B1(B/Brisbane/60/2008)批号为15/312和13/254、B2(B/Phuket/3073/2013)批号为14/248。以上标准品均购于英国NIBSC。
1.1.3 主要试剂:琼脂糖购自Invitrogen公司,裂解剂3-磺甲基十四烷基二甲铵(N-tetradecyl-N,N-dinethyl-3 ammonio-1-propanesulfonate)(商品名为zwittergent)购自美国Sigma公司,考马斯亮蓝购自国药集团化学试剂有限公司。
1.2 实验方法
1.2.1 单向免疫扩散法:采用SRID测定血凝素含量,将B型病毒特异性抗血清,如B1 875μl或250 μl、B2 350μl,分别添加于融化并冷却至56℃的25 ml 1.5%琼脂糖中,混匀后平铺于10 cm×10 cm规格的玻璃板,凝固后垂直打孔,孔径为3 mm。待检样品/抗原参考品与10%裂解剂按9∶1体积比充分混合后,于室温20~25℃放置30~90 min使其裂解。裂解后的血凝素抗原按实验设计加样,每孔为10μl;每种血凝素抗原,包括参考品或待测样品,每个稀释度至少重复两孔,加样后的凝胶板水平置于20~25℃湿盒内18~24 h,经浸泡,干燥,考马斯亮蓝染色并脱色后,抗原与特异性抗血清反应会在胶膜上形成清晰的、蓝色的免疫沉淀环。测量沉淀环的直径,对应于标准抗原制作的线性回归方程,算出样品的血凝素抗原含量。
1.2.2 常规浓度干扰试验:在每个B1血清琼脂糖板(简称为血清板),每次加入B1标准品抗原对照、B1单价样品、B1+B2混合单价样品。标准品和样品分别稀释至血凝素终浓度为 10、20、30、40μg/ml。在每个B2血清板,每次设B2标准品抗原对照、B2单价样品、B1+B2单价样品。两者稀释方法同上。根据B1或B2标准抗原浓度作直线回归,分别求出直线回归方程,带入相应的样品沉淀环直径,得出其血凝素含量,试验重复3次,求平均值、标准差(SD)和变异系数(CV)。
1.2.3 高浓度干扰试验:配制三价流感疫苗(含A1A3B1或A1A3B2)为基质,其各种血凝素含量是商品苗的二倍66μg/ml,以体积比1∶1加入另一B型病毒连续稀释的血凝素中,混合后其三价疫苗各种血凝素终浓度为33μg/ml,使用高浓度的B型血凝素进行观察。待观察的B1血凝素终浓度分别为115、100、75、50、40、30、20、10 μg/ml,B2 血凝素样品终浓度分别为 140、120、100、75、50、40、30、20、10 μg/ml。
固定一个谱系B型病毒血凝素终浓度为30 μg/ml,分别加入另一个谱系不同稀释度的B型血凝素,B1 血凝素含量分别为 115、100、75、50、40、30、20、10 μg/ml,B2 血凝素含量分别为 140、120、100、75、50、40、30、20、10 μg/ml。
在B1血清板上,加入的B2血凝素含量由高到低浓度依次为 280、240、200、250、200、80、60、40、20 μg/ml,在B2血清板上加入的B1血凝素浓度分别为 230、200、150、100、80、60、40、20 μg/ml。
同时标准B1或B2血凝素抗原分别稀释至160、100、80、60、40、30、20、10 μg/ml,以其沉淀环的直径对其相应浓度作散点图,并根据其分布趋势,利用指数函数、幂函数以及多项式函数模型作线性拟合。
2 结果
本研究运用SRID,分别在10~40μg/ml和10~160μg/ml两个血凝素检测范围内作沉淀环直径-血凝素含量线性回归,以评价高浓度血凝素时线性拟合有无偏差。
2.1 常规检测浓度干扰试验在流感疫苗血凝素检测范围10~40μg/ml之内时,根据以往结果,所计算的直线回归方程其R2均近似于1,B1 HA、B2 HA含量与沉淀环直径的直线回归方程分别为:y=16.572x-69.634,R2=0.998;y=18.978x-79.44,R2=0.998,说明检测的血凝素含量与沉淀环直径呈正比关系,结果见表1。

表1 常规检测浓度干扰试验中B1、B2流感血凝素含量与沉淀环直径的关系Tab.1 The relations between B HA content and the diameters of the sedimentation rings under standard concentrations
在每个B型血清琼脂糖板(简称为血清板),每次加入该B型标准品抗原对照、单价样品、B1+B2混合单价样品。两种标准品和样品分别稀释至血凝素终浓度为10、20、30、40 μg/ml。 根据 B1 或 B2 标准抗原浓度作直线回归,分别求出直线回归方程,带入相应的样品沉淀环直径,得出其血凝素含量,求平均值、标准差(SD)和变异系数(CV)。该试验重复3次,结果见表2。
从表2可见,以B1标准抗原的直线回归方程计算B1单价样品与B1+B2混合单价样品中的B1的血凝素含量,比较40、30、20、10 μg/ml各项中 B1 单价样品与B1+B2混合单价样品中的B1的血凝素含量,P>0.05,差异无统计学意义。
从表2可见,计算同上,以B2标准抗原为标准方程。 40、30、20、10 μg/ml各项中 B2单价样品与B1+B2混合单价样品中的B2的血凝素含量比较,P>0.05,差异无统计学意义。
表2中血凝素浓度10μg/ml孔的结果,其变异系数CV>15%,数据不正常可能是因为测量沉淀环直径太小太接近加样孔直径造成的误差。
血凝素浓度20~40μg/ml,是常规检查疫苗中各种血凝素的最佳范围,准确性高,变异系数也小。
2.2 高浓度干扰试验第1组以配制三价流感疫苗(含A1A3B1或A1A3B2)为基质加入连续稀释另一B型病毒血凝素抗原,第2组以固定1种B型血凝素终浓度为30μg/ml为基质,加另1种B型病毒不同稀释度的血凝素,与第3组单一B型不同稀释度的血凝素进行比较,以确定含有基质中测定两种B型流感血凝素有无互相干扰,结果见表3。
将标准B1或B2血凝素抗原分别稀释至160、100、80、60、40、30、20、10 μg/ml,以其沉淀环的直径对其相应浓度作散点图,并根据其分布趋势,利用指数函数,幂函数以及多项式函数模型作曲线回归。结果显示,三元线性回归方程与所有数据拟合度最高,决定系数R2可达到0.999以上(图1)。
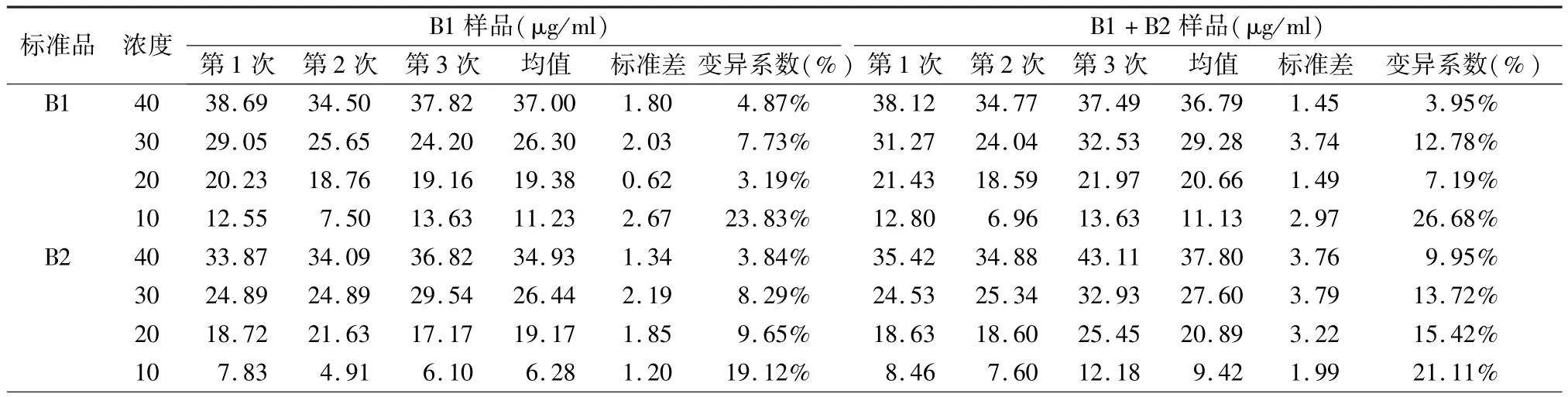
表2 单一B型血凝素样品与两型混合血凝素样品检测结果比较Tab.2 The results of determination of B HA content in single influenza B virus samples or mixture of two influenza B viruses samples
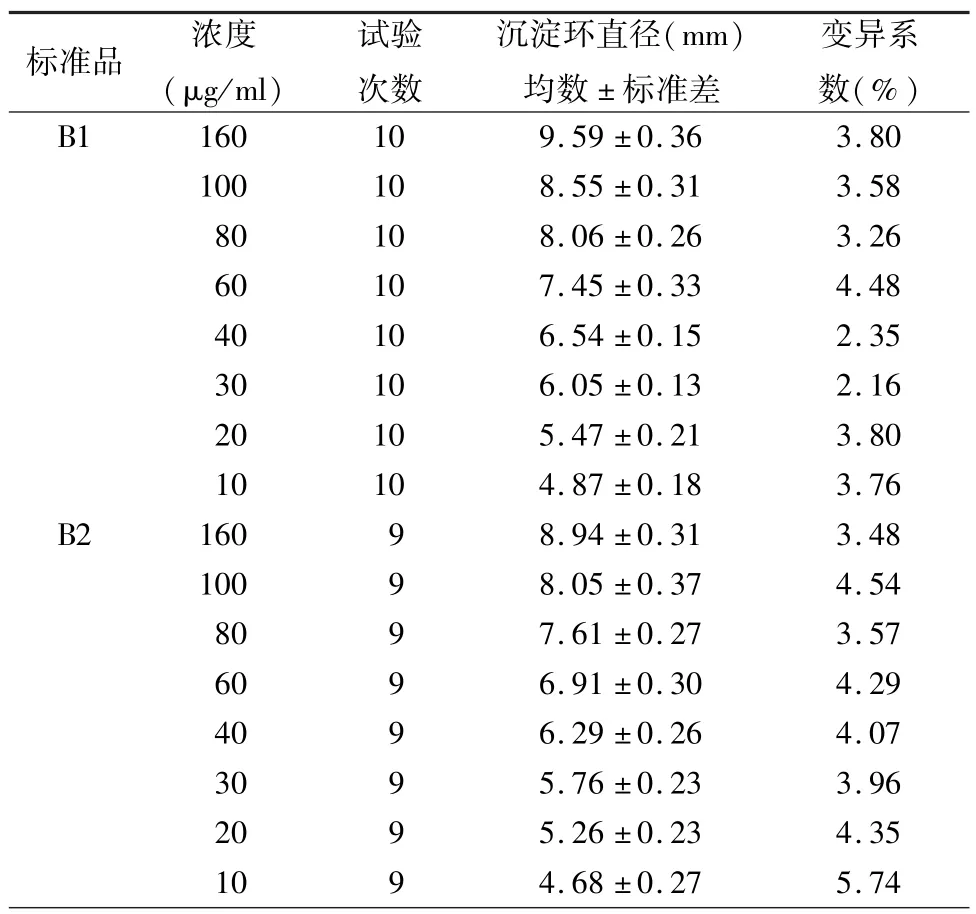
表3 B型流感高浓度血凝素含量与沉淀环直径曲线关系Tab.3 The relations between B HA contents and the diameters of the sedimentation rings in high HA content condition

图1 B型流感高浓度血凝素含量-沉淀环直径曲线回归图Fig.1 Curve regression diagram of high B HA content-the diameters of the sedimentation rings
以标准B1或B2血凝素抗原的浓度与相应抗体的沉淀环区直径绘制直线回归图时,决定系数R2低,发现抗体浓度越高,其产生的抗原抗体沉淀环区直径越不成正比,抗原浓度高者与理论值相比,偏离更多。其最接近线性关系仅表现于抗原浓度在10~40μg/ml之间,这也是原方法测定流感疫苗血凝素浓度时的配置范围。
以下实验中,所有全部高浓度血凝素浓度观察时均改作曲线回归,此方法比直线回归法高浓度偏移较少,其血凝素更接近于理论值。结果见表4。
表4中,在B1血清板上,三价苗中对不同浓度的B1血凝素的含量测定,高浓度≥50μg/ml时偏低。在B2血清板上,三价苗中存有不同浓度B2的血凝素的含量测定,浓度≥40μg/ml时,其值轻度偏低。
表4中,在B1血清板上以三价苗为基质和固定B2血凝素30μg/ml为基质,测定不同浓度B1血凝素,3组趋势相同,结果相似。与单一的B2不同血凝素浓度测定也无明显差别,3组互相比较P>0.05。
表4:在 B2血清板上,能够检测到三价苗(A1A3B2)基质组中和B2血凝素基质组中的B2血凝素含量,随B1血凝素浓度增加略有增加。两组B2血凝素值无明显差异,P>0.05。单一的B1血凝素组中,从高浓度到低浓度没有见任何免疫沉淀环,说明B2抗血清是高度型特异性的没有检出B1血凝素中与它反应的共同抗原。从表4中,每次试验时均设有四价流感疫苗为阳性对照,结果测定B1或B2血凝素值范围30.05~36.65μg/ml,多数在33μg/ml左右,这说明本试验方法稳定,重复性高。
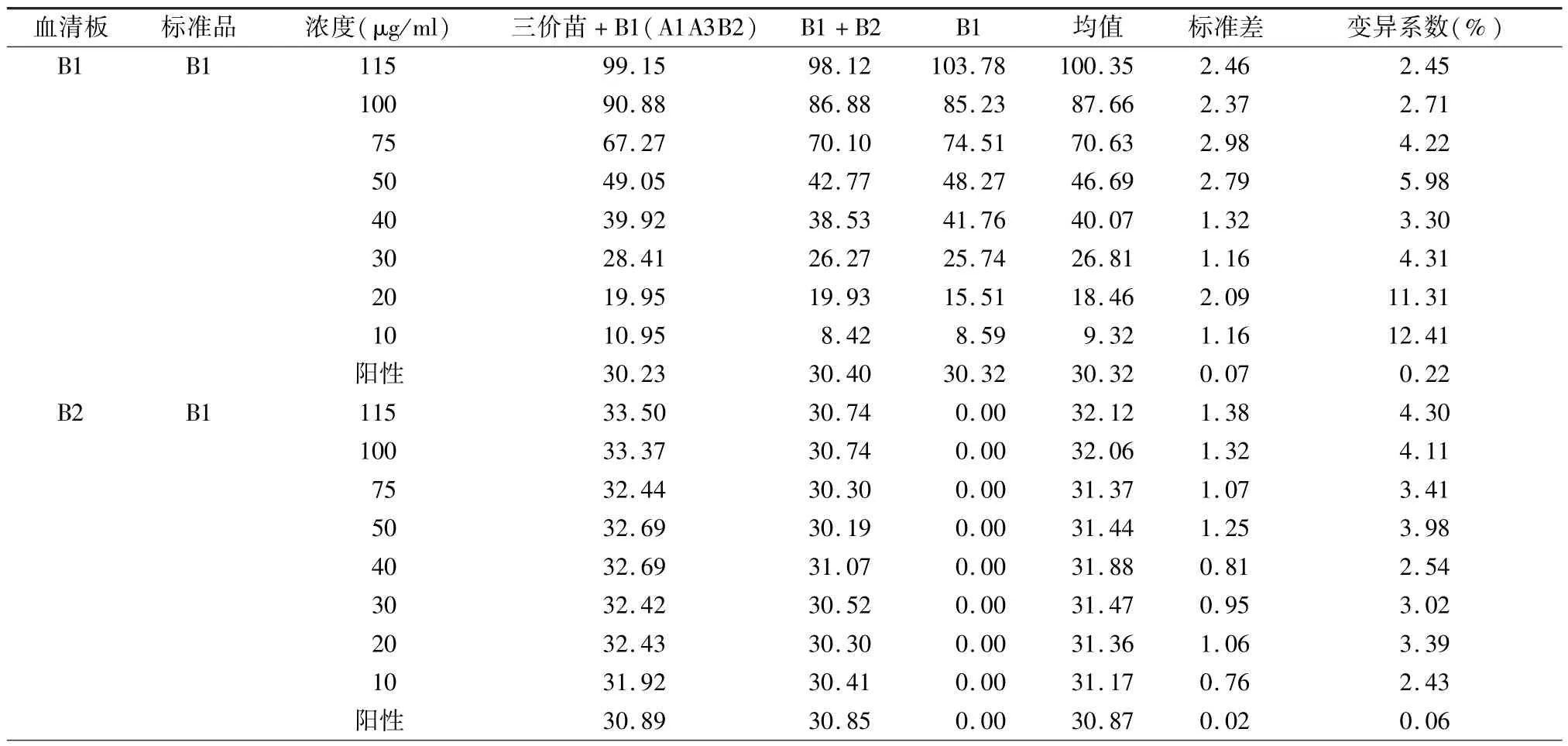
表4 在B1或B2血清琼脂糖凝胶板上不同混合样品中B1血凝素含量测定结果Tab.4 B1 HA contents in different mixture samples on B1 or B2 serum agarose gel plates

表5 在B1或B2血清琼脂糖凝胶板上不同混合样品中B2血凝素含量测定结果Tab.5 B2 HA contents in different mixture samples on B1 or B2 serum agarose gel plates
在表5中,除在B2血清板上,B2+B1组在B2血凝素浓度为140μg/ml时,其测定值为174.58μg/ml。B2血凝素为单一抗原在10μg/ml一行的值为3.34,其变异系数太高(43.01%),不正常,其产生原因是人工卡尺测定近孔径的沉淀环误差太大所致。其余结果互相比较,3组无明显差异,P>0.05。
表5中,在比较 B1血清板测定三价苗(A1A3B1)、B1血凝素(30μg/ml)为基质和单一B2组中B2血凝素结果。在三价苗组和B1血凝素组中测定所显示B1的血凝素含量,在高浓度的B2血凝素存在时,略有增加。两组无明显差异,P>0.05。单一B2血凝素从高浓度到低浓度没有见任何免疫沉淀环,说明B1抗血清是高度型特异性抗血清,没能检出B2血凝素与它反应的共同抗原。
3 讨论
本研究所用四价流感病毒裂解疫苗是江苏金迪克生物技术有限公司已研制的预防用生物制品,属1类新药。除国外已批准上市,国内没有这类产品。该公司为第一家申报公司,目前已完成Ⅲ期临床试验,正在报批中。SRID测定单价原液血凝素含量是配制四价流感病毒裂解疫苗的主要依据。根据Kinnunen等[7]的研究,两种谱系的B型流感病毒演化自同一起源,那么,两种谱系B型血凝素抗原测定时是否有干扰;SRID是否能准确反映四价疫苗中两种谱系的B型血凝素抗原含量;在原三价疫苗中的血凝素成分对新增加的B型病毒血凝素抗原浓度检测是否有影响。事关产品质量和免疫效果,国内外并未发现资料能回答这些问题。为了准确检测新疫苗的两种B型病毒血凝素,保证新疫苗的质量,本研究设计相对复杂的实验予以验证。
本研究先从正常测定血凝素浓度范围着手,确定常规测定方法的准确性,明确检测的血凝素含量与沉淀环直径呈正比关系。在此浓度范围内测定单一血凝素和两型混合血凝素样品中的B1或B2血凝素含量存在另一B型血凝素时对测定结果无明显影响。随后以配制三价流感疫苗(含A1A3B1或A1A3B2)为基质和以固定一种B型血凝素终浓度为30μg/ml为基质,加另一种B型病毒不同稀释度的血凝素,并与单一B型不同稀释度的血凝素进行比较,高浓度B型血凝素抗原浓度与其沉淀环直径呈三元线性回归。无论在B1血清板上,三价苗中对不同浓度的B1血凝素的含量测定,还是在B2血清板上,三价苗中存有不同浓度B2的血凝素的含量测定,各组间均无显著差异。并且在B2血清板上,加入单一的B1血凝素,从高浓度到低浓度没有见任何免疫沉淀环;反之亦然。B1和B2血清是高度型特异性抗体,在存在高浓度另一B型血凝素时仍未出现交叉反应,保证了SRID的准确性。以上结果均表明,使用 B/Brisbane/60/2008和 B/Phuket/3073/2 013两种特异性血清在SRID测定流感疫苗中B/Brisbane和B/Phuket病毒的两种B型血凝素抗原时未发现交叉干扰。
利益冲突无

