寡聚度对低聚阳离子季铵盐表面活性剂的聚集行为、油-水界面性能及润湿性的影响
侯研博,乔富林,江建林,秦 冰
(中国石化 石油化工科学研究院,北京 100083)
低聚表面活性剂是指将两个到数十个两亲基元,通过联接基团在靠近亲水头基处以化学键的方式联接而成的一类表面活性剂。作为寡聚度最低的一类低聚表面活性剂,Gemini表面活性剂的临界胶束浓度(cmc)相比传统单链表面活性剂有了数量级的降低,聚集、起泡、乳化、润湿等多种性能有了质的飞跃[1-6]。这种性能上质的飞跃源于联接基团拉近了分子内两个两亲基元之间的距离,从而增强了两个两亲基元之间的协同作用。因此,相比单链表面活性剂,寡聚度的提高使得Gemini表面活性剂的性质有了巨大的提升。
在Gemini表面活性剂的基础上进一步增加寡聚度,分子内的多个两亲基元之间的协同作用变得更强,表面活性剂的聚集能力进一步得到提高,性能更加优异。In等[7-8]研究发现,随寡聚度增大,梳状阳离子季铵盐表面活性剂可以聚集形成线状胶束(12-3-12及12-3-12-3-12)和环状聚集体(12-3-12-4-12-3-12),这使得表面活性剂具有多样的流变性能。Hou等[9-12]研究了一系列具有星状刚性酰胺键联接基团的三聚(DTAD和DDAD)、四聚(PATC)及六聚(PAHB)阳离子季铵盐表面活性剂。结果表明,寡聚度越大,分子内多条疏水尾链之间的疏水协同作用变得更强[11],表面活性剂的临界聚集浓度(CAC)降低,聚集能力大大增强,聚集行为更加丰富,乳化[11]及杀菌[12]能力更加优异。笔者所在课题组[13]对一系列树枝状非离子低聚表面活性剂的研究表明,该类表面活性剂具有较高的除油能力和较强的降低油-水界面张力的能力。综上所述,低聚表面活性剂有望成为高效低耗的新一代表面活性剂,应用潜力很大。然而,由于低聚表面活性剂的合成难度较大,目前对低聚表面活性剂的研究和应用仍不够深入和全面,寡聚度对低聚表面活性剂性质的影响依然缺乏系统性的研究。
笔者合成得到了如图1所示的Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12,并通过传统单链阳离子季铵盐表面活性剂十二烷基三甲基溴化铵(DTAB)、Malic-2C12和Citric-3C12之间的对比,研究了寡聚度对低聚表面活性剂聚集行为、油-水界面特性和润湿性的影响,以期对高效低耗的低聚表面活性剂的实际应用提供指导。
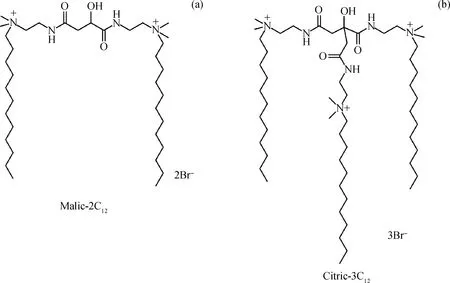
图1 Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12的分子结构Fig.1 Chemical structures of the Gemini and trimeric cationic quaternary ammonium surfactant Malic-2C12 and Citric-3C12(a) Malic-2C12; (b) Citric-3C12
1 实验部分
1.1 试剂
Gemini阳离子季铵盐表面活性剂Malic-2C12和三聚阳离子季铵盐表面活性剂Citric-3C12为实验室自制[14]。正辛烷(分析纯)购自北京通广精细化工公司。48~50℃切片石蜡购自国药集团化学试剂有限公司。实验过程中均使用Mili-Q水(18.2 mΩ·cm)。
1.2 产物结构表征
1.2.1 Gemini阳离子季铵盐表面活性剂Malic-2C12的谱图数据
1H NMR(CD3OD,400 MHz):δ=0.87(三重峰,6H,—CH3),1.29~1.80(多重峰,40H,CH3—(CH2)10—CH2—N+—),2.71~2.85(多重峰,4H,CH3—(CH2)10—CH2—N+—),3.13~3.20(多重峰,12H,—N+(CH3)2),3.45~3.52(多重峰,7H,—CO—NH—CH2—CH2—N+—,—NH—CO—CH2—CH(OH) —CO—NH—),3.55~3.76(多重峰,4H,—CO—NH—CH2—CH2—N+—),4.46(三重峰,1H,—NH—CO—CH2—CH(OH) —CO—NH—)。
MS-ESI(m/z):理论值 772.82;测试结果:306.6([M-2Br]2+/2)。1H NMR及MS-ESI结果表明产物和目标产物一致。
元素分析结果(质量分数):理论值:C36H76N4O3Br2:C,55.95%;H,9.91%;N,7.25%。测试结果:C,55.90%;H,9.88%;N,7.20%。
1.2.2 三聚阳离子季铵盐表面活性剂Citric-3C12的谱图数据
1H NMR(CD3OD,400 MHz):δ=0.88(三重峰,9H,—CH3),1.29~1.39(多重峰,54H,CH3—(CH2)9—CH2—CH2—N+—),1.80(单峰,6H,CH3—(CH2)9—CH2—CH2—N+—),2.64~2.91(多重峰,6H,CH3—(CH2)9—CH2—CH2—N+—),3.16~3.25(多重峰,18H,—N+(CH3)2),3.45~3.55(多重峰,11H,—CO—NH—CH2—CH2—N+—,—NH—CO—CH2—,—OH),3.65~3.72(多重峰,6H,—CO—NH—CH2—CH2—N+—)。
MS-ESI(m/z):理论值1146.64;测试结果:495.40([M-2Br]2+/2)。1H NMR及MS-ESI结果表明产物和目标产物一致。
元素分析结果(质量分数):理论值:C54H113N6O4Br3:C,56.39%;H,9.90%;N,7.31%。测试结果:C,56.26%;H,9.82%;N,7.29%。
1.3 实验方法
1.3.1 表面张力实验
表面张力实验采用德国KRUSS公司的K100型表面张力仪,使用吊环测定不同浓度表面活性剂水溶液的表面张力。测量温度控制在(25.00±0.05)℃。每条表面张力曲线至少重复测试2遍。
1.3.2 电导实验
电导实验在上海智光仪器仪表有限公司DDS-11A型实验室电导率仪上进行。实验过程中,将表面活性剂溶液置于恒温水浴中,使实验过程中溶液温度恒定为(25.0±0.1)℃。
1.3.3 动态光散射(DLS)
光散射所用仪器为美国BROOKHAVEN仪器公司BI-DS1型激光光散射仪,采用的入射光源为氦氖激光,入射光角度为90°,所有样品均经过孔径为0.45 μm的过滤膜过滤。光散射数据的相关函数通过拟合后可得到粒子表观水合直径 (Dh)分布曲线。实验温度为(25.0±0.1)℃。
1.3.4 油-水界面张力实验
采用美国CNG公司的TX-500C型界面张力仪测定表面活性剂溶液的油-水界面张力,测试温度为(25.0±0.1)℃,转速为6000 r/min,所用油相为正辛烷。
1.3.5 润湿性实验
先在80℃下将切片石蜡融化成液体,均匀涂覆在载玻片表面,自然冷却。然后采用德国KRUSS公司的DSA100型界面黏弹性测量仪测定表面活性剂溶液与石蜡界面的接触角。如无特别说明,实验所记录的接触角均为平衡10 min后所测得的值。整个实验过程中,温度控制在25℃。
2 结果与讨论
2.1 Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12的临界聚集浓度(CAC)及聚集行为
采用表面张力和电导实验,分别研究了Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12的CAC及水溶液中的聚集行为,结果如图2所示。

图2 25℃时Malic-2C12和Citric-3C12在水溶液中的表面张力(γ)和电导率(κ)随表面活性剂摩尔浓度(C)的变化曲线Fig.2 Plots of surface tension (γ) and conductivity (κ) versus the surfactant molar concentrations (C) of Malic-3C12 and Citric-3C12 in aqueous solutions at 25℃(a), (c) Malic-2C12; (b), (d) Citric-3C12
由图2(a)可知,表面张力曲线在1.00 mmol/L处出现了1个拐点。当Malic-2C12摩尔浓度低于1.00 mmol/L时,随着浓度增大,表面张力线性降低。这表明表面活性剂分子不断在水-气界面吸附,分子在水-气界面的排列越来越紧密。当Malic-2C12摩尔浓度高于1.00 mmol/L之后,表面张力曲线出现平台,表面张力保持恒定值33.26 mN/m不变。这表明此时表面活性剂分子在水-气界面的吸附达到饱和,开始在水溶液体相中聚集。因此,通过表面张力方法可以得到Malic-2C12的CAC为1.00 mmol/L,γCAC值为33.26 mN/m。相应地,电导率曲线也存在1个拐点,图2(c)中拐点对应的浓度即为电导率法测得的CAC,其值为1.48 mmol/L。
由图2(b)和(d)可知,Citric-3C12的表面张力与电导率曲线同样存在拐点。通过表面张力法可以得到Citric-3C12的CAC为0.24 mmol/L,γCAC为33.01 mN/m。电导率实验的结果表明Citric-3C12的CAC为0.32 mmol/L。
通过上述结果可以发现,Malic-2C12和Citric-3C12通过表面张力及电导法得到的CAC值均能够较好地吻合。因此,Malic-2C12和Citric-3C12只有1个CAC。在这里,将两种方法得到的CAC的平均值定为该表面活性剂的CAC。所以,Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12的CAC值分别为1.24 mmol/L和0.28 mmol/L。作为对比,分子内含有1个疏水尾链的阳离子季铵盐表面活性剂DTAB的CAC值为14.0 mmol/L,γCAC为38.6 mN/m[15]。
对比DTAB、Malic-2C12和Citric-3C12的CAC值可以发现,每增加1个寡聚度,阳离子季铵盐表面活性剂的CAC都会降低1个数量级,这说明寡聚度的增加使得表面活性剂在体相中的聚集能力大大增强。另一方面,寡聚度的增加使得表面活性剂的γCAC逐渐降低。而且,随着阳离子季铵盐表面活性剂的寡聚度由DTAB增加至二聚,γCAC值的降低程度比从二聚到三聚降低的明显。梳形阳离子季铵盐表面活性剂的γCAC随寡聚度增加也有类似的变化趋势[16]。显然,随着寡聚度的增大,联接基团拉近了两亲基元之间的距离,使得两亲基元在水-气界面上的排列更加紧密,导致γCAC值降低。但同时,寡聚度的增大使得表面活性剂分子在水-气界面上紧密排列的位阻增大,因而γCAC降低的程度变小。对一些含有星状刚性联接基团的阳离子季铵盐表面活性剂,由于分子之间紧密排列的位阻太大,γCAC随寡聚度的增大不降甚至反而增加[17]。
同时,通过计算电导率曲线拐点前后电导率曲线斜率的比值,即可得到聚集离子化度(α)。DTAB、Malic-2C12和Citric-3C12的α值分别为0.24[15]、0.32、0.41。通过对比3种不同寡聚度阳离子季铵盐表面活性剂的α值可以发现,随着寡聚度的增加,阳离子季铵盐的α值逐渐增大。这表明随寡聚度的增加,阳离子季铵盐表面活性剂在体相中形成的聚集体表面结合的反离子(Br-)的量较少。然而,In等[8]对一系列梳形低聚表面活性剂的研究发现,寡聚度对该类表面活性剂的α值影响不大,12-3-12、12-3-12-3-12和12-3-12-4-12-3-12的α值均在0.22左右,没有明显差别。王毅琳课题组对一系列含有星状刚性酰胺键联接基团的三聚(DDAD,DTAD)[10]、四聚(PATC)[9]和六聚(PAHB)[11]阳离子季铵盐表面活性剂的研究结果表明,四聚表面活性剂PATC的α值最大,六聚表面活性剂PAHB的α值最小。这表明,低聚阳离子季铵盐的α值随寡聚度的变化趋势与联接基团结构密切相关。
2.2 Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12在水溶液中的聚集形貌及聚集机理
通过DLS实验研究了Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12分别在2倍、5倍及10倍于CAC浓度下在水溶液中的聚集体水合直径,结果如图3所示。由图3(a)看到,当Malic-2C12浓度超过CAC时,体相中聚集体直径为1~5 nm的小的球形胶束。图3(b)表明,当浓度超过CAC时,三聚阳离子季铵盐表面活性剂Citric-3C12在水溶液中聚集形成直径为100~300 nm的大聚集体。
图4给出了Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和Citric-3C12在水溶液中可能的聚集机理。当Gemini阳离子季铵盐表面活性剂Malic-2C12浓度超过CAC之后,疏水尾链之间的疏水相互作用增强。同时,由于分子中联接基团含有羟基及酰胺键,分子联接基团之间存在氢键相互作用。在疏水相互作用和氢键相互作用的共同作用下,Malic-2C12聚集形成小的球形胶束(见图4(a))。

图3 25℃时DLS测得的Malic-2C12和Citric-3C12分别在2倍、5倍及10倍于CAC浓度下形成的聚集体水合直径(Dh)分布Fig.3 Dh of Malic-2C12 and Citric-3C12 by DLS measures with concentrations of 2CAC, 5CAC and 10CAC at 25℃(a) Malic-2C12; (b) Citric-3C12
由图4(b)可见,Citric-3C12分子中3个带正电的季铵盐头基之间的静电排斥很强,使得分子内的3个疏水尾链彼此相互远离。同时,分子的联接基团具有一定的刚性,导致疏水尾链之间无法靠得很近。在头基间静电排斥和联接基团刚性的共同作用下,Citric-3C12倾向于以相对伸展的爪状构象存在[10]。这种爪状分子构象使Citric-3C12的临界堆积参数高于1/2,在联接基团中酰胺键及羟基之间氢键相互作用的辅助下,聚集形成大聚集体。

图4 Gemini及三聚阳离子季铵盐表面活性剂Malic-2C12和 Citric-3C12的聚集模型Fig.4 Possible model of the aggregation of the Gemini and trimeric cationic quaternary ammonium surfactant Malic-2C12 and Citric-3C12(a) Malic-2C12; (b) Citric-3C12
2.3 单链、Gemini及三聚阳离子季铵盐表面活性剂DTAB、Malic-2C12和Citric-3C12的油-水界面性能比较
上述结果表明,低聚阳离子季铵盐表面活性剂的表面性质及体相聚集性质随寡聚度增大具有规律性的变化,这是由于寡聚度的增加改变了表面活性剂在水-气界面及体相聚集体中的分子排布所引起的。表面活性剂分子排布的改变不仅能够影响其表面性质及聚集行为,而且可以影响表面活性剂的油-水界面性质。以正辛烷为油相,考察了DTAB、Malic-2C12和Citric-3C12的油-水界面张力随表面活性剂浓度的变化,结果如图5所示。

图5 25℃下DTAB、Malic-2C12及Citric-3C12水溶液与正辛烷之间的界面张力(IFT)随表面活性剂摩尔浓度的变化曲线Fig.5 Plots of the interfacial tension (IFT) between n-octane and aqueous solutions of DTAB, Malic-2C12 and Citric-3C12 versus the surfactant molar concentration at 25℃
由图5可以看出,DTAB、Malic-2C12和Citric-3C12的正辛烷-水界面张力随着表面活性剂浓度增大均先下降直至达到平台,平台界面张力值分别为6.82、8.24和6.24 mN/m。三者的界面张力值处于同一个数量级且非常接近,说明寡聚度的增大对表面活性剂分子在正辛烷-水界面的排布没有产生显著影响。这可能是由于寡聚度的增大一方面拉近了两亲基元间的距离,另一方面增加了分子紧密排列的空间位阻的缘故。
从图5还看到,DTAB、Malic-2C12和Citric-3C12的界面张力到达平台区所需要的表面活性剂摩尔浓度分别为15.00、1.00和0.50 mmol/L。这说明随着寡聚度的增大,表面活性剂在正辛烷-水界面达到饱和吸附所需的浓度有了数量级的降低,这与表面张力结果相吻合。这是因为Malic-2C12和Citric-3C12的分子中均含有刚性联接基团,使得表面活性剂能够以较为规整的伸展状分子构象吸附到正辛烷-水界面上,大大提高了表面活性剂降低油-水界面张力的效率,最终导致界面张力达到平台所需的表面活性剂浓度随寡聚度的增大有了数量级的降低。
2.4 单链、Gemini及三聚阳离子季铵盐表面活性剂DTAB、Malic-2C12和Citric-3C12的润湿性比较
低聚表面活性剂分子独特的油-水界面特性,促使笔者进一步研究了表面活性剂液滴在石蜡表面的润湿性。图6给出了DTAB、Malic-2C12和Citric-3C12液滴在石蜡表面的接触角随表面活性剂摩尔浓度的变化曲线。

图6 25℃下DTAB、Malic-2C12和Citric-3C12水溶液液滴与石蜡之间的接触角随表面活性剂摩尔浓度的变化曲线Fig.6 Plots of the contact angle between paraffin and aqueous drops of DTAB, Malic-2C12 and Citric-3C12 versus the surfactant molar concentration at 25℃
如图6所示,DTAB、Malic-2C12及Citric-3C123种表面活性剂水溶液液滴与石蜡的接触角随浓度增大均先保持高于100.0°的较大值不变,然后在拐点浓度附近开始剧烈降低,最后达到平台。DTAB、Malic-2C12和Citric-3C12的拐点摩尔浓度分别为10.00、1.00和0.50 mmol/L,接近各自的CAC值。这表明随寡聚度增大,表面活性剂能够在更低浓度下在水-石蜡界面达到饱和吸附,从而起到润湿效果。同时,3种表面活性剂平台区的接触角值分别为51.1°、53.5°和54.1°。这表明寡聚度增大对表面活性剂的润湿能力无明显差别,3种表面活性剂均具有良好的润湿性能,能够将接触角降至较低值。
在DTAB、Malic-2C12和Citric-3C123种表面活性剂的接触角随浓度变化曲线的平台区分别选择了50.00 mmol/L DTAB、5.00 mmol/L Malic-2C12和1.00 mmol/L Citric-3C12作为代表性摩尔浓度,考察了在该浓度下表面活性剂溶液液滴在石蜡表面的接触角随时间的变化曲线及不同时间对应的液滴在石蜡表面的照片,结果如图7所示。作为参照,水的液滴照片也同时给出。

图7 25℃下50.00 mmol/L DTAB、5.00 mmol/L Malic-2C12和1.00 mmol/L Citric-3C12水溶液与石蜡之间的接触角随时间的变化曲线及在不同时间点时对应的液滴在石蜡表面的照片Fig.7 Plots of the contact angle between n-octane and aqueous solutions of 50.00 mmol/L DTAB, 5.00 mmol/L Malic-2C12 and 1.00 mmol/L Citric-3C12 versus time (t) at 25℃ and the corresponding photos at different time(a) Contact angle vs t; (b) Corresponding photos
由图7(a)可以看出,50.00 mmol/L DTAB和5.00 mmol/L Malic-2C12溶液在开始与石蜡接触时,界面接触角分别为55.0°和60.9°左右。此后随时间增加,接触角略有降低,在4 min左右达到平台区,平台区接触角为50.3°和54.7°左右。这说明50.00 mmol/L DTAB及5.00 mmol/L Malic-2C12的溶液液滴在刚接触到石蜡表面时,接触角即可接近并达到平衡值,具有明显的润湿效果。这个过程中液滴的状态如图7(b)所示。
图7(a)中对于1.00 mmol/L Citric-3C12溶液,液滴在刚接触到石蜡表面时接触角较大(95.0°),当平衡时间超过2 min后,接触角开始迅速降低,在3 min左右降至60.0°。此后随时间增加,接触角缓慢降低,直至9 min左右到达平台区(53.5°)左右。结合图7(b)所示液滴照片发现,液滴在刚接触到石蜡表面时没有润湿效果;而当平衡4 min后,液滴即可较好地润湿石蜡表面;当平衡时间延长至10 min 时,润湿效果更好。
笔者推测三聚阳离子季铵盐表面活性剂Citric-3C12的润湿性能随时间的变化应该与其分子构象转变及聚集状态有关。在液滴体相中,表面活性剂分子以爪状构象聚集形成大聚集体。同时,有一部分表面活性剂分子单体存在于水溶液中。当液滴接触到石蜡表面时,Citric-3C12单体率先吸附到液滴与石蜡界面上。同时,体相中大聚集体与表面活性剂单体之间的动态平衡被打破,聚集成大聚集体的Citric-3C12分子逐渐解聚成单体,吸附到液滴与石蜡界面上[18]。这个过程中,由于爪状构象的Citric-3C12分子3个疏水尾链之间的疏水相互作用相比DTAB及Malic-2C12要更强,而且联接基团之间的氢键相互作用也更强,使得大聚集体中的Citric-3C12分子解聚集更加困难。因此,Citric-3C12分子在液滴与石蜡界面达到吸附平衡所需的时间更长,使得表面活性剂液滴对石蜡表面的润湿具有时间响应性。
3 结 论
(1)对于DTAB、Malic-2C12和Citric-3C12,随寡聚度增大,阳离子季铵盐表面活性剂的CAC有了数量级的降低,表面活性增强,聚集能力大大提高。当表面活性剂浓度高于CAC时,Malic-2C12聚集形成小的球形胶束。Citric-3C12以爪状分子构象存在,聚集形成大聚集体。
(2)对于DTAB、Malic-2C12和Citric-3C12,随寡聚度增大,阳离子季铵盐表面活性剂降低油-水界面张力的能力及其在石蜡表面的润湿性能没有明显变化,但效率大大增加, 降低油-水界面张力及润湿石蜡表面所需的浓度有数量级的降低。
(3)当三聚表面活性剂Citric-3C12浓度高于CAC时,由于其在大聚集体中的分子间相互作用较强,导致相应的解聚成单体的过程较慢,使得Citric-3C12液滴对石蜡表面的润湿具有时间响应性。
[1] ZANA R. Dimeric and oligomeric surfactants. Behavior at interfaces and in aqueous solution: A review[J].Advances in Colloid and Interface Science 2002, 97(1-3): 205-253.
[2] HAN Y, WANG Y. Aggregation behavior of Gemini surfactants and their interaction with macromolecules in aqueous solution[J].Physical Chemistry Chemical Physics, 2011, 13(6): 1939-1956.
[3] 范雅珣,韩玉淳,王毅琳. Gemini表面活性剂分子结构对其水溶液中聚集行为的影响[J].物理化学学报, 2016, 32(1): 214-226.(FAN Yaxun, HAN Yuchun, WANG Yilin. Effects of molecular structures on aggregation behaviors of Gemini surfactants in aqueous solutions[J].Acta Physico-Chimica Sinica, 2016, 32(1): 214-226.)
[4] MENGER F M, KEIPER J S. Gemini surfactants[J].Angew Chem Int Ed, 2000, 39: 1906-1920.
[5] 赵修太,陈安胜,王彦玲,等.N,N′-乙撑双[N(乙磺酸钠)-十二酰胺]的柴油乳化性能[J].石油学报(石油加工), 2011, 27(5): 725-731.(ZHAO Xiutai, CHEN Ansheng, WANG Yanling, et al. Emulsifying properties ofN,N′-ethylenebis[N(sodium ethylene sulfonate)-dodecanamide] for diesel oil[J].Acta Petrolei Sinica (Petroleum Processing Section), 2011, 27(5): 725-731.)
[6] 陈泽华,赵修太,王增宝,等. 季铵盐型Gemini表面活性剂水溶液的表面和油/水界面特性[J].石油学报(石油加工), 2015, 31(5): 1156-1163.(CHEN Zehua, ZHAO Xiutai, WANG Zengbao, et al. Interfacial properties of quaternary ammonium Gemini surfactants in aqueous solutions[J].Acta Petrolei Sinica (Petroleum Processing Section), 2015, 31(5): 1156-1163.)
[7] IN M, AGUERRE-CHARIOL O, ZANA R. Closed-looped micelles in surfactant tetramer solutions[J].Journal of Physical Chemistry B, 1999, 103(37): 7747-7750.
[8] IN M, BEC V, AGUERRE-CHARIOL O, et al. Quaternary ammonium bromide surfactant oligomers in aqueous solution: Self-association and microstructure[J].Langmuir, 2000, 16(1): 141-148.
[9] HOU Y, HAN Y, DENG M, et al. Aggregation behavior of a tetrameric cationic surfactant in aqueous solution[J].Langmuir, 2010, 26(1): 28-33.
[10] WU C, HOU Y, DENG M, et al. Molecular conformation-controlled vesicle/micelle transition of cationic trimeric surfactants in aqueous solution[J].Langmuir, 2010, 26(11): 7922-7927.
[11] FAN Y, HOU Y, XIANG J, et al. Synthesis and aggregation behavior of a hexameric quaternary ammonium surfactant[J].Langmuir, 2011, 27(17): 10570-10579.
[12] ZHOU C, WANG F, CHEN H, et al. Selective antimicrobial activities and action mechanism of micelles self-assembled by cationic oligomeric surfactants[J].ACS Applied Materials and Interfaces, 2016, 8(6): 4242-4249.
[13] 侯研博,秦冰,李本高,等. 一种非离子型低聚表面活性剂及其制备方法: CN,2014105533144[P].2016-05-11.
[14] XU D, QI B, FANG D, et al. Preparation, characterization and properties of novel cationic gemini surfactants with rigid amido spacer groups[J].J Surfactants Deterg, 2016, 19(1): 91-99.
[15] ESUMI K, TAGUMA K, KOIDE Y. Aqueous properties of multichain quaternary cationic surfactants[J].Langmuir, 1996, 12(16): 4039-4041.
[16] LASCHEWSKY A, WATTEBLED L, AROTCARÉNA M, et al. Synthesis and properties of cationic oligomeric surfactants[J].Langmuir, 2005, 21(16): 7170-7179.
[17] 韩玉淳,范雅珣,伍春娴,等. 寡聚表面活性剂的合成及其聚集行为的研究[J].中国科学:化学, 2015, 45(4): 327-339.(HAN Yuchun, FAN Yaxun, WU Chunxian, et al. Synthesis and aggregation behavior of oligomeric surfactants[J].SCIENTIA SINICA Chimica, 2015, 45(4): 327-339.)
[18] THEODORAKIS P E, MULLER E A, MATAR O K, et al. Insights into surfactant-assisted superspreading[J].Current Opinion in Colloid and Interface Science, 2014, 19(4): 283-289.

