基于416例I期NSCLC肺叶切除术后随访结果探讨早期NSCLC术后随访策略
戴亮 闫万璞 康晓征 付浩 杨永波 周海涛 梁震 熊宏超 林瑶 陈克能
肺癌是全世界目前最常见的恶性肿瘤之一,而且发病率和死亡率仍在持续升高。非小细胞肺癌(nom-small cell lung cancer, NSCLC)是肺癌最常见的类型,其治疗有依赖于原发肿瘤(tumor, T)、淋巴结(node, N)和转移病灶(metastasis, M)的分期而决定[1]。早期NSCLC的主要治疗方法是以治愈为目的的外科治疗,然而并非所有早期患者均能被治愈,即便是I期NSCLC术后仍有复发转移。因此,NSCLC患者术后需要终生随访,目的在于早期发现肿瘤的复发转移,进行适当的治疗,最终改善生存。但目前国际上对NSCLC的随访间隔时间及随访内容并未达成共识,各指南对于不同病理类型、不同分期NSCLC的随访策略一概而论、毫无差别,NSCLC术后2年内每3个月门诊随访,3年-5年为每半年门诊随访,5年后每年门诊随访[1,2]。我们假设认为早期NSCLC随访内容过多、频率过高,会造成资源浪费甚至医源性伤害。因此,亟需相关的研究为临床提供可靠的参考数据。我科自2000年肺癌前瞻性数据库建立后,一直坚持定期门诊随访术后患者,积累了大量真实可靠的肺癌手术患者随访资料。本研究回顾性分析了经外科手术治疗的416例I期NSCLC的随访资料,总结其复发转移的部位及时间,为制定该类患者的随访策略提供参考。
1 对象与方法
1.1 研究对象 选取我科肺癌前瞻性数据库中2000年1月-2013年10月单一医生组连续行解剖性肺叶切除手术的肺癌患者1,290例作为筛选对象。入组标准:①肺原发性NSCLC者;②接受解剖性肺叶切除及系统性淋巴结清扫手术治疗者;③根据第8版国际抗癌联盟(Union for International Cancer Control, UICC)/美国癌症联合会(American Joint Committee on Cancer, AJCC)NSCLC TNM分期系统,术后病理分期为I期者;④手术切缘阴性(R0切除)。排除标准:①既往恶性肿瘤病史者;②术前行新辅助治疗者;③围手术期死亡者(术后90天内)。根据入组及排除标准,最终共416例纳入研究。
1.2 诊断与治疗策略 术前分期检查包括胸部增强增强计算机断层扫描(computed tomography, CT)、全身正电子发射计算机断层显像(positron emission tomography/CT,PET/CT)(2008年以后)、头颅增强磁共振成像(magnetic resonance imaging, MRI)、全身骨扫描、颈腹部超声及气管镜检查,对于影像怀疑纵隔淋巴结阳性者行支气管内超声(endobroncheal ultrasonography, EBUS)穿刺或电视纵隔镜检查。肿瘤分期采用UICC和AJCC联合制定的第8版TNM分期系统[3]。手术以根治性为目的,全腔镜或开放手术行解剖性肺叶切除术加系统性淋巴结清扫。
1.3 随访方式 术后2年之内每3个月门诊复查一次,3年-5年每半年门诊复查一次,5年以后每年门诊复查一次。复查内容详细记录患者近期主诉及症状,检查内容包括胸部增强CT及颈腹部超声;头颅增强MRI/CT及全身骨扫描每半年至一年复查;全身PET/CT无症状时术后2年及5年复查;支气管镜及EBUS穿刺等检查根据患者症状及检查结果决定,不作为常规。本组患者均为门诊随访,截止日期为2018年1月15日或死亡,随访率98.7%;存活患者中位随访时间为71.2个月(12个月-208个月)。
1.4 研究指标 临床信息包括性别、年龄、吸烟史、术前合并症、手术信息、肿瘤病理及分期、肿瘤表皮生长因子受体(epithelial growth factor receptor,EGFR)基因突变情况及术后随访资料(末次随访状态、总生存时间、首次复发转移时间及部位)等。
1.5 统计学方法 统计分析采用SPSS 22.0分析(SPSS公司,芝加哥,伊利诺斯,美国)。临床因素组间复发转移比较采用卡方检验;单因素生存分析采用Kaplan-Meier法,用Logrank进行显著性检验。统计结果均按照P<0.05定义为差异具有统计学意义。
2 结果
2.1 基本资料 由1,290例筛选出I期NSCLC肺叶切除者416例,中位年龄62岁,18岁-82岁;其中男性214例(51.4%),女性202例(48.6%);吸烟者166例(39.9%),非吸烟者250例(60.1%);术前合并心肺疾病者148例(35.6%);手术为全胸腔镜者192例(46.2%),传统开胸手术者224例(53.8%);术后病理为腺癌者321例(77.2%),鳞癌者61例(14.7%),其他类型者34例(8.2%);根据AJCC/UICC第8版TNM分期系统,术后病理分期为T1a者28例(6.7%),T1b者124例(29.8%),T1c者90例(21.6%),T2a者174例(41.8%)。全组共119例腺癌患者行肿瘤原发灶EGFR基因检测,阳性者90例(75.6%),阴性者29例(24.4%)(表1)。
2.2 全组患者术后生存分析及复发转移特征 全组患者5年DFS与OS分别为82.4%和85.4%。全组患者随访期间共有76例(18.3%)出现复发转移,复发转移部位中最常见依次为肺转移21例(5.0%),脑转移20例(4.8%),骨转移12例(2.9%),纵隔淋巴结转移12例(2.9%),肝转移6例(1.4%),胸膜转移3例(0.7%),皮下转移结节2例(0.5%)。术后每年新增复发转移情况见图1。生存分析计算最常见复发转移部位2年、5年的累计复发率,肺转移者分别为2.3%(95%CI: 0.7%-3.9%)和4.8%(95%CI: 2.6%-7.0%);脑转移者分别是2.5%(95%CI: 0.9%-4.1%)和6.0%(95%CI:3.3%-8.7%);骨转移者分别是1.5%(95%CI: 0.3%-2.7%)和3.3%(95%CI: 1.5%-5.1%);纵隔淋巴结转移者分别是1.6%(95%CI: 0.4%-2.8%)和3.9%(95%CI: 1.2%-6.6%)。
2.3 复发转移患者危险因素的单因素分析 研究在不同年龄、性别,是否吸烟、心肺合并症,不同肿瘤位置、手术方式、病理类型、pT分期及EGFR突变情况中,比较复发转移的情况及5年DFS。发现pT2a者复发转移率高于pT1者(P=0.006),5年DFS分别为73.8%和87.6%(P=0.002),5年OS分别为77.7%和90.3%(P=0.011)(图2);有术前心肺合并症者5年DFS较无心肺合并症者差(75.9%vs85.3%,P=0.031)(表1)。
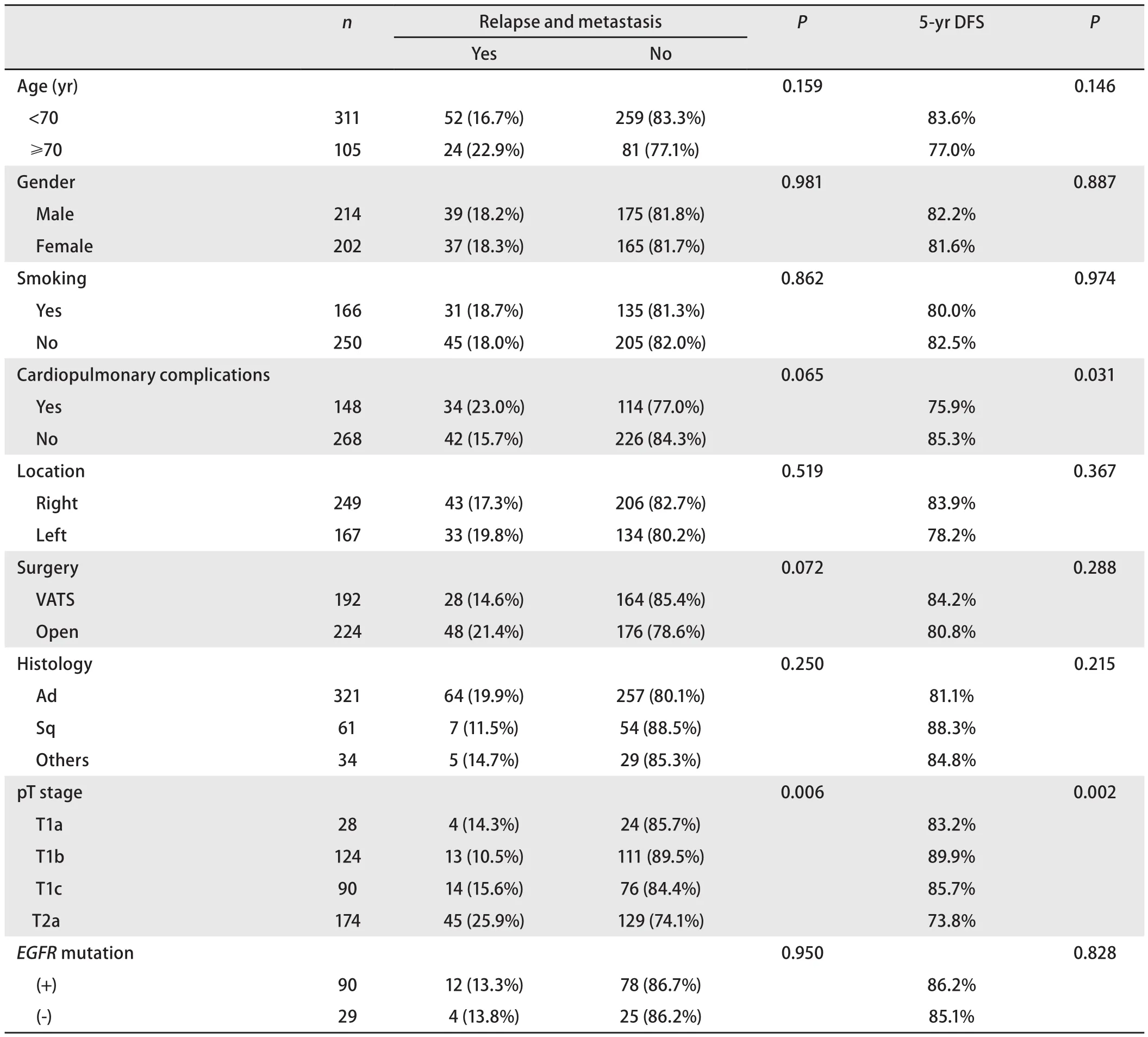
表 1 患者基本资料及5年DFSTab 1 Baseline characteristics and 5-yr DFS of patients

图 1 pT1期与pT2a期NSCLC术后患者OS Kaplan-Meier曲线Fig 1 OS Kaplan-Meier curves for all 416 NSCLC patients with pT1 and pT2a after lobectomy.OS: overall survival; NSCLC : non-small cell lung cancer.

图 2 pT1期与pT2a期NSCLC术后患者DFS Kaplan-Meier曲线Fig 2 DFS Kaplan-Meier curves for all 416 NSCLC patients with pT1 and pT2a after lobectomy.DFS: disease free survival.
2.4 患者症状与复发转移部位的关系 肺及纵隔淋巴结转移者绝大多数(85.7%和91.7%)就诊时无症状,以常规胸部增强CT检查发现;肝转移者大多数(66.7%)也是无症状就诊常规超声检查发现;胸膜、脑及骨转移的者大多数(66.7%、60.0%和58.3%)是因症状就诊检查发现;皮下转移结节均为患者自行发现后就诊(图3)。
3 讨论
外科是早期NSCLC的标准治疗,但术后仍然有复发转移,部分患者还会出现第二原发肿瘤[4]。因此,术后的随访监测显得尤为重要,目的是早期发现及治疗复发转移或第二原发肿瘤,最终改善生存。但目前国际上对于NSCLC的随访模式上并未达成共识,相关的临床证据也十分有限。究其原因,缺乏早期NSCLC术后长高质量随访导致此类患者术后复发转移模式不明确。
文献报道I期NSCLC的5年DFS为84%-87%,本组患者5年DFS与OS分别为82.4%和85.4%,同以往报道近似[5-7]。Hung等[8]报道的756例手术治疗NSCLC,2年局部无复发率和无远处转移率分别为90.7%和82.1%,5年OS和复发率分别为57.3%和70.2%;T分期是影响总生存、整体复发率和远处转移率的主要因素,同时吸烟患者及非鳞癌患者的远处转移风险更高。但文章没有描述复发转移的具体部位和时间。我们全组患者随访期间仅有76例(18.3%)出现复发转移,低于文献报道,可能原因如下:①本组患者均为病理I期NCSLC,未混杂临床I期;②术前分期检查规范、统一,包括全身PET/CT检查,最大限度除外隐匿的远传转移;③单中心单一手术组病例,手术质量均一,全组患者均行系统淋巴结清扫,确切N0分期;④手术切除方式为标准肺叶切除,不包含亚肺叶切除病例。通常,肺癌术后常见复发转移部位依次为肺(包括支气管残端)、纵隔淋巴结、脑、骨、肝及肾上腺等,但早期肺癌由于大多数为周围性肺癌,解剖性肺叶切除术后极少出现局部支气管残端复发,有别于中心型肺癌复发转移部位。本组患者中复发转移部位中最常见依次为肺转移21例(5.0%),脑转移20例(4.8%),骨转移12例(2.9%),纵隔淋巴结转移12例(2.9%),而肝转移,胸膜转移在早期肺癌术后患者中属于罕见转移。转移时间上,从术后第一年就开始出现复发转移,绝大多数的复发转移出现在术后5年之内,2年内与3年-5年的复发转移率无明显差别;5年之后再复发转移率仅为1.9%。
对于NSCLC术后复发转移的预测因素,既往研究较多,所涉及的因素也很多,包括肿瘤TNM分期、围手术期治疗、肿瘤基因特性等,但最为大家接受的仍然是TNM分期[9]。本研究的对象均为I期NSCLC,手术方式为统一的肺叶切除及系统性淋巴结清扫,消除了手术因素对预后产生的偏倚。在分析其他临床特征与预后关系时,我们发现T分期仍然是决定复发转移的最大因素。虽然有研究认为相对于其他病理类型,早期腺癌术后更容易出现复发转移,但我们研究发现,是否腺癌和EGFR基因是否突变均不会影响早期NSCLC的复发转移[10]。
肺癌手术治疗后的最初2年,是公认的复发高危期,因此大多学者均支持在这段时间给予患者相对高密度的随访,以期及早发现复发病灶。在临床实践中,由于缺乏针对早期NSCLC的随访指南,不同单位、不同部门甚至不同医生的随访策略差别迥异。我科目前的随访策略是:术后2年之内,每3个月进行随访;3年-5年期间,每6个月进行随访;5年以后,每年进行随访。检查内容包括:血液及生化室检查、胸部CT、颈部及腹部超声、头颅MRI(每6个月一次)、全身骨扫描或PET/CT(每年一次)。然而,本研究结果告诉我们,这种随访策略在早期NSCLC患者中并不恰当,可能存在随访过度。早期NSCLC术后复发转移率低,虽主要集中在术后5年之内,但2年内复发转移风险并不高于3年-5年,因此2年内复发间隔时间无需更频繁。而在随访内容方面,肺及纵隔淋巴结转移仍然是最常见转移,且少有症状,只能靠定期复查发现,因此术后前5年复查项目中仍应保留每年1次-2次胸部增强CT检查,5年后由于复发转移风险降低可每年1次;对于危害更大的脑、骨、肝脏等部位转移,大多数患者因相应的临床症状就诊发现,鉴于其同样的低发生率,建议头颅MRI及骨扫描检查可只在有症状时实施,5年后是否要加强随访值得考虑。在更理想的随访策略应当根据患者不同的复发和死亡风险进行分层,高风险者(如T2a者)给予相对积极和严格的随访,低风险者(如T1者)则相对保守和宽松。
本研究回顾性分析了I期NSCLC经肺叶切除术后的长期生存结果,通过其复发转移特点探讨了对于此类患者的远期随访策略。但作为一项回顾性、单中心研究,不可避免的存在一些局限性和偏倚,应在外部数据库进行验证及对照研究。

