雷珠单抗与康柏西普治疗湿性年龄相关性黄斑变性的效果比较
舒宝君,雷淑红,陈 瑜,朱佳丽
(陕西省商洛国际医学中心医院 眼科中心,陕西 商洛,726000)
年龄相关性黄斑变性(AMD)与视网膜色素上皮代谢功能减退有关,是视网膜黄斑区结构的衰老性改变,会造成患者视功能减退,严重者将导致失明[1]。AMD的发病原因尚不明确,主要与光线的损伤、营养的缺乏、年龄性老化或遗传因素等相关[2]。研究[3]显示,人种也是AMD的一个危险因素,白种人的发病率远高于黄种人和黑种人。根据临床表现可将AMD分为干性和湿性两种,虽然湿性AMD的比例仅占10%左右,但临床中90%的视力丧失病例为湿性AMD[4]。调查[5]显示,湿性AMD在中国45岁以上人群中发病率约为15%,其中在75~85岁老年人中的发病率高达30%。目前临床治疗主要采用抗血管内皮生长因子(VEGF)药物,常见的有雷珠单抗、贝伐单抗和康柏西普等[6]。本研究比较雷珠单抗与康柏西普治疗湿性AMD的疗效,现报告如下。
1 资料与方法
1.1 一般资料
选取2017年5月—2018年3月本院收治并确诊的湿性AMD患者80例,共80只眼,均为单眼,其中男43例,女37例,年龄60~79岁。纳入标准: 所有患者经眼底荧光素血管造影和光学断层扫描确诊为湿性AMD,近3个月未使用过眼部治疗药物,对本研究知情并同意。剔除标准: 合并其他眼病患者,既往眼科手术史者,有心、肝、肾等重要脏器疾病患者,妊娠和哺乳期患者,不愿签署研究知情同意书者。将80例患者随机分为2组各40例。A组采用雷珠单抗治疗,男22例,女18例;年龄61~79岁,平均年龄(68.42±2.29)岁,病程5~104月,平均病程(52.37±2.54)月。B组采用康柏西普治疗,男21例,女19例;年龄60~78岁,平均年龄(66.93±2.67)岁,病程6~106月,平均病程(53.07±2.68)月。2组年龄、性别、病程等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 研究方法
2组均行玻璃体腔注药手术。碘伏冲洗结膜囊,采用爱卡因表面麻醉,用开睑器开睑,采用1.0 mL注射器角膜缘3.5 mm处睫状体平坦部垂直穿刺入玻璃体腔内,A组注射0.1 mL雷珠单抗(商品名: 诺适得,瑞士诺华制药有限公司,进口药品注册证号S20140003),B组注射0.1 mL康柏西普(成都康弘生物科技有限公司,国药准字S20130012),拔针后行抗感染处理。2组患者每月治疗1次,均连续治疗3个月。
1.3 评价指标
2组患者在治疗后1、3个月复查。① 采用早期治疗糖尿病性视网膜病变研究(ETDRS)视力表评估患者的裸眼视力水平,以所测得的字母数作为计量资料。② 采用光学相干断层扫描仪定量测量黄斑中心视网膜厚度。③ 采用眼底荧光素血管造影观察脉络膜新生血管形成(CNV)渗漏情况。渗透消失: 新生血管不渗漏;渗漏减少: 渗漏面积减少超过50%以上;渗漏持续: 渗漏面积减少低于50%;渗漏增加: 渗漏面积扩大;复发: 患者渗漏处消失后又重新渗漏。CNV渗漏总改善率=(消失+减少)/总例数×100%。④ 观察2组患者眼部并发症。
1.4 统计学方法
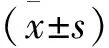
2 结 果
2.1 2组视力水平比较
治疗前和治疗后3个月,2组视力水平比较无显著差异(P>0.05);治疗后1个月,B组视力水平改善程度显著优于A组(P<0.05),见表1。
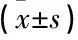
表1 2组视力水平比较
与A组比较,*P<0.05。
2.2 2组黄斑中心视网膜厚度比较
治疗前和治疗后3个月,2组黄斑中心视网膜厚度比较,差异无统计学意义(P>0.05);治疗后1个月,2组黄斑中心视网膜厚度比较有显著差异(P<0.05),见表2。
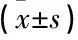
表2 2组黄斑中心视网膜厚度比较 μm
与A组比较,*P<0.05。
2.3 2组治疗后CNV渗漏情况比较
眼底荧光素血管造影属于有创检查,不适宜频繁检查,故注射后1个月无CNV渗漏情况数据。治疗3个月后,2组CNV渗漏总改善率比较,差异无统计学意义(P>0.05),见表3。

表3 2组CNV渗漏改善情况比较[n(%)]
2.4 2组不良反应比较
2组均出现轻微不良反应,A组不良反应3例,包括高眼压2例,结膜出血1例,不良反应发生率为7.50%;B组不良反应2例,包括高眼压1例,结膜出血1例,不良反应发生率为5.00%。经对症处理后均缓解,未对本研究产生影响。2组不良反应发生率比较,差异无统计学意义(P>0.05)。
3 讨 论
研究[5]显示,AMD已成为高龄人群中仅次于糖尿病的第2位致盲病,而中国的AMD老年患者数超过400万,严重危害患者的健康。AMD发病原因尚不清楚,可能与老化、环境影响、遗传因素、后极部视网膜慢性光损伤、自身免疫性疾病和营养缺陷等相关,其中衰老和退变是引发AMD的重要因素[7]。湿性AMD主要为玻璃膜损伤,引起CNV渗漏,导致黄斑区视网膜或色素上皮有浆液或出血,最终形成机化疤痕[8]。VEGF是湿性AMD中CNV渗漏的重要调节因子之一,因此目前主要采用抗VEGF药物来进行治疗。
雷珠单抗在2006年被美国食品及药物管理局(FDA)批准用于治疗湿性AMD,是第2代的重组鼠抗VEGF单克隆抗体,可同时作用于多个VEGF亚型及其降解产物,抑制新生血管生成[9]。康柏西普是中国自主研发的一种全人源化氨基酸序列重组融合蛋白,与VEGF亲和力高,可有效抑制受VEGF所诱导的血管内皮细胞生长、迁移和血管新生等[10]。本研究分别采用雷珠单抗(A组)和康柏西普(B组)治疗湿性AMD。治疗1个月后,B组视力显著优于A组(P<0.05);A组治疗1个月后黄斑中心视网膜厚度为(368.79±40.42) μm,B组为(350.02±40.23) μm,B组黄斑中心视网膜厚度改善情况显著优于A组(P<0.05);治疗3个月后,2组视力和黄斑中心视网膜厚度比较,差异均无统计学意义(P>0.05),说明康柏西普治疗湿性AMD的前期疗效好,但是后期疗效和雷珠单抗基本相当,与文献报道[11]相吻合。其原因可能为康柏西普是一种融合蛋白,而雷珠单抗作为单克隆抗体结合的受体较为单一。
牛静宜等[12]指出,康柏西普和雷珠单抗都可以结合VEGF-A受体,而康柏西普还可以结合VEGF-B、VEGF-C等受体。本研究中,2组CNV渗漏治疗改善率相比无显著差异(P>0.05),表明康柏西普和雷珠单抗的治疗效果基本一致。有研究[13-14]指出,康柏西普因其结构特殊,半衰期相对于雷珠单抗较长,因而在眼内作用更为稳定,药效时间较长。关于药物安全性分析,2组均有轻微不良反应,经对症处理后均缓解,A组并发症发生率为7.50%,B组为5.00%,差异无统计学意义(P>0.05),表明康柏西普和雷珠单抗治疗的安全性相当。叶瑞珍等[15]提出,康柏西普是中国拥有自主知识产权的药物,而雷珠单抗为进口药物,价格接近康柏西普的2倍,在两种药物治疗等效性和安全性一致的情况下,康柏西普对于国内患者的性价比更高。
综上所述,康柏西普治疗湿性AMD的前期效果优于雷珠单抗,对视力和黄斑中心视网膜厚度改善较好。随着治疗周期的延长,两种药物后期疗效相同,且安全性相近。

