例谈以实验促进化学的综合学习
——以部分有机化学实验的设计、改进和教学研究为例
首都师范大学教育学院(100048) 刘秀英
首都师范大学化学系(100048) 冯晓颖
以实验为基础是化学学科的重要特征之一。化学实验是研究和学习物质及其变化的基本方法,是科学探究的一种重要途径。为了突出化学学科特征,更好的发挥实验的教育功能,可从“引导学生综合运用所学的化学知识和技能,进行实验设计和实验操作,分析和解决与化学有关的实际问题”入手。有机化学作为中学化学的一部分,是重点也是难点。在中学化学教学过程中,我们发现了一些中学教师和学生易出错和易忽视的重要实验,尤其是有机化学实验。实践考察表明,因为设计性实验对学生要求较高,需要学生对反应物与生成物的性质、反应条件、实验的安全性与可行性等多方面内容都要有较深入的了解。因此,通常因“太难”而被搁置,起不到教材编制者预期的效果。而对教材中已有实验装置的改进,需要教师和学生对化学实验进行深入的思考和评价,属于实验的创新,是一个不断探索的过程,这个过程通常耗时长且有较大的难度,因此也经常被忽略。因此如果能够很好的设计和改进相关实验,将对学生深入理解实验原理,学习实验中包含的物质制备、分离、除杂等无机化学知识起到极大的帮助作用,并可以以此促进学生对有机化学和无机化学知识的整体掌握,提升学生分析问题和解决问题的综合能力。
下面,对中学《有机化学基础》教材中的一个设计性实验——溴苯的制备,以及两个有机改进性实验——乙酸乙酯的制备和醇的催化氧化分别进行讨论。
1 溴与苯反应的实验设计
溴与苯的反应在《有机化学基础》教材中的思考与交流栏目中,教材中明确提出要进行的实验装置设计是教学中要求做的实验,但很多中学教师却选择忽略。在维普中文期刊数据库中,以“溴与苯的反应”和“溴苯的制备”为关键词,检索时间默认设置为1989到2018,得到的文章较少,这也在某种程度上说明了化学教师对该实验的忽视。其中,检索到的文献——谈溴苯的制备实验,1999年由刘一兵和祁志富发表在《化学教育》期刊上,作者提出了基于当年教材中实验方案的改进实验,给出了实验装置并注明了实验方法和实验说明。但并未提及如何借助实验设计教学,促进学生对相关化学知识的学习,且实验设计与我们提出的方案不同。因此,有必要对此实验再做研究。鉴于实验的难点不是做实验而是设计实验装置,对此笔者设计了如图1所示的实验装置,制备溴苯并检验反应是否发生。
实验原理:苯与液溴在铁粉的催化下发生取代反应,生成溴苯和溴化氢。实验发生装置下端放置NaOH溶液,用来吸收Br2。a试管中盛放CCl4溶液,除去Br2,b试管中盛放石蕊或AgNO3溶液,检验HBr的生成。最后连接尾气处理装置。
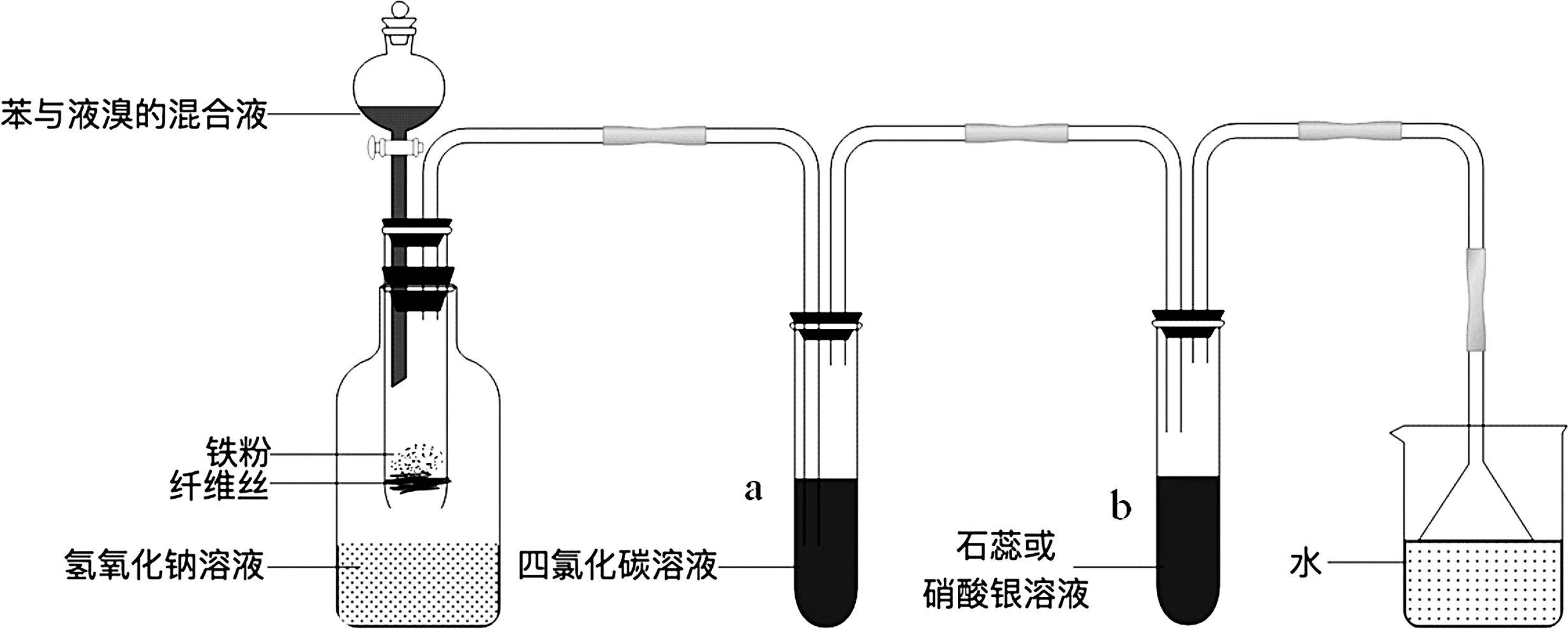
图1 溴苯的制备
对如何借助此装置进行教学,做出了相应的教学设计,具体内容如下(借助于对部分学生的访谈,主要给出教师对学生的系列引导以及我们对此做出的分析,以表明教学设计的目的和方向)。
问:(给出实验装置图)从这个装置中,可以获得哪些信息?
访谈中笔者发现,多数学生觉得无从下手,反映出学生提取信息的能力较差。
问:要处理什么气体?防止哪种气体倒吸?
经过大量的练习,学生对一些常见的问题有了条件反射性的回答,但对问题的实质并不十分理解。学生通常会说:极易溶于水的气体。
问:可能是什么气体呢?
(此处意在引导学生从装置中获取信息)找出这种“极易溶于水的气体”是HBr。
问:HBr是怎样过去的?前面的试管为什么没有进行防倒吸设计?
引导学生观察:第一个试管长进短出,说明不怕倒吸,第二个试管没有伸入液面中,说明怕倒吸。而倒吸本质上是发生在水溶液中的,怕倒吸说明溶剂是水,不怕倒吸说明可能是有机溶剂。在中学阶段,学生常见的溶剂有两种,无机溶剂是水,有机溶剂最常见的是CCl4。因此推测a试管中可以是CCl4溶液。
问:如何证明反应发生了?为什么b试管要防倒吸?为什么a中要用CCl4溶液?
引导学生自主分析:证明反应的发生可通过证明产物的生成来实现。可证明生成了溴苯,或证明生成了溴化氢。证明溴苯较难,可证明HBr的生成,即证明氢离子(用石蕊)或者溴离子(用AgNO3溶液)的存在,而石蕊和AgNO3溶液都是水溶液,因此第二个试管要防倒吸。同时,苯与Br2的反应放热,在挥发出的HBr气体中会混有Br2,Br2与H2O反应生成HBr和HBrO,会干扰对苯与Br2反应产生的HBr的检验,因此要除去挥发出来的Br2,故a试管中可用CCl4溶液。
问:如何得到纯净的溴苯?
涉及到提纯与除杂的相关知识。引导学生分析杂质是什么,再逐步除去。从反应装置中掉入瓶内的是苯、溴苯、溴单质与水,如何除掉溴单质?可以引导学生利用元素周期律,考虑溴与氯是同主族的,性质相似,Cl2用NaOH溶液吸收,所以Br2也可以,用NaOH吸收因此瓶子下端可放NaOH溶液。如何除掉溴苯中的苯?先分液,得到水层和有机层。要分离苯和溴苯,在找不到合适方法时,可利用两者沸点的不同,通过蒸馏将苯与溴苯分开,苯先气化,因为其相对分子质量小,沸点小。
在本实验中,倒吸问题、气体的溶解度问题、物质的检验及分离除杂问题等完全与无机化学实验的内容相吻合,在课堂中若能帮助学生从有机化学中找到无机化学的影子,将两者结合起来促进学生对化学知识的整体掌握,实验教学必将事半功倍。
2 制备乙酸乙酯和醇的催化氧化实验的改进
2.1 制备乙酸乙酯
制备乙酸乙酯的实验装置如图2所示。对于课本上的实验装置,要引导学生理清以下几点。
(1)饱和碳酸钠溶液起什么作用?
利用溶质Na2CO3吸收挥发出的CH3COOH;利用Na2CO3溶液便于乙酸乙酯的析出,因为乙酸乙酯在碳酸钠这种盐溶液中溶解度非常小;加热时C2H5OH也会挥发出来,可以利用溶液中的水除去C2H5OH。
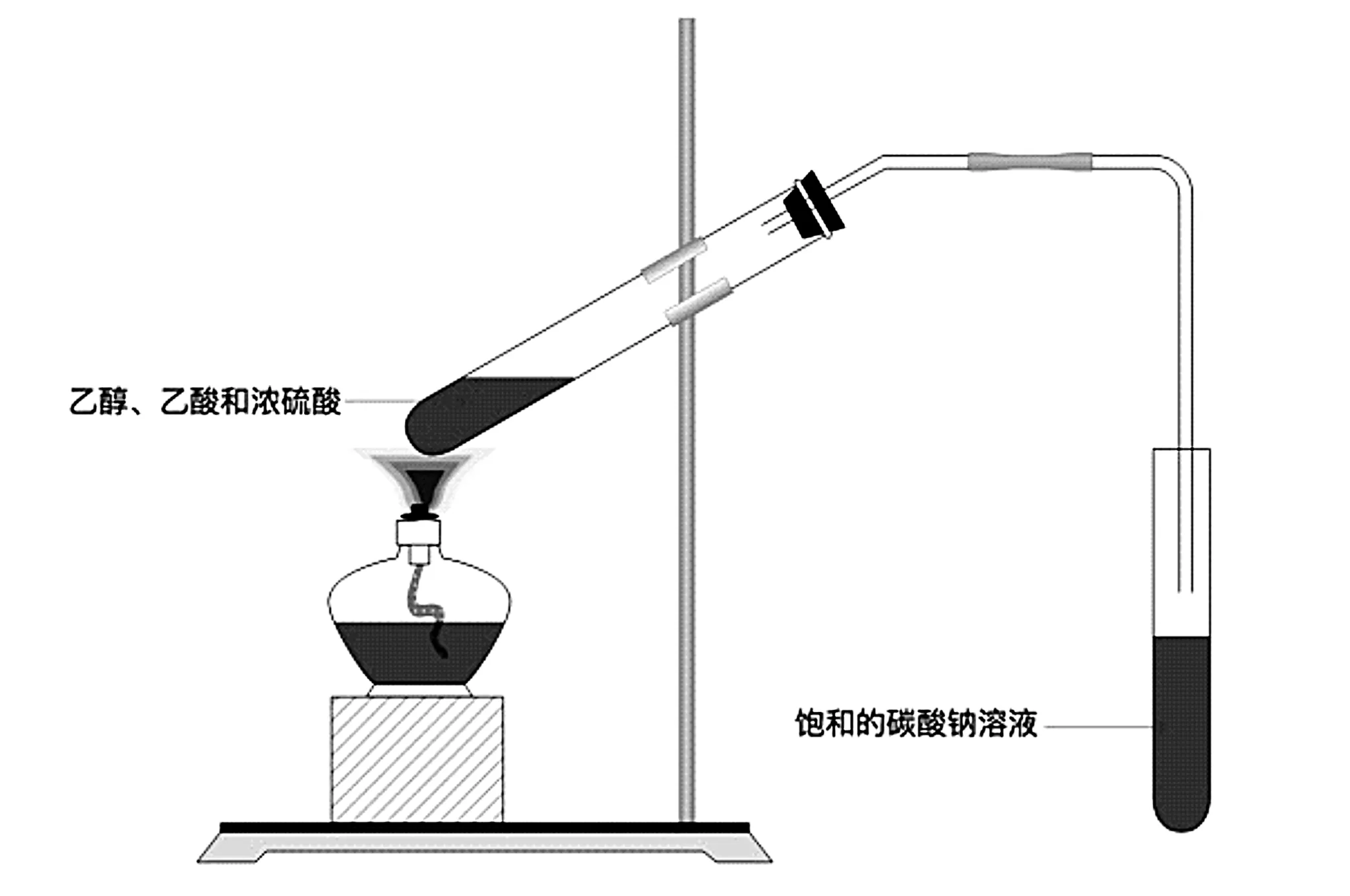
图2 实验室制取乙酸乙酯
(2)教材中右侧导管为什么不伸进入液面以下?
学生会习惯性的认为是为了防止倒吸,但是CH3COOC2H5不溶于水,挥发出的CH3COOH和C2H5OH都比较少,究竟为什么需要防倒吸,学生并不是非常清楚。此处主要是防止左侧试管受热不均试管内气压不稳定引起倒吸,因为有机物气化速度不均匀,实验时火苗也不稳定。
(3)有机实验中液体加热通常要加沸石或者碎瓷片,这是从实验安全的角度考虑的,但很多中学教师对此强调不足。
在维普中文期刊数据库中,以“乙酸乙酯的制备”为关键词,时间默认1989年至今,期刊范围选择“核心期刊”,搜索到两篇符合该主题的文献。孔令琦和丁伟比较了人教版、苏教版和上科版三个版本教材中乙酸乙酯制备实验存在的问题,并用正交实验法得出制备乙酸乙酯时各试剂的最佳配比、实验时的温度等,但并未对装置进行大的改进。丁爱军和王金龙提出乙酸乙酯的制备有诸多方法,包括乙酸酯化法、乙醛缩合法、乙醇脱氢法和乙烯加成法等,介绍了各种制法的反应原理和工艺特点,并强调乙酸酯化法是一种落后的生产工艺,已逐步被市场淘汰。文献中也没有提供明确的实验改进装置,提出对于工业生产而言,乙酸酯化法已逐步被淘汰,但这并不能否定乙酸酯化法制备乙酸乙酯的方法在中学化学教学中的重要作用。为了深化学生对乙酸乙酯制备内容的学习,设计了改进后的装置,如图3所示。
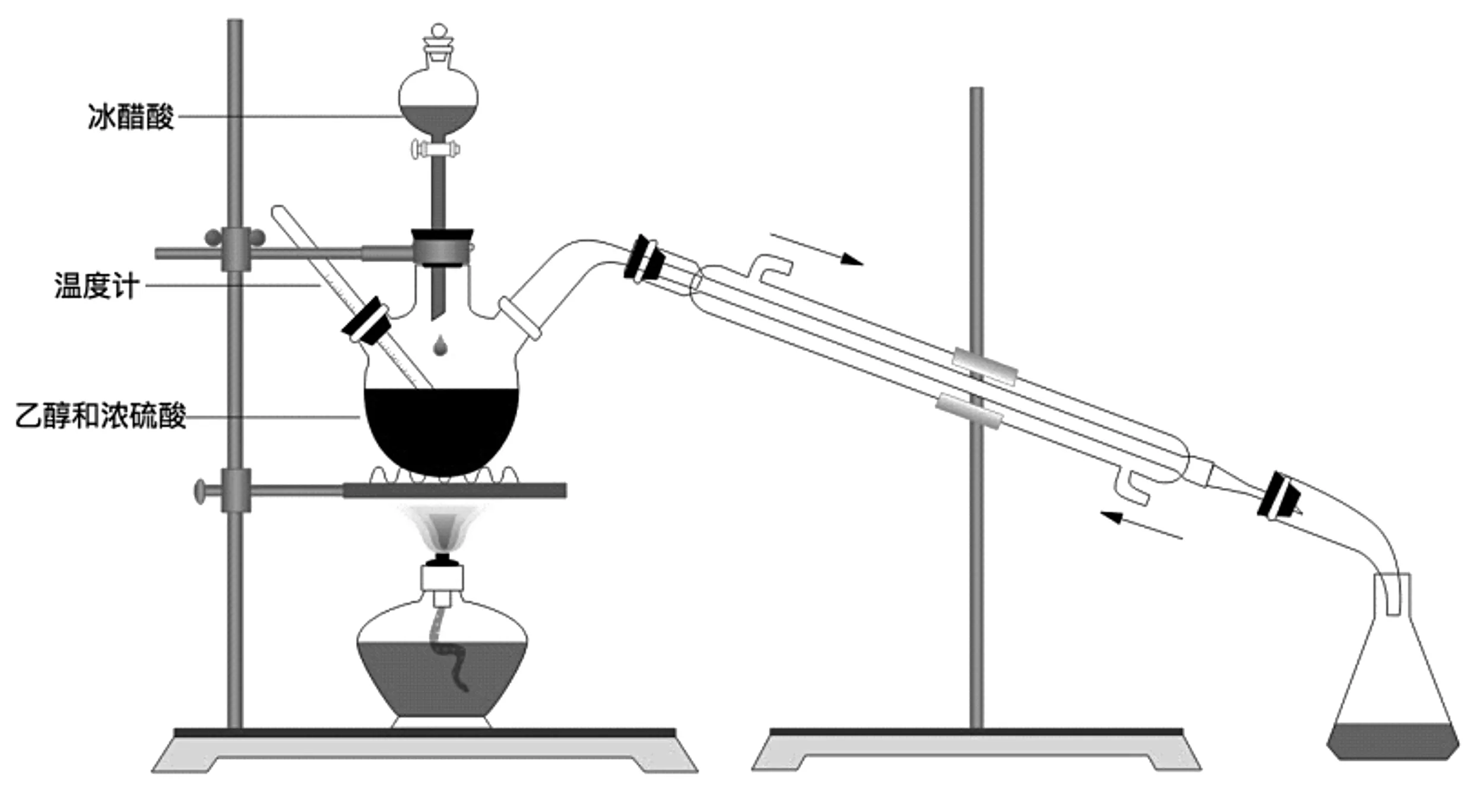
图3 乙酸乙酯的制备
该装置有以下优点:
(1)实验开始时,先加入C2H5OH,浓硫酸,再用分液漏斗逐滴加入冰醋酸,这样三种试剂的加入顺序就明了了;
(2)利用温度计较准确的测量乙酸乙酯的气化温度,保证“小火加热”,量化实验;
(3)利用冷凝管取代长导管,使气体充分液化,最终收集到液态的乙酸乙酯,减少其挥发浪费;
(4)利用分液漏斗可不断的滴加冰醋酸,促使平衡向正向移动,提高产率。
对应的主要教学设计如下:
问:新的实验装置有什么优点和缺点呢(鼓励学生去说)?
实践考察表明,看到温度计,学生会说控制温度;看到分液漏斗,会说控制反应速度。这样的说法是不严谨的。要说明怎样控制温度,控制什么的温度,具体是怎样控制反应速度的。
问:对于该实验,教材上要求“小火加热”,为什么不能大火加热?
引导学生从实验原理进行思考。CH3COOH和C2H5OH两者的沸点分别为117.9 ℃、78.3 ℃,较为接近,如果用大火加热,会促使大量的CH3COOH和C2H5OH一起挥发出来。实验表明,当采用大火加热时,右侧锥形瓶上方很快有一层厚厚的油状液体,但是将其拿起来震荡,锥形瓶中产生大量气泡,当气泡不再发生时,试管中液体就剩下一层了。因为此时出来的主要是CH3COOH和C2H5OH,反应根本没有来得及生成CH3COOC2H5。
如果有一个温度计准确指示CH3COOC2H5的气化温度,就能保证出来的主要是CH3COOC2H5了。目标产物是CH3COOC2H5,因此需要测量的是它的气化温度,由此提醒学生联想蒸馏实验,蒸馏实验中测量的就是物质的气化温度,而在蒸馏实验中,对温度计的水银球的位置是有要求的,应置于蒸馏烧瓶支管口处稍靠下的位置。该装置虽然不是蒸馏装置,也不是测CH3COOC2H5沸点的实验,但是实验目的是得到CH3COOC2H5,温度计的水银球若从溶液中抬出来,离开加热的液面,这样就能测量液体气化的温度,从而更好的控制反应的温度,获得目标产物。而给出的装置图中,温度计的水银球在液面以下,这在一定程度上可以说是该装置的一个缺点。
问:分液漏斗起什么作用?
教材中滴加3种药品的顺序,没有具体说明,但是文字部分提到“在试管中加入乙醇,浓硫酸,乙酸”。对于试剂的加入顺序,部分教师和学生并不是很清楚。许多教师认为从安全性角度考虑,应最后加浓硫酸,那么,书上的顺序能调整吗?若先加C2H5OH和CH3COOH,加入浓硫酸后放出大量热,两者就会都挥发,损失试剂较多,若把浓硫酸放在中间加入,加入浓硫酸后待到冷却室温再加另外一种试剂,便可以减少试剂的浪费。而CH3COOH和C2H5OH相比,C2H5OH的密度较小,因此,先加C2H5OH,再加浓硫酸,最后加入CH3COOH。
对于基础较好的学生,也可引导他们从另外一个角度考虑:催化剂的催化机理是改变反应的路径,降低活化能,而催化剂本身的质量和化学性质不改变。在有机化学中,中学层面对浓硫酸的讨论主要是作为催化剂、脱水剂,在此反应中浓硫酸如何催化反应?依然是改变反应路径。先加C2H5OH再加浓硫酸,发生醇和无机酸的酯化,C2H5OH与浓硫酸反应生成磺酸乙酯(C2H5OSO3H),再加入CH3COOH,酸类部分与磺酸发生酯交换,生成CH3COOC2H5。如此,弄清楚了反应机理,就很容易理解药品加入的顺序了。
2.2 乙醇的催化氧化
该实验的原理是乙醇与氧气在催化剂和加热的条件下生成乙醛和水。在维普中文期刊数据库中,以“乙醇的催化氧化”为关键词检索1989年至今的核心期刊,得到的文献不多。其中李周平和张乐伟对实验的发生装置提出改进建议,将铜丝换成铜片,并置于三脚架上加热,然后向铜片上滴加乙醇,达到更好的实验效果。樊会武、朱旋农和姚志红“采用洗耳球鼓入空气的方法成功地解决了产物的量和产物能否顺利进入检测体系的问题”并给出了实验装置,文章指出改进后的实验取得了较为良好的效果。两篇文献都为达到更好的实验效果上提出了改进措施,但本文提出的改进措施与文献中不尽相同,且考虑到教材中只简单描述了发生装置,没有氧气的制备装置和产物的检验装置,本研究补充这些装置,以加深学生对化学相关知识的理解和应用,并改进实验发生装置,使实验更加准确和严密。具体装置如图4所示。
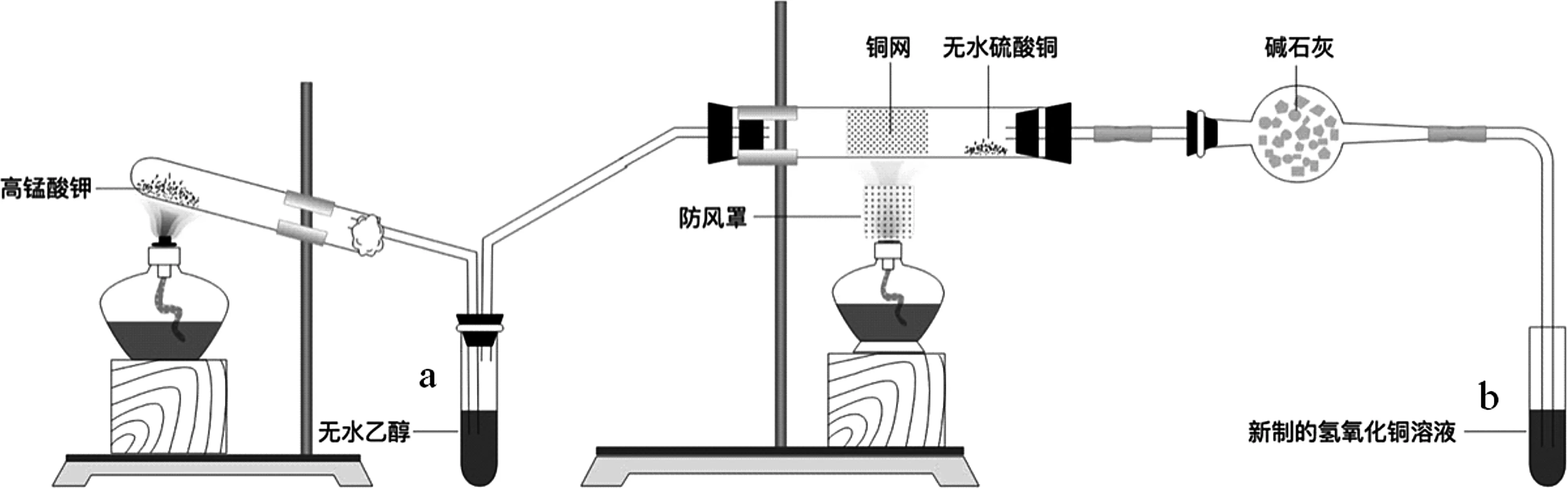
图4 乙醇的催化氧化
装置说明:第一个发生装置是制氧气的装置,a试管中的液体是无水乙醇,第二个发生装置中有铜,干燥管中装碱石灰,b试管中加入新制的氢氧化铜。已知乙醇的沸点为78.3 ℃。相关教学设计如下。
问:第一个发生装置中应放什么?
引导学生观察实验装置并从中提取信息,结合安全性等条件选择最优原料。装置中试管向下倾斜,所以试管中应加入的是固体,不能为过氧化氢。可以是高锰酸钾或氯酸钾与二氧化锰混合物。有学生可能会想到氯酸钾,但是氯酸钾是一种危险品,根据实验安全的要求,最好放高锰酸钾。试管口应放一团棉花,防止高锰酸钾颗粒冲出去。
问:a试管中液体是无水乙醇,已知乙醇的沸点是78.3 ℃,如何使乙醇平稳气化?
如何有效利用题目中的数据,这是在教学中要帮助学生学会获得的重要信息。实践发现,学生通常答:水浴。这是不规范的。水浴有冷水浴,也有热水浴,说加热也不合适。因此,讲解时应强调“从题目中提取信息的能力”,比较严谨的回答是:置于略高于78.3 ℃的热水中加热。
问:导管从a试管中出来,斜向上,为什么?为什么不平放,或者向下?
引导学生关注细节,深入理解实验设计的每一部分。乙醇的沸点78.3 ℃,当离开水浴的温度,乙醇就会液化,如果平放或者向下就可能会有液态乙醇流入接下来的催化氧化装置中,产生安全隐患。斜向上导管的作用是:导气同时可将液化的乙醇流回试管中。
问:在这个装置中需要加热的装置有哪些?
引导学生关注整个实验装置,综合考虑问题。高锰酸钾加热、乙醇水浴加热、催化剂加热、新制氢氧化铜检验醛基也要加热。
问:高锰酸钾和铜加热的顺序是怎样的?
帮助学生深入理解实验原理。有的学生认为若先加热铜,空气中的氧气会与铜反应,因此不可取。反观教材,做此实验时把铜丝弯成螺旋状,在酒精灯火焰上灼烧、至红热(烧黑变成氧化铜,再烧红是氧化铜升温的过程)也是在空气中加热,对实验没有太大影响。若先加热高锰酸钾,则氧气通过铜时,不会发生反应,浪费氧气。因此,需要先加热催化剂铜,再加热高锰酸钾,最后再水浴加热无水乙醇,使乙醇蒸汽与氧化铜反应。
问:在这个反应中能否不使用干燥管?
帮助学生建立“只要检验的气体与空气中某种气体的成分相同,必须防止从装置尾端倒流入的气体”的思维方式。要想检验醇催化氧化的产物,即水的生成,就必须防止空气中的水蒸气进入导管。因此,干燥管中加碱石灰,以检验水的生成,尤其是在装置尾端,新制氢氧化铜加热,水蒸气很容易倒流回去。
该实验也是有机化学与无机化学一个非常好的结合点,包括硫酸铜检验水的问题、水浴加热的问题、加热顺序问题、导管问题,这些都是无机化学中的重要知识点。
3 研究启示
3.1 深度挖掘教材中的实验,深化教材教学价值
教材是沟通教师与学生的主要凭借,是教师进行教育教学工作的主要依据,是学生获得系统科学知识、形成正确价值观念的重要工具。教材能够帮助学生在学习过程中获得更加系统化、规范化的知识,并便于学生自主学习、复习和完成作业。教材的编写汇集了该学科诸多教育教学工作者的智慧,教材的每一部分内容都是精心设计的,思考交流栏目中的问题,作为教材重要的一部分,也是考试命题的重要参考,要引起教师的足够重视。
3.2 在有机化学的学习中关注实验,从有机实验与无机实验的关联中找到实验考查的关键点
有机化学与无机化学是中学化学的核心内容,长期以来,两者被人为的分离,导致一些学生对某一方面内容的害怕或者厌恶,而另一方面却可以学得很好。然而,化学作为一门基础性学科,其中有机与无机的内容更是基础中的基础,基础性的内容是不可分割的,两者有着诸多的联系,只是因为学科的精细化,便于教师的教和学生的学才人为地划分为有机化学和无机化学等。在有机化学教学中,无机化学实验的教学至关重要,而如同上文提到的溴苯制备等有机实验中,都蕴含着重要的无机化学知识。在教学中,若能在有机实验的教学中提醒学生将无机化学的知识点联系起来,找到实验要考查的关键点,便可以帮助学生融会贯通,起到事半功倍的效果。

