β1受体阻滞剂对早期脓毒性休克病人心肌损伤及预后的影响
沈雯雯,徐前程,钱言,陈尚华
脓毒症(sepsis)是由感染引起的失控性全身炎症反应综合征,可发展为脓毒性休克,最终导致多脏器官衰竭。脓毒症病人心功能受到抑制,心脏收缩功能降低、顺应性下降,对心脏造成一定程度损伤[1]。而β1受体阻滞剂用于脓毒性休克可以稳定循环,改善心肌损伤[2],但由于其对心脏的直接作用有时会导致或加重低血压,使得应用受限。关于β1受体阻滞剂对脓毒性休克病人心肌损伤及预后的影响,目前国内外研究甚少,为此,笔者回顾性对比分析54例早期脓毒性休克病人β1受体阻滞剂治疗后组织代谢指标变化以及影响预后的危险因素,为临床提供一定参考。
1 资料与方法
1.1一般资料采用回顾性研究方法,收集2013年1月至2015年12月芜湖市第二人民医院重症医学科54例确诊为脓毒性休克病人的临床资料。
1.2纳入标准和排除标准纳入标准:(1)符合2016 年美国重症监护医学会(SCCM)“拯救脓毒运动:脓毒症和脓毒性休克的管理国际指南”诊断标准[3];(2)年龄>18岁;(3)各项监测指标资料齐全;(4)治疗组入科后48 h开始使用β1受体阻滞剂。排除标准:(1)入科后3 d内死亡或自动出院者;(2)入院前48 h使用过β1受体阻滞剂者;(3)肿瘤晚期及各种疾病的终末期,不可逆转的临终状态。本研究符合《世界医学协会赫尔辛基宣言》相关要求,征得病人或其近亲属同意并签署知情同意书。
1.3研究方法以是否使用β1受体阻滞剂将所有病人分为治疗组与对照组,再根据28 d的生存结局分为存活组和死亡组。病人均按照2012年严重脓毒症与脓毒性休克治疗国际指南给予规范治疗,包括液体复苏,血管活性药物应用,抗菌药物治疗策略以及其他脏器支持治疗,治疗组在对照组基础上加用鼻饲β1受体阻滞剂重酒石酸美托洛尔片12.5 mg,每日两次。收集所有病人的一般资料,包括性别、年龄、感染部位、合并基础疾病情况等,记录入院24 h内急性生理和慢性健康评分(APACHEⅡ评分)和治疗72 h后血流动力学指标变化、血清降钙素原(PCT)、肌钙蛋白I(CTnI)、血乳酸(Lac)水平,并观察病人的转归情况。
2 结果
2.1一般资料的比较治疗组和对照组性别、年龄、APACHEⅡ评分及合并基础疾病等一般资料比较,差异无统计学意义(P>0.05);治疗组住ICU时间缩短,差异有统计学意义(P<0.05)。见表1。
2.2心肌标志物和循环指标的比较72 h后治疗组心室率(HR)和CTnI水平低于对照组(P<0.05),两组病人心指数(CI)、平均动脉压(MAP)、血管活性药物去甲肾上腺素(NE)的用量、72 h液体平衡量以及Lac水平差异无统计学意义(均P>0.05),见表2。
2.3不同预后组一般资料的比较死亡组APACHEⅡ评分、CTnI、Lac高于存活组(P<0.05);死亡组β1受体阻滞剂使用率低于存活组(P<0.05);两组性别、年龄、PCT、PLT、MAP、PaO2(动脉血氧分压)和基础疾病等比较差异无统计学意义(P>0.05),见表3。
2.4脓毒症病人预后影响因素的ROC及logistic回归分析ROC分析知:APACHEⅡ评分最佳预测值为19.5分,曲线下面积0.92,灵敏度和特异度分别为0.91、0.84。以CTnI水平作预测病人预后的ROC曲线,CTnI水平最佳预测值为1.21 μg/L,曲线下面积0.79,灵敏度和特异度分别为0.84、0.77。以APACHEⅡ评分19.5分、CTnI水平1.21 μg/L作为分界点,logistic回归显示APACHEⅡ评分>19.5分、CTnI>1.21 μg/L是早期脓毒性休克病人死亡的危险因素,而β1受体阻滞剂是病人预后的保护性因素(P<0.05),见图1、图2、表4。

表1 脓毒性休克54例一般资料两组比较
注:①肺部②腹腔③血流④软组织⑤其它;“—”表示采用Fisher确切概率法

表2 脓毒性休克54例心肌标志物和循环指标的分组比较
注:HR为心室率,CI为心指数,MAP为平均动脉压,NE为去甲肾上腺素,Lac为动脉血乳酸;1 mmHg=0.133 kPa

表3 脓毒性休克不同预后组一般资料的比较
注:PCT为血清降钙素原,CTnI为肌钙蛋白I,Lac为血乳酸,MAP为平均动脉压,PaO2为动脉血氧分压
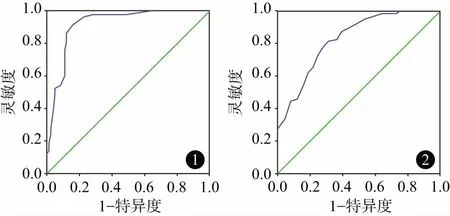
图1 APACHEⅡ评分预测脓毒性休克病人预后的ROC曲线图2 CTnI预测脓毒性休克病人预后的ROC曲线
3 讨论
脓毒性休克内源性交感系统过度激活,造成交感风暴,β1肾上腺素增多可促进心肌收缩力和心率增加,从而增加心肌氧耗,导致心肌能量供需失衡,另外持续的β1肾上腺素增多亦可刺激白细胞介素-6、肿瘤坏死因子等炎性因子分泌增加,进一步加重心肌损伤[4]。近年来的研究发现β受体阻滞剂可以改善脓毒症病人的心血管功能、免疫功能和凝血功能[5],但其负性肌力作用又使得应用受到限制。
越来越多的研究已证实β1受体阻滞剂在早期脓毒性休克病人中使用的安全性[5],目前的研究数据支持它的使用主要针对于经过液体复苏和小剂量血管活性药物可以稳定血流动力学的病人,在使用β1受体阻滞剂后不增加血管活性药物的剂量[6]。本研究结果发现治疗组住ICU时间缩短,但28 d病死率未下降,与 Galbois等[7]报道的一致。但最近Fuchs C等[6]研究表明长期口服β1受体阻滞剂的病人发生脓毒性休克后继续服用该药可以缩短住院时间,降低90 d以内的病死率。动物实验中,Irada等[8]研究亦发现艾司洛尔可以通过调节CAMP和TNFSF10基因表达,从而抑制脓毒症诱导的免疫反应,提高生存率。研究结论不一致的可能原因为临床试验混杂因素较多,如病人年龄、合并基础疾病情况、感染部位、感染的病原体类型等均可能影响试验结果,另外使用β1受体阻滞剂的类型、剂量以及干预时间点的不同也可对试验结果造成影响。

表4 早期脓毒性休克病人预后影响因素的logistic回归分析
本研究中,鼻饲美托洛尔显著地降低了早期脓毒性休克病人的HR,而治疗组和对照组病人的液体平衡量、血管活性药物的使用剂量差异无统计学意义。Lac是体内糖代谢的中间产物,其升高程度及清除率反映脓毒症病人病情严重程度的变化[9],两组间Lac水平亦差异无统计学意义,提示β1受体阻滞可减少心脏做功、降低心肌耗氧量,且未引起病人血流动力学的恶化,对病人组织灌注无影响,有助于纠正组织氧供需的失衡。本研究还检测了血CTnI水平,它是心肌细胞受损甚至坏死时血浆诊断标志物,与脓毒症休克病人的预后密切相关[10]。王春源等[11]研究发现急诊脓毒性休克以及老年严重脓毒症病人CTnI水平愈高提示病人预后愈差。本研究中死亡组CTnI水平显著高于存活组,治疗组CTnI低于对照组。近期的meta分析亦显示,β1受体阻滞可以降低脓毒性休克病人的心率、CTnI水平,但对血流动力学参数影响不大[12],基本支持本研究以上的结论。
本研究还对早期脓毒性休克病人预后影响因素进行logistic回归分析,显示APACHEⅡ评分>19.5分、CTnI>1.21 μg/L是影响病人预后的危险因素,而使用β1受体阻滞剂可以改善此类病人预后。推测β1受体阻滞剂改善心功能和预后的可能机制有以下几点:一方面β1受体阻滞剂上调了心肌 β1受体含量,改变β肾上腺素能受体各亚型的比例,减轻心肌线粒体的损伤,改善心肌的能量代谢,提高心功能[13];另一方面阻断β1受体将通过下调细胞因子的表达下调炎症反应[14];此外,脓毒性休克病人感染诱发的高肾上腺素状态导致机体的代谢由平衡向分解代谢的方向移动,如高血糖、高乳酸血症及蛋白分解增加,而β1受体阻滞剂在一定程度上可减少底物耗竭[5],这可能为我们后续进一步研究指明方向。
综上所述,本研究结果表明β1受体阻滞剂组总体上可以改善早期脓毒性休克病人的心肌损伤,缩短住ICU时间,但由于本研究样本量较小,为回顾性研究,具有局限性,且对于使用的时机、剂量、心率控制范围和对病人的长期预后仍需更大规模的前瞻性临床研究。

