IVIM-DWI对TACE序贯氩氦刀治疗肝癌疗效的评估价值
程瑞文 ,李 平 ,邓梨平 ,谢太喜
(湖南中医药大学第一附属医院①血管肿瘤介入科,②放射科,湖南 长沙 410007)
肝癌是临床上常见的消化道恶性肿瘤,发现时多为中晚期而失去外科手术机会。TACE为无法外科手术切除肝癌患者的首选治疗方法,其疗效已得到公认[1]。介入在内的综合治疗是肝癌的发展趋势,TACE联合氩氦刀冷冻消融治疗中晚期肝癌是有效的综合治疗方法之一[2-3]。本研究尝试使用基于体素内不相干运动弥散功能成像(intravoxel incoherent motion-diffusion weighted imaging,IVIM-DWI),即双指数模型DWI对TACE序贯氩氦刀治疗肝癌的疗效评估价值进行探讨。
1 资料与方法
1.1 研究对象 随机选取2016年1月至2017年12月我院收治的40例肝癌患者,均为男性;年龄37~67岁,平均(55.0±9.2)岁。纳入标准:①符合中国抗癌协会肝癌专业委员会制定的肝癌诊断标准[4];②均经病理活检或影像学检查及血清甲胎蛋白(AFP)检测等明确诊断;③肝内肿瘤数目≤5个;④肝功能Child A级或B级,使用Karnofsky行为状态评分标准(Karnofsky performance status,KPS)[5],KPS 评 分 均 ≥60分。排除标准:①肝功能Child C级或D级;②原发性肝癌已确诊远处脏器转移者;③术后未复查DWI者;④脱访或随访时间少于6个月者。其中原发性肝细胞癌38例,胆管细胞癌2例;3例为原发性肝癌外科根治性术后复发,其他37例均未行外科手术治疗。肝内结节单发33例,多发7例;肝功能Child A级25例,Child B级15例;合并肝门区或腹膜后淋巴结转移4例,均无门脉癌栓形成。
1.2 治疗方法 40例行影像学检查及血清AFP检测后,先接受TACE、术后4周内序贯氩氦刀冷冻消融治疗。①TACE:根据术前CT增强扫描显示的肿瘤病灶(图1a),使用5F-RH导管联合2.4F微导管行超选择腹腔干及肠系膜上动脉造影,造影证实后均使用奥沙利铂0.1 g、氟尿嘧啶1.0 g联合灌注化疗[6-7],根据肿瘤大小注入超液化碘化油5~15 mL乳剂栓塞肿瘤供血血管,栓塞至对比剂停留2个心动周期时停止(图1b)。TACE术后1~2周复查MRI平扫+IVIM-DWI检查,通过 MRI确定活性病灶[8-10],针对活性区域于TACE术后4周内行氩氦刀冷冻消融术(图1c)。②氩氦刀冷冻消融术:根据术前MRI显示肿瘤的大小、形态、位置及活性区域,制订CT引导下冷冻方案。在CT引导下逐个穿刺点使用氩氦刀穿刺针进入肝内病灶,给予氩气(纯度99.999%)冷冻消融15 min(压力 3 500 kPa),CT扫描检测冷冻范围,氦气(纯度 99.999%)复温 3 min(压力 2 500 kPa),重复1次。拔针,压迫止血并包扎。术后行CT平扫复查,确保冰球完全覆盖肿瘤活性部分边缘范围大于1 cm(图 1d)[8]。
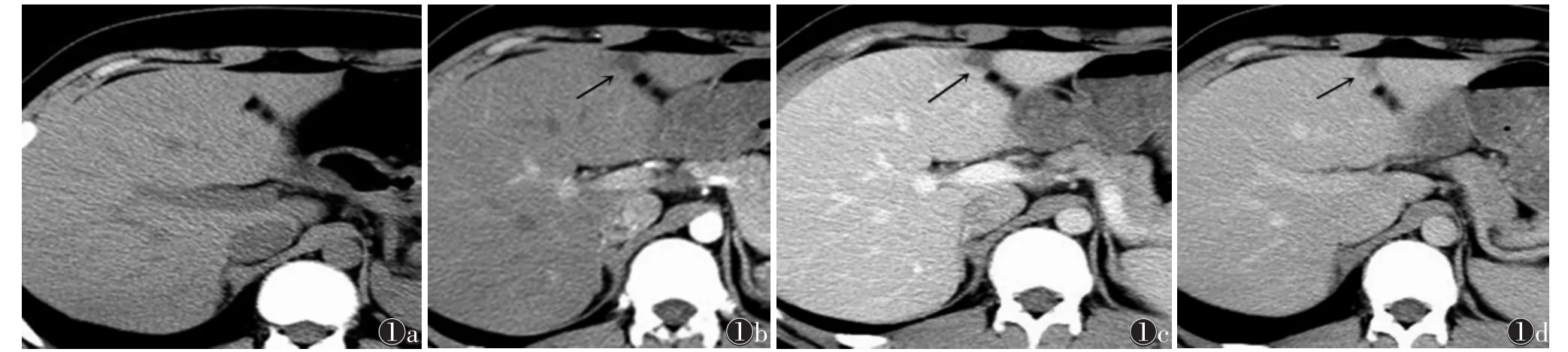
图1 男,61岁,原发性肝癌 图1a CT增强扫描动脉期示右肝SⅦ段直径约2.3 cm结节,动脉期明显强化(箭头) 图1b TACE术后显示肝癌病灶碘油沉积(箭头) 图1c DWI示病灶呈高信号,提示肿瘤有活性(箭头) 图1d 活性病灶行CT引导下氩氦刀冷冻消融术(箭头)
1.3 MRI检查方法
1.3.1 扫描方法 采用GE Signa HD 3.0 T MRI仪与腹部专用表面线圈。采用呼吸门控防止运动伪影。先行上腹部平扫,再行多b值DWI及动态增强扫描。传统单指数模型DWI,b值取0和1 000 s/mm2,矩阵 80×128,NEX 4;IVIM-DWI的多 b 值(b=0、50、100、200、400、800、1 000 s/mm2)DWI,矩阵 96×130,TR 9 000 ms,TE 最小值,层厚 4 mm,层距 1 mm。动态增强扫描:横轴位LAVA技术,层厚5 mm。蒙片扫描结束后注射对比剂莫迪斯,流率2 mL/s,剂量0.2 mL/kg体质量,17 s后开始连续2次增强扫描(动脉早期、动脉晚期),50 s后扫门脉期,5 min后扫延迟期,50 min后再次扫延迟期。
1.3.2 图像后处理 扫描结束后将原始图像数据传至AW4.6工作站,应用Functool软件中的ADC软件对DWI图像进行后处理,在治疗术后DWI高、低信号区标记ROI。以MRI动态增强扫描图像为参考,在显示病灶最清楚的相应b值的DWI图像上手动放置病灶ROI。ROI会在相应解剖层面,以相同位置同步复制到standard ADC值伪彩参数图或Slow ADC值、Fast ADC值及f值伪彩参数图上,并自动得到单指数模型DWI检查的ADC值,及IVIM-DWI检查的Slow ADC 值、Fast ADC 值及 f值(图2)。
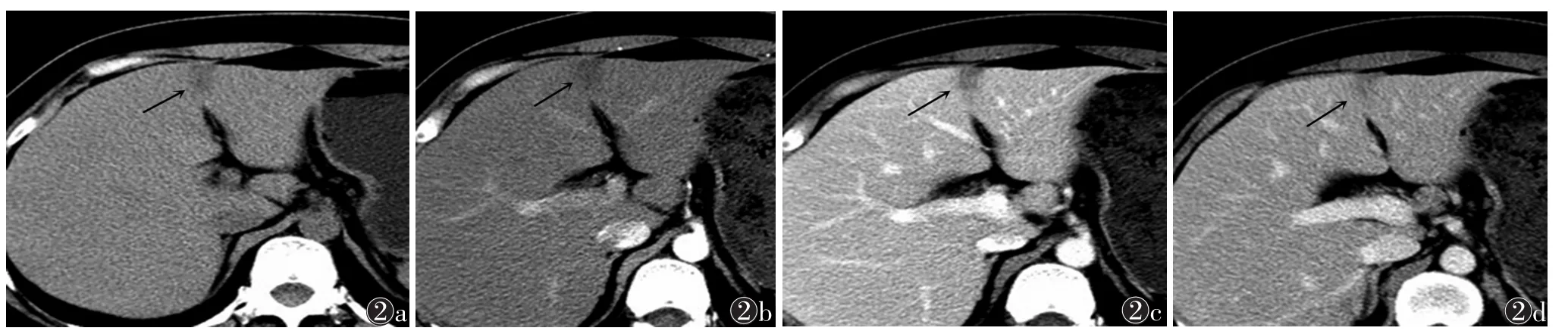
图2 男,47岁,TACE联合氩氦刀冷冻消融术后4周 图2a DWI示2个可疑残留病灶(箭头) 图2b b=800 s/mm2时后处理测量ADC值图2c 体素内不相干运动(IVIM)-DWI测量Fast ADC值 图2d IVIM-DWI测量Slow ADC值
1.4 CT扫描方法 采用Philips 64排128层brilliance CT对肝脏行3期扫描。使用对比剂碘海醇(剂量1.8 mL/kg体质量)经高压注射器团注扫描,流率3.0 mL/s。层厚、层距均为5 mm,25~27 s扫动脉期,65 s扫门脉期,5 min扫延迟期。扫描结束后将原始图像数据传至EBW工作站行三维重建。治疗术后平扫无碘油沉积区为重点观察区,在显示病灶强化最明显的区域手动放置病灶ROI,测量动脉期CT值,复制同样大小ROI至平扫期相同位置,测量CT值,相减得出CT净增值(图3)。
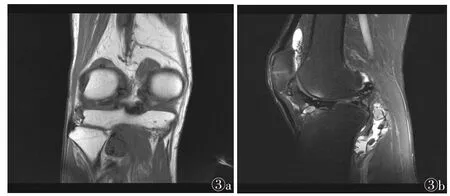
图3 男,46岁,TACE术后行CT增强扫描 图3a 平扫可见碘油沉积部分缺损,CT值38.77 HU 图3b 增强扫描可见碘油沉积缺损区外缘明显强化,CT值92.82 HU,得出CT净增值为54.05 HU
1.5 评价指标 临床判断标准:DWI检查后行经皮穿刺活检术,行免疫组化检查明确病灶性质;连续2次以上的影像学检查,持续随访6个月以上观察病灶;病灶变化:进展为残留灶,无变化为坏死灶,新增病灶并持续进展为新发灶[9]。
CT增强扫描病灶活性区域界定标准[10]:与术前对比,选择术前可疑活性区域,测量病灶平扫、增强扫描CT值及CT净增值。增强扫描表现为典型“快进快出”特征或CT值增加40 HU以上考虑有活性,小于10 HU考虑病灶无活性,10~40 HU无法判断,由3位副高以上职称专家单独阅片判读有无活性。
DWI界定标准[11]:在后处理工作站观察 DWI图像,并与术前原发癌灶对比,观察信号特点,测量原发癌灶氩氦冷冻区域或新发病灶的ADC、Slow ADC、f值及Fast ADC值,用以判断肝癌氩氦刀冷冻术后的坏死灶、残留灶或新发灶。若病灶信号均匀、ADC值高于周围肝实质或绝对值>1.5×10-3mm2/s,考虑坏死,诊断为坏死灶;若有常规扫描信号可疑区域,该处ADC值<1.0×10-3mm2/s,则判断病灶仍有活性部分,诊断为残留灶;术后出现的新发病灶,且ADC值<1.0×10-3mm2/s,诊断为新发灶;ADC值为(1.0~1.5)×10-3mm2/s,需结合临床综合诊断,由 3位副高以上职称专家单独阅片判读。IVIM模型以b值增高至1 000 s/mm2时病灶仍呈高信号判断为残留灶;病灶与周围组织等信号判断为坏死灶;随访中新增病灶且为高信号判断为新发灶。
1.6 统计学方法 采用SPSS 17.0分析软件进行数据分析。定量资料以±s表示。肝癌治疗后残留灶、坏死灶、新发灶间ADC值、Slow ADC值、Fast ADC值及f值的比较采用单因素方差分析;ADC值与Slow ADC值比较、ADC值与f值比较采用配对t检验。以P<0.05为差异有统计学意义。ADC值、Slow ADC值、CT净增值对活性病灶评估的敏感度及特异度采用诊断实验的ROC曲线分析。
2 结果
2.1 一般情况 TACE序贯氩氦刀冷冻治疗40例,原发病灶46个;术后1个月CT及MRI共发现病灶46个;术后4个月CT及MRI共发现病灶54个。不同影像学检查对病灶性质判断能力见图4。

图4 不同影像学检查对肝癌治疗后病灶检出柱形图(单位:个)
术后4个月CT平扫加增强扫描共发现病灶47个,MRI平扫加增强扫描共发现病灶52个。CT平扫加增强扫描与MRI平扫加增强扫描在肝癌TACE序贯氩氦刀治疗后病灶数目检出方面差异无统计学意义(P=0.076)。
将影像学检查所见病灶性质分为可判断(坏死灶+残留灶+新发灶)与无法判断2组。CT平扫加增强扫描发现47个病灶,其中性质可判断30个,无法判断17个;IVIM-DWI发现病灶54个,其中性质可判断52个,无法判断2个。经检验不符合方差齐性,采用非参数Kruskal-Wallis检验,IVIM-DWI与CT平扫加增强扫描在判断病灶性质方面差异有统计学意义(P=0.000)。
2.2 各组间单指数模型DWI及IVIM-DWI各参数比较
2.2.1 TACE序贯氩氦刀冷冻消融治疗后肝癌活性残留灶、坏死灶、新发灶的4项参数,均符合正态分布且符合方差齐性。单因素方差分析结果显示,3组间ADC值、Slow ADC值、f值差异均具有统计学意义(均P<0.05),Fast ADC值差异均无统计学意义(均 P<0.05)(表 1)。
表1 治疗后不同病灶各参数均值及单因素方差分析(±s)

表1 治疗后不同病灶各参数均值及单因素方差分析(±s)
组别 ADC值(10-3mm2/s) Slow ADC值(10-3mm2/s) f值(%) Fast ADC值(10-3mm2/s)残留灶 1.17±0.18 1.05±0.15 9.18±1.87 15.24±4.58新发灶 1.11±0.12 0.96±0.11 16.10±7.87 18.69±4.58坏死灶 1.84±0.36 1.69±0.21 8.33±1.52 1.73±0.60 F值 110.03 188.19 13.21 4.56 P值 0.000 0.000 0.032 0.230
2.2.2 3组间进一步两两比较,新发灶与残留灶的Slow ADC值、ADC值差异无统计学意义(均P>0.05),坏死灶与残留灶及新发灶的ADC及Slow ADC间比较差异均有统计学意义(均P<0.01)(表2)。

表2 肝癌治疗后不同病灶各参数两两比较结果
2.3 IVIM-DWI与单指数模型DWI及CT净增值诊断敏感度、特异度比较 临床以病理学检查或6个月以上随诊及连续2次以上影像学检查为标准确定病灶有无活性,分别将活性病灶(残留灶及新发灶)与无活性病灶(坏死灶)的ADC值及Slow ADC与临床标准为对比,绘制ROC曲线(表3)。结果显示,IVIM-DWI的Slow ADC值测定在敏感度、特异度上均高于单指数模型DWI的ADC值及CT净增值测定。

表3 ADC值与Slow ADC值ROC曲线下面积、敏感度、特异度及界值
3 讨论
3.1 肝癌治疗后疗效评估 肝癌治疗后疗效评估方法主要有3种:生存分析法、血清AFP监测和影像学检查。生存分析需大样本、长期间随访,不适合介入术后短期个体化评估。血清AFP是评估肝癌活性的重要指标之一,但AFP短期波动性大,阳性率低,特异度不高,35%的肝细胞癌患者AFP检测呈假阴性(包括肝内胆管癌、低分化肝细胞癌、部分高分化肝细胞癌或肝细胞癌已坏死液化者),仅靠单纯AFP检测不能有效诊断[12]。影像学检查因简单易行、图像直观,广泛应用于肝癌介入治疗后疗效评估。
MRI能有效、清晰、直观地反映病灶特征,已成为肝癌介入术后常规检查方法,并已成为共识[13-16]。本研究也证实,IVIM-DWI的Slow ADC值测定在敏感度、特异度上均高于单指数模型DWI的ADC值及CT增强扫描中CT净增值。DWI作为一种功能性成像技术,无需注射对比剂,可在分子水平对生物体的组织结构及功能状态进行无创检查,在鉴别坏死与活性肿瘤组织上具有明显优势[17]。
3.2 IVIM-DWI扫描技术及呼吸门控技术 本研究中,为了尽量忽略血流、微循环等对弥散产生的影响,在多 b 值 DWI中,采用 7 个 b 值(0、50、100、200、400、800、1 000 s/mm2),b=1 000 s/mm2时图像质量仍较清晰(图 4),与报道[7,18]推荐使用 8 个 b 值(0、25、50、75、100、200、500、800 s/mm2)有一定差异,分析与本研究MRI扫描加用呼吸门控技术有关。
3.3 IVIM-DWI的局限性 ①本研究已经证实,IVIMDWI在肝癌治疗后活性病灶评估中具有较高的特异度,但单纯使用IVIM-DWI会遗漏直径<0.5 cm病灶,使用DSA可证实病灶。②部分病灶在消融术后1个月内信号不稳定,判断病灶活性存在困难。③各研究中心采用的IVIM-DWI参数及后处理软件有差距,得出的界定良恶性病灶的ADC值或Slow ADC值也存在一定差距[18-20]。因此,在具体临床实践中需总结经验,结合多种影像学检查及血清AFP检测等。
总之,IVIM-DWI所得到的参数能对肝癌氩氦刀冷冻消融术后残留灶、坏死灶及新发灶进行有效评估。且IVIM-DWI扫描技术评估肝癌TACE序贯氩氦刀治疗的疗效价值,明显优于单指数模型DWI及CT增强扫描,对肝癌的临床治疗及预后判断具有重要意义,可指导临床后续治疗方案的制订,值得推广应用。

