分子结构对辛烯基琥珀酸淀粉酯荷载多酚行为影响的研究
邹妍,王力,王梅,董楠,*
(1.贵州轻工职业技术学院,贵州 贵阳 550025;2.贵州省农业科学院生物技术研究所,贵州 贵阳 550025)
糖基类表面活性剂是典型的非离子型生物表面活性剂,通常以单糖、寡糖和多糖与长链脂肪醇、羧酸及羧酸衍生物发生酯化、醚化或酰化而合成[1-2]。通常以脂肪酸和辛烯基琥珀酸酐作为长链脂肪酸的供体。它们的亲水基团为糖基,疏水基团为长链脂肪酸。除具有表面活性外,同时具有良好的生物相容性、可降解性和安全性等优点[2]。研究报道中,作为多糖基类表面活性剂与单糖和寡糖类表面活性剂相比,不仅能够形成分子间自聚集体,而且还能形成分子内自聚集体。它们在稀溶液状态下,仍能保证一定的乳化效果[3],还具有更好的分散、乳化、增稠和稳定性能。目前,亲水性胶体包括淀粉[4]、菊粉[5]、透明质酸[6-8]、魔芋葡甘露聚糖[9]等均已实现疏水分子的嫁接,形成辛烯基琥珀酸多糖酯。前期文献研究发现,辛烯基琥珀酸淀粉酯可在溶液内部,通过疏水基团相互靠拢,缔合形成以淀粉分子中疏水链段为非极性内核,亲水长链与水接触的极性外壳的胶束。胶束结构有两种形态:1)单个分子链即能够卷曲成团,疏水链段缔合形成脱水状态(单分子胶束);2)分子之间相互缠结,缔合成多分子胶束。近几年,利用这种结构搭载多酚等疏水性应用性研究成为热点。但少有文献关注到多酚结构对其与辛烯基琥珀酸淀粉酯相互作用的影响。本文以辛烯基琥珀酸淀粉酯为载体,荷载不同结构类型的多酚,以期为探明二者相互作用的机制而提供参考。
1 材料与方法
1.1 材料与试剂
糯玉米淀粉:湛江市恒煜淀粉有限公司;2-辛烯基琥珀酸酐(纯度>99%):美国Sigma-Aldrich 公司;高良姜素、山奈素、槲皮素、桑色素、芹菜素、木犀草素、香叶木素、黄芪素、染料木素、芒柄花黄素、异鼠李素、柚皮素、圣草酚、柚皮素:成都普瑞法科技开发有限公司,纯度>98%;黄芪苷、大豆苷、大豆苷元、染料木苷、芦丁、杨梅素、杨梅苷、柚皮苷、邻香豆酸、间香豆酸、表儿茶素(epicatechin,EC)、表儿茶素没食子酸酯(epicatechin gallate,ECG)、表没食子儿茶素(epigallocatechin,EGC)、表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)、对香豆酸、咖啡酸、阿魏酸、芥子酸、原儿茶素、香草酸、没食子酸、丁香酸:北京索莱宝科技有限公司,纯度>98%;乙腈(色谱纯):成都市科龙化工试剂厂;盐酸、氢氧化钠、磷酸、甲醇、乙醇、异丙醇(分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
85-1 型恒温磁力搅拌器、PHS-3C 型 pH 计:上海仪天科学仪器有限公司;QL-866 型漩涡混合器:海门市其林贝尔仪器制造有限公司;METTLER AE100 型分析天平:梅特勒-托利多仪器上海有限公司;20A 高效液相色谱仪:日本岛津公司;ZORBAX Eclipse Plus C18色谱柱:美国 Agilent 公司;DSC 4000 差示扫描量热仪:美国Perkin-Elmer 公司;TGL-20M 型台式高速冷冻离心机:长沙迈佳森仪器设备有限公司;LGJ-10型真空冷冻干燥机:北京松源华兴科技发展有限公司。
1.3 试验方法
1.3.1 辛烯基琥珀酸淀粉酯的制备
辛烯基琥珀酸淀粉酯的制备:参照文献[10]稍作修改,用电子天平准确称取糯玉米淀粉50.0 g(干重),按质量分数35%将其分散于去离子水中,不断搅拌,得到淀粉浆。取1.5 mL(淀粉质量的3%)辛烯基琥珀酸酐,用7.5 mL 异丙醇稀释。淀粉浆置于35 ℃恒温水浴锅中,边搅拌边滴加稀释后的辛烯基琥珀酸酐,同时滴加NaOH 溶液控制反应体系pH 8.5±0.1,辛烯基琥珀酸酐滴加完后(控制在2 h 内加完),保持pH 值不变,继续搅拌反应30 min,用稀HCl 溶液调节pH 值至6.5±0.1。过滤,所得滤渣用去离子水洗涤3 次,再用70 %乙醇洗涤3 次,抽滤,干燥,过100 目筛后即制得辛烯基琥珀酸淀粉酯,真空袋保存备用。取代度经滴定法[11]测定为 0.232±0.043。
1.3.2 多酚单体与辛烯基琥珀酸淀粉酯的相互作用
多酚单体与辛烯基琥珀酸淀粉酯的相互作用:准确称取辛烯基琥珀酸淀粉酯40 mg,用20 mL 去离子水混匀,液体加热至沸后5 min,冷却至室温。而后加入多酚1 mg,在恒温(25 ℃)磁力搅拌器中作用24 h,经过离心(8 000×g,10 min),收集上清液,测定多酚在辛烯基琥珀酸淀粉酯中的溶解度(μg/mL)。以未加辛烯基琥珀酸淀粉酯的多酚溶液为对照,测定多酚在蒸馏水中的溶解度(μg/mL)。根据标准曲线计算多酚浓度并计算辛烯基琥珀酸淀粉酯对多酚的荷载量:
多酚荷载量/(μg/mg)=[(C1-C0)×V]/(C×V)
式中:C1为辛烯基琥珀酸淀粉酯中的多酚浓度,μg/mL;C0为对照多酚浓度,μg/mL;V 为体系总体积,mL;C 为辛烯基琥珀酸淀粉酯的浓度,mg/mL。
1.3.3 多酚的测定
准确称取各多酚单体0.100 0 g,溶于1 000 mL 甲醇中,配制成浓度100 μg/mL 的母液,分别稀释至5、10、15、20、30、40 μg/mL 的多酚溶液,用于制作标准曲线。多酚单体的高效液相色谱(high performance liquid chromatography,HPLC)条件如下:色谱柱为ZORBAX Eclipse Plus C18(250 mm×4.6 mm,5 μm),以2 %(质量分数)磷酸(A)和甲醇(B)为流动相,运行时间50 min,柱温30 ℃,流速0.8 mL/min,检测波长280 nm,进样量10 μL。各多酚单体的流动相配比如表1所示。

表1 多酚单体的流动相配比Table 1 The mobile phase during the elution of polyphenol monomer
1.4 数据处理
使用SPSS 22.0 进行数据分析。用Tukey’s HSD 进行方差分析,结果以平均值±标准偏差表示。
2 结果与分析
为考察多酚与辛烯基琥珀酸淀粉酯的相互作用,试验共选取多酚种类7个,单体36 种。其中多酚种类为黄酮类、异黄酮类、黄酮醇类、黄烷醇类、黄烷酮类、羟基肉桂酸类和羟基苯甲酸类。不同多酚的结构及辛烯基琥珀酸淀粉酯对多酚单体的荷载量见表2。
由表2可知,多酚结构不同,辛烯基琥珀酸淀粉酯对多酚单体的荷载量差异显著。首先,7个种类多酚与辛烯基琥珀酸淀粉酯的相互作用差异显著;其次,同种多酚不同单体与辛烯基琥珀酸淀粉酯的相互作用也不同,这主要是因为同一主体中不同单体羟基数量、甲氧基或甲基及糖苷化不同,最终导致各单体与辛烯基琥珀酸淀粉酯的荷载量不同。
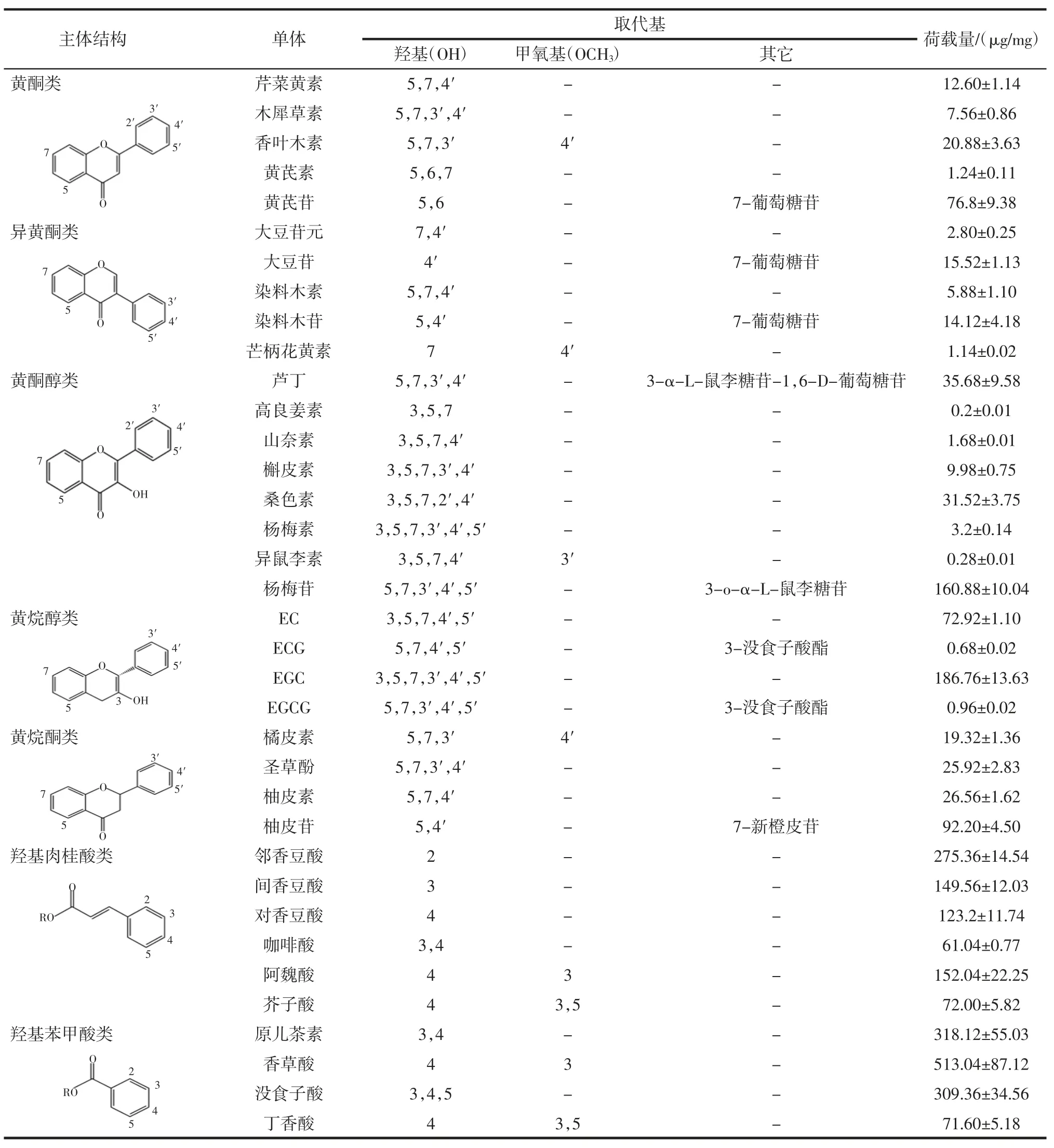
表2 多酚主体结构及辛烯基琥珀酸淀粉酯对多酚单体的荷载量Table 2 Chemical structure of polyphenol and polyphenol carrying capacity of starch octenylsuccinate
试验选取两组羟基数量相同,但主体结构不同的类黄酮类多酚,以进一步考察类黄酮主体碳架结构对辛烯基琥珀酸淀粉酯多酚荷载量的影响。两组羟基数量相同的多酚单体分别为①3个羟基的多酚单体:高良姜素、芹菜黄素、柚皮素、染料木素;②4个羟基的多酚单体:山奈素、木犀草素、圣草酚。与辛烯基琥珀酸淀粉酯的相互作用从小到大为①高良姜素<染料木素<芹菜黄素<柚皮素;②山奈素<木犀草素<圣草酚。不同类黄酮异构体与辛烯基琥珀酸淀粉酯的作用以黄酮醇最强,其次为黄酮,再次为异黄酮,黄烷酮作用最弱。
2.1 羟基化作用对辛烯基琥珀酸淀粉酯-多酚相互作用的影响
黄酮类多酚是由一个氧原子、一个3 碳链和两个苯环连接而成的三环结构(C6-C3-C6 分别对应A、C、B 环)。黄酮类多酚两个苯环间的电子共振对其抗氧化活性及其它生理活性有重要作用。羟基化对辛烯基琥珀酸淀粉酯多酚荷载量的影响见表3。

表3 羟基化对辛烯基琥珀酸淀粉酯多酚荷载量的影响Table 3 Effects of hydroxylation of flavonoids on their loading into starch octenylsuccinate
如表3所示,黄酮类单体的羟基数量不同,与辛烯基琥珀酸淀粉酯的相互作用差异显著。在B 环的3′碳位置(芹菜黄素→木犀草素)、C 环的3 碳原子(芹菜黄素→山奈素)和B 环的2′碳原子(槲皮素→杨梅素)上引入羟基使得黄酮类物质和黄酮醇类物质荷载量显著降低。羟基数目相同,辛烯基琥珀酸淀粉酯对其荷载量也有所不同,如辛烯基琥珀酸淀粉酯对山奈素荷载量低于木犀草素。由此可知,B 环的3′H→OH 比C环的3H→OH 更有利于与辛烯基琥珀酸淀粉酯的作用。在碳原子上引入羟基后,单体发生变化,辛烯基琥珀酸淀粉酯对其荷载量也产生相应变化,如辛烯基琥珀酸淀粉酯对槲皮素的荷载量比对木犀草素的荷载量高32.0%,而槲皮素即为木犀草素C 环上引入羟基变化而来;在黄酮醇B 环的4′碳原子上引入羟基,辛烯基琥珀酸淀粉酯对其荷载量提高了740.0%;在山奈素B 环的3′和5′碳原子上引入羟基变为槲皮素和桑色素,辛烯基琥珀酸淀粉酯对它们的荷载量分别提高了476.1%和1 778.0%。
尽管槲皮素和桑色素B 环上的羟基数量相同,但辛烯基琥珀酸淀粉酯对槲皮素(9.98±0.75)μg/mg 的荷载量低于桑色素(31.52±3.75)μg/mg。这说明辛烯基琥珀酸淀粉酯与B 环5′碳原子上的羟基作用强于B 环3′碳原子上的羟基。槲皮素B 环2′碳原子上引入羟基变为杨梅素,辛烯基琥珀酸淀粉酯对其荷载量反而降低了68.0%。大豆苷元A 环5 碳原子引入羟基变为染料木素,辛烯基琥珀酸淀粉酯对它的荷载量提高了101.0%。同时,柚皮素B 环的4′碳原子上引入羟基变为圣草酚,辛烯基琥珀酸淀粉酯对其荷载量也有所提高。
2.2 糖苷化作用对辛烯基琥珀酸淀粉酯/菊粉酯-多酚相互作用的影响
植物中大多数黄酮以β-糖苷的形式存在,主要包括3-O-糖苷和7-O-糖苷。糖苷化对辛烯基琥珀酸淀粉酯多酚荷载量的影响见表4。

表4 糖苷化对辛烯基琥珀酸淀粉酯多酚荷载量的影响Table 4 Effects of glycosylation of flavonoids on their loading into starch octenylsuccinate
由表4可知,黄酮糖苷化后辛烯基琥珀酸淀粉酯对其荷载量均显著提高。与各自的配基相比,辛烯基琥珀酸淀粉酯对黄芪苷荷载量提高了6 093.5%,对杨梅苷荷载量提高了15 768%,对芦丁荷载量提高了257.5 %,对大豆苷荷载量提高了454.3 %,对染料木苷荷载量提高了140.3 %,对柚皮苷荷载量提高了377.2 %。这可能是因为糖苷化使得黄酮的水溶性提高,亲水基团更容易与辛烯基琥珀酸淀粉酯的亲水外壳发生作用。
2.3 甲基化作用对辛烯基琥珀酸淀粉酯/菊粉酯-多酚相互作用的影响
甲基化和甲氧基化对辛烯基琥珀酸淀粉酯多酚荷载量的影响见表5。
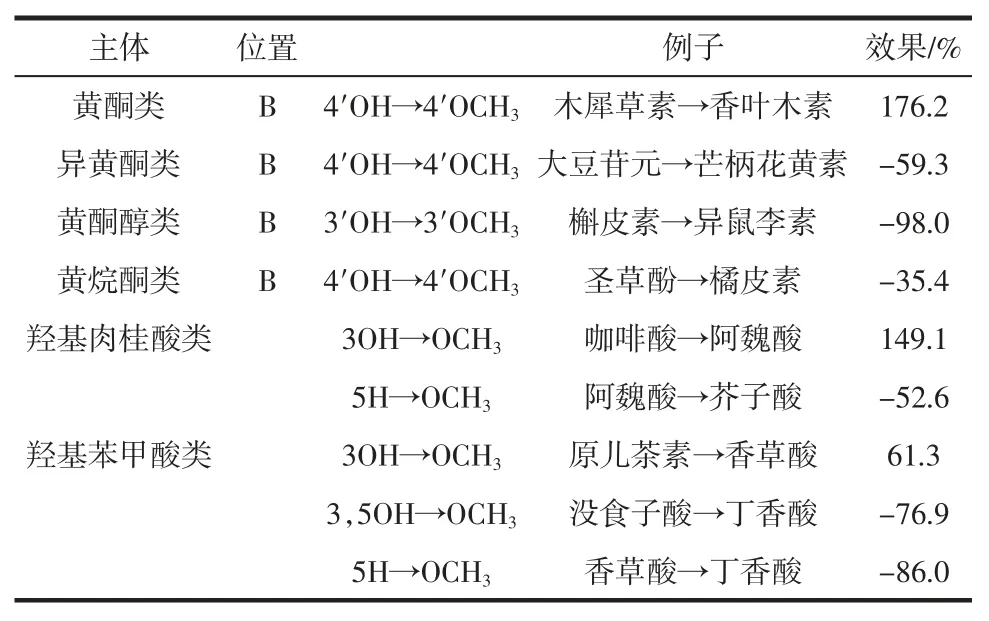
表5 甲基化和甲氧基化对辛烯基琥珀酸淀粉酯多酚荷载量的影响Table 5 Effects of methylation and methoxylation of polyphenols on their loading into starch octenylsuccinate
由表5可知,甲基化对多酚的影响较为复杂。在黄酮类主体木犀草素单体B 环4′碳原子上引入甲基,辛烯基琥珀酸淀粉酯对其荷载量提高了176.2%。然而,当甲基化发生在异黄酮类大豆苷元,辛烯基琥珀酸淀粉酯对其荷载量下降了59.3%;甲基化发生在黄酮醇类槲皮素,辛烯基琥珀酸淀粉酯对其荷载量下降了98%;甲基化发生在黄烷酮类圣草酚,辛烯基琥珀酸淀粉酯对其荷载量下降了35.4%。就羟基肉桂酸而言,当咖啡酸甲基化变成阿魏酸,辛烯基琥珀酸淀粉酯对其荷载量提高了149.1%;阿魏酸甲氧基化变成芥子酸,辛烯基琥珀酸淀粉酯对其荷载量则降低了52.6%。对于羟基苯甲酸而言,原儿茶素3位碳原子甲基化变成香草酸,辛烯基琥珀酸淀粉酯对其荷载量提高了61.3%。没食子酸和香草酸分别甲基化和甲氧基化后变成丁香酸,辛烯基琥珀酸淀粉酯对它们衍生物的荷载量均有所降低。
2.4 香豆酸和儿茶素与辛烯基琥珀酸淀粉酯/菊粉酯-多酚相互作用的对比
如表2所示,辛烯基琥珀酸淀粉酯对香豆酸同分异构体荷载量的顺序为:对位<间位<邻位。这可能是因为香豆酸官能团所处的位置不同,活性不同,最终导致辛烯基琥珀酸淀粉酯对它们的荷载量存在差异。邻香豆酸和间香豆酸主要以氢键的方式与辛烯基琥珀酸淀粉酯结合,相互作用效果较强;而对香豆酸主要是疏水基与之结合,相互作用较弱。EC 经过没食子酸酰化后变为 ECG,荷载量由(72.92±1.10)μg/mg 下降为(0.68±0.02)μg/mg,荷载量显著降低;同样,EGC经过没食子酸酰化后辛烯基琥珀酸淀粉酯对其荷载量明显降低。这可能是因为儿茶素引入没食子酸后,分子的疏水性变强,亲水性变弱。
3 结论
多酚与辛烯基琥珀酸淀粉酯之间相互作用受到多酚结构影响显著。不同主体结构间与其作用强度存在显著差异,且同一主体结构中,羟基数量、糖苷化、甲基或甲氧基化都会影响到最终与辛烯基琥珀酸淀粉酯的相互作用。类黄酮异构体与辛烯基琥珀酸淀粉酯的作用强弱顺序为:黄烷酮<异黄酮<黄酮<黄酮醇。糖苷化后,黄酮与辛烯基琥珀酸淀粉酯的相互作用显著提高。辛烯基琥珀酸淀粉酯对香豆酸的荷载力高低顺序为:对香豆酸<间香豆酸<邻香豆酸。辛烯基琥珀酸淀粉酯与EC 和 EGC 的相互作用强于与 ECG 和EGCG 的相互作用。

