花椒麻味物质分子印迹预组装体系的分子模拟与吸附性能
陈晓龙 李 耀 阚建全,2*
(1西南大学食品科学学院 重庆 400715
2重庆市农产品加工及贮藏重点实验室 重庆 400715)
分子印迹聚合物(MIPs)是指模拟自然界所存在的分子识别作用机理,如酶与底物、抗体与抗原等的特异性识别,以目标分子为模板,将具有结构互补的聚合物功能单体通过共价键或非共价键方式与模板分子结合,再加入交联剂和引发剂进行聚合和交联,反应结束后将模板分子洗脱而形成的能识别模板分子空穴的一类高分子聚合物[1-3]。MIPs具有构效预定性、选择识别性和广泛实用性等特点,在处理环境污染物、分离手性药物、分离检测食品中痕量物质等方面有着十分广泛的应用[4-8]。它的合成受模板分子、功能单体的种类、模板分子与功能单体的比例、溶剂、交联剂以及聚合条件等因素的影响[9-11]。目前,对分子印迹聚合物中功能单体、溶剂的选择主要是根据以往的经验或相关的文献报道进行,具有一定的盲目性,缺少理论指导[12]。随着计算机技术及量子化学理论的发展,计算机分子模拟技术逐渐应用到分子印迹体系的研究中,在解释分子聚合物识别机理[13],筛选功能单体[14-16],确定模板分子与功能单体的最佳比例[17]以及选择合适的溶剂等[18]方面发挥作用,可以减少试验工作量,缩短试验周期。
花椒麻味物质是花椒中一类具有麻味的链状不饱和脂肪酰胺类物质,主要成分是(羟基)-α-山椒素、(羟基)-β-山椒素、(羟基)-γ-山椒素等,是一类“蝌蚪型”少结合位点物质,其具有麻醉、兴奋、杀虫、抑菌、祛风除湿和镇痛等功效[19-22]。目前,对花椒麻味物质的分离提取方法主要有水提法[23]、有机溶剂提取法[24-26]、超临界 CO2萃取法[27,28],这些方法虽能较好地提取花椒麻味物质,但其提取的步骤繁琐,提出物杂质含量较高,且未对花椒麻味物质进行纯化。寻找一种新的花椒麻味物质分离纯化方法制备对应标准品物质具有十分重要的意义。本课题组研究发现,花椒麻味物质分子结构中含有较多的双键,如果直接作为模板分子,则会与功能单体发生反应,使得麻味物质难以洗脱。为了克服麻味物质难以洗脱的困难,采用作者合成的花椒麻味类似物作为模板分子,其结构见图1。

图1 花椒麻味类似物Fig.1 The analogue of numb-taste components
本文运用Gaussian03W中的PM3与Hartree-Fock法筛选出可用于制备花椒麻味类似物分子印迹聚合的功能单体、致孔剂以及模板分子与功能单体的物质的量比。在此基础上,选择3种功能单体和3种致孔剂以表面分子印迹法合成印迹聚合物,通过评价聚合物的动态吸附与静态吸附能力来验证计算机分子模拟的效果,以期为快速制备分子印迹聚合物提供理论支持。
1 材料与方法
1.1 材料与试剂
花椒麻味类似物物结晶体,自制,纯度95%,相对分子质量271;硅胶(120~160目),青岛海洋化工有限公司;盐酸、乙酸、无水甲苯、丙酮、甲醇均为分析级级,成都市科龙化工试剂厂;甲基丙烯酸(MAA),Sigma 公司;EDMA,成都市科龙化工试剂厂;甲基亚氨基二乙酸,成都市科龙化工试剂厂;乙烯基苯甲酸,成都市科龙化工试剂厂;偶氮二异丁腈(AIBN),成都市科龙化工试剂厂;r-(甲基丙烯酰氧)丙基三甲氧基硅烷(KH-570),南京创世化工助剂有限公司。
1.2 仪器与设备
真空干燥箱DZF-6020,上海齐欣科学仪器有限公司;氮吹仪UGC-12C,北京优晟联合科技有限公司;磁力搅拌器,上海齐欣科学仪器有限公司;高效液相色谱仪Agilent1200,德国。计算机模拟平台:DALL电脑,2.00G的内存,500G硬盘,Windows操作系统;Gaussian 03W、Gaussian view软件。
1.3 原理和方法
1.3.1 计算机分子模拟技术
1.3.1.1 功能单体的筛选 以花椒麻味类似物为模板分子,选择常见制备分子印迹聚合物的功能单体甲基丙烯酸(MAA)、丙烯酸(AA)、三氟甲基丙烯酸(TFMAA)、乙烯基苯甲酸、丙烯酰胺(MA)、1-乙烯基咪哚、2-甲基-1-乙烯基咪哚、2-吡啶(2-VPy)、4-吡啶(4-VPy)、甲基丙烯酰胺、甲基丙烯酸羟乙酯、甲基亚氨基二乙酸、N-乙烯基吡咯烷酮(NVP)、亚氨基二乙酸,运用Gaussian 03W中的PM3法优化筛选出功能单体,得出模板分子与功能单体的最低能量构象图及各原子上的Mulliken电荷,找出模板分子与功能单体的质子结合点与给出点。以式(1)计算模板分子与各功能单体的结合能△E,结合能越大表示模板分子与该功能单体相互作用越强,所形成的MIPs稳定性越好[29-31]。

式中:E(聚合物)——模板分子-功能单体聚合物单点能,kJ·mol-1;n——功能单体数量;E(功能单体)——功能单体单点能,kJ·mol-1;E(模板)——模板分子单点能,kJ·mol-1。
1.3.1.2 模板分子与功能单体比例的确定 根据1.3.1.节优选出的功能单体,模拟模板分子与功能单体可能的结合情况,得出模板分子与功能单体理论上的物质的量比,再根据试验结果确定模板分子与功能单体实际的物质的量比。
1.3.1.3 致孔剂的筛选 选取乙腈、氯仿、四氯化碳、甲醇4种具有代表性的致孔剂,采用Hartree-Fock方法,6-31G+(d)基组,极化连续溶剂模型(Polarizable continuum model,PCM),按 式 (2)计算溶剂化能。溶剂化能越小表明该溶剂对模板分子与功能单体的作用力越小,越适合用作体系的致孔剂[32-33]。
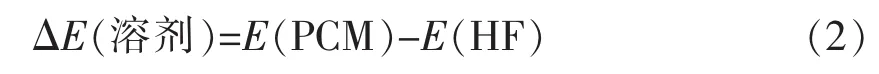
式中:ΔE(溶剂)——体系的溶剂化能,kJ·mol-1;E(PCM)——溶剂状态下体系的单点能,kJ·mol-1;E(HF)——气态状况下体系的单点能,kJ·mol-1。
1.3.2 MIPs、NIPs的制备 在计算机分子模拟结果的基础上,优选的3种功能单体与3种溶剂采用表面分子印迹的方法制备MIPs、NIPs,分别记为 MIP1、MIP2、MIP3、MIP4、MIP5、MIP6和 NIP1、NIP2、NIP3、NIP4、NIP5、NIP6。
1)硅胶活化与硅烷化 取硅胶10 g,先用10%的盐酸回流12 h,除去硅胶中少量的无机杂质并增加硅胶表面的羟基数目。用蒸馏水洗至中性,60℃真空干燥,备用[34-35]。
N2保护条件下,将10 g活化硅胶以及100 mL无水甲苯加入250 mL圆底烧瓶中,在磁力搅拌条件下加入KH-570硅烷偶联剂10 mL,于80℃条件下回流反应24 h,将反应后的硅胶过滤,制得表面被不饱和C=C双健修饰的改性硅胶。将所得产物依次用甲苯、丙酮、甲醇洗涤,于100℃条件下干燥12 h,得到硅烷化硅胶[34-36]。
2) MIP1、MIP2、MIP3的制备 取 271 mg(约 1 mmol)花椒麻味类似物分散于50 mL乙腈中,在搅拌条件下加入4 mmol甲基亚氨基二乙酸(乙烯基苯甲酸、MAA)、16 mmol乙二醇二甲基丙烯酸酯(EDMA)和1.5 g表面修饰的活化硅胶,超声30 min使其充分分散,最后加入30 mg偶氮二异丁睛,N2鼓泡出氧5 min,放入水浴磁力搅拌锅中,在60℃、N2保护下聚合反应24 h,冷却至室温,将反应物抽滤,60℃真空干燥10 h后,用甲醇-乙酸(9∶1,V/V)索氏抽提 18 h。 最后用甲醇抽提 18 h,以彻底除去乙酸和模板分子,制得MIP1(MIP2、MIP3)。 NIP1、NIP2、NIP3的制备过程与上述方法类似,只是在制备过程中不加入花椒麻味类似物[37]。
3) MIP4、MIP5、MIP6的制备 MIP4、MIP5、MIP6的制备过程与2)类似,只是在制备过程中将功能单体确定为甲基亚氨基二乙酸,变化致孔剂为乙腈、甲醇、氯仿。NIP4、NIP5、NIP6的制备过程与上述方法类似,只是在制备过程中不加入花椒麻味类似物。
1.3.3 聚合物的动态吸附性考察 准确称取20 mg MIPs及NIPs于10 mL离心管中,加入200 μg/mL花椒麻味物质5 mL,恒温(20℃)水浴振荡0.5,1.5,2.5,3.5,4.5,5.5,6.5 h,同时以空白为对照。吸附一段时间后,3 000 r/min离心10 min,吸取上层清液,用0.22 μm滤头过滤后高效液相色谱测定其浓度,平行3次,按式(3)计算其对花椒麻味物质的吸附容量Q(μg/mg),并绘制吸附容量一时间关系曲线,以此来考察分子印迹聚合物对花椒麻味物质的结合速度,确定吸附达到平衡的时间[38]。

式中:C0——花椒麻味物质的初始质量浓度(μg/mL);Ct——上层清液中花椒麻味物质的质量浓度 (μg/mL);V——所取花椒麻味物质溶液的体积(mL);m——聚合物的质量(mg)。
高效液相色谱分析条件:采用Agilent高效液相色谱仪,色谱柱Zorbax XDB C18(4.6 mm×150 mm,5 μm);流动相 A:40%超纯水;流动相 B:60%甲醇;流速:1 mL/min;进样量:10 μL;柱温:40 ℃;检测波长254 nm[26]。
1.3.4 聚合物的静态吸附性研究 准确称取20 mg MIPs及NIPs于10 mL离心管中,加入25,50,100,150,200,250 μg/mL花椒麻味物质溶液5 mL,恒温(20℃)水浴振荡 4.5 h后,3 000 r/min离心10 min,吸取上层清液,用0.22 μm滤头过滤后高效液相色谱测定其浓度,平行3次,按式(3)计算花椒麻味物质的吸附量Q(μg/mg),并绘制吸附容量-浓度关系曲线[38]。
1.4 试验数据处理方法
采用Origin 8.0、Microsoft excel 2007软件对试验数据进行分析。所有试验平行重复3次,结果表示为平均值±标准偏差。
2 结果与分析
2.1 计算机分子模拟的试验
2.1.1 功能单体的筛选 用Gaussian 03W 中的PM3法优化模板分子与功能单体。优化后花椒麻味类似物与各功能单体的主要质子给出点和结合点见表1。
原子所带负电荷越大,接受质子的能力越强;所带正电荷越大,给出质子的能力越强[39]。花椒麻味类似物既能接受质子,也能给出质子;功能单体AM、甲基丙烯酰胺、N-乙烯基吡咯烷酮(NVP)虽存在很好的质子结合点,但其质子给出点电荷小,给质子能力弱;1-乙烯基咪哚、2-甲基-1-乙烯基咪哚、2-VPy、4-VPy质子接合点、给出点电荷均较小,与花椒麻味类似物结合稳定性低。初选出功能单体AA、TFMAA、MAA、乙烯基苯甲酸、甲基丙烯酸羟乙酯、甲基亚氨基乙二酸、亚氨基乙二酸。
在此基础上,运用gaussian 03W中的PM3法将优选出的花椒麻味类似物与功能单体按照1∶2的比例进行结合物最低能量结构优化 (见图2),根据式(1)计算结合能(见表2)。
分子印迹预聚合过程中形成聚合物的相互作用能ΔE(即结合能)越高,模板分子与功能单体在预聚合时形成的聚合物越稳定[29-31]。对于同一模板分子来说,与该功能单体的结合能越高印迹效果越佳。由表3可看出,ΔE(花椒麻味类似物-甲基亚氨基二乙酸)>ΔE(花椒麻味类似物-乙烯基苯甲酸)>ΔE(花椒麻味类似物-亚氨基二乙酸)>ΔE(花椒麻味类似物-MAA)>ΔE (花椒麻味类似物-AA)>ΔE(花椒麻味类似物-TFMAA)>ΔE(花椒麻味类似物-甲基丙烯酸羟乙酯),说明甲基亚氨基二乙酸与花椒麻味类似物形成的聚合物最稳定,乙烯基苯甲酸次之,甲基丙烯酸羟乙酯最差。后续试验选择甲基亚氨基二乙酸(功能单体1)、乙烯基苯甲酸(功能单体2)、MAA(功能单体3)作为分子印迹的功能单体制备相应的MIPs。

表1 花椒麻味类似物与各功能单体的主要质子给出点和结合位点Table1 The main proton give point and combine point of the functional monomer and numb-taste components analogue

图2 花椒麻味类似物与功能单体的模拟优化结合图Fig.2 Combination chart of the numb-taste components analogue and functional monomer

表2 花椒麻味类似物与功能单体的模拟结合能表Table2 Binding energy meter of the numb-taste components analogue and functional monomer
2.1.2 模拟确定的模板分子与功能单体比例 功能单体为MIPs提供特定的结合位点,其添加量少,会导致MIPs的专一识别位点少,印迹空穴少;其添加量过多,则会引入更多的游离功能基团,导致特异性吸附位点减少,非特异性吸附位点增多[40]。花椒麻味类似物作为模板分子时,其O19,电荷为-0.366,H44,电荷为 0.194,是很好的质子结合点与给出点。理论上花椒麻味类似物与功能单体甲基亚氨基二乙酸、MAA、乙烯基苯甲酸按1∶2的比例反应,然而考虑到实际情况中甲基亚氨基二乙酸等不能完全与花椒麻味类似物反应,确定花椒麻味类似物与功能单体的比例为1∶4[39]。
2.1.3 致孔剂的模拟筛选 利用式(2)计算体系的溶剂化能,见表3、表4。ΔE(甲基亚氨基二乙酸-乙腈)<ΔE(甲基亚氨基二乙酸-甲醇)<ΔE(甲基亚氨基二乙酸-氯仿)<ΔE(甲基亚氨基二乙酸-四氯化碳);ΔE(花椒麻味类似物-乙腈)<ΔE(花椒麻味类似物-甲醇)<ΔE(花椒麻味类似物-氯仿)<ΔE(花椒麻味类似物-四氯化碳)。模板分子与功能单体在致孔剂乙腈中的溶剂化能最小,说明乙腈与花椒麻味类似物和功能单体的相互作用力小,适合于该分子印迹体系;甲醇次之,四氯化碳最差。后续试验选择乙腈(致孔剂1)、甲醇(致孔剂2)、氯仿(致孔剂3)作为分子印迹的致孔剂制备相应的MIPs。
2.2 实际分子印迹聚合物的动态、静态吸附性
2.2.1 不同功能单体制备的MIPs动态、静态吸附性 对3种功能单体制备的MIPs进行动态、静态吸附性考察 (图3),发现不同功能单体制成的MIPs的饱和吸附容量及平衡吸附时间不同。在200 μg/mL的花椒麻味物质溶液中,MIP1的平衡吸附时间为 4.5 h,饱和吸附容量Q(MIP1)=27.62μg/mg;MIP2、MIP3的平衡吸附时间为 5.5 h,饱和吸 附 容 量 Q(MIP2)=22.19 μg/mg,Q(MIP3)=19.43 μg/mg。 相对于 MIP2、MIP3来说,MIP1达到平衡吸附的时间更快,饱和吸附容量更大,这是由于甲基亚氨基二乙酸结合质子,给出质子的能力强,能迅速与花椒麻味物质发生氢键结合,形成稳定的印迹聚合物。由图3b可知,MIP1在花椒麻味物质溶液质量浓度大于200 μg/mL时,聚合物达到饱和吸附,而MIP2、MIP3在溶液质量浓度低于200 μg/mL 时就达到饱和吸附,且 Q (MIP1)>Q(MIP2)>Q(MIP3),说明 MIP1的印迹结合位点多,能更多地吸附花椒麻味物质,与计算机分子模拟结果相符。

表3 不同溶剂下甲基亚氨基二乙酸的溶剂化能Table3 The solvent energy of N-(carboxymethyl)-Glycine in different solvents

表4 不同溶剂下花椒麻味类似物的溶剂化能Table4 The solvent energy of the numb-taste components analogue in different solvents
以上结果说明,运用计算机分子模拟中的PM3法来优化花椒麻味类似物与功能单体的分子结构,通过Mulliken电荷及结合能来筛选功能单体具有实用性。

图3 不同功能单体的MIPs动态、静态结合曲线Fig.3 Dynamic binding and static binding curves of MIPs with different functional monomers
2.2.2 不同致孔剂制备的MIPs动态、静态吸附性 不同致孔剂下合成的MIPs,其饱和吸附容量及平衡吸附时间存在差异。由图4a可知,在200 μg/mL花椒麻味物质溶液中,MIP4、MIP5的饱和吸附容量相近,分别为 27.62 μg/mg 和 26.28 μg/mg,平衡吸附时间相同,均为4.5 h,这可能是由于致孔剂乙腈和甲醇对花椒麻味类似物及功能单体的相互作用力均较小的缘故,符合计算机分子模拟结果;MIP6的饱和吸附量为20.35 μg/mg,平衡吸附时间为5.5 h,说明氯仿对花椒麻味类似物及功能单体的作用力较大,不利于MIPs的合成。由图4b可知,MIP4在低于200 μg/mL的花椒麻味物质溶液中快速吸附花椒麻味物质,当溶液质量浓度大于200 μg/mL时,吸附容量不再增加;而MIP5、MIP6在低于200 μg/mL花椒麻味物质溶液中达到饱和吸附。MIP4在高浓度溶液中达到饱和吸附且吸附容量大,说明MIP4印迹空穴多,与计算机分子模拟结果相符。
以上结果说明,采用计算机Hartree-Fock方法,运用6-31G+(d)基组选取极化连续溶剂模型(PCM),以溶剂化能筛选致孔剂具有实用性。
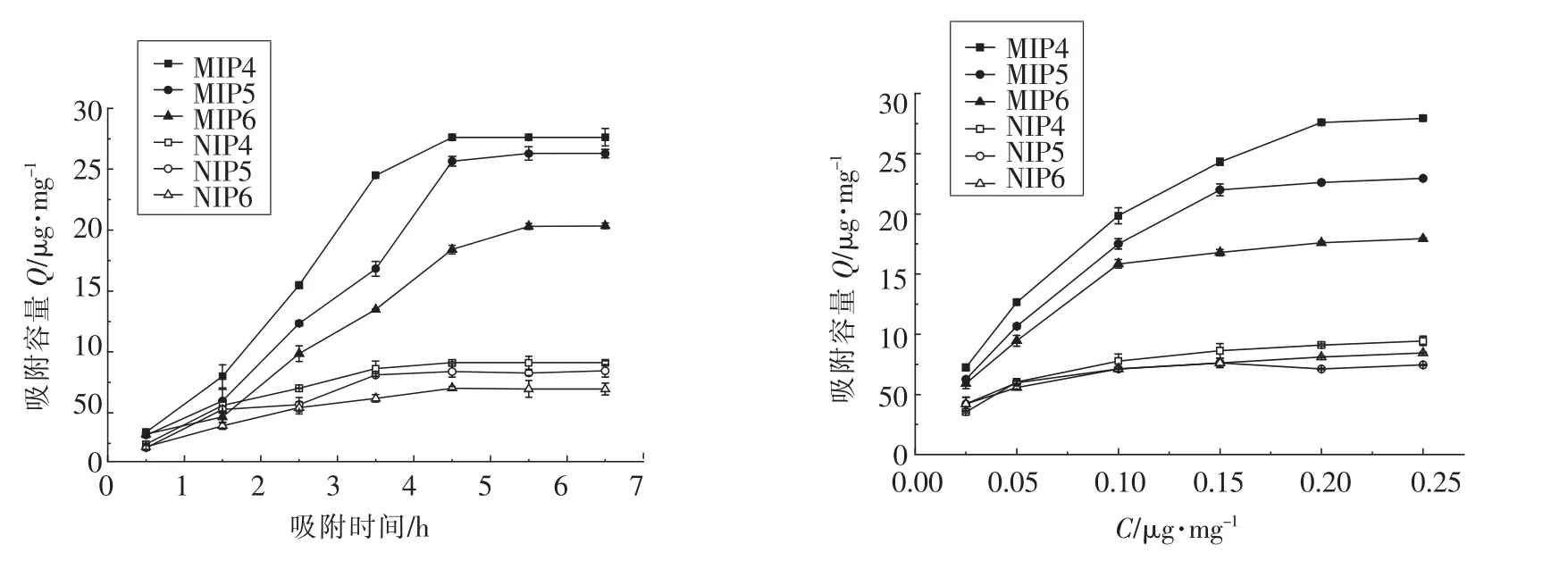
图4 不同致孔剂的MIPs动态、静态结合曲线Fig.4 Dynamic binding and static binding curves of MIPs with different pore forming agents
3 结论
运用计算机分子模拟技术筛选出适合于花椒麻味类似物的功能单体为甲基亚氨基二乙酸,致孔剂为乙腈,并根据实际情况确定花椒麻味类似物与功能单体的物质的量比为1∶4。在此基础上,用甲基亚氨基二乙酸、乙烯基苯甲酸、MAA3种功能单体及乙腈、甲醇、氯仿3种致孔剂制备相应的MIPs,通过考察它们的动态吸附与静态吸附能力,得出与计算机分子模拟相符的结果,验证了计算机分子模拟结果的准确性。

