氚在RAFM钢表面的吸附研究
陆光达,向 鑫,张桂凯,范东军,包锦春,陈长安,唐 涛
(中国工程物理研究院 材料研究所,四川 江油 621907)
RAFM钢作为氚增殖包层的结构材料,其与氘氚的相互作用性质,包括氘氚的溶解、扩散、渗透与释放、氚在表面的吸附、氢致机械性能的变化等,都是聚变堆工程设计者关心的问题。此前,国内外研究者较少关心氚在各种金属材料表面的吸附问题,相对来说,日本学者的研究较多[1-7],但研究对象主要是作为氚包容的不锈钢结构材料。
氚在RAFM钢表面的吸附、释放性质,关系到聚变堆运行过程中的环境放射性控制、近距离操作时的人身安全和含氚废物的处置。开展氚在RAFM钢表面的吸附行为研究,对于聚变堆氚安全与废物处理方案设计有重要意义,对于涉氚材料性质的认识及氚处理工艺系统或器件的设计也有重要意义。本工作进行氚在国产RAFM钢表面的吸附实验研究,并在完全相同的条件下,用316L和1Cr18Ni9Ti钢进行实验比较。
1 氚吸附的理论分析
1) 氚在金属表面吸附的基本性质概述
固体表面原子因处在不对称力场中,会自发捕获气相分子,降低表面自由能,形成表面吸附。按吸附作用力性质,可将吸附分为物理吸附和化学吸附,它们的主要区别列于表1。

表1 物理吸附和化学吸附性质比较Table 1 Comparison of physical and chemical adsorption property
吸附的过程为:碰撞到固体表面的气体分子被暂时物理吸附于固体表面,停留一段时间后,被重新蒸发;在物理吸附状态下,如果分子具有足够能量,可越过激活能势垒,转为化学吸附。
固体表面吸附气体量的大小,与气体种类、固体元素种类和原子排列状态有关。通常,固体原子的自由价越高,价键力越强,单位表面积内裸露的活性原子数越多(越粗糙)、缺陷越多,吸附气体的能力越强。
氚及其同位素在金属表面的吸附,首先是分子态物理吸附,能否形成化学吸附层取决于氢与金属原子能否形成化学键。常温下高活性碱金属(如Li)易形成氢的化学吸附;高温下有些金属变得活泼也会发生化学吸附。化学吸附时,被激活的分子离解为2个原子,每个氢原子占据1个金属原子,以共价键方式形成化学吸附。化学吸附最多只能吸附1个原子层。
化学吸附层上,依然可叠加物理吸附层;气体分子的物理吸附量与温度有重要关系:临界温度以下,气体可有多层物理吸附;临界温度以上,气体不能被液化,而物理吸附下的分子类似液态,故吸附分子易蒸发,不会发生多分子层吸附[8-10]。氢同位素的临界温度在33~40 K之间,所以,常温下氢同位素分子的物理吸附不可能超过1个单分子层。
2) 表面吸附的定量分析
(1) 吸附速率ra
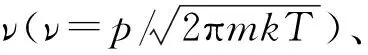
(1)
其中:σ为凝聚系数,即碰撞吸附概率;p为气体压力;m为气体分子质量;k为玻尔兹曼常数;θ为覆盖度;Ea为摩尔气体分子的吸附活化能;R为气体常数;T为热力学温度。
(2) 脱附速率rd
rd与覆盖度θ、超过脱附活化能的分子数exp(-Ed/RT)呈正比,即:
rd=σ′θexp(-Ed/RT)
(2)
其中:σ′为脱附比例系数;Ed为摩尔气体的脱附活化能。吸附平衡时,ra=rd,则有:
kap(1-θ)=kdθ
(3)
(4)
kd=σ′exp(-Ed/RT)
(5)
由式(3)~(5)可得:
(6)
(7)
其中:b=ka/kd为吸附系数,Pa-1,与温度有关;Q=Ea-Ed为吸附热。
式(6)称为Langmuir吸附等温式。
以qad表示单位表面的吸附气量,则qad与覆盖度θ呈正比,由式(6)可得:
(8)
其中,b′为Langmuir常数,mol/(m2·Pa),与温度有关。如果吸附热Q和气体压力p足够小,则吸附量与气体压力呈正比,这正是氢在大多数金属表面吸附的情况。
物理吸附的氢分子在金属表面解离为原子,可被化学吸附。氚的化学吸附属于解离吸附,在覆盖度较小时,其吸附量表达式为:
qad,c=cp1/2exp(-Qc/RT)
(9)
其中,c为与温度有关的常数,mol/(m2·Pa1/2)。化学吸附不能超过1层,但其上又可叠加物理吸附层。
如果金属晶格能溶入氢原子,则会产生溶解和渗透。因此,氢在金属中能渗透,且是扩散控制,意味着表面解离相对快速;室温下的渗透虽极微弱,也说明可解离并会被化学吸附。
3) 吸附与脱附动力学
吸附达到平衡前,ra-rd>0;气体压力降低时,ra-rd<0。如果得出式(1)、(2)中的各项参数,即ka和kd的表达式,便可得出吸附/脱附动力学方程。
实际的固体表面不光滑、原子排列也不均匀,靠近表面的晶体缺陷就成为氢的强陷阱,气体分子、吸附分子与固体表面原子之间的相互作用性质随位置不同而改变,使得ra和rd与1-θ和θ一般不是简单的线性关系,当覆盖度变化时,σ、σ′、Ea、Ed都会相应地发生变化。
实验上,欲得出ka和kd表达式,需具备非常精密的仪器设备,且因吸附是无处不在的,也使得对测量操作的要求严格而复杂,这正是实验的困难性。
2 氚吸附与测量方法
国产RAFM钢有CLAM[11]和CLF-1[12]2种,本工作选用CLAM钢进行氚吸附实验。
通常,气体吸附研究需要吸附质有较大的吸气量[13],这对于块材钢是无法实现的。受制于实验的困难性,并考虑到一些常用不锈钢的表面氚吸附研究已有文献报道,将316L和1Cr18Ni9Ti钢作为参比样品,期望通过实验比较,对RAFM钢表面氚吸附性质有较为准确的掌握或预测。
CLAM、316L和1Cr18Ni9Ti钢3种材料的主要组成元素及其含量列于表2。可见,含量最大的元素都是Fe,其次是Cr,第3是Ni,其余W、Mn、Mo等都小于2.5%,可忽略;3种主要元素在室温下都能化学吸附氢,这是材料最重要的吸氚性质,所以,将316L和1Cr18Ni9Ti钢作为参比材料是合理的。
CLAM钢母材是1 cm厚的板料,将其加工成图1所示的片状样品,尺寸为89.9 mm×19.8 mm×1.28 mm,每片的总表面积为38.41 cm2;样品表面经过抛光,但因其硬度大、抛光困难,最终达到的粗糙度约为0.8 μm。316L钢使用的是外径φ6 mm、壁厚1 mm、内外抛光管,表面粗糙度为0.2~0.3 μm,总面积为53.63 cm2。1Cr18Ni9Ti钢样品是厚度1 mm的片状材料,表面粗糙度为0.1~0.2 μm,总面积为40.1 cm2。
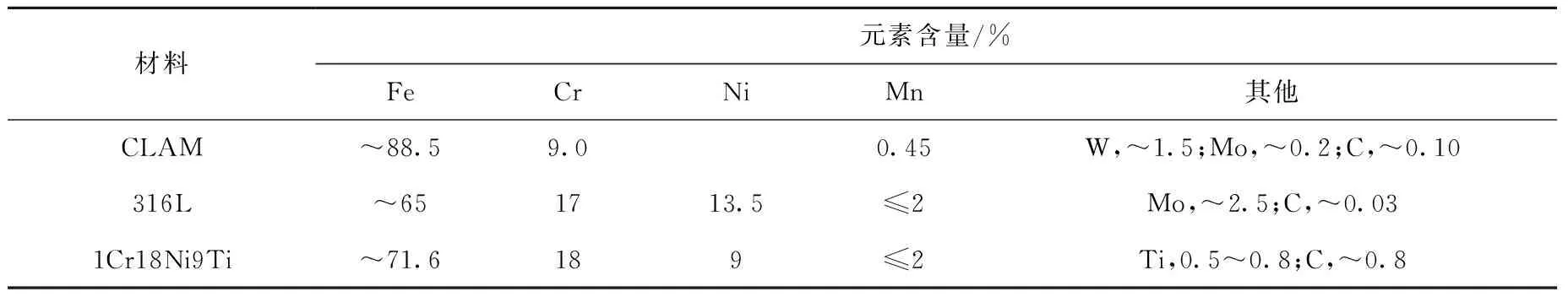
表2 RAFM、316L和1Cr18Ni9Ti钢的主要元素组成Table 2 Main element composition of RAFM, 316L and 1Cr18Ni9Ti steel

图1 CLAM钢吸附氚实验样品Fig.1 CLAM sample used in tritium adsorption experiment
所有样品经严格清洗、干燥后一起置于不锈钢容器内,再连接在真空系统上,经两次边缓慢加热至473 K边抽真空至0.1 Pa并持续2 h以上,以除去表面吸附的杂质。样片容器除气后,在室温下充入压力1 220 Pa、氚丰度36.5%的氘氚混合气体,贮存12 d后,用铀床吸除容器内的氘氚,再转入充Ar密封手套箱中,分装至各自的释氚容器内。
样品表面吸附氚量的测量使用2种方法:1) Ar气氛中自然释放出氚再配合电离室测量;2) 纯水浸泡交换出氚再配合液闪测量。根据测得的样品释放总氚量,计算单位表面积吸附氚量。
使用电离室测量时,让高纯Ar以一定流速流过样品容器,载带容器中的氚进入电离室,测出氚的峰面积,进而换算为释氚量。这种测量方法需要对电离室进行标定,以得出流洗测量的灵敏度。标定方法是:用与样品容器相同、腔体积104.1 cm3的不锈钢容器,在实验温度(24.5±0.5) ℃下,充入总活度Q标=3.616 MBq的含氚氩气,在流速fAr=0.4 L/min的Ar气载带下进入电离室,测得氚的峰面积S标=839.3 GBq·s/m3;设该流速下电离室测得未知氚峰的面积为ST,则流过氚量Q(MBq)的计算公式为:
Q=(Q标/S标)ST=4.308 35×10-3ST
(10)
电离室测量要求的氚量较大,经预估使用了5片CLAM钢样片;为保证氚均匀吸附,样片被扎成1捆,首尾两端以φ0.5 mm的不锈钢丝将各样片隔开。
使用液闪测量时,灵敏度相对较高,水浸泡交换测量使用CLAM钢(1片)、316L钢和1Cr18Ni9Ti钢样品。
吸氚样品在充Ar手套箱气氛中分装,由于环境水汽很难彻底清除,分装过程必须快速,避免水分的竞争性吸附导致吸附氚的释放。实际操作过程中,3种样品置入纯净水瓶的过程简单快速,氚释放应可忽略;但对电离室测量样品的转装过程稍慢,氚释放可能对测量结果稍有影响。
3 结果与讨论
3.1 气相脱附测量结果
将分装了吸氚CLAM钢样品(5片)的容器接入电离室测氚系统,让高纯Ar从容器的一端以0.4 L/min的流速流入,载带脱附的氚流经电离室,数据记录仪会绘出氚浓度随时间的变化曲线。在近5个月的时间内,对CLAM钢进行了10次脱附氚量的测量,随着脱附次数的增加,脱附氚量越来越小,以至于不易准确测量,因此在最后阶段,对样品连续进行了3次加热脱附测量,目的是使样品表面吸附的氚彻底脱附(包括样品容器内表面二次吸附的氚)。第1、2次加热温度为523 K,第3次为573 K,其中第2次加热实际上是重复了4次,第3次加热实际上是重复了2次,所得数据则是重复测量之和;当第3次测量结束时,脱附氚量已非常低,所以结束了整个测量,全部数据列于表3。
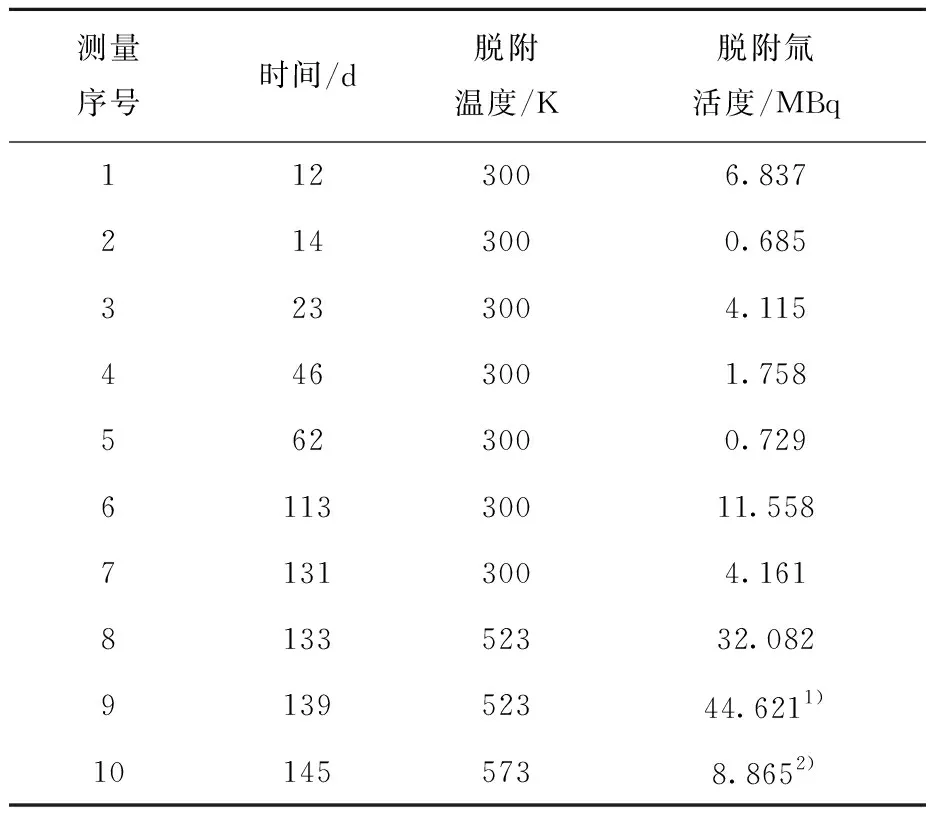
表3 不定间隔期内CLAM钢样品的脱附氚量Table 3 Quantity of tritium desorbed from CLAM sample surface
注:1) 4次加热脱附的总和 2) 2次加热脱附的总和
由表3数据得,样品累计脱附氚活度为10.7 MBq,换算成单位表面的脱附氚活度为55.7 kBq/cm2,即单位表面脱附的氚原子数为3.12×1013cm-2。脱附总氚量随时间的变化如图2所示。
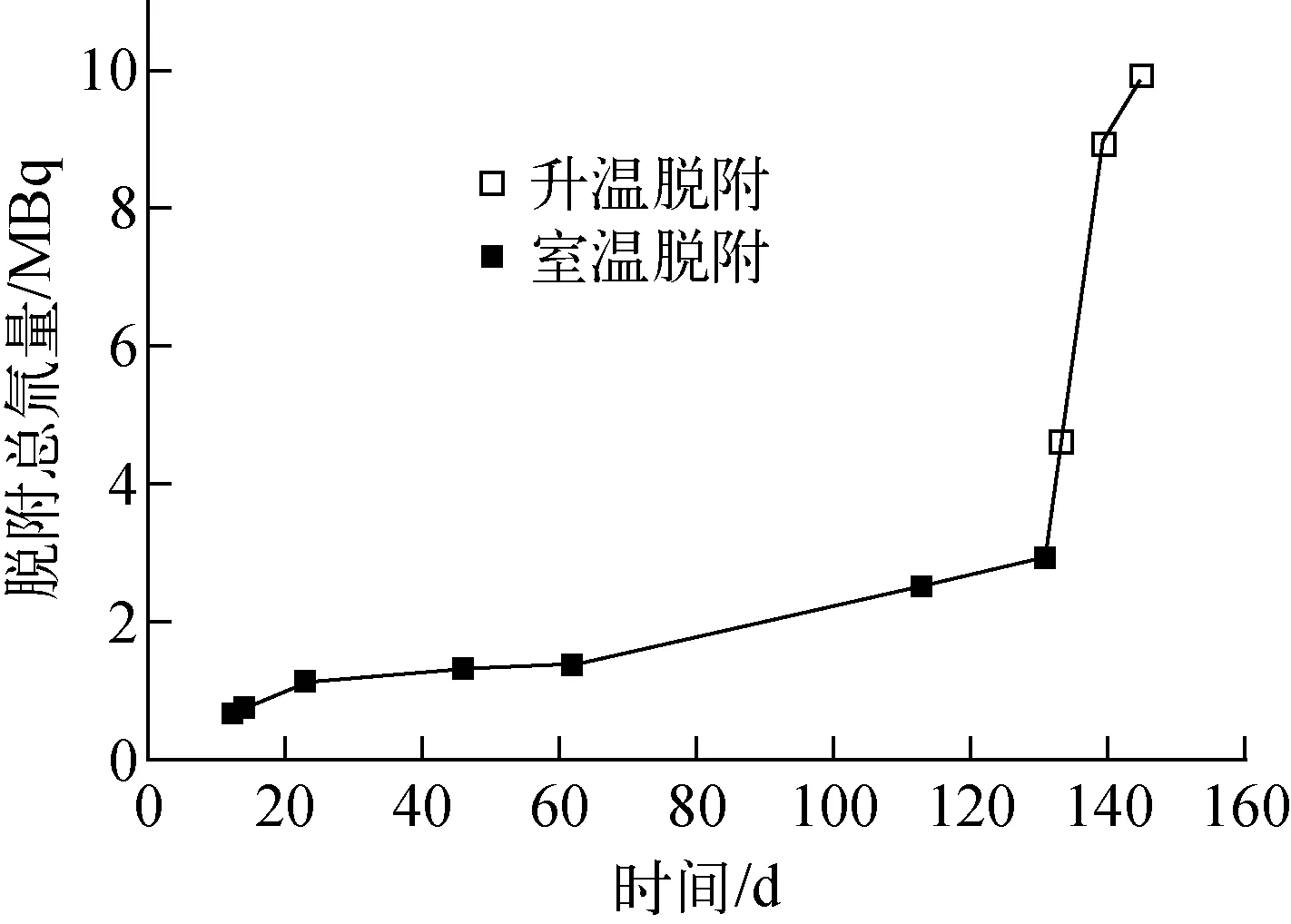
图2 Ar气中CLAM钢表面脱附总氚量随时间的变化Fig.2 Quantity of tritium desorbed from CLAM surface with time
由图2可见,CLAM钢表面吸附的氚在Ar气中的脱附速率是相当缓慢的,4个多月中的总释放量只占总吸附量的30%。按图中的自然释放趋势,可能需要几年才能全部释放完,因此必须通过热脱附来测量其吸附氚总量。
3.2 水浸泡交换测量结果
吸附了氚的3种钢样品被分别浸泡于装有500 mL纯水、室温存放的玻璃瓶中,表面氚与水交换,会将氚释放到水中。每隔一定时间从瓶中定量吸取1 mL水,用液体闪烁计数器测量其中的氚浓度。为防止水中氚浓度不均,取样前一般要进行摇晃或搅拌。取样后瓶中减少的1 mL水用纯水补充。用液体闪烁计数仪测量时,闪烁液的添加量为10 mL,每次计数的时间是2 min,每个样品测量2次,取平均值计算氚浓度。各次测量结果列于表4。
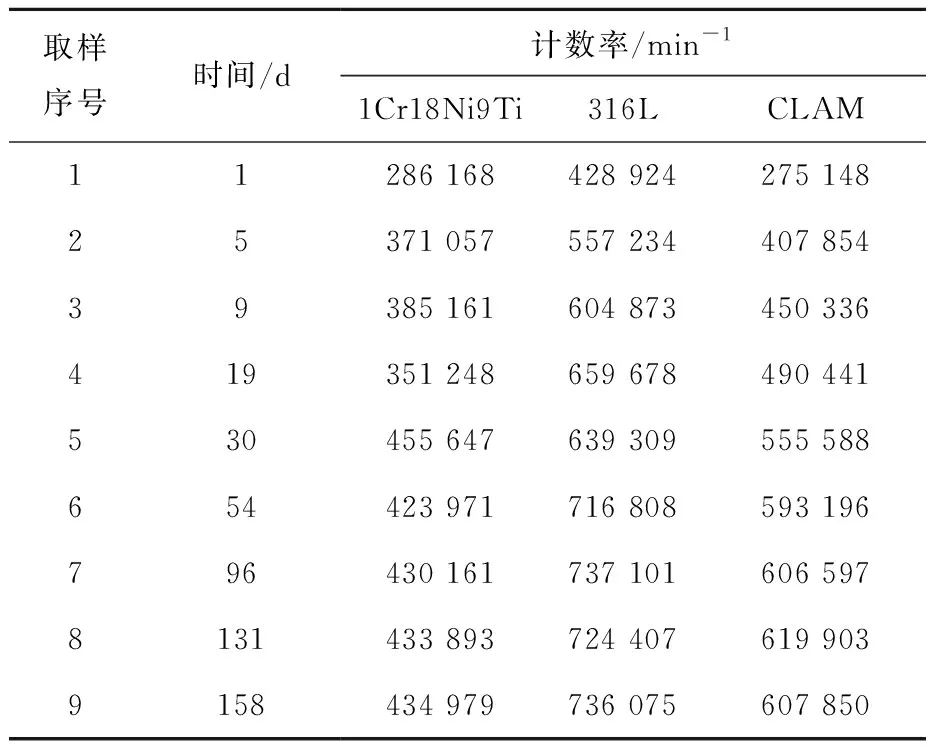
表4 浸泡样品水的氚活度随时间的变化Table 4 Tritium activity in water with sample steeping time measured by LSD
由表4数据得出,单位面积CLAM钢的脱附氚活度为133.2 kBq/cm2,316L钢的为114 kBq/cm2,1Cr18Ni9Ti钢的为90.2 kBq/cm2。单位面积的交换脱附氚量随时间的变化示于图3。
上述结果表明,氚在CLAM、316L和1Cr18Ni9Ti钢表面的吸附活度在量级上是一致的,考虑到吸附量大的样品表面粗糙度也较大,则3种材料的氚吸附性质很接近。
由图3还可见,3种材料表面氚的水交换脱附速率远大于Ar气中的脱附,在1个月的时间内,总释放氚量可占总吸附氚量的85%~90%,4个月的浸泡可认为已全部脱附。
3.3 讨论
1) 测量可靠性分析
在气体载带脱附氚-电离室测量过程中,影响准确性的因素有:(1) 样品转装时暴露于手套箱气氛的时间相对较长,氚释放不可忽略;(2) 流洗气经过测量系统的管道、阀门及电离室本身时,氚的二次吸附不可忽略;(3) 热释放的温度上限仅300 ℃,残留氚不可忽略。上述预期因素都使测得的数据偏小。

图3 浸泡水中样品单位表面总脱附氚量随时间的变化Fig.3 Time-dependent variation of total desorption tritium per unit surface of sample in immersed water
在水浸泡交换脱附-液闪测量过程中,影响准确性的因素有:(1) 取样量准确性;(2) 液闪计数器本身的准确性。目前这两个因素都能控制得较好,因此,液闪测量法的数据更可靠。
本实验中,水浸泡交换测得的数据较气相脱附法的大1倍多,表明水浸泡交换脱附-液闪测量法更准确。另外,文献[14-15]也得出了一致的结论。
2) 样品材料的氚吸附性质比较
(1) 3种材料的主要成分都是Fe,而CLAM的Fe含量最高,约为88.5%;其余两种材料的Fe含量约为70%。在这些材料的合金元素中,Fe的化学活性相对最强,对氚的吸附作用应最强。
(2) CLAM样的表面粗糙度约为0.8 μm,316L的约为0.2~0.3 μm,1Cr18Ni9Ti的约为0.1~0.2 μm。粗糙度越大,实际表面积与几何面积之比也越大;实际表面积越大,吸附量也越大。
(3) CLAM钢是bcc晶体结构和马氏体的金相组织,不同于316L和1Cr18Ni9Ti钢的fcc晶体结构和奥氏体组织。晶体结构和金相组织的差异会影响原子面密度,从而影响到氚的吸附量;另一个差别是材料缺陷的体积密度,这些缺陷往往是氚的陷阱,会增加氚的吸附面密度。
(4) 据浸泡所得数据,CLAM、316L和1Cr18Ni9Ti钢表面氚的吸附量之比为1.47∶1.26∶1;考虑到粗糙度和Fe含量双重差异,CLAM钢的吸附能力最强是合理的。3种材料表面的氚吸附性能差异较小,不仅在数量级上一致,在数值上差异也较小。显然,CLAM钢的氚吸附特性与316L和1Cr18Ni9Ti钢的差异很小。
3) 氚吸附性质的综合分析
因为氚吸附研究的困难性,迄今国内所做工作还很少[7]。综合分析国内外研究结果,可确认常用钢材表面吸附氚的存在形式、深度分布及平衡吸附时间等。
(1) 金属表面所吸附氚的存在形式,主要为HTO,HT只占少部分(≤10%)。
日本原子能研究所用598 K下抽真空的316钢样品暴露于HT气体,然后以5 K/min的速率程序升温,测得的气体脱附谱示于图4[2]。图中,HTO的脱附峰位于540~570 K处且相当宽大,HT的3个脱附峰分别位于约430、750、970 K处,4个峰的面积比为89∶5∶2∶4。
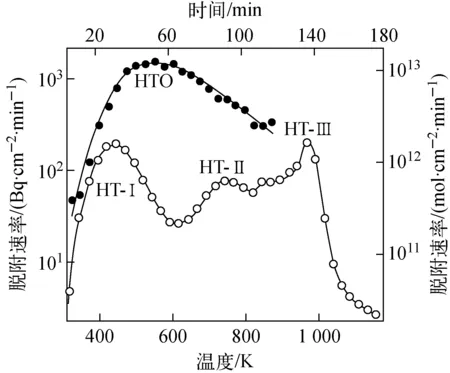
图4 316钢表面氚物种热释放谱[2]Fig.4 Thermal desorption spectrum of tritium species from 316 steel surface[2]
因为316钢的表面氚吸附性质与CLAM钢和1Cr18Ni9Ti钢的类似,可推测,CLAM钢表面吸附氚的存在形式也相同,除非表面洁净到无吸附水。
(2) 金属表面吸附氚的分布深度为μm级,表面浓度远大于基体浓度。
日本富山大学氢同位素研究中心用316L钢样品(15 mm×15 mm×0.5 mm)在573 K、1.2 kPa的H/T混合气体(CT=24%)中浸泡3 h后,通过化学刻蚀-液闪计数法检测了氚的深度分布。结果表明,氚主要分布于表面约7 μm厚度内,当将样品置于纯Ar气中135 d后,表面氚的分布深度变窄,且溶解在基体中的氚有向外扩散的趋势,如图5a[5]所示;将H/T换成D/T(CT=1%)浸泡5 h,所得结果示于图5b[6],表面氚的分布深度只有约2.5 μm,平均比活度≥108Bq/cm3,远大于室温下基体中氚的溶解度。
中国工程物理研究院核物理与化学研究所也研究过316L钢表面吸附氚的深度分布,实验使用了3个常温下吸氚、空气中存放3 a、表面活度差异较大的样品,同样通过化学蚀刻-液闪计数法检测,所得结果示于图6[7],表面氚的深度分布约为2~4 μm,氚存在形式是HTO(≥90%)和HT(≤10%)。
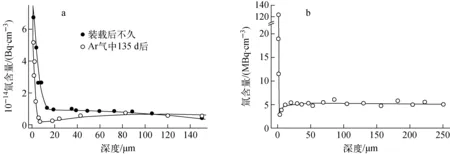
图5 316L钢在573 K下浸泡H/T[5]和D/T[6]后氚浓度随深度的分布Fig.5 Tritium depth profile after exposed to H/T[5] and D/T[6] mixture at 573 K on 316L steel surface
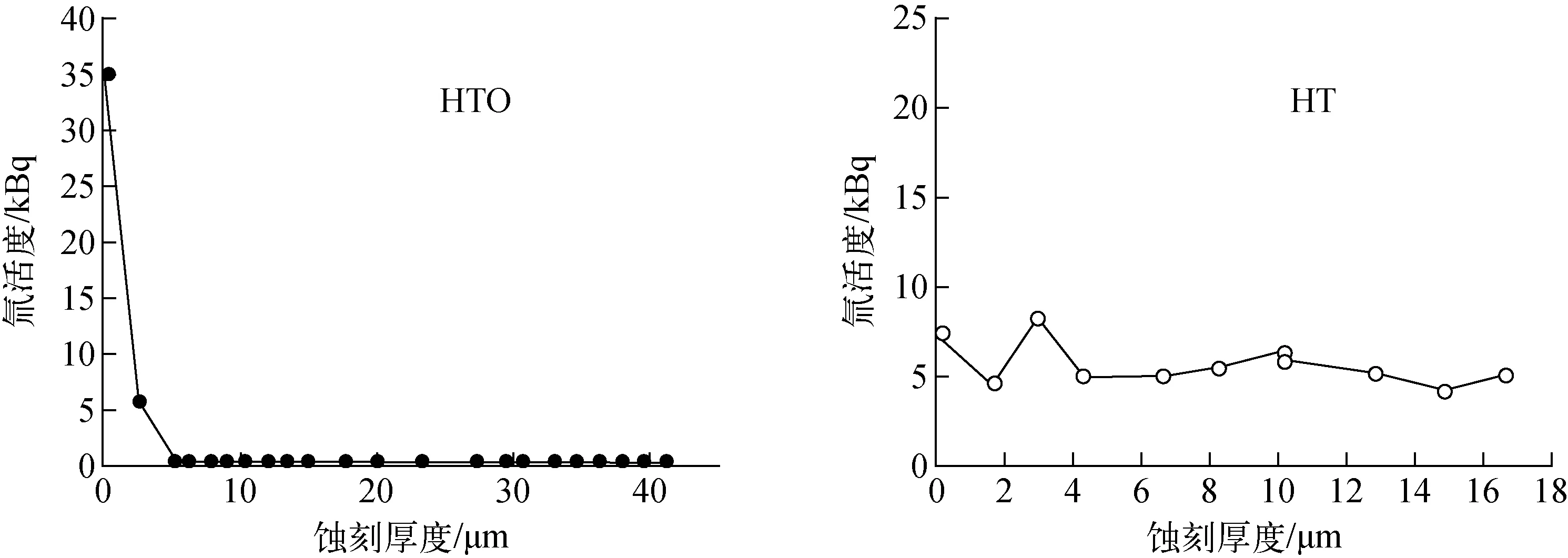
图6 室温下吸附氚的316L钢空气中存放3 a后表面氚的深度分布[7]Fig.6 Tritium depth profile on 316L steel surface after exposed to tritium and laid in ambient air for 3 years[7]
综上所述,室温下316L钢表面吸附氚形成富氚层,分布深度为μm级,体积浓度远大于室温下的基体浓度。因316L钢的元素组成与316钢的差异很小,可推测,CLAM、316L及1Cr18Ni9Ti钢等材料的表面氚分布深度大体也在数μm,但RAFM钢的扩散率和渗透率都大于316L钢的,预计表面富氚层厚度最大可达10 μm;另外也再次确认,吸附氚的存在形式以HTO为主,HT含量≤10%。
(3) 吸附机制及吸附量分析
吸附氚的存在形式(即吸附物种类)主要是HTO[16],只有少量的分子氚,推测产生这种效果的机制是常温下氚在金属表面的吸附能力很弱,而水分子吸附能力强;当样品暴露于气态氚时,氚与表面吸附水在射线的催化作用下,发生下列同位素交换:

铁与水的反应活性较强,化学吸附可达满分子层,理论上可得出此时的吸附分子面密度约为1.03×1015cm-2(H2O)。化学吸附水层上还可有多层物理吸附水,实际吸附状态与温度、水分压和吸附时间等因素有关。欲除去表面吸附水,通常需较长时间的真空加热除气(图4):在120 ℃以上真空除气,可除去表面物理吸附水;在200 ℃以上真空除气,可除去表面化学吸附水(图4中显示约550 K,即约280 ℃下水的脱附速率达到最大);温度越高、时间越长,清除越彻底。
实验得到CLAM、316L及1Cr18Ni9Ti钢3种材料的氚吸附活度分别为133.2、114、90.2 kBq/cm2,等效于HTO分子面密度分别约为RAFM钢7.46×1013cm-2、316L钢6.38×1013cm-2、1Cr18Ni9Ti钢5.05×1013cm-2,分别约为满分子层吸附量的7.4%、6.3%和5%。虽然吸附量相当小,但也符合物理规律,只要结合图4分析即可理解,因样品在200 ℃真空除气4 h,表面吸附水其实已充分释放。
氚与吸附水交换反应的速率与氚体积浓度有关,因为氚浓度越高,放射性催化作用也越强。除交换反应外,还有氚的解离吸附、在近表面的渗透、被陷阱捕陷等过程,因此,氚在钢表面的吸附平衡时间,在氚浓度较低(<10%)时约需30 d,在浓度较高时约需10~20 d[1]。交换平衡时,吸附水的氢同位素组成与气相氢同位素组成一致。
CLAM钢中Cr含量只有9%,电极电位依然为负,对水的吸附能力较316L和1Cr18Ni9Ti钢更强,在相同除气条件下,保留下来的水分应会多些。实验样品事先经过了加热200 ℃、4 h以上的抽真空,物理吸附的水分子应基本释放完全,但化学吸附水应未释放完全。据水浸泡交换法所得数据计算,本实验条件下CLAM钢表面吸附的氚原子密度为7.46×1013cm-2;按含氚化水90%、分子氚10%估计,表面残余水分子面密度为1.84×1014cm-2,不到满分子层的1/5。同法得出316L钢表面残余水分子面密度为1.57×1014cm-2,1Cr18Ni9Ti钢的为1.25×1014cm-2。这些数据完全符合逻辑。
4 结论
室温下RAFM钢表面的氚吸附与释放性质与316L钢、1Cr18Ni9Ti钢的非常相似,相同表面状态的样品,在相同实验条件下的吸附氚量相差不超过50%。根据316L钢的氚吸附性质,可推测室温下RAFM钢暴露于氚时,氚吸附于表面形成富氚层,厚度不大于10 μm,其氚的体积浓度远大于基体溶解浓度,一般高几个量级;表面吸氚量与暴露氚丰度和压力有关,与表面状态也有关,即表面越洁净、初始吸附水越少、粗糙度越小,表面吸附量越少。室温下暴露氚30 d左右,表面吸附可达平衡,氚丰度和压力越高,平衡速度越快。光滑、洁净、经真空干燥的表面吸氚量有极限,约为1×1015cm-2;热脱附时氚化水占90%~95%,分子氚约占5%~10%。
RAFM、316L和1Cr18Ni9Ti钢表面氚吸附性质的相似性,应源于它们的主要组成元素都是Fe,表面吸附水的相似性是最直接原因,而材料的晶体结构、金相组织不同造成近表面缺陷密度差异,因捕陷氚占总吸附量的比例较小,所以影响较为次要。
室温下RAFM钢表面的吸附氚在干燥气氛中释放非常缓慢,从趋势预测需要数年或更长时间;水浸泡能加速氚的释放,100 d基本能将吸附氚释放完全;由此预测潮湿空气中的释放速率也远大于干燥空气中的速率。

