动态浊度法评价一次性无菌注射器及塑料容器对细菌内毒素的吸附
魏 霞, 耿 雪,刘 娜,祝清芬
(山东省食品药品检验研究院,山东 济南 250101)
2017版的《中国药典分析检测技术指南》细菌内毒素检查法中对于直接接触供试品的器具(称量、溶解、稀释、注射等)做了应无菌、无热原的要求,并未对材质有禁止规定;方法对使用塑料器械的要求为:应选用标明无内毒素并且对试验无干扰的器械。日常热原检验工作中,各实验室常会使用一次性无热原注射器,样品稀释可能会使用无热原的离心管或细胞培养瓶作为容器具;在细菌内毒素(内毒素)检查过程中,样品和标准品的稀释也可能会使用塑料容器具。为明确目前一次性无菌注射器和塑料制品是否对细菌内毒素存在吸附,无吸附时间窗是多少而开展本次研究。
1 仪器与材料
1.1 仪器
PKF96 型细菌内毒素测定仪(美国ACC公司);洁净工作台(苏州净化设备有限公司);ZH-2 BLENDER振荡仪(天津药典标准仪器厂)。
1.2 材料
动态浊度法鲎试剂(湛江安度斯,批号:1809270);细菌内毒素工作标准品(中国食品药品检定研究院,批号:150601-201784);细菌内毒素用水(湛江安度斯,批号:1810170);一次性无热原枪头(Axygen);一次性无菌注射器(规格5,10 ml,山东新华安得医疗用品有限公司,批号:180329,失效日期202103,筒身为聚丙烯,密封圈为合成橡胶,执行标准为企标Q/AD 3151515-2015);10 ml无热原塑料离心管(管身、瓶盖均为聚丙烯,Corning公司);25 cm2细胞培养瓶(矩形,斜颈,透气盖,瓶身、瓶盖均为聚苯乙烯材质,Corning公司)。
2 方法与结果
本文依据《中国药典》2015年版第四部通则1143 细菌内毒素检查法[1](方法2:光度测定法)建立标准曲线,按建立的方法对各注射器和塑料容器进行与内毒素共存后的定量检测。
2.1 标准曲线的建立
用细菌内毒素检查用水将细菌内毒素标准品依次稀释至2,0.5,0.125,0.03125 EU/ml,每个浓度取0.1 ml加至3支反应试管中,同时取细菌内毒素用水0.1 ml加至2支反应试管中作为阴性对照。各管依次加入0.1 ml复溶好的动态浊度法鲎试剂(取1支,加1.25 ml细菌内毒素检查用水复溶),充分混合放入预热到37.0±0.1 ℃的 PKF96型细菌内毒素测定仪中,混匀时避免产生气泡,反应时间为3600 s,检测波长为660 nm。反应结束后以各浓度的平均反应时间对数值(LgT)为纵坐标,相应细菌内毒素浓度对数值(LgC)为横坐标,绘制标准曲线(见表1)。由表1可得标准曲线方程:LgT=2.88-0.263 LgC(r=-0.993)(|r|>0.980),平行管之间的变异系数均小于10 %,阴性对照的反应时间大于标准曲线最低浓度的反应时间,表明标准曲线符合规定。

表1 标准曲线可靠性试验结果
2.2 一次性无菌注射器与标准内毒素共存
本次试验选取5,10 ml注射器各2支,选取30,120 min 2个共存时间点,制备0.5 EU/ml的标准内毒素,根据注射器的量程,使内毒素溶液均匀充满注射器,分别在第1,2个时间点取样,样本分为两种混匀形式,第一种为未混匀前将溶液取出另置,加样前混匀30 s(外混匀),第二种为注射器内溶液直接混匀30 s加样(内混匀)。两种规格注射器同法操作,每个检测时点均取待测液0.1 ml,加入0.1 ml动态浊度法鲎试剂中,并同时做标准内毒素对照,标准内毒素对照盛放于无热原的玻璃试管内。检测条件及注意事项同标准曲线的建立。结果见表2。
表2结果显示,各样本细菌内毒素的回收率在50 %~200 %之间,阴性对照的检测值小于标准曲线最低点的检测值。表明共存放置2 h后,注射器内细菌内毒素浓度基本无变化。
2.3 塑料存储容器与内毒素共存
取离心管和细胞培养瓶,制备0.25 EU/ml的标准内毒素,根据其各自的容积,离心管、细胞培养瓶分别盛放10,30 ml标准细菌内毒素溶液,垂直放置于室温的净化工作台内,旋紧盖子保存,分别于2,5,7,30,48 h 5个时间点取样,,样本分为两种混匀形式,操作同2.2,离心管和细胞培养瓶同法操作,每个时间点均取待测液0.1 ml,加入0.1 ml动态浊度法鲎试剂中。同时做标准内毒素对照,标准内毒素对照盛放于无热原的玻璃试管内,但只在48 h试验结束时做检测,检测条件及注意事项同2.1。结果见表3、图1。结果表明,标准细菌内毒素与两种材质不同的塑料存储容器共存后,48 h内,细菌内毒素的回收率均在50 %~200 %之间,7 h内均未见标准内毒素浓度的降低;离心管与细菌内毒素共存后,在30 h、48 h两个时点,离心管、玻璃管内涡旋混匀,细菌内毒素的浓度均呈下降趋势;细胞培养瓶与细菌内毒素共存48 h后,细菌内毒素浓度未见明显变化。

表2 一次性无菌注射器与标准细菌内毒素共存后的内毒素含量
3 讨论
一般实验室常用的吸头、移液管等都使用聚丙烯材质,细胞培养板/细胞培养瓶一般采用聚苯乙烯材质,而塑料离心管可能会采用多种材质。目前,一次性使用无菌注射器执行的标准为GB 15810-2001,该标准对于筒身的材质要求为聚丙烯、聚苯乙烯或聚乙烯/丙烯腈共聚物,活塞为高质量的天然橡胶,表面涂以聚二甲基硅氧烷进行润滑。经调研,目前市场上一次性无菌注射器筒身多采用聚丙烯,本次试验采用的离心管也是聚丙烯材料,该材料的特点是半透明,为结晶性塑料,化学及温度稳定性较好,但在低温下会变脆,细胞培养瓶采用的是聚苯乙烯材料。有研究指出,一次性器具应选择聚苯乙烯,尽可能不要用聚丙烯材料,它会加剧内毒素的损耗(吸附内毒素)。本研究依据检验过程中的样品与注射器、塑料容器的共存情况,评价不同塑料制品对细菌内毒素的吸附作用,为检验工作提供数据。
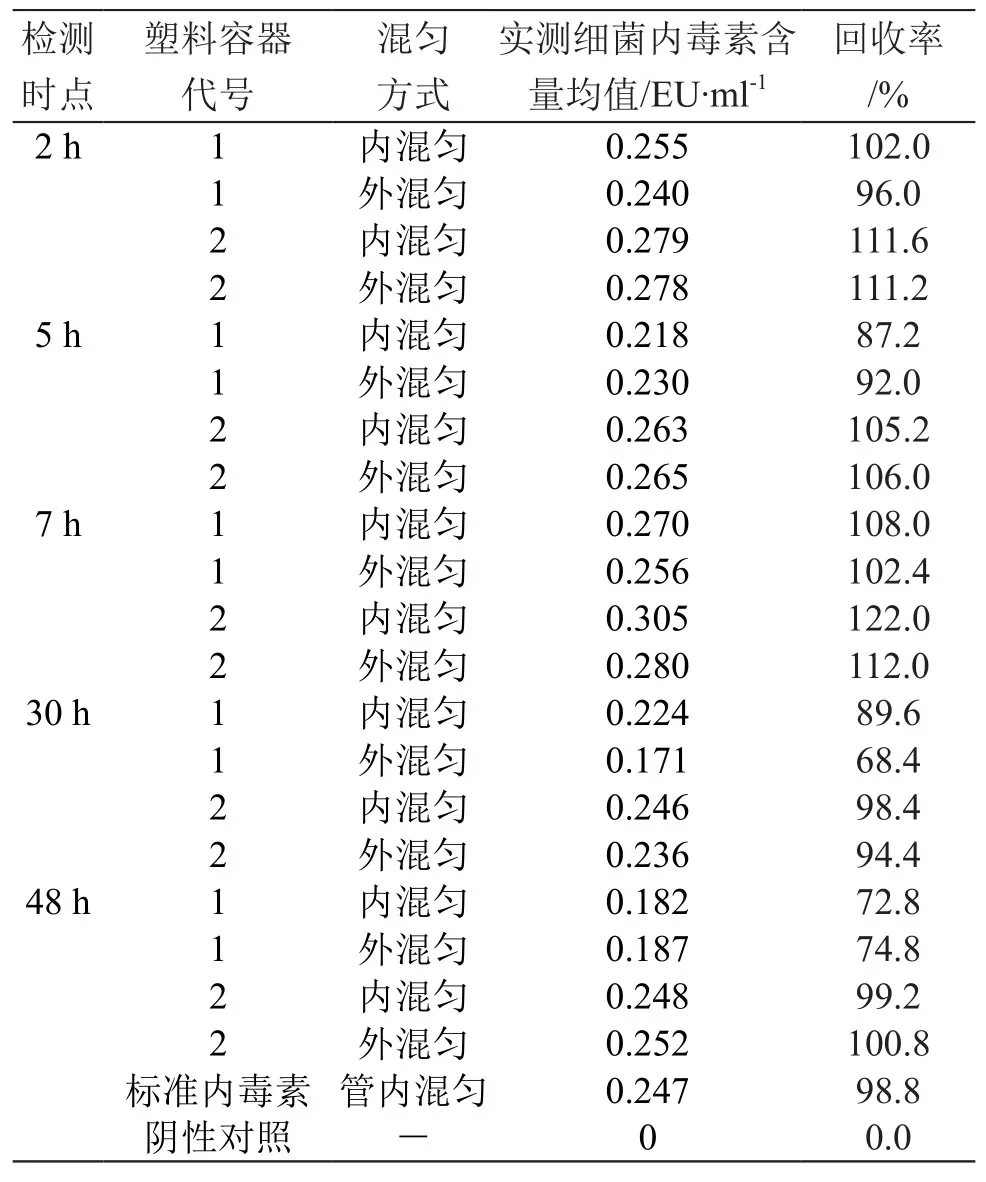
表3 塑料存储容器与标准细菌内毒素共存后的内毒素含量

图1 塑料存储容器与标准内毒素共存后的内毒素变化趋势
内毒素是革兰阴性菌细胞死亡后解体释放出的脂多糖类物质,对塑料等疏水性强的物质有很强的吸附能力,同时对不同材料也有很高的亲和力,如金属、陶瓷[2]、二氧化硅、锆[3]、丙烯酸树脂[4],甚至钛和钛合金[5]等。有文献[6]指出细菌内毒素实验中所使用的一次性吸头、酶标板等塑料制品,一定要使用无菌、无内毒素、无吸附作用且对内毒素实验不存在干扰的产品。聚丙烯材料制成的枪头对内毒素的吸附也被公认为是干扰内毒素检查的因素之一,因此,任何聚丙烯材料的试验器材不可用于内毒素的检查;但有实验证明由聚丙烯材料制成的加样吸头,与实验溶液的短暂接触对内毒素的回收没有影响[7]。
常规检验操作中,存于玻璃试管中的标准内毒素放置超过5 min及更长时间,加样前必须涡旋30 s后加样,以保证检验结果的准确性。本次研究采用了容器内、外两种模式进行混悬后加样,于细胞培养瓶中共存放置48 h后,未混悬取出的标准内毒素,其浓度与管内浓度未见明显差异,可见标准内毒素的吸附较少。根据试验结果,聚苯乙烯较聚丙烯材质,对细菌内毒素的吸附较少。实际检验过程中,可采用聚苯乙烯材料的无热原稀释器具进行热原、细菌内毒素检查用样品的稀释,稀释后也应尽快使用。在热原检查中,采用一次性无菌注射器抽取样品溶液后,应尽快或于2 h内完成注射。

