太平洋牡蛎在活品流通过程中的质谱-肽组学分析
陈李品 张晓梅 胡玲萍 毕诗杰 林黎明 李兆杰 张鸿伟 薛长湖

摘 要 在实验室模拟太平洋牡蛎保活流通过程,采用超高效液相色谱-四极杆飞行时间质谱联用技术(UHPLC-Q-TOF)分析太平洋牡蛎在活品流通过程中内源肽的变化,利用化学计量学方法筛选出各流通阶段的多肽标志物,以期筛选出一组评价太平洋牡蛎活品流通过程中品质变化的新指标。根据肽组学技术对整个活品流通阶段的3个环节(清洗、暂养净化以及无水保活)共7个关键时间点的样品进行内源肽提取,使用UHPLC-Q-TOF分离鉴定,并获得各个流通阶段的肽组轮廓。通过主成分分析(PCA)和正交偏最小二乘判别分析(OPLS-DA)等多元统计分析进行数据挖掘,并筛选出潜在的多肽标志物,经过在线数据库比对,鉴定出多肽氨基酸序列。结果表明,在清洗、暂养净化以及无水保活阶段分别筛选出3、10、8条潜在的多肽标志物。以潜在的多肽标志物DYDPVDK为例,建立可用于日常分析的基于液相色谱-三重四极杆质谱多反应监测(MRM)的分析方法。本研究采用肽组学技术对活品太平洋牡蛎在不同流通阶段的内源肽进行组学表征,筛选出指征不同流通阶段的潜在的多肽标志物,为活品贝类的流通过程提供检测依据。
关键词 超高效液相色谱-四极杆飞行时间质谱; 太平洋牡蛎; 肽组学; 多反应监测; 活品流通; 化学计量学
1 引 言
牡蛎属软体动物门,瓣鳃纲,牡蛎目,牡蛎科,是一种重要的海洋水产资源,其营养丰富,肉质鲜嫩,深受消费者的喜爱。随着世界上贝类海产品的产品结构发生变化,国内外市场上特别是一些内陆地区对鲜活贝类需求也越来越高。因此,需要建立与优化活品牡蛎的生鲜供应链[1~3],完善活品牡蛎供应链的前提是建立精准的、针对活品牡蛎的品质评价方法。
随着捕捞后流通时间的延长,活品牡蛎的体内会发生一系列变化,导致品质不断下降直至死亡。在流通过程中因缺少摄食而需要消耗自身能量物质维持生命活动,造成脂肪、蛋白、糖原等能量物质的下降,以及活力水平(超氧化物歧化酶、ATP等)、风味及营养品质下降。牡蛎活品在流通过程中面临多种环境胁迫,包括饥饿、干露和温度胁迫等,造成流通过程中其品质变化的复杂性。目前,对活品牡蛎在流通过程中的品质评价主要依靠传统的风味指标、能量代谢产物以及生命特征等[1,3],尚未有国家标准,难以全面反映牡蛎的整体品質[4]。因此,需要不断完善品质评价体系。
随着检测技术与分析技术的进步,尤其是高分辨质谱(High resolution mass spectrometry,HRMS)[5]技术的成熟和相关数据处理软件的升级,组学技术已成为品质评价的重要技术[6~9]。近年提出的食品组学技术[10] ,不仅可以解决食品基质复杂的难题[11],更能从整体生物学角度分析品质[9]。肽组学是一个来源于蛋白质组学的新兴领域[12],研究生物样本中的所有内源性多肽,可缩小蛋白组与代谢组的差距[13] 。肽组学与蛋白质组学的技术方法体系有许多相似之处,但在分析内容如研究对象、解析深度等方面也存在显著差异。总体而言,在以质谱技术为基础的组学分析中,肽的分析难度小于完整蛋白,因此,肽作为分析目标与蛋白相比更具吸引力。目前,蛋白组被广泛应用于水产品品质变化的检测,如Bosworth等[14]对受低氧胁迫的斑马鱼的鱼肉进行研究分析,发现低氧对6种低丰度蛋白产生影响,而不影响蛋白的表达模式,而肽组学技术则多被应用于食源性活性肽结构的鉴定,如Wu等[15]利用肽组学中的LC-MS/MS并辅以定量构效关系对大豆蛋白源ACE抑制肽进行了纯化和表征,阐明5条三肽序列分别为IVF、LLF、LNF、LSW和 LEF; 肽组学也被用于人类疾病标志物的筛查[12,16]。但在活品牡蛎流通过程中内源肽是否发生变化以及结构鉴定方面尚未见报道。
本研究采用超高效液相色谱-四极杆飞行时间质谱(UHPLC-Q-TOF)技术,结合化学计量学方法,分析筛选出各流通阶段活品太平洋牡蛎潜在的多肽标志物,并建立了可用于日常分析的基于液相色谱-三重四极杆质谱多反应监测(MRM)的分析方法。本研究利用肽组学技术阐明太平洋牡蛎在流通阶段内源肽的变化规律,并筛选出太平洋牡蛎在活品流通过程中与品质变化有关的多肽标志物,以期建立一组分子水平上的评价指标,完善活品牡蛎的品质评价体系。
2 实验部分
2.1 仪器与试剂
Nexera X2 30A高效液相色谱仪(日本岛津公司); 1290高效液相色谱(美国Agilent 公司); AB SCIEX Triple TOF 5600质谱仪、Triple QuadTM 5500三重四极杆质谱仪(美国SCIEX 公司); MQS50001型超纯水系统(美国Millipore公司)。
甲酸(质谱级)、二硫苏糖醇(DTT)、碘乙酰胺(IAA) (美国Sigma公司); 乙腈(美国Fisher公司); 其它试剂均为分析纯。
2.2 实验方法
2.2.1 样品的采集 活品太平洋牡蛎选用山东乳山(36°49′38.66′′ N,121°42′3.84′′E)的2 龄贝[壳高(108.32± 2.5 )mm,体质量(76.23±3.5)g],确保每组实验样品大小均一,采捕于2018年4月。太平洋牡蛎捕捞到岸后,加冰运至实验室,立刻取出30只牡蛎作为起始点(编号为a组),并对牡蛎进行常规清洗,再次取样(编号为b组)。清洗后,对太平洋牡蛎进行暂养净化处理24 h,进行真空包装,于4℃进行保活实验(1~9 d),于第1、3、5、7和9 d进行取样。
2.2.2 多肽样品制备 按上述采样时间准时采样,随机采取30只牡蛎,迅速取可食部位并用液氮速冻后研磨。取20 g研磨后的粉末,95℃加热灭酶10 min,在4℃以15000 r/min离心15 min,收集上清液,得肽粗提液。
取上清液,分别加入1 mol/L DTT100 μL,60℃水浴振摇反应30 min,然后冷却至室温,再加入1 mol/L现配的IAA溶液750 μL,室温避光反应1 h。将上述溶液使用ODS-C18固相萃取小柱(1 mg/6 mL)[17]除盐,冻干。冻干样品用200 μL 0.1% 甲酸-水复溶,转移到超滤离心管(10 kDa,Millipore公司)中,在室温以8000 r/min 超滤离心20 min,收集肽段滤液。
2.2.3 仪器数据采集的质量控制(Quality control,QC)
在本实验中,共进样45个(样品),包括生物学重复与技术重复。为更好地表征所有样液的质谱特征,质控样品采用合并样液的方式制备,将7个取样点的太平洋牡蛎样本的多肽提取液各取200 μL,充分混匀后作为质控样品(QC sample)。在DDA分析模式的采集中,质控样品的进样顺序和进样频率安排如下: (1)在进样序列分析前,QC 样品连续进样5次以平衡整个液相色谱-质谱分析体系; (2)在进样序列中,大约每隔15个样品,进样一针 QC 样品,共计8次穿插进样,以覆盖整个序列,保证对整个分析时长进行测定稳定性评估; (3)形成“QC(连续5次)-试样(1~15)-QC6-试样(16~30)- QC7-试样(31~45)-QC8”的分析序列[18]。同时,在整个实验中,以每5个样品校准一次的频率进行质量轴校准。
2.2.4 UHPLC-Q/TOF数据依赖性采集(DDA) 采用本研究组已优化的方法进行检测[17]。 采用超高效液相色谱-四极杆飞行时间质谱(UHPLC-Q-TOF)对提取出的多肽滤液进行分析鉴定。使用安捷伦AdvanceBio Peptide Map column(150 mm×2.1 mm,13 nm,2.7 μm)色谱柱; 柱温: 40℃。流动相A为0.1%甲酸-水,B为0.1%甲酸-乙腈。梯度洗脱: 0~2 min,5% A; 2~27 min,5%~0% A; 27~37 min,20%~35% A; 37~39 min,35%~80% A; 39~42 min,80% A; 42~46 min,5% A。流速: 0.25 mL/min; 质谱分析采用AB SCIEX TripleTOF 5600检测,TOF扫描范围: 350~1500Da,电喷雾正离子(ESI+)模式; 喷雾电压: 5500 V; 雾化气压力: 60 psi (1 psi=6.895 kPa); 辅助加热气压力: 50 psi; 气帘气压力: 35 psi; 离子源温度: 525℃; 解簇电压: 100 V。
2.2.5 潜在的多肽标志物的筛选 原始数据导入MarkerView(1.2.1,AB Sciex)进行峰的提取,并使用该软件利用总峰面积对数据进行归一化校正。归一化后的数据使用SIMCA-P(14.0,Umetrics)进行相关化学计量学分析,以筛选潜在的多肽标志物,主要包括主成分分析(PCA)和正交偏最小二乘判别分析(OPLS-DA),即分别进行无监督与有监督分类。
将每个样品3次平行采集的DDA数据使用Protein Pilot(5.0.2,AB Sciex)软件进行多肽的鉴定,检索NCBI(https://www.ncbi.nlm.nih.gov)太平洋牡蛎(Crassostrea gigas)的蛋白数据库(75135蛋白质序列,2018年11月下载)。主要鉴定参数设置如下: 半胱氨酸(Cys)烷基化试剂: Iodoacetic acid; 水解酶: None; 允许生物学修饰和氨基酸替代; 搜索设置: Thorough ID; 可信阈值: Unused Protscore(Conf)>1.3(95%); 假阳性错误率(False Discovery Rate,FDR): <1%。
2.2.6 质谱多反应监测(MRM)确认筛选出的潜在的多肽标志物 采用液相色谱串联Triple QuadTM 5500三重四极杆质谱仪建立多反应监测(MRM)方法[19,20]。液相色谱柱为AdvanceBio Peptide Map column(150 mm×2.1 mm,13 nm,2.7 μm); 柱温: 40℃。流动相A为0.1%甲酸-水,流動相B为0.1%甲酸-乙腈; 流速: 0.35 mL/min。梯度洗脱: 0~0.5 min,5% A; 0.5~17.0 min,5%~5% A; 17.0~17.5 min,35%~95% A; 17.5~20.0 min,95% A; 20.0~20.1 min,95%~5% A; 20.1~25.0 min,5% A。
电喷雾正离子(ESI+)模式; 喷雾电压: 5500 V; 雾化气压力: 60 psi; 辅助加热气压力: 50 psi; 气帘气压力: 35 psi; 离子源温度: 575℃。
使用 Skyline 工具构建潜在的多肽标志物的MRM离子对,采用 Analyst 软件(Version 1.6.2,SCIEX)进行数据分析[21]。
3 结果与讨论
3.1 数据分析前处理
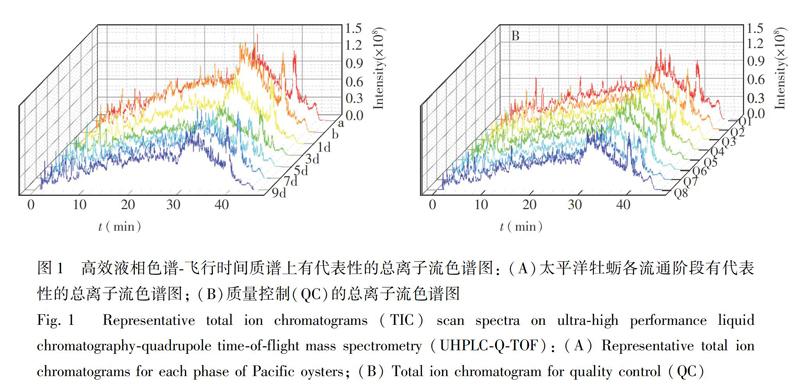
由活品太平洋牡蛎各流通时期的总离子流色谱图(图1A)可见,峰形较好,可用于肽的组学分析,不同流通阶段的总离子流图高度相似,说明不同品质的牡蛎内源肽比较相似,在活品流通期间内源性多肽仅有轻微的变化。在这种情况下,需通过化学计量学方法分析不同流通时间肽组的变化,进行品质区分。此外,从8个QC样本的总离子流色谱图(图1B)可见,QC样本表现出良好的谱图重复性,说明在实验期间仪器状态稳定,实验结果可信度高[22]。
3.2 数据统计分析
3.2.1 基于不同流通阶段的肽组轮廓分析 PCA分析属于无监督的化学计量学分析方法,通过主成分的提取实现数据降维。图2A为流通过程中各实验组的PCA分析得分图(Score plots),其中椭圆性区域为在95%置信限水平霍特林T2检验的可信区域,所有样品均位于霍特林T2的置信椭圆内。不同流通阶段的内源肽有一定差异,可进一步筛选流通过程中变化较大的多肽标志物。
为更深层次地分析不同品质内源多肽物的差异,克服无监督方法PCA分析在变量差异寻找方面的局限性,本实验采用有监督的OPLS-DA进一步进行数据信息的挖掘[23]。图2B给出流通过程中各实验组的OPLS-DA模型得分图。由图2B可见,不同流通阶段的牡蛎在OPLS-DA得分图中得到了非常清晰的区分效果,所有组的数据均紧密聚集,均位于霍特林T2的置信椭圆内。相比PCA分析,OPLS-DA模型中数据的聚集紧密度和分类清晰度均有显著提升。在构建的OPLS-DA模型中,拟合优度(R2X(cum)、R2Y(cum))和预测能力Q2(cum)的值分别为0.945、0.985和0.934,可见构建的OPLS-DA模型具有很好的拟合优度和模型预测能力。OPLS-DA模型的稳健性评估见图3C,在随机进行的200次置换检验中,所有随机置换模型的R2和Q2参数值均显著低于已构建模型的相应参数值,置换回归曲线的截距分别为R2=0.355; Q2=0.648,提示构建的模型稳健,不存在过拟和。
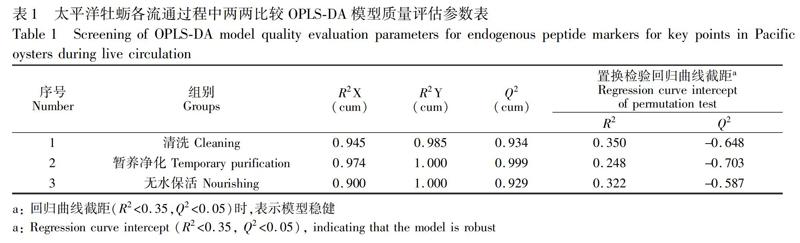
3.2.2 OPLS-DA两两比较及潜在的多肽标志物的筛选 聚类分析表明,不同流通阶段肽组有差异。为了筛选对流通阶段品质变化具有较大贡献的潜在的多肽标志物,需要进一步构建两两比较OPLS-DA模型进行差异分析。具体流程如下: (1)使用不同流通阶段的样本两两比较构建OPLS-DA分析模型(分为3组: 清洗、暂养、无水保活); (2)进行OPLS-DA模型质量评估; (3)按设定的过滤规则进行品质多肽标记物的发现。两两比较模型的质量评估参数见表1。所有构建的OPLS-DA模型在拟合优度(R2X(cum),R2Y(cum))、预测能力Q2(cum)、稳健度(R2,Q2的回归曲线截距)方面均满足要求。
为保证筛选出的多肽标志物具有统计学意义,根据多肽在OPLS-DA模型中的VIP值、变化倍数(Fold change)和p|corr|值对结果进行过滤,并通过载荷图刀切置信区间进行检验(以清洗与未清洗组的筛选过程进行图示说明,图3)。最终筛选结果以及前体蛋白见表2。结果表明,在清洗、暂养净化以及无水保活阶段分别筛选出3、10和8条潜在的多肽标志物,前体蛋白包括超氧化物歧化酶、肌球蛋白轻链和激肽释放酶等,主要涉及能量代谢、脂质氧化以及免疫水平等,说明在太平洋牡蛎的不同流通阶段均涉及多种应激反应,引起内源肽的变化。
3.3 多反应监控模式下对潜在的多肽标志物的归属
三重四极杆质谱作为低分辨质谱的代表,相比高分辨质谱其主要优势是靶向分析中的高灵敏度、高选择性和高重现性,通常用于目标组分的定量分析。所以,本实验对通过高分辨质谱筛选到的潜在的多肽标志物(以DYDPVDK为例进行说明)进行合成(南京金斯瑞公司,纯度>98%)并建立可用于日常分析的基于液相色谱-三重四极杆质谱的多反应监测(MRM)分析方法。使用Skyline软件处理MRM数据。对于每种肽,MS/MS谱中最强的3~5个峰被手动选择为初步的MRM传输离子对[24],仅选择了b-或y-碎片离子见表3。 Skyline预测了去簇电压和碰撞能量值。每个MRM传输离子对的停留时间设置为5 ms。图4为筛选出的潜在的多肽标志物(DYDPVDK)经MRM转换后的样品与标品中的代表性提取离子色谱图(XIC)。根据同一肽的MRM离子对具有相同的保留时间,以及离子比率是否位于鉴定分析的容许范围(30%的变异范围)内判断肽段序列的正确性。由图4可见,样品中该肽段的保留时间与合成肽段保留时间基本相同,在合成的肽段中,2对MRM离子对的离子比率为0.72∶0.28(峰高比),而在太平洋牡蛎样品中相应的2对MRM传输离子对离子比率则为0.73∶0.27,表明此肽段的序列鉴定结果的正确性以及MRM方法的适用性。
4 结 论
采用超高效液相色谱-四极杆飞行时间质谱(UHPLC-Q-TOF),结合化学计量学方法,分析筛选出太平洋牡蛎各流通阶段的潜在的多肽标志物,并验证篩选方法的正确性以及建立可用于日常分析使用的基于液相色谱-三重四极杆质谱的多反应监测(MRM)分析方法的可行性。本研究利用肽组学技术分析太平洋牡蛎在活品流通过程中的内源肽,以期筛选出一组新的评价指标,完善其保活流通过程中品质变化的评价体系。肽组学技术已成为生物标志物筛查的新方法,具有广阔的发展空间。本方法为后续的太平洋活品牡蛎品质评价提供了一个新思路。
References
1 Chinnadurai S,Kripa V,Venkatesan V,Mohamed K S. J. Mar. Biol. Ass. India.,2013,55(2): 83-86
2 Garrido V. Shellfish Safety and Quality. Beijing: Woodhead PublishingLtd Press,2009: 295
3 Madigan T,Kiermeier A,Carragher J,Lopes M,Cozzolino D. Innov. Food Sci. Emerg.,2013,19: 204-209
4 Berg R A,Hoefsloot H C,Westerhuis J A,Smilde A K,Werf M. J. Bmc Genomics.,2006,7: 142-147
5 YANG Xiao,HUANG Hua-Wei,WU Yuan-An,WANG Yi-Wen,LI Xiao-Ling,HUANG Xiang-Rong. Chinese Journal of Chromatography,2019,37(5): 505-511
杨 霄,黄华伟,伍远安,万译文,李小玲,黄向荣. 色谱,2019,37(5): 505-511
6 Gorrochategui E,Casas J,Porte C,Lacorte S,Tauler R. Anal. Chim. Acta,2015,854: 20-33
7 Gan J,Robinson R C,Wang J,Krishnakumar N,Manning C J,Lor Y,Breck M,Barile D,German J B. Food Chem.,2019,274: 766 -774
8 ZHU Wei-Xia,YANG Ji-Zhou,LI Sui,HU Kai,ZHANG Li. Chinese Journal of Chromatography,2017,35(2): 156-161
祝伟霞,杨冀州,李 睢,胡 锴,张 莉. 色谱,2017,35(2): 156-161
9 Chen S,Zhang C,Xiong Y,Tian X,Liu C,Jeevithan E,Wu W. Innov. Food Sci. Emerg.,2015,31: 185-195
10 Skov T,Honoré A H,Jensen H M,Naes T,Engelsen S B. TRAC-Trend. Anal. Chem.,2014,60: 71-79
11 Prandi B,Lambertini F,Faccini A,Suman M,Leporati A,Tedeschi T,Sforza S. Food Control,2017,74: 61-69
12 Li Q,Li J,Chen L,Gao Y,Li J. J. Cell. Biochem.,2018,119(6): 4636-4643
13 Dallas D C,Guerrero A,Khaldi N,Borghese R,Bhandari A,Underwood M A,Lebrilla C B,German J B,Barile D. J. Nutr., 2014,144(6): 815-820
14 Bosworth C A,ChauW C,Cole R B,Bernard B R. J. Proteome Res.,2005,5(5): 1362-1371
15 Gu Y C,Wu J P. Food Chem.,2013,141(3): 2682-2690
16 Schrader M,Schulz-Knappe P,Fricker L D. Open Proteomics,2014,3: 171-182
17 Dallas D C,Guerrero A,haldi N,Castillo P A,Martin W F,Smilowitz J T,Bevins C L,Barile D,German J B,Lebrilla C B. J. Proteome Res.,2013,12(5): 2295-2304
18 Zhang H,Zhang X,Zhao X,Xu J,Lin C,Jing P,Hu L,Zhao S,Wang X,Li B. Food Chem.,2019,274: 592-602
19 Hu L,Zhang H,Zhang X,Zhang T,Chang Y,Zhao X,Xu J,Xue Y,Li Z,Wang Y,Xue C. J. Agric. Food Chem.,2018,66(40): 10567-10574
20 Zha H,Cai Y,Yin Y,Wang Z,Li K,Zhu Z. Anal. Chem.,2018,90(6): 4062-4070
21 ZHOU Guang-Yun,WANG Gui-Ji,REN Hao-Wei. Chinese J. Anal. Chem.,2017,45(2): 205-210
周廣运,王桂姬,任皓威. 分析化学,2017,45(2): 205-210
22 Yi L,Dong N,Yun Y,Deng B,Ren D,Liu S,Liang Y. Anal. Chim. Acta,2016,914: 17-34
23 Huang B,Chen T,Xiao S,Zha Q,Luo P,Wang Y,Cui X,Liu L,Zhou H. RSC Adv.,2017,7(74): 46839-46851
24 Prandi B,Lambertini F,Faccini A,Suman M,Leporati A,Tedeschi T,Sforza S. Food Control,2017,74: 61-69

