百药煎HPLC指纹图谱的建立及其中5种成分的含量测定
陈晶晶 张振凌 曹淼淼 张颖 杨佳宁
中图分类号R284.1
文献标志码A
文章编号 1001-0408(2020)02-0173-06
DOI 10.6039/j.issn.1001-0408.2020.02.09
摘要 目的:建立百药煎的高效液相色谱( HPLC)指纹图谱,同时测定其中5种成分的含量及优选百药煎的原料酒糟。方法:采用HPLC法,色谱柱为Waters Symmetry ShieldTM RP18,流动相为乙腈-0.1%三氟乙酸水溶液(梯度洗脱),流速为0.8 mL/min,检测波长为280 nm,柱温为30℃,进样量为5μL。以没食子酸为参照,绘制14批百药煎样品的HPLC指纹图谱;采用《中药色谱指纹图谱相似度评价系统》(2012版)进行相似度评价,确定共有峰;采用SPSS 20.0软件进行聚类分析。结果:14批百药煎样品共有11个共有峰,相似度为0.424-0.998,其中A1-A5相似度<0.850;B1-B9样品中为共指认出5个成分,分别为没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6-三-O-没食子酰-β-D-葡萄糖、2,4,6一三一O一没食子酰-a-D-葡萄糖。聚类分析结果显示,14批样品可聚为3类,A1-A5聚为一类,B1、B6聚为一类,B2-B5、B7-B9聚为一类。上述5种成分的质量浓度线性范围分别为29.96-599.2μg/mL(r=0.999 6)、0.832-416 μg/mL(r=0.999 6)、0.102-51 μg/mL(r=0.999 8)、0.286 4-143.2 μg/mL(r=0.999 8)、0.286 4-143.2 μg/mL( r=0.999 8);定量限分别为0.060、0.104、0.017、0.029、0.057 μg/mL,检测限分别为0.018、0.031、0.005、0.009、0.017μg/mL;精密度、稳定性、重复性、耐用性试验的RSD均小于3qo;加样回收率分别为97.16% -101.88 qo( RSD= 1.60%,n=6)、96.98% -99.24%(RSD= 0.85%,n=6)、97.70% -101.64%(RSD= 1.54%,n=6)、97.77% -103.08%( RSD=1.82%,n=6)、98.16% - 101.88%( RSD= 1.24%,n=6)。结论:本研究所建HPLC指纹图谱和聚类分析可用于评价百药煎的质量;所建含量测定方法操作简便,可用于同时测定百药煎中5种成分的含量;稻壳类酒糟不适用于发酵百药煎。
关键词 百药煎;指纹图谱;高效液相色谱法;含量测定;酒糟;聚类分析
百药煎为五倍子、酒糟、茶叶经发酵加工而成饮片[1],始载于《太平惠民和剂局方》[2],具有润肺化痰、生津止渴的功效,临床多用于久咳痰多、咽痛、便血、久痢脱肛、口疮、牙疳、痈肿疮疡等的治疗[3-4]。历代古籍《本草纲目》[5]中记载“五倍子1斤,真茶1两,酵糟4两”;《本经逢原》[6]记载“五倍末1斤,桔梗、甘草、真茶各1两,酵糟2两”;由此可见,百药煎为五倍子、酒糟及其他辅料制成的发酵品。目前,仅有《浙江省中药炮制规范》[7]和《四川省中药饮片炮制规范》[1]中记载百药煎处方为“五倍子、茶叶、酒糟”。酒糟不仅是百药煎的处方组成之一,同时也可为百药煎发酵提供碳源、能量以及发酵菌种;五倍子主要含有鞣质类成分,其在肠道内易与食物中的蛋白质结合形成不溶于水的沉淀物,从而刺激胃肠黏膜,引起食欲不振等不良反应[8],但在百药煎的发酵过程中,该成分可水解为没食子酸,进而可减弱其收敛作用,减少胃肠黏膜刺激性及食欲不振等不良反应的发生[9-11]。目前,关于百药煎的发酵工艺研究多以单一成分没食子酸为评价指标[12-14],相关标准也仅有《浙江省中药炮制规范》[6]中规定了百药煎中没食子酸不得少于35.0%,这并不能全面评价百药煎的质量,且也尚未见不同酒糟种类对百药煎发酵过程及其成品质量影响的报道。中药指纹图谱能够较为全面地反映中药所含化学成分的种类与数量,进而反映其质量[15-17]。基于此,本研究建立了百药煎的高效液相色谱(HPIC)指纹图谱,并测定了其中没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰- β-D-葡萄糖的含量,同时结合聚类分析比较了不同酒糟发酵后百药煎的质量差异,旨在为控制百药煎的质量及优化其炮制工艺提供参考。
1 材料
1.1 仪器
1525-2489型HPLC仪,包括二元泵、二极管阵列检测器(美国Waters公司);HWS-250型恒温恒湿培养箱(天津市莱玻特瑞仪器设备有限公司);BT25S型十万分之一电子分析天平、BS2IOS型万分之一电子分析天平[赛多利斯科学仪器(北京)有限公司];FW-200型高速万能粉碎机(北京中兴伟业仪器有限公司);KQ-500DV型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 药品与试剂
没食子酸对照品(批号:PS08121401,纯度:98.5%)、没食子酸甲酯对照品(批号:PS161028-01,纯度:98%)、(一)一表没食子儿茶素对照品(批号:PS000167,純度:98.5%)均购自成都普思生物科技股份有限公司,2,4,6---O-没食子酰-a-D-葡萄糖对照品(批号:20150824-1,纯度:98%)、2,4,6一三-O-没食子酰-β-D -葡萄糖对照品(批号:20150824-2.纯度:98%)均由河南中医药大学药学院自制;甲醇、乙腈为色谱纯,其他试剂均为分析纯,水为双蒸水。
1.3 饮片及药材
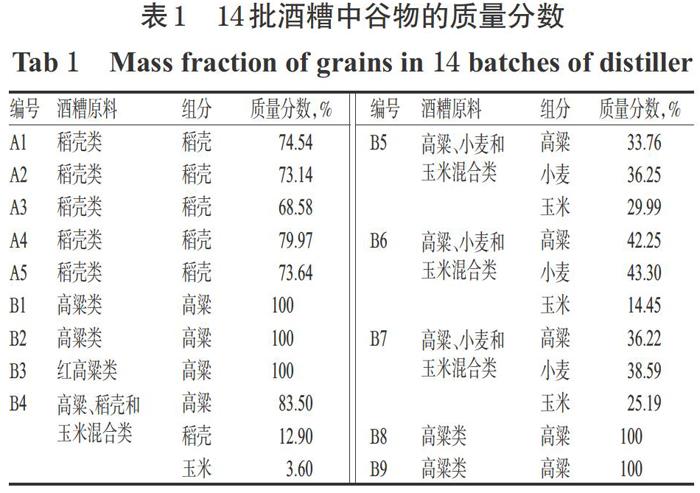
百药煎(浙江桐君堂中药饮片有限公司,编号:Sl,批号:160618;四川辅正药业有限责任公司,编号:S2,批号:160801;四川得恩德药业有限公司,编号:S3,批号:160822);五倍子药材(批号:160429)购自安徽石田中药饮片有限公司,经河南中医药大学药学院张振凌教授鉴定为漆树科植物盐肤木(Rhus chinensis Mill)等叶上的虫瘿,由五倍子蚜(Melaphis chinensis Baker)寄生而形成;茶叶(绿茶,信阳吴记梦之绿茶叶有限公司,批号:20160810);酒糟(编号:A1~A5,雅安迅康药业有限公司;编号:B1~B9,北京华邈药业有限公司)。取干燥酒糟约100 g,分离酒糟中各谷物,称定质量,计算其质量分数,详见表1。
2 方法与结果
2.1 样品的制备
按《浙江省中药炮制规范》[6]项下百药煎的炮制方法制备百药煎样品:取五倍子、茶叶、酒糟[100:6.2:25,m/m/m]。茶叶不粉碎,加15倍量水煎煮20 min,煎煮3次,滤过,合并滤液,浓缩;将五倍子粉末与酒糟混匀后,加入上述浓缩后的茶叶汁,制成含水量为45%的软材,置于35℃、相对湿度85%的恒温恒湿培养箱中发酵5d,取出,切块,60℃烘干,即得。
2.2 百药煎的HPLC指纹图谱建立
2.2.1 色谱条件 色谱柱:Waters Symmetry ShieldT TMRP18( 250 mmx4.6 mm,5μm);流动相:乙腈(A)一0.1%三氟乙酸水溶液(B),梯度洗脱(0~40 min,IO%A→16%A;40~41 min, 16%A→18%A;41~55 min,18%A→ 19%A;55~75 min, 19% A→24% A; 75~90 min, 24% A→IO%A);流速:0.8 mL/min;检测波长:280 nm;柱温:30℃;进样量:5 μL。
2.2.2 供试品溶液的制备精密称取“2.1”项下制备的百药煎样品(编号同对应的酒糟编号A1~A5、B1~B9,过四号筛)0.2 g,置于100 mL锥形瓶中,加甲醇50 mL,静置2h,超声(功率:300W,频率:60 kHz)提取40 min,放冷,再次称定质量,用甲醇补足减失的质量,摇匀,经0.22 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 混合对照品溶液的制备分别取没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰- β-D-葡萄糖对照品各适量,精密称定,加甲醇溶解,制得含上述5种成分质量浓度分别为599.2、416.O、51.0、143.2、143.2 mg/L的混合对照品溶液。
2.2.4 精密度试验取“2.2.2”项下供试品溶液(编号:Bl)适量,按“2.2.1”项下色谱条件连续进样测定6次,以没食子酸峰的保留时间和峰面积为参照,记录各共有峰的相对保留时间和相对峰面积。结果,11个共有峰相对峰面积的RSD均小于3.73%(n=6),相对保留时间的RSD均小于0.28%(n=6),表明该方法精密度良好。
2.2.5 稳定性试验取“2.2.2”项下供试品溶液(编号:Bl)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.2.1”项下色谱条件进样测定,以没食子酸峰的保留时间和峰面积为参照,记录各共有峰的相对保留时间和相对峰面积。结果,11个共有峰相对峰面积的RSD均小于3.92%(n=6),相对保留时间的RSD均小于0.23%(n=6),表明供试品溶液于室温下放置24 h内稳定性良好。
2.2.6 重复性试验取百药煎样品(编号:B1)适量,共6份,按“2.2.2”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,以没食子酸峰的保留时间和峰面积为参照,记录各共有峰的相对保留时间和相对峰面积。结果,11个共有峰相对峰面积的RSD均小于3.80%(n=6),相对保留时间的RSD均小于0.15%(n=6),表明本方法重复性良好。
2.2.7 HPLC指纹图谱的生成取五倍子药材及17批百药煎样品(A1~A5、B1~B9、S1~S3)各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,采用《中药色谱指纹图谱相似度评价系统》(2012版)对样品指纹图谱进行分析。由于百药煎市售样品S1~S3图谱提取吸收信号较强、峰形明显、稳定性较好,故以其共有峰生成标准图谱,并作为参照图谱(S参)进行对比。结果发现,各批样品色谱峰之间存在一定差异,样品AI~A5与五倍子药材图谱(S五倍子)较为相似,样品B1~B9与S参差异较小,推测样品A1~A5可能未成功发酵为百药煎,详见图1。
2.2.8 相似度评价采用《中药色谱指纹图谱相似度评价系统》(2012版),以S参为对照,进行整体相似度评价,结果见表2。由表2可见,14批样品(A1~A5、B1~B9)与S参的相似度分别为0.424、0.478、0.458、0.469、0.362、0.995、0.993、0.993、0.992、0.994、0.998、0.994、0.991、0.983;样品间相似度差异较大,样品A1~A5相似度<0.850,提示A1~A5样品可能未发酵成功。进一步以S。倍子为对照,对样品A1~A5进行相似度评价,结果样品A1~A5与S五倍子的相似度分别为0.686、0.776、0.915、0.873、0.877,提示样品A1~A5未发酵成功,故稻壳类酒糟不适用于发酵百药煎。
2.2.9 共有峰的指认由于A1~A5样品未发酵成功,故仅对样品BI~B9进行共有峰指认。结果,样品B1~B9共有11个共有峰,通过与混合对照品溶液的HPLC图谱对比,共指认出5个成分,分别为1号峰(没食子酸)、2号峰[(一)-表没食子儿茶素]、3号峰(没食子酸甲酯)、7号峰(2,4,6一三-O-没食子酰- β-D-葡萄糖)、9号峰(2,4,6一三-O-没食子酰-a-D-葡萄糖),详见图2。由图2可知,1号峰(没食子酸峰)在图谱中所占的比例较大,与相邻色谱峰的分离度良好,符合参考峰要求,因此以其为参照峰。以1号峰保留时间和峰面积为参照,计算其他峰的相对保留时间和相对峰面积,结果详见表3、表4。
2.3 14批百药煎样品的聚类分析
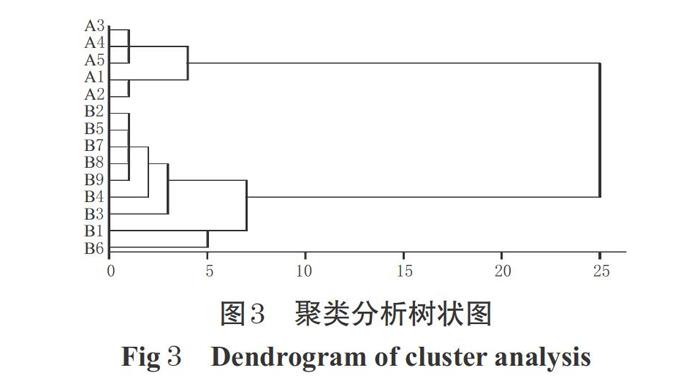
以各共有峰的峰面积为原始数据(由于样品A1~A5在共有峰的出峰时间下未检测到峰面积,故以0为原始数据),采用SPSS 20.0软件,以组间平均数联结法,夹角余弦为样品相似度的距离公式对14批样品(A1~A5,B1~B9)進行聚类分析,详见图3。由图3可知,14批样品可聚为3类,A1~A5聚为一类;B1、B6聚为一类;B2~B5、B7~B9聚为一类。
2.4 百药煎中5种有效成分的含量测定
2.4.1 色谱条件同“2.2.1”项下色谱条件。
2.4.2 溶液的制备按“2.2.2”项下方法制备供试品溶液,即得;按“2.2.3”项下方法制备混合对照品溶液,即得;以甲醇为阴性对照溶液。
2.4.3 系统适用性试验取“2.4.2”项下混合对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.2.1”项下色谱条件进样测定,记录色谱,详见图4。由图4可知,5种成分峰的分离度均大于1.5,理论板数均大于10 000,阴性对照对测定无干扰。
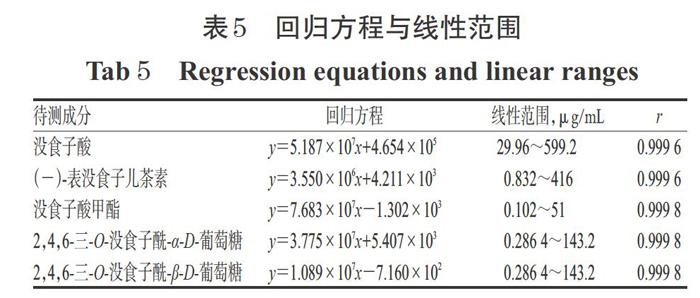
2.4.4 线性关系考察取“2.4.2”项下混合对照品溶液1 mL,分别置于1、2、5、10 mL量瓶中加甲醇稀释至刻度,摇匀;另精密量取稀释10倍的混合对照品溶液1mL,分别置于2、5、10、25、50 mL量瓶中,加甲醇稀释至刻度,摇匀,得系列线性工作溶液。分别精密吸取上述线性工作溶液各20 μL,按“2.4.1”项下色谱条件进样测定,记录峰面积。以各待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,结果见表5。
2.4.5 定量限与检测限考察分别精密吸取“2.4.2”项下混合对照品溶液适量,加甲醇倍比稀释,按“2.4.1”项下色谱条件进样测定,记录峰面积,以信噪比10:1、3:1分别计算定量限、检测限。结果,没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰- β-D-葡萄糖的定量限分别为0.060、0.104、0.017、0.029、0.057 μg/mL,检测限分别为0.018、0.031、0.005、0.009、0.017 μg/mL。2.4.6精密度试验取“2.4.2”项下混合对照品溶液适量,按“2.4.1”项下色谱条件连续进样测定6次,记录峰面积。结果,没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰—β-D一葡萄糖峰面积的RSD分别为1.07%、0.82%、0.34%、1.24%、1.69%(n=6),表明仪器精密度良好。
2.4.7 稳定性试验取“2.4.2”项下供试品溶液(编号:Bl)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.4.1”项下色谱条件进样测定,记录峰面积。结果,没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰- β-D-葡萄糖峰面积的RSD分别为1.50%、0.57%、1.07%、1.97%、1.68%(n=6),表明供试品溶液于室温下放置24h内稳定性良好。
2.4.8 重复性试验取百药煎样品(编号:B1)适量,共6份,按“2.4.2”项下方法制备供试品溶液,再按“2.4.1”项下色谱条件进样测定并按标准曲线法计算样品中5种成分的含量。结果,没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰-β一D一葡萄糖的平均含量分别为40.75%、23.21%、0.61%、1.75%、2.76%,RSD分另0为1.22%、0.06%、1.73%、1.35%、0.92%(n=6),表明该方法重复性良好。
2.4.9 加样回收率试验取百药煎样品(编号:B1)共6份,每份约0.1 g,精密称定,分别加入一定量的没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6-三-O-没食子酰-a-D-葡萄糖、2,4,6-三-O-没食子酰—β-D一葡萄糖对照品,按“2.4.2”项下方法制备供试品溶液,再按“2.4.1”项下色谱条件进样测定,記录峰面积并计算加样回收率,结果见表6。
2.4.10 耐用性试验取百药煎样品(编号:B1)适量,按“2.4.2”项下方法制备供试品溶液,再参照“2.4.1”项下色谱条件,以不同流动相(B)浓度(0.08%、0.1%、0.12%)、不同流速(0.7、0.8、0.9 mL/min)、不同柱温(25、30、35℃)进样测定,记录峰面积并按标准曲线法计算样品中5种成分的含量。结果,含量RSD均小于3%(n=3),表明该方法能够满足试验要求,耐用性良好。
2.4.11 样品含量测定取14批百药煎样品各适量,按“2.4.2”项下方法制备供试品溶液,再按“2.4.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算样品中5种成分的含量,平行操作3次,取平均值,结果见表7。
3 讨论
本研究通过对14批酒糟发酵后得到的百药煎样品分别与S参、S五倍子图谱进行对比后发现,样品A1~A5与百药煎参照图谱的相似度均小于0.48,而与五倍子药材图谱相似,相似度均大于0.68;样品B1~B9与百药煎参照图谱相似,相似度均大于0.98。这提示A1~A5批样品未发酵成功,B1~B9批样品成功发酵为百药煎。
《浙江省中药炮制规范》中规定,百药煎中没食子酸不得少于35.O%[7]。本研究14批样品中A1~A5没食子酸的含量为4.89%~6.29%,不符合上述规定;BI~B9没食子酸的含量为35.11%~48.27%,符合规定。编号为BI~B9的9批酒糟包括5批高梁类(B1~B3、B8~B9)和4批高粱及玉米等混合类(B4~B7)。其中,5批高粱类酒糟发酵后得到的百药煎中没食子酸、(一)一表没食子儿茶素、没食子酸甲酯、2,4,6一三-O-没食子酰-a-D-葡萄糖、2,4,6一三-O-没食子酰—β-D一葡萄糖含量分别为39.47%~45.22%、23.21%~40.35%、0.05%~0.60%、1.75%~8.25%、2.77%~10.64%,4批高粱及玉米等混合类酒糟发酵后所得百药煎样品的含量分别为35.11%~48.27%、15.73%~31.14%、0.04%~0.53%、1.83%~6.69%、2.22%~9.49%,各批样品间含量存在较大差异,可能与各批酒糟中所含菌种的种类、发酵过程中菌种复苏的数量以及环境的湿度不均匀有关[9-11]。
综上所述,本研究所建HPLC指纹图谱和聚类分析可用于评价百药煎的质量;所建HPLC含量测定方法操作简便,可用于同时测定百药煎中5种成分的含量。
参考文献
[1] 四川省食品药品监督管理局,四川省中药饮片炮制规范[S].成都:四川科学技术出版社,2015:13.
[2]宋·太平惠民和剂局所,太平惠民和剂局方[M].上海:上海人民出版社,2005:179.
[3]江苏新医学院.中药大辞典[M].上海:上海人民出版社,1977:865.
[4]彭璐,龚千锋,李小宁,等.百药煎炮制历史沿革及现代研究[J].江西中医药大学学报,2016,28(2):113-116.
[5]明·李时珍,本草纲目[M].北京:人民卫生出版社,1982:2236
[6]清·张璐本经逢原[M]上海:上海科學技术出版社,1959:199.
[7]浙江省食品药品监督管理局.浙江省中药炮制规范[S]航州:浙江科学技术出版社,2015:432-433.
[8]王和英.五倍子的发酵炮制[J].基层中药杂志,2000,14(4):40.
[9]胡梦,百药煎传统炮制过程中微生物的分离、鉴定及降解鞣质最佳菌种组合的筛选[D].上海:中国医药工业研究总院,2018.
[10]胡梦,程玉冰,张培燕,等.百药煎中转化鞣质生成没食子酸的最佳菌种组合筛选[J].中国现代中药,2018,20(4):453-457.
[11]胡梦,王瑞生,文雯,等,百药煎传统炮制过程中微生物的分离与初步鉴定及其鞣质水解能力测定[J].中国现代中药,2017,19(8):1120-1125.
[12]李柯柯,张振凌,于文娜,等.百药煎发酵过程中pH值与没食子酸含量动态变化的研究[J].时珍国医国药,2017,28(7):1637-1639.
[13]孙翼飞,张振凌,李柯柯,等.百药煎发酵过程中没食子酸含量动态变化的研究[J].中华中医药学刊,2016,34(7):1630-1633.
[14] 史莲莲,邓德英,张振凌,等.绿茶对五倍子发酵品的影响[J].中成药,2015,37(4):836-839.
[15]王珊,时伟朋,田文月,等,莲子心HPLC指纹图谱研究及不同产地生物碱含量测定[J].中华中医药学刊,2018,36(6):1454-1457.
[16] 牛晓静,鲁静,孙广科,等.淫羊藿总黄酮提取物的HPLC指纹图谱建立及其中8种成分的含量测定[J].中国药房,2018,29(24): 3376-3380.
[17]尚莹莹,胡辉,刘源才.金樱子配方颗粒提取工艺优化及质量标准、指纹图谱研究[J].中国药房,2018,29 (14):1922-1927.
(收稿日期:2019-07-01修回日期:2019-11-02)
(编辑:陈宏)
△基金项目:国家重点研发计划项目(No.2018YFC1707200);公益性行业科研专项项目(No.201507004-03);河南中医药大学研究生科研创新基金项目( No.YJS2018814)
*硕士研究生。研究方向:中药饮片及新药研究。E-mail:401327039@qq.com
#通信作者:教授,博士生导师,博士。研究方向:中药饮片及新药研究。电话:0371-65680970。E-mail: zhangz16758@163.com

