酰胺化衍生-高效液相色谱-四极杆-高分辨飞行时间质谱法测定食品接触塑料材料中7种烷基胺
区硕俊 岑建斌 梁俊发* 李秀英 郭新东寻知庆 罗曼妮 曾广丰
1(广州海关技术中心, 广东省动植物食品进出口措施研究重点实验室, 广州 510623)2(广州检验检测认证集团有限公司, 国家加工食品质量检验中心(广东), 广州 511447)3(广州质量监督检测研究院, 广州 511447)
1 引 言
烷基胺是脂链烃类和脂环烃类等烷烃的氨基取代物, 属于一类亲核型固化促进剂。在接触性食品塑料包装材料及塑料制品的生产过程中, 烷基胺类固化促进剂能同时对环氧树脂和酸酐起双重作用, 因此在塑料包装材料的生产工业中广泛应用[1,2]。随着塑料包装材料与食品的接触时间增长, 塑料包装材料及塑料制品中残留的有机胺会向食品中迁移, 从而对食品造成污染[3,4]。烷基胺类物质具有一定的毒性, 如乙醇胺对雌性小鼠经口服的半数致死量为2650 mg/kg[5]。此外, 一些有机胺在亚硝化剂的条件下容易形成具有强致癌性的N-亚硝基化合物[6]。GB4806.6-2016规定1,6-己二胺在食品接触材料 聚酰胺(Polyamide, PA) 中的特定迁移限量为2.4 mg/kg[7], 而欧盟指令(EU)No.10/2011要求, 食品接触材料的芳香族伯胺 PAAs 在食品或食品模拟物中的迁移限量为0.01 mg/kg[8]。建立准确测定食品接触材料中烷基胺类化合物的方法具有重要的实际意义。
目前, 关于塑料包装材料中的胺类物质研究主要是针对毒性较强的不饱和芳香胺和酰胺类物质的检测技术和迁移行为, 对烷基胺类物质的相关报道较少。已报道的胺类物质相关检测方法主要为高效液相色谱法[4,9,10]、气相色谱法[11,18]、液相色谱-串联质谱法[12,20,21]和气相色谱-质谱法[13]。针对食品接触材料中较多使用的2,2,4-三甲基-1,6-己二胺(2,2,4-Trimethyl-1,6-hexanediamine)、N,N'-二甲基-1,3-丙二胺(N,N'-Dimethyl-1,3-propanediamine)、N,N-二乙基-1,3-丙二胺 (N,N-Diethyl-1,3-propanediamine)、1,6-己二胺 (1,6-Hexanediamine)、1,4-丁二胺 (1,4-butanediamine)、5-氨基-1,3,3-三甲基环己甲胺 (5-amino-1,3,3-trimethylcyclohexylamine)和4,4'-亚基双环己胺(4,4'-methylenebiscyclohexylamine)等烷基胺类物质的相关报道仅有离子色谱法[14~16]、毛细管电泳法[17]、气相色谱法[18]、气相色谱-质谱法[19]和液相色谱-串联质谱法[20,21], 但离子色谱法要求检测成分之间的含量差不宜太大, 而塑料材料中的烷基胺含量差异较大; 毛细管电泳法则存在电渗会因样品组成而变化的问题, 进而影响分离重现性; 高效液相色谱法检出限高, 且色谱图杂质较多, 影响分析结果, 同时因为烷基胺类化合物极性较大, 在色谱分析的过程中, 难以保留, 导致色谱行为较差, 且分析时间长; 同样难以应用于气相色谱分析, 尽管可对目标物进行衍生, 但仍难以消除杂质对目标物的影响; 液相色谱-串联质谱法具有检出限低, 杂质影响小, 不需衍生即可测定的优点, 因此更适用于实际分析, 但同样存在色谱行为较差的情况, 对于分子量小的烷基胺, 仪器的响应低, 检出限高, 重复性较差。为实现对食品接触材料中的烷基胺进行准确测定, 本研究以氯甲酸苄酯为衍生剂, 对烷基胺进行酰胺化衍生, 增强了烷基胺的稳定性, 并提高了检测的灵敏度, 同时降低了分析物极性, 有效改善了色谱行为, 结合高分辨飞行时间质谱精确测定分子量, 相比直接测定的LC-MS/MS法具有更高的定性分析能力, 进一步降低假阳性, 建立了同时测定接触性食品塑料包装材料及塑料制品中的7种烷基胺类物质(结构式见图1)的HPLC-Q-TOF/MS法。
2 实验部分
2.1 仪器与试剂
Triple TOF®5600+高分辨质谱仪 (美国ABsciex公司); LC-20AD高效液相色谱仪 (日本岛津公司); Milli-Q超纯水仪(美国Millipore公司)。塑料包装材料(广州市售), 样品包括酸奶杯(PP), 矿泉水瓶(PET), 食品包装袋(PE)和一次性塑料杯(PC)。 无水Na2CO3、NaCl(分析纯, 广州试剂厂); 氯甲酸苄酯Cbz-Cl(≥ 96%, CNW Technologies GmbH); 乙腈(色谱纯, 美国Fisher公司);N,N-二乙基-1,3-丙二胺、 1,4-丁二胺、 1,6-己二胺、N,N'-二甲基-1,3-丙二胺、 2,2,4-三甲基-1,6-己二胺、 5-氨基-1,3,3-三甲基环己甲胺、 4,4'-亚基双环己胺标准品(≥ 98%, 德国CNW公司); 实验用水为经Milli-Q纯水系统制得的超纯水(电阻率为18.2 MΩ·cm)。
2.2 实验方法
2.2.1 标准溶液的配制分别准确称取7种烷基胺标准品各0.1000 g, 用乙腈溶解并定容至100 mL棕色具塞容量瓶中, 配制成1000 mg/L储备液。吸取上述7种标准的储备液, 用乙腈稀释并配制成10 mg/L混合标准工作溶液。分别准确移取混合标准工作溶液各0、5、10、25、50、100和250 μL至已加入5 mL 1.5% Na2CO3溶液的顶空进样瓶中, 补加0.4% Cbz-Cl-乙腈溶液至5 mL, 得到混标待测样品, 浓度分别为0、10.0、20.0、50.0、100、200和500 μg/L。
2.2.2 样品前处理用剪刀将样品剪成面积小于0.5 cm×0.5 cm的碎片, 混合均匀。准确称取1.00 g样品于顶空进样瓶中, 加入5 mL 1.5% Na2CO3溶液, 再加入5 mL 0.4% Cbz-Cl-乙腈溶液, 加盖, 于50℃水浴90 min, 取出后放冷, 加入1.5 g NaCl, 加盖, 摇匀10 s, 静置分层, 上清液用0.22 μm滤膜过滤, 待测。
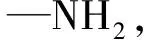
2.2.4 色谱及质谱条件X-Bridge C18色谱柱(100 mm×2.1 mm, 3.5 μm, Waters公司); 柱温: 40℃; 进样量: 2 μL; 流动相A为乙腈, B为0.1%甲酸, 采用梯度洗脱方式洗脱分离; 流速: 0.5 mL/min。梯度洗脱程序: 0.0~10 min, 5%~90% A; 10~13 min, 90% ~100% A; 13~16 min, 100% A; 16~17 min, 100%~5% A; 17~20 min, 5% A。
离子源: ESI和APCI复合源(ESI为化合物测定离子源, APCI为校准离子源); 正离子扫描方式; APCI源连接AB sciex公司自动校正系统(CDS), 每10个样品自动校正1次, APCI正离子校正液流速0.30 mL/min, 气帘气: 40 psi(1 psi=6.895 kPa), 离子源雾化气: 50 psi, 离子源加热辅助气: 50 psi, 离子源温度: 550℃, 离子源电压5500 V。一级TOF-MS扫描准确质量范围: 100~1000 Da, 数据采集时间100 ms, 去簇电压: 90 V, 碰撞能量: 10 V; 二级IDA-MS扫描准确质量范围: 50~1000 Da, 去簇电压: 90 V, 碰撞能量: (35±15) V; 高灵敏模式, 数据采集时间50 ms, 信号阈值100 cps, IDA实验每循环采集6次数据, 动态背景减法扣除。
2.2.5 数据分析方法所有质谱数据经AB Sciex公司的Analyst TF 1.6软件采集, 数据用PeakView 2.0, MasterView 2.0和MultiQuant 3.0等软件定性定量处理分析。根据TOF-MS和IDA-MS高分辨质谱获得7种烷基胺衍生物的准确分子量, 结合各级碎片参数进行定性和定量分析。
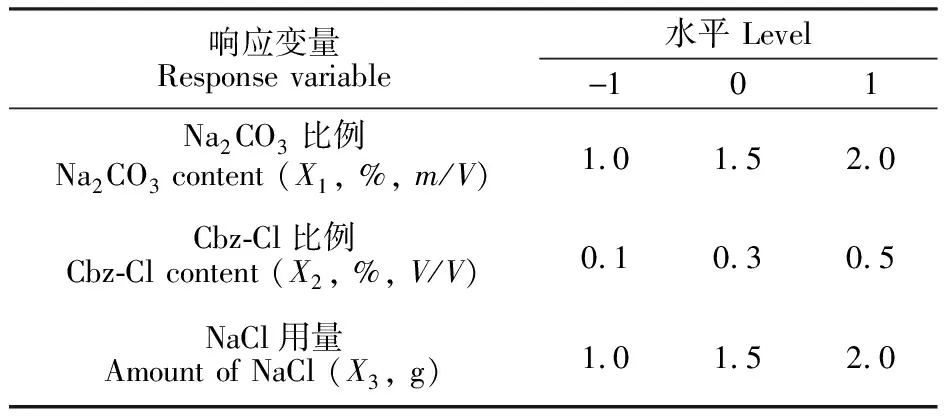
2.2.6 响应曲面设计前期研究发现, 前处理条件对7种烷基胺的衍生有影响, 因此, 基于优化后的衍生温度和时间, 采用响应曲面设计优化Na2CO3比例、Cbz-Cl比例和NaCl用量3个前处理衍生条件。采用Box Behnken设计模型设计衍生因素条件。该设计模型的理论是xi=Xi-X0=ΔX, 其中,xi为Xi独立变量值,X0为Xi独立变量的中心值, ΔX为变量截距值。三因素响应因素设计变量分别是Na2CO3比例(X1), Cbz-Cl比例(X2), NaCl用量(X3), 变量参数见表1。
表1 响应曲面设计因素水平表
Table 1 Factors and levels of response surface methodology
3 结果与讨论
3.1 色谱条件的选择及定性和定量分析依据
7种待分析的烷基胺衍生物均含有N原子, 因此更倾向于得到质子, 初步扫描后, 在ESI+模式下均得到[M+H]+的准分子离子峰, 因此,在流动相中加入甲酸可增加离子化效率。考察了乙腈-0.1%甲酸和甲醇-0.1%甲酸为流动相体系时烷基胺衍生物的色谱行为和离子化程度, 结果表明, 乙腈-0.1%甲酸为流动相时, 7种烷基胺衍生物的响应均高于甲醇-0.1%甲酸为流动相时的响应值, 且峰形更好, 故选择乙腈-0.1%甲酸作为流动相, 并优化了梯度洗脱程序, 7种烷基胺衍生物可在13 min内完成分析。
在一级质谱的模式下, 用保留时间和分子离子的精确质量数对待测的7种烷基胺衍生物进行初步定性分析。6个加标样品连续进样后, 7种烷基胺衍生物保留时间的相对标准偏差均小于0.2%; 实验测定的分子离子质量数与理论质量数的误差在-0.6×10-6~0.9×10-6之间(表2)。在IDA-MS模式下, 可获得待测物的二级质谱图, 通过特征性子离子精确质量数, 确定元素组成, 从而推测母离子裂解途径, 进一步增强了对待测物的确证能力。7种烷基胺衍生物的母离子提取离子流色谱图和裂解途径分别见图2和图3。
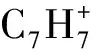
表2 7种烷基胺衍生物的母离子元素组成及精确质量
Table 2 Elemental composition and accurate mass measurement of seven alkylamine-derivatives
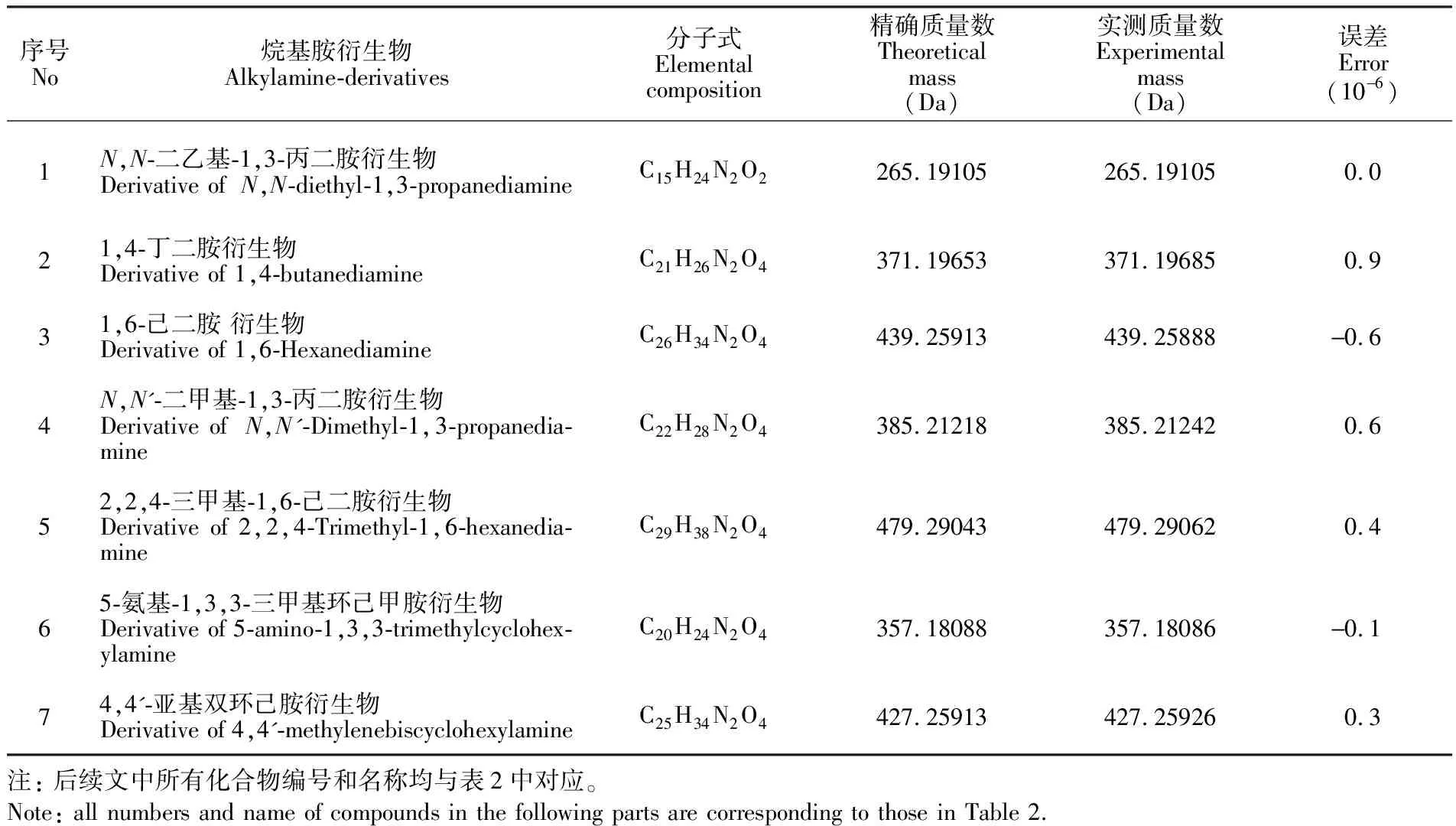
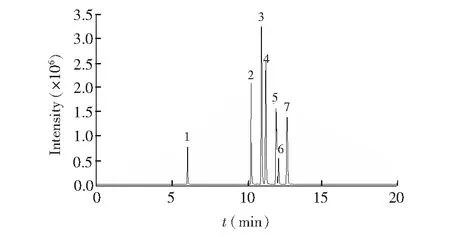
图2 7种烷基胺衍生物母离子的提取离子流色谱图。化合物编号和名称与表2中对应
Fig.2 Extracted ion chromatograms of parent ions of seven alkylamine-derivatives The numbers and name of compounds are corresponding to those in Table 2
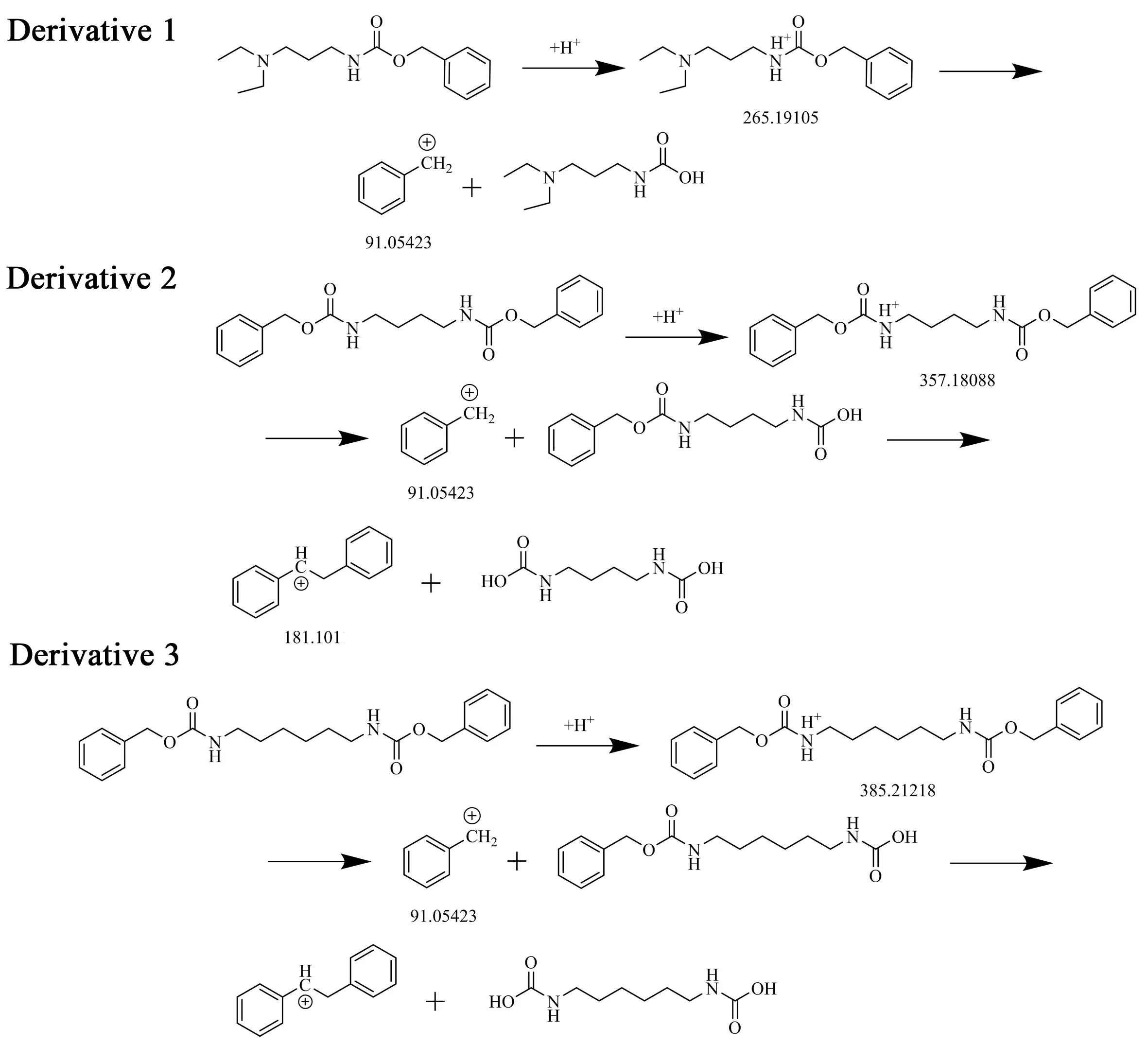
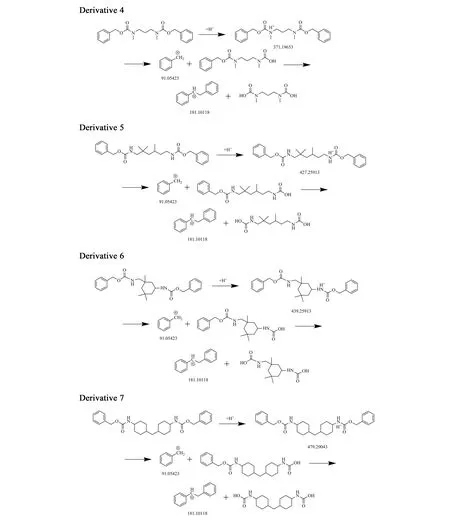
图3 7种衍生物母离子的二级质谱裂解图, 化合物编号和名称与表2中对应Fig.3 Cleavage pathway of parent ions of seven derivatives. The number and name of compounds are corresponding to those in Table 2
3.2 衍生条件的优化
由于7种烷基胺中有6种具有两个伯胺和仲胺, 因此衍生过程中会产生单胺衍生物和双胺衍生物两种。 而双胺衍生物较单胺衍生物分子量更大, 响应更高且极性也更低, 有助于在前处理中随乙腈层析出, 因此为准确测定, 需要优化衍生化反应条件使伯胺和仲胺得到充分衍生。考察了温度和时间对烷基胺衍生效率的影响, 结果表明, 50℃下衍生率最高, 随着温度升高, 衍生率下降(图4); 在衍生反应时间为90 min时, 7种衍生物的响应强度达到最高, 随着反应时间延长, 响应强度变化不明显(图5)。因此, 本研究选择在50℃下衍生反应90 min, 在此条件下, 烷基胺最终衍生产物的响应值与相应的浓度呈良好的线性关系。7种烷基胺各形态衍生物信号强度见图6, 双胺衍生物响应远高于单胺衍生物, 说明反应进行完全, 反应平衡系数较大。
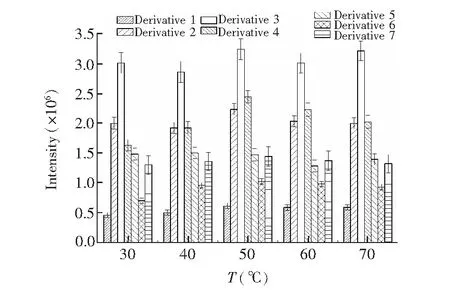
图4 衍生温度对响应强度的影响, 化合物编号和名称与表2中对应Fig.4 Effect of derivatization temperature on response (500 μg/L, 60 min). The number and name of compounds are corresponding to those in Table 2
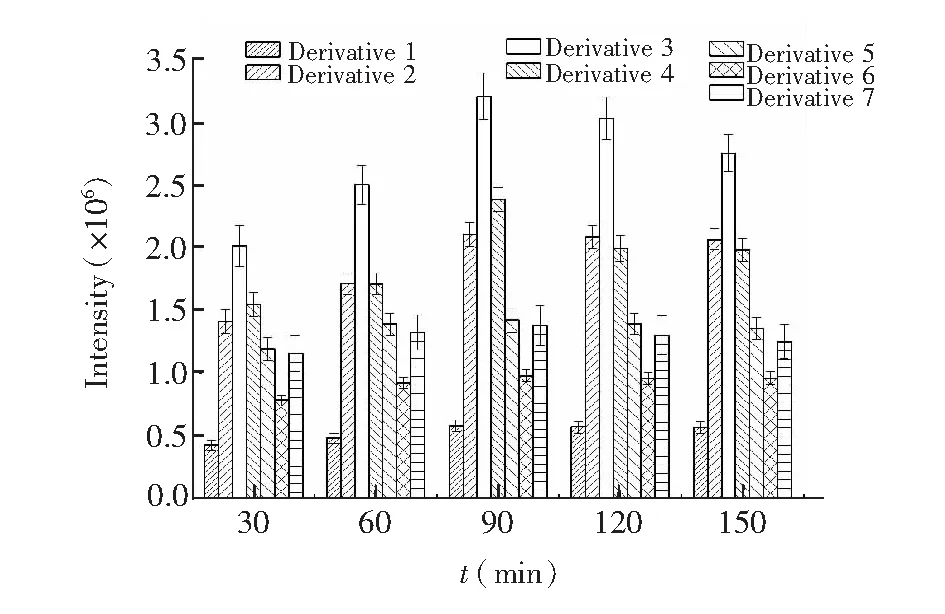
图5 衍生时间对响应强度的影响, 化合物编号和名称与表2中对应Fig.5 Effect of derivatization time on response(500 μg/L, 50℃). The number and name of compounds are corresponding to those in Table 2
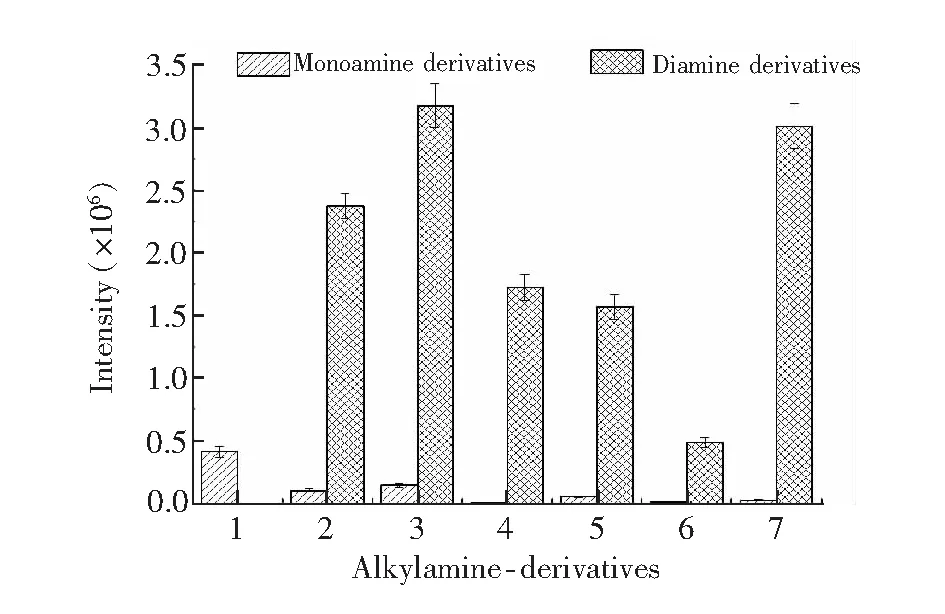
图6 7种烷基胺衍生物响应强度, 化合物编号和名称与表2中对应Fig.6 Response intensity of derivatives of seven alkylamine (500 μg/L). The number and name of compounds are corresponding to those in Table 2
3.3 响应曲面设计优化衍生条件
为了得到前处理方法对测定食品接触塑料材料中7种烷基胺的最佳衍生条件, 采用响应曲面设计优化Na2CO3比例(X1)、Cbz-Cl比例(X2)和NaCl用量(X3)等衍生条件。考察了衍生温度和时间对目标衍生物响应值的影响, 结果表明, 在50℃下衍生反应90 min目标衍生物响应值最高, 因此, 在此条件下进行响应曲面设计优化实验, 结果见表3。
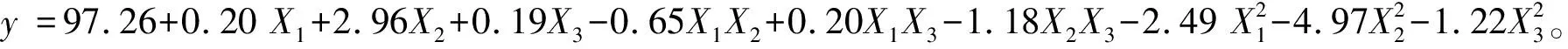
表3 响应曲面设计优化实验结果
Table 3 Results of response surface methodology optimization
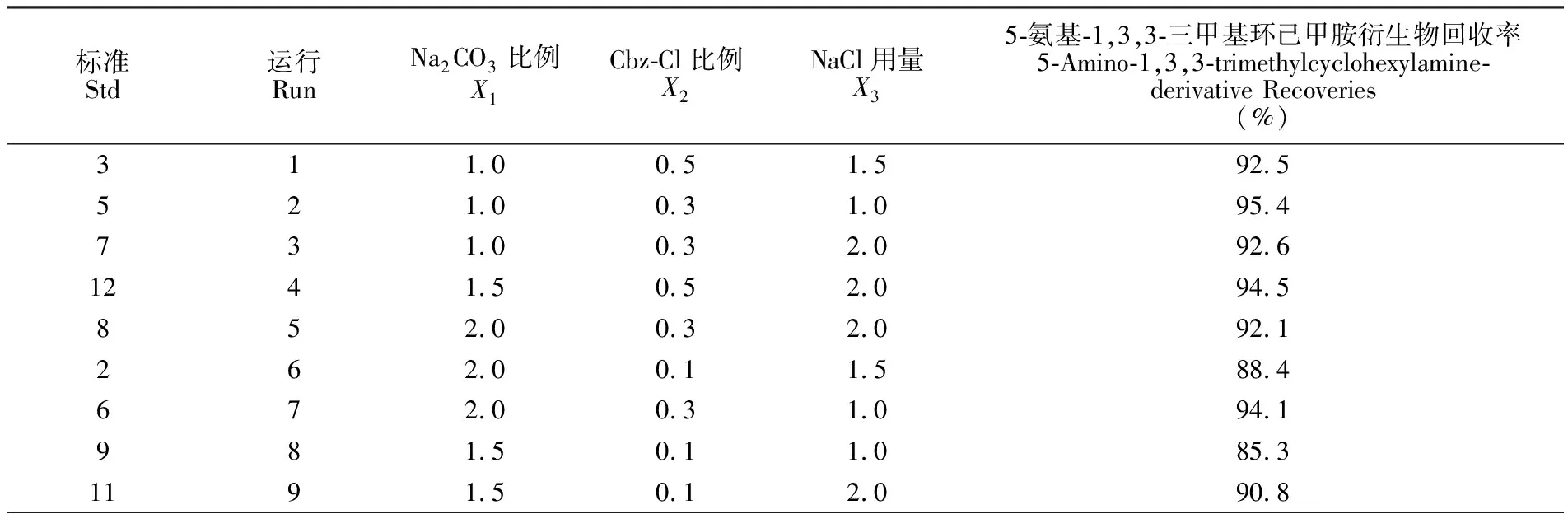
标准Std运行RunNa2CO3比例X1Cbz-Cl比例X2NaCl用量X35-氨基-1,3,3-三甲基环己甲胺衍生物回收率5-Amino-1,3,3-trimethylcyclohexylamine-derivative Recoveries(%)311.00.51.592.5521.00.31.095.4731.00.32.092.61241.50.52.094.5852.00.32.092.1262.00.11.588.4672.00.31.094.1981.50.11.085.31191.50.12.090.8
续表3(Continued to Table 3)
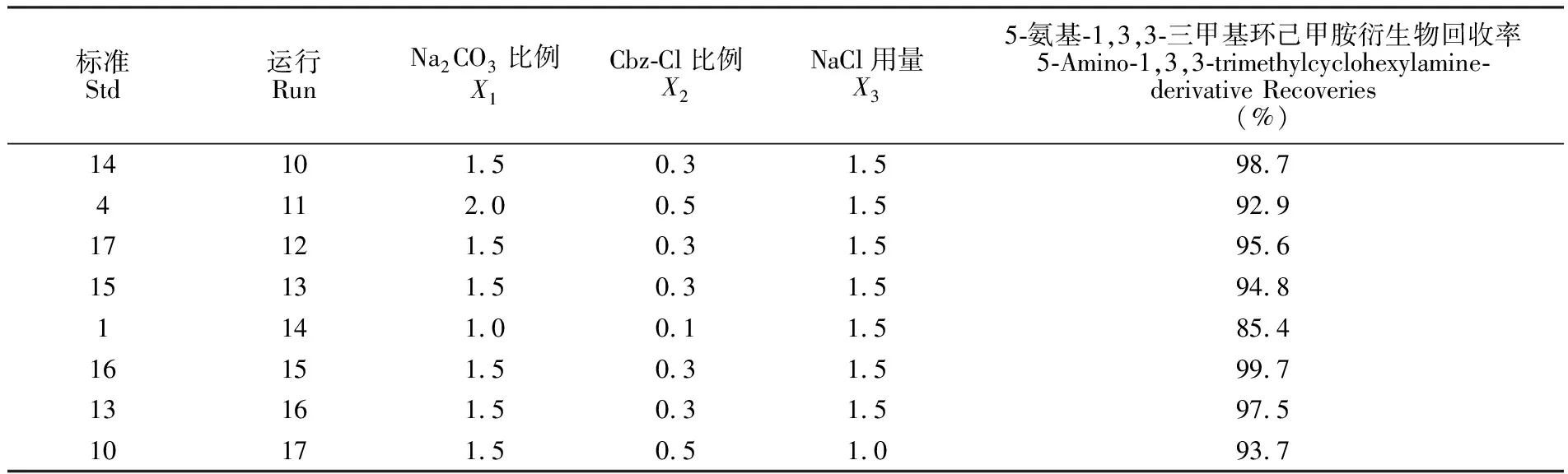
标准Std运行RunNa2CO3比例X1Cbz-Cl比例X2NaCl用量X35-氨基-1,3,3-三甲基环己甲胺衍生物回收率5-Amino-1,3,3-trimethylcyclohexylamine-derivative Recoveries(%)14101.50.31.598.74112.00.51.592.917121.50.31.595.615131.50.31.594.81141.00.11.585.416151.50.31.599.713161.50.31.597.510171.50.51.093.7
为进一步表示模型中三因素及三因素交互效应对烷基胺回收率的影响, 得到相应曲面设计的影响因素三维立体图(图7)。响应曲面设计模型根据实验所得5-氨基-1,3,3-三甲基环己甲胺的回收率, 进行模型建立与预测, 获得最佳的因素水平组合, 即Na2CO3比例为1.5%, Cbz-Cl比例为0.4%, NaCl用量为1.5 g。在此优化后的因素水平组合下, 可以获得最佳的烷基胺的平均回收率, 因此, 实际检测样品时, 均采用此因素水平组合和优化后的衍生温度和时间进行样品前处理。
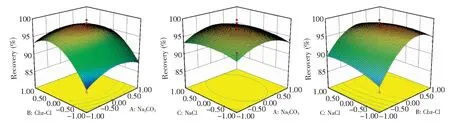
图7 响应曲面设计实验结果三维图Fig.7 3D plot of response surface methodology of different parameters on isophorondiamine recovery
3.4 基质效应
按照2.2.2节的前处理方法分别对实验空白(不添加样品)和7种烷基胺呈阴性的PET样品进行处理, 得到溶剂空白液和基质液。分别移取500 μg/L的衍生后标准溶液50 μL各两份, 其中一份加入950 μL的溶剂空白液, 另一份加入950 μL基质液, 摇匀后进行测定。以基质标准液和溶剂标准液的响应比值K为评判依据, K值范围在0.90~1.10之间, 则认为基质效应不明显。结果表明, 7种烷基胺衍生物的K值在0.95~1.01之间, 说明本方法基质效应不明显, 因此采用溶剂标准曲线进行定量分析。
3.5 分析方法线性方程、检出限与定量限
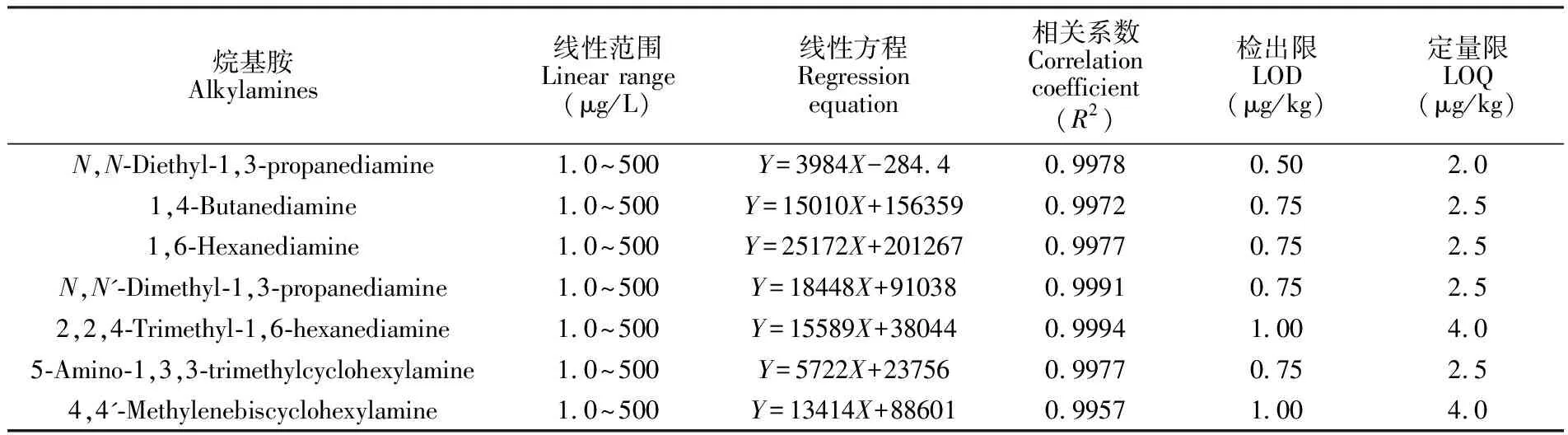
按照优化的前处理及色谱、质谱条件进行分析, 以峰面积Y对进样浓度X(μg/L)进行线性回归, 7种烷基胺衍生物的响应值与其浓度呈良好的线性关系, 相关系数均大于0.9957, 7种烷基胺的检出限(LOD,S/N=3)为0.5~1.0 μg/kg, 定量限(LOQ,S/N=10)为2.0~4.0 μg/kg, 表明本方法具有较高的灵敏度。目标分析物的线性方程、相关系数、检出限和定量限见表4。
3.6 回收率及精密度
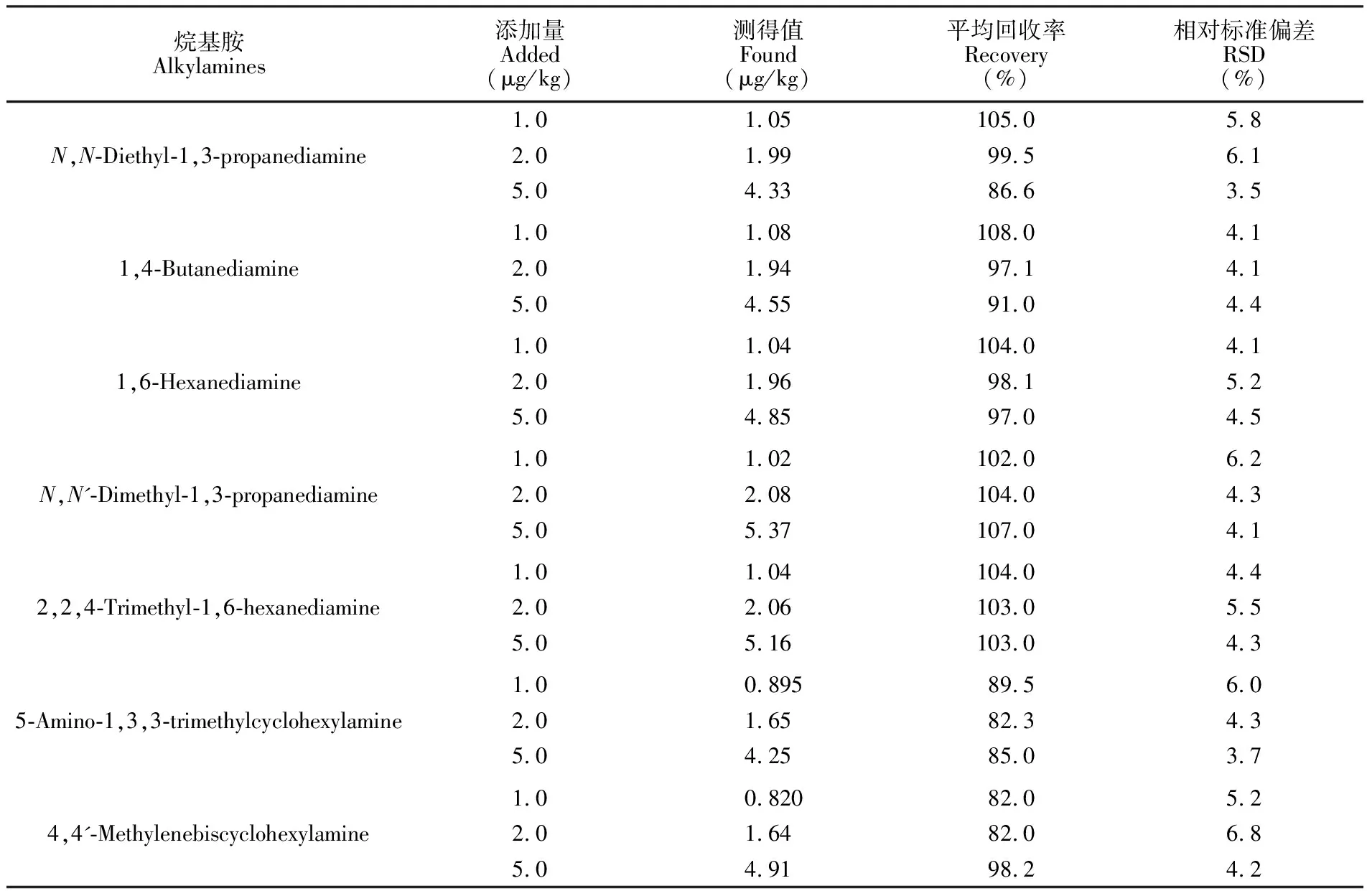
为进一步验证酰胺化衍生前处理方法对测定食品接触性塑料材料中烷基胺分析方法的可行性, 选择阴性样品, 进行3个浓度水平的加标回收实验。在1.00 g样品中分别加入10、20和50 μL浓度为100 μg/L的乙腈混合标准溶液, 得到浓度为1.0、2.0和5.0 μg/kg的加标样品, 对每个水平日内重复测定6次。由表5可知, 7种烷基胺的平均回收率为82.0%~108.0%, RSD为3.5%~6.8%, 表明本方法可满足7种烷基胺的分析测定要求。
表4 7种烷基胺的线性范围、线性方程、相关系数、检出限及定量限
Table 4 Linear ranges, linear regression equations, correlation coefficient, limit of detection (LOD) and limit of quantification (LOQ) of seven kinds of alkylamines
烷基胺Alkylamines线性范围Linear range(μg/L)线性方程Regressionequation相关系数Correlationcoefficient(R2)检出限LOD(μg/kg)定量限LOQ(μg/kg)N,N-Diethyl-1,3-propanediamine1.0~500Y=3984X-284.40.99780.502.01,4-Butanediamine1.0~500Y=15010X+1563590.99720.752.51,6-Hexanediamine1.0~500Y=25172X+2012670.99770.752.5N,N'-Dimethyl-1,3-propanediamine1.0~500Y=18448X+910380.99910.752.52,2,4-Trimethyl-1,6-hexanediamine1.0~500Y=15589X+380440.99941.004.05-Amino-1,3,3-trimethylcyclohexylamine1.0~500Y=5722X+237560.99770.752.54,4'-Methylenebiscyclohexylamine1.0~500Y=13414X+886010.99571.004.0
表5 食品接触性塑料材料中7种烷基胺的加标回收率(n=6)
Table 5 Recoveries of 7 kinds of alkylamines in food contact plastic materials (n=6)
烷基胺Alkylamines添加量Added(μg/kg)测得值Found(μg/kg)平均回收率Recovery(%)相对标准偏差RSD(%)N,N-Diethyl-1,3-propanediamine1,4-Butanediamine1,6-HexanediamineN,N'-Dimethyl-1,3-propanediamine2,2,4-Trimethyl-1,6-hexanediamine5-Amino-1,3,3-trimethylcyclohexylamine4,4'-Methylenebiscyclohexylamine1.01.05105.05.82.01.9999.56.15.04.3386.63.51.01.08108.04.12.01.9497.14.15.04.5591.04.41.01.04104.04.12.01.9698.15.25.04.8597.04.51.01.02102.06.22.02.08104.04.35.05.37107.04.11.01.04104.04.42.02.06103.05.55.05.16103.04.31.00.89589.56.02.01.6582.34.35.04.2585.03.71.00.82082.05.22.01.6482.06.85.04.9198.24.2
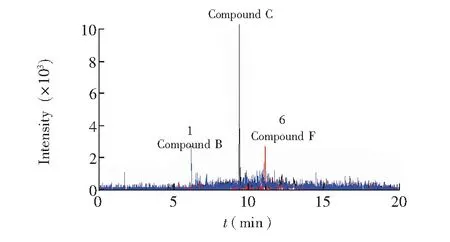
图8 阳性样品的提取离子色谱图Fig.8 Extracted ion chromatograms obtained for thepositive sample. The number and names are corresponding to those in Table 2
3.7 实际样品分析
采用本方法分析随机抽取的4种食品接触塑料材料, 包括酸奶杯(PP)、矿泉水瓶(PET)、食品包装袋(PE)和一次性塑料杯(PC)各10种。分析结果表明, 所有酸奶杯(PP)均检测到N,N-二乙基-1,3-丙二胺和1,4-丁二胺, 浓度范围分别为5.20~5.80 μg/kg和90.0~125 μg/kg, 而其中有一部分酸奶杯(PP)检出5-氨基-1,3,3-三甲基环己甲胺。N,N-二乙基-1,3-丙二胺和1,4-丁二胺也在水瓶(PET)中检出, 浓度为7.70~8.80 μg/kg和68.0~82.5 μg/kg。 阳性样品的提取离子色谱图见图8。
4 结 论
建立了HPLC-TOF/MS同时测定食品接触塑料材料中的7种烷基胺方法, 对烷基胺进行酰胺化柱前衍生, 增大了分析目标物的响应值; 结合响应曲面设计, 优化了烷基胺的酰胺化衍生条件。结果表明, 目标物在13 min内分离良好, 分析速度快; 利用高分辨质谱对目标物进行了定性与定量分析。本方法灵敏度高、重现性好、准确度高, 可为烷基胺类物质的毒理研究及评估食品接触塑料材料中烷基胺类物质危害提供灵敏且可靠的分析测定方法。

