三嗪含硫羧酸金属配合物的合成及性质表征*
倪 旭,李 静,张雪嫣,宋宝红,罗 琴,梁玲玲
(西安医学院药学院,陕西 西安 710021)
配位化学作为拥有蓬勃生命力的学科,得到了国内外科学家的关注和研究,其与物理化学、材料科学、生命科学等领域的交叉渗透,使配合物被广泛应用于工业生产、功能材料、生命科学等领域,并不断创新。金属配合物具有丰富多样的结构特性,在催化、磁性材料、杀虫剂、染料吸附、提取剂、药物释放等领域应用广泛[1-2],尤其是金属有机框架材料与药物研究方面具有巨大的潜在应用价值。近年来配位聚合物在各个领域的广泛应用和巨大潜力,使得配合物的研究蓬勃发展。多羧酸配体具有多个配位点和多样化的配位模式,与金属合成配合物的过程中会生成结构丰富、多种多样的配合物。柔性多羧酸配体本身存在可以自由旋转的柔性位点,与金属离子构筑时,具有多变的配位模式,从而产生各种性能优异的配合物结构,这种多样化的特点和独特的构效关系引起了国内外研究者的广泛关注[3]。
本文设计合成了一个含硫的柔性三脚架羧酸配体2,2′,2″-[1,3,5-三嗪-2,4,6-三(硫代)]三乙酸(H3TTTA),该配体结构灵活,配位点多,配位模式多样;含巯基的三脚羧酸配体中的硫原子本身呈现出柔软的特性,在自组装过程中能够形成更结构丰富的构型,而不同的构象可以在空间随意扭转以克服一些位阻效应,从而形成有趣的空间结构。配体与六种过渡金属硝酸盐(铜,铁,钴,镍,锰,锌)采用普通溶剂法反应,合成六种金属配合物,通过红外光谱、元素分析、热重分析等方法进行表征,并推测了配合物的结构。
1 实 验
1.1 仪器与试剂
仪器:氮气发生器,北京中惠普分析技术研究所;核磁共振波谱仪,德国布鲁克公司;STA 449C型热重分析仪,德国耐驰公司;Bruker TENSOR27红外光谱仪,德国布鲁克公司;Vario EL III CHNOS型元素分析仪,美国珀金埃尔默公司;显微熔点仪,上海佳航仪器仪表有限公司。
试剂:所有试剂均购于国药集团化学试剂有限公司,未进一步纯化直接使用。
1.2 2,2′,2″-[1,3,5-三嗪-2,4,6-三(硫代)]三乙酸的合成
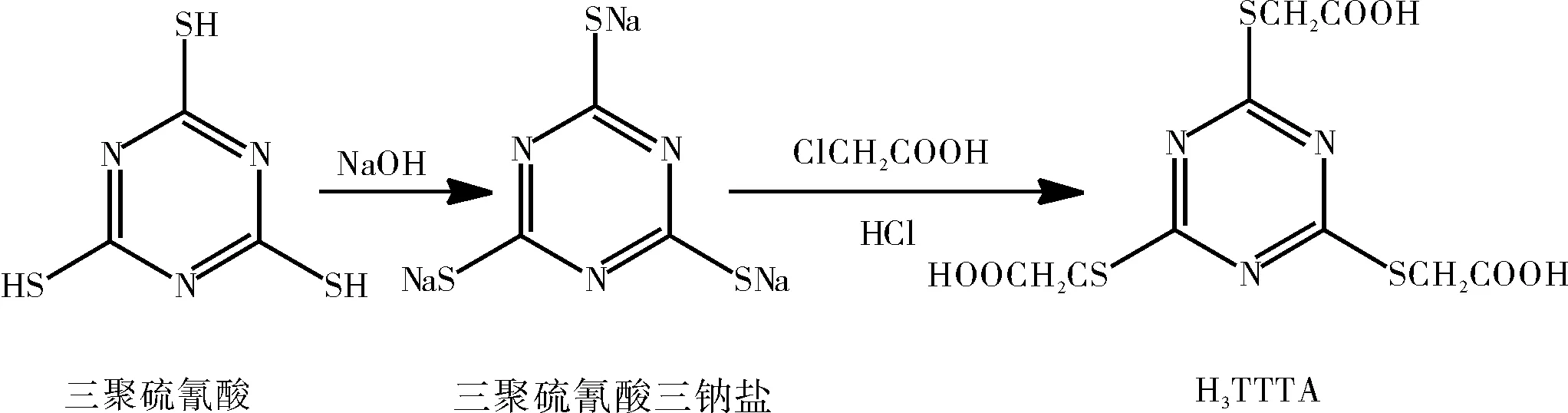
图1 配体的合成Fig.1 Synthesis of the ligand
参考文献的合成方法[4-5],称取1.2 g(0.03 mol)的氢氧化钠溶于10 mL蒸馏水中,在搅拌下滴加1.77 g(0.01 mol)的三聚硫氰酸水溶液,滴加完毕继续搅拌30 min,过滤除去杂质,用0.5%的氢氧化钠溶液调节pH约为11~12,得到淡黄色透明澄清溶液,即三聚硫氰酸三钠盐溶液。
准确称量3.85 g(0.03 mol)的氯乙酸溶于10 mL蒸馏水中,在氮气保护条件下,逐滴加入到上述三聚硫氰酸三钠盐溶液中,用0.5%的氢氧化钠溶液调节pH为10~11,室温下搅拌24 h。在溶液中加入盐酸,静置,有大量白色沉淀生成,抽滤,并用少量蒸馏水洗涤。真空干燥,得到白色固体粉末2.78 g,产率为79.20%,熔点为201.5~202.5 ℃。该有机物不溶于水、乙醇、氯仿、乙腈,易溶于甲醇、丙酮。
1.3 配合物的合成
配合物1[C9H6N3O6S3Cu3·5H2O]的合成:准确称取0.3513 g(0.001 mol)的H3TTTA,加水搅拌,滴加氢氧化钠使其恰好溶解。0.7248 g(0.003 mol)的三水合硝酸铜水溶液,加入到上述配体溶液中,常温搅拌4 h,过滤,真空干燥,得到0.24 g蓝色固体粉末,产率为38.15%。
配合物2[(C9H9N3O6S3)2Fe3·4H2O)]的合成:准确称取0.3513 g(0.001 mol)的H3TTTA,加水搅拌,滴加氢氧化钠使其恰好溶解。1.2120 g(0.003 mol)的九水合硝酸铁水溶液,加入到上述配体溶液中,常温搅拌4 h,过滤干燥,得到0.42 g棕色粉末,产率为44.85%。
配合物3(C9H6N3O6S3Co3·4H2O)的合成:准确称取0.3513 g(0.001 mol)的H3TTTA,加水搅拌,滴加氢氧化钠使其恰好溶解。0.8731 g(0.003 mol)的六水合硝酸钴水溶液,加入到上述配体溶液中,常温下搅拌6 h,待溶剂挥发后,取沉淀,干燥,得到0.21 g红色粉末,产率为31.77%。
配合物4(C9H6N3O6S3Ni3·2H2O)的合成:准确称取0.3513 g(0.001 mol)的H3TTTA,加水搅拌,滴加氢氧化钠使其恰好溶解。0.8724 g(0.003 mol)的六水合硝酸镍,用水溶解后,加入到配体溶液中,常温下搅拌4 h,待溶剂挥发后,取沉淀,干燥,得到0.28 g绿色粉末,产率为49.99%。
配合物5[(C9H9N3O6S3)2Mn3·3H2O]的合成:准确称取0.3513 g(0.001 mol)的H3TTTA,加水搅拌,滴加氢氧化钠使其恰好溶解。量取1.07 mL(0.003 mol)的50%的硝酸锰溶液,加入到配体溶液中,常温下搅拌6 h,过滤,取沉淀,干燥,得到0.34 g棕色粉末,产率为37.13%。
配合物6[(C9H9N3O6S3Zn3(H2O)3]的合成:准确称取0.3513 g(0.001 mol)的H3TTTA,加水搅拌,滴加氢氧化钠使其恰好溶解。准确称取0.8925 g(0.003 mol)的水合硝酸锌,用水溶解后,加入到配体溶液中,常温下搅拌4 h,过滤,取沉淀,干燥,得到0.29 g白色粉末,产率为48.44%。
2 结果与讨论
2.1 配体的H3TTTA的核磁共振氢谱
用氘代二甲基亚砜作溶剂溶解样品,由核磁共振氢谱图上氢信号的位移值可推测得,化学位移值13.02处为配体上羧基(-COOH)上的氢信号,化学位移值4.07处为配体上亚甲基(-CH2-)上的氢信号,化学位移值2.51为DMSO的溶剂峰,样品中两组氢信号积分面积之比为1:2,据此推测其氢核数目之比为1:2,符合配体2,2′,2″-[1,3,5-三嗪-2,4,6-三(硫代)]三乙酸两组氢信号数目之比。

图2 H3TTTA的核磁共振氢谱图Fig.2 1H NMR of H3TTTA
2.2 配合物的元素分析
配合物1的实验值(%):C,17.02;N,6.151;H,2.783。理论值C,17.18;N,6.68;H,2.56。
配合物2的实验值(%):C,22.96;N,8.928;H,2.515。理论值C,23.09;N,8.648;H,2.15。
配合物3的实验值(%):C,18.39;N,7.31;H,2.527。理论值C,18.10;N,7.04;H,2.36。
配合物4的实验值(%):C,19.90;N,6.009;H,2.028。理论值C,19.29;N,7.50;H,1.80。
配合物5的实验值(%):C,22.51;N,8.626;H,2.153。理论值C,23.61;N,9.18;H,1.98。
配合物6的实验值(%):C,17.59;N,6.463;H,2.061。理论值C,18.06;N,7.02;H,2.02。
2.3 配合物的红外光谱

图3 配体和配合物1~6的红外光谱图Fig.3 IR spectra of the ligand and the complexes 1~6
配合物1~6的红外光谱如图3所示。由于配体与金属离子发生了配位反应,羧基发生去质子化[6],配合物的υ-COO的对称和不对称伸缩振动峰位移出现在1493 cm-1和1385 cm-1(配合物1);1483 cm-1和1396 cm-1(配合物2);1593 cm-1和1384 cm-1(配合物3);1485 cm-1和1385 cm-1(配合物4);1615 cm-1和1420 cm-1(配合物5);1487 cm-1和1386 cm-1(配合物6)。羧基的去质子化说明配体完成了与金属离子的配位反应。配合物1~6在3400 cm-1处的水峰对应于配合物中的游离水。
2.4 配合物的热重分析
氮气气氛下,以10 ℃/min的升温速率将样品从室温加热至800 ℃,对配合物1~6进行热分析(图4)。
从配合物1的失重曲线,可以看出配合物1分两步失重,第一步失重发生在室温到177 ℃,可以归属为失去5分子H2O,失重13.75%(理论值为14.31%);在177 ℃配合物骨架发生崩塌,直至800 ℃分解完全,剩余残渣质量为39.74%,理论值为37.93%。
从配合物2的失重曲线可以看出,配合物2在室温到150 ℃时发生第一次失重,失重9.42%(理论值为7.69%),这归属于配合物中失去4分子H2O;在150~210 ℃时保持稳定,从210 ℃开始,配合物继续分解,直至800 ℃时,剩余残渣质量为28.27%,其理论值为25.63%。
配合物3的失重曲线可以看出,配合物3第一次失重发生在室温到185 ℃,失重20.59%,对应于配合物中4分子H2O和样品中游离水的失去。从185 ℃开始,配合物结构开始坍塌,直至800 ℃分解完全,剩余残渣质量为28.93%。

图4 配合物1~6的热重分析图Fig.4 TG of the complexes 1~6
配合物4的失重曲线分析看出,配合物4在80~120 ℃时发生第一次失重,失重20.16%,对应于配合物中2分子H2O和样品中游离水的失去。在120~280 ℃时保持稳定,从280 ℃开始,配合物开始分解,至800 ℃分解完全,剩余残渣质量为23.27%。
配合物5的失重曲线表明,配合物5第一次失重发生在室温到180 ℃,可以归属为失去了3分子H2O,失重5.41%(理论值为5.89%),第二阶段是配合物在180~305 ℃保持稳定,第三阶段则是在大于305 ℃时,配合物骨架发生坍塌,直至800 ℃分解完全,剩余残渣质量为35.05%。
配合物6的失重曲线表明,配合物在180 ℃之前保持稳定,200 ℃时发生第一次失重,失重7.15%,归因于配合物失去配位水。在200~320 ℃时保持稳定,从320 ℃开始,继续分解,直至800 ℃分解完全,剩余残渣质量为43.98%,推测为ZnO,其理论值为42.79%。
3 结 论
本文合成了具有三个羧基的柔性羧酸配体2,2′,2″-[1,3,5-三嗪-2,4,6-三(硫代)]三乙酸(H3TTTA),通过普通溶剂法合成六种过渡金属配合物,结果发现常温常压下采用溶剂法合成金属配合物,其操作简便,耗时较短,但是产率极低,杂质较多。通过紫外、红外、元素分析,热重分析、核磁共振氢谱等对配体和配合物进行表征,并推测了配合物的结构。

