蜡油加氢脱硫集总动力学模型研究
朱永红,霍鹏举,杨天华,李伟,韩磊,杨程
(1陕西延长石油有限责任公司碳氢高效利用技术研究中心,陕西西安710065;2西北大学化工学院,陕西西安710069)
减压蜡油(VGO)作为催化加氢裂化的一种原料主要用来生产清洁燃料油[1-2]。若VGO 直接作为催化裂化原料,一方面VGO 中硫、氮、金属组分等杂质以及稠环芳烃含量高,容易造成催化剂中毒失活,进而影响目标产品收率、分布和质量等[3-7];另一方面,随着国家第六阶段机动车污染物排放标准以及国际海事组织(IMO)对全球所有船舶燃料油环保政策等的实行,国内外市场对燃料油的洁净品质要求更高,这也对VGO 加氢处理提出了更高的要求。对VGO 进行加氢预处理脱除硫、氮等杂质,可明显改善后续工艺的原料性质,获得高品质、环境友好型清洁油品[8]。
VGO 加氢反应动力学模拟研究不仅促进对其反应机理的认识,也为工艺流程的设计、优化以及工业化装置操作提供参考。近年来,众多研究学者[1-2,9-17]对加氢脱硫(HDS)反应动力学进行了研究,其中,HDS 动力学的研究主要以模型化合物为主[9-13],也有少部分学者对渣油、页岩油、煤焦油以及VGO HDS动力学等进行了研究[1-2,14-17]。
由于VGO 中硫化物种类繁多,各种硫化物结构复杂,HDS 反应性能差别大,因此其动力学研究比模型化合物研究更为复杂[1]。鉴于应用现有分析手段较难检测到油品中硫化物种类和含量,因此很难用复杂的反应网络来描述VGO HDS 反应,从而建立动力学模型[2]。集总模型通过将动力学性质相似的组分用一个虚拟集总组分代替,然后构造这些集总组分的反应网络,再通过建立相应反应动力学模型,结合实验数据与计算机方法估算得到动力学参数。研究表明,采用集总动力学理论对渣油、柴油以及页岩油HDS 建立动力学模型,适应范围广,外推性强,模型拟合度高[14-15,18]。
因此,本文以VGO 为原料,通过将VGO 中硫化物划分为若干集总,建立了HDS 集总动力学模型,并对该动力学模型进行了计算和应用,旨在为VGO HDS 试验和工业装置操作条件优化等提供一定的理论依据和参考。
1 实验部分
1.1 实验原料
原料为山东省某炼厂VGO,其基本物化性质见表1。
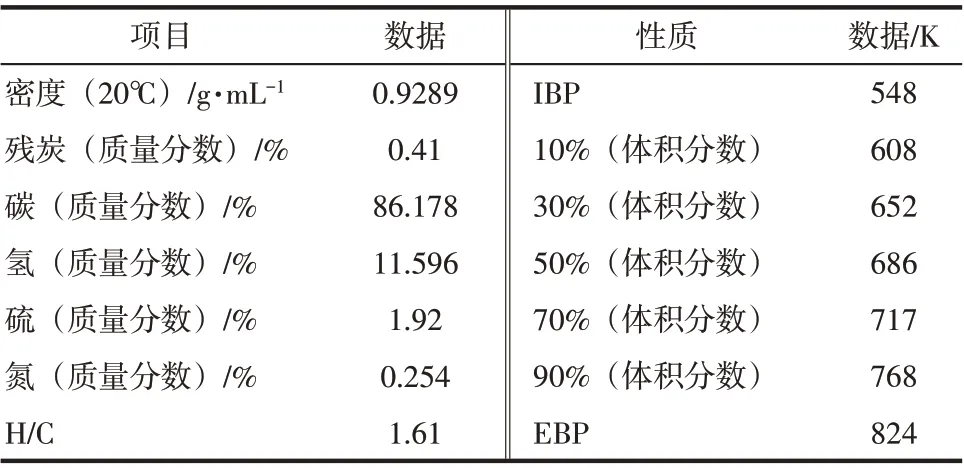
表1 原料基本性质
1.2 实验装置与工艺流程

图1 实验装置工艺流程
实验在30mL 单管固定床装置中进行。内层炉瓦三段,第一段为预热段,第二段为反应段,第三段为保温段。加氢装置由气体进料部分、液体进料部分、反应部分、产物收集部分组成,实验装置工艺流程图如图1所示:原料罐内的VGO用氮气压至柱塞泵,由泵抽送后与氢气充分混合进入反应器。在反应器内预热后,反应物料在设定的工艺条件下经过反应器催化剂床层进行反应。反应产物进入产物收集系统后首先进入热高压分离器,分离出的液相产物进入热低压分离器,分离出的气相产物进入冷高压分离器,冷高压分离器底部分离后的液相进入冷低压分离器,顶部分离出的气体进入碱洗罐后经湿式气表计量后放空或进行取样分析。
1.3 催化剂
实验使用自制CoMoP/Al2O3加氢催化剂,具体理化性质见表2。
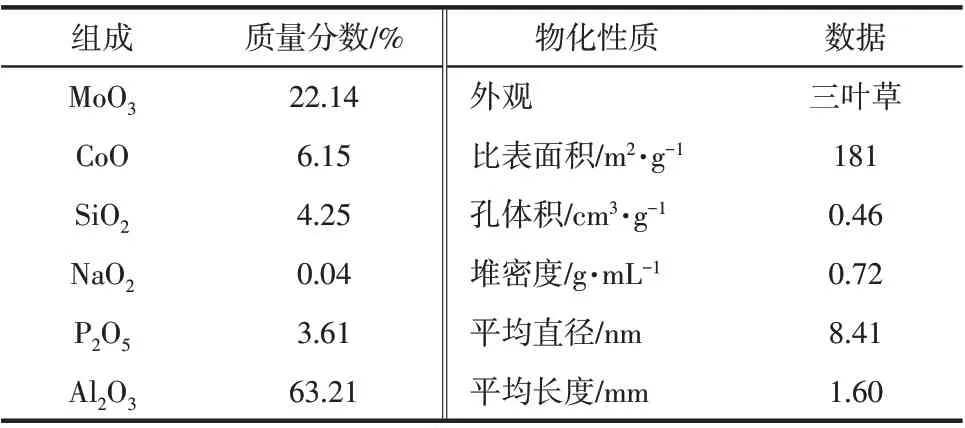
表2 催化剂理化性质
1.4 分析方法及仪器
采用硫氮分析仪(KY-3000SN 型,江苏科苑有限公司)按照GB/T387—90《深色石油产品硫含量测定法》分别测定VGO 原料油和液体产品中总硫含量。
1.5 VGO加氢脱硫实验
本次VGO HDS 实验采用反应器内湿法预硫化技术对装填的加氢精制催化剂进行预硫化处理,硫化油为直馏柴油复配二甲二硫醚(质量分数为2%),硫化工艺条件为:压力8MPa,氢油体积比600∶1,温度230℃保持4h,260℃保持6h,345℃保持6h,升温速率均为5℃/h。硫化结束后,待床温降到320℃后,硫化油切换为原料油,维持6h,钝化程序结束后,升温至第一个工况温度点,每个工况点取两次6h 平行样。在较宽反应压力区间2.0~6.0MPa,反应温度区间653~663K,反应液时空速1.0~2.0h-1,氢油体积比500 条件下,进行了VGO HDS精制反应。
2 HDS集总动力学模型建立
2.1 模型假设和反应网络建立
考虑到VGO 原料组成的复杂性和HDS 反应机理,对VGO HDS 集总动力学模型作出以下简化和假设[14-19]:
①固定床反应器为理想平推流反应器;
②VGO HDS反应体系为拟一级均相反应体系;
③每个硫化物集总之间不发生相互转化反应,硫化物直接加氢脱硫生成硫化氢;
④压力对HDS 反应的影响采用幂指数形式修正;
⑤温度对HDS反应的影响符合Arrhenius方程;
⑥忽略催化剂失活影响。
硫化物在VGO 中以不同形态存在,每种形态硫化物的加氢脱除难度不同。根据李术元等[15,18-19]对渣油、页岩油、柴油HDS 反应集总动力学的研究方法和上述假设,将VGO 中硫化物按其加氢反应速率的快慢划分为3个集总,即快反应速率集总F、中反应速率集总M 和慢反应速率集总S。基于以上硫化物集总划分,建立三集总HDS反应模型,图2为VGO HDS三集总反应网络。
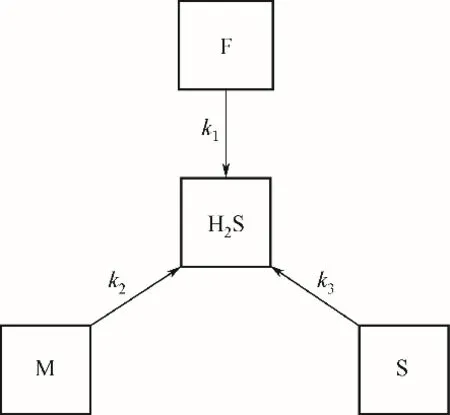
图2 VGO HDS三集总反应网络
2.2 集总动力学方程
VGO HDS 反应效果主要影响因素是反应温度T、反应压力P、液时空速LHSV 以及氢油体积比V(H2)/V(Oil)影响。根据上述假设和VGO HDS 反应网络,各集总硫化物的HDS 动力学方程可由式(1)表示。

式(1)积分得式(2)。

式(2)中
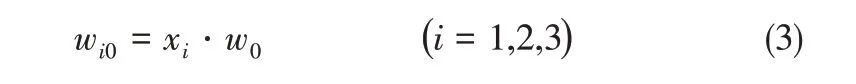
其中

用Arrhenius 方程表示表观反应速率常数ki,见式(5)。

引入修正因子ai对P采用幂指数形式表示,则有式(6)。

考虑到在实际反应器中物料流动并非理想的平推流形式,引入修正因子bi对反应时间t进行修正,即式(7)。

得到VGO HDS反应动力学模型方程见式(8)。

3 结果与讨论
3.1 动力学方程参数求解
由式(8)可知,动力学方程中每个集总有xi、ki0、Ei、ai、bi五个未知参数,T、P和LHSV为自变量,wS为因变量。因此,需要测定VGO 原料总硫含量和不同T、P 和LHSV 条件下HDS 反应产物的总硫含量。采用Levenberg-Marguardt 算法求解VGO HDS 集总动力学模型参数,其目标函数如式(9)所示。当SSE达到最小值,计算程序终止,输出结果。
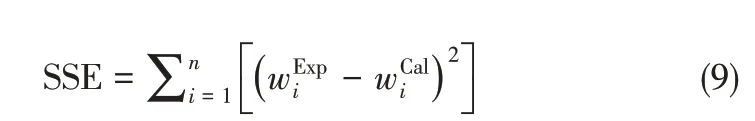
3.2 HDS集总动力学模型参数计算和验证
选择T(653~663K)、P(2~6MPa)、LHSV(1~2h-1)以及氢油体积比500 进行VGO 加氢反应,并测定产物油中的硫含量,表3为加氢过程各实验点工艺条件和产物中硫含量结果。
利用上述算法,对表3实验数据进行拟合,得到集总动力学方程参数,列于表4。
加氢反应后,产物中硫含量的实验值与模型计算值比较见图3。模型拟合平均相对误差-Er由式(10)进行计算。从图3 可以看出,产物中硫含量的实验值和计算值非常接近,其平均相对误差只有5.18%。这说明该集总动力学模型是可靠合理的,可以很好预测和描述VGO 加氢过程中硫化物的脱除情况[14-15]。

表3 VGO加氢过程各实验点工艺条件和产物中硫含量结果

表4 VGO HDS集总动力学模型参数

图3 产物中硫含量的实验值与模型计算值比较

为进一步验证该集总动力学模型的外推可靠性,在T=663K、P=4MPa、LHSV=1.5h-1以及氢油体积比500 的条件下,运用表4 中动力学参数计算VGO 加氢后产物硫含量,并与实验值进行对比。结果表明,实验值(wExpS=1865μg/g) 与计算值(wCalS=1926μg/g)相对误差仅为3.27%,模型预测效果较好,具有良好的外推性。
3.3 HDS集总动力学模型参数分析
VGO 中的硫主要以硫醚、噻吩、苯并噻吩、二苯并噻吩以及少量其他稠环噻吩类硫化物存在[15]。其中,硫醚和大部分噻吩硫在加氢条件下较容易脱除,苯并噻吩和部分二苯并噻吩加氢脱除难易程度居中,而部分二苯并噻吩和其他稠环噻吩类硫化物很难脱除[20-21]。由表4 中集总动力学模型参数可知,VGO HDS快反应速率集总(F)的质量分数为68.68%,其硫化物Ei约为73.66kJ/mol,因此推断该集总硫化物包括硫醚和大部分噻吩硫。VGO HDS 中反应速率集总(M)的质量分数为22.71%,其硫化物Ei约为144.08kJ/mol,因此推断该集总硫化物包括苯并噻吩和部分二苯并噻吩。VGO HDS 慢反应速率集总(S) 的质量分数为8.61%,其硫化物Ei约为184.73kJ/mol,因此推断该集总硫化物包括部分二苯并噻吩和其他稠环噻吩类硫化物。
随着不同硫化物集总(F→M→S)HDS难度增加,ai也相应增大,其中(F)和(M)集总ai值接近,(S)集总ai较大。这说明反应压力对脱除活性低的硫化物HDS 影响比较大,对脱除活性相对较高的硫化物HDS 影响小。这与油品实际加氢精制反应规律相符[14]。bi随着硫化物集总HDS 难度增加而增加,其中(F)集总bi较小,(M)和(S)集总bi值较大。这说明硫化物脱除理论反应时间和实际反应时间有一定偏差,对于较易脱除的(F)集总硫化物,存在HDS 反应时间的负向补偿,对于较易脱除的(M)和(S)集总硫化物,存在HDS反应时间的正向补偿。
3.4 HDS集总动力学模型应用
为得到不同反应条件对加氢过程的影响规律,由该集总动力学模型预测了在不同T、P 和LHSV工况下,VGO HDS 过程中硫化物转化规律。定义VGO HDS反应脱硫率yHDS按式(11)进行计算。

式 中,yFHDS、yMHDS、ySHDS和yTHDS分 别 为 产 物 中(F)、(M)、(S)集总以及总硫的脱硫率,T=F+M+S。
3.4.1 液时空速对VGO HDS反应的影响
图4 为在T=658K、P=6MPa、V(H2)/V(Oil)=500条件下,VGO HDS 产物中总硫(T)含量以及(F)、(M)、(S)集总硫含量随LHSV的变化曲线。

图4 VGO HDS集总动力学模型预测的产物中不同集总硫含量随LHSV的变化规律
由图4可知,在设定工艺条件下,产物中总硫(T)含量随着LHSV的增大而增大,yTHDS随着LHSV的增大而减小的趋势明显,即降低LHSV 有利于VGO HDS 反应进行。(F)集总硫化物脱除速率非常快,在LHSV 为0.5~2.5h-1范围内,其硫化物基本已全部脱除,硫含量均小于111μg/g,yFHDS达到了98.5%以上。这说明LHSV 对(F)集总HDS 反应影响很小。(M)集总硫化物脱除速率稍小于(F)集总。以LHSV=1h-1为分界点,当LHSV>1h-1时,随着LHSV 增大(1h-1→2.5h-1),(M)集总硫含量迅速增加(50μg/g→1411μg/g),yMHDS快速减小(98.8%→67.6%);当LHSV 在0.5~1h-1时,(M)集总硫化物已基本全部脱除,yMHDS稳定在99%以上。(S)集总HDS反应速率非常慢,随着LHSV由1.0h-1降为0.5h-1,硫含量逐渐降低(1415μg/g→968μg/g),但yMHDS最大也仅为41.1%。当LHSV 在1~2.5h-1范围时,(S)集总硫含量始终稳定在1415~1600μg/g,ySHDS小于11.7%,脱除效果整体比较差。
因此,(M)和(S)集总硫化物需要相对更长的反应时间才能达到理想的HDS 效果,而反应时间对(F)集总硫化物的HDS转化影响很小。综上所述,VGO HDS 的最佳LHSV 应该为0.5h-1。但考虑到实际工业加氢精制装置产能尽可能高的要求,其实际LHSV 往往会更高一些。因此,LHSV 为0.5~1h-1应该为VGO HDS 优选工艺区间,根据实际需要,可适当调整反应条件苛刻度,使LHSV接近1.0h-1。
3.4.2 反应温度对VGO HDS反应的影响
图5 为在P=6MPa、V(H2)/V(Oil)=500 条件下,VGO HDS 产物中总硫(T)含量以及(F)、(M)、(S)集总硫含量在不同反应温度(T)下随LHSV的变化曲线。

图5 VGO HDS集总动力学模型预测的产物中不同集总硫含量在不同反应温度下随LHSV的变化规律

由图5 还可发现,随着LHSV 增加(0.5h-1→2.5h-1),T 对产物中(M)集总硫含量的影响程度显著增加,对产物中(F)集总硫含量的影响程度变化不大,对产物中(S)集总硫含量的影响程度逐渐减小。这是因为当LHSV>1h-1时,(M)集总硫化物脱除率随LHSV增加迅速降低(图4),通过提高T,可以增加(M)集总硫化物在高LHSV 下的HDS 速率,进而提高脱除率;LHSV 在0.5~2.5h-1范围内,非常高,(F)集总硫化物基本都被脱除,所以T 变化对(F)集总硫含量影响不大;而(S)集总硫化物由于本身HDS 活化能高,在较低LHSV下,T对影响较大;在较高LHSV下,反应时间对(S)集总硫化物HDS反应已有较大的抑制作用,因此温度对影响程度逐渐减小。
3.4.3 反应压力对VGO HDS反应的影响
图6 为在T=658K、V(H2)/V(Oil)=500 条件 下,VGO HDS 产物中总硫(T)含量以及(F)、(M)、(S)集总硫含量在不同P下随LHSV的变化曲线。

图6 VGO HDS集总动力学模型预测的产物中不同集总硫含量在不同P下随LHSV的变化规律
由图6 可知,在相同LHSV 下,随着P 增大(2MPa→6MPa),产物中总硫(T)含量及(F)、(M)、(S)集总硫含量均明显降低,和相应增加。P在6MPa→2MPa区间内,相同压降ΔP 对产物中(F)、(M)、(S)集总硫含量以及总硫含量(T)的增加幅度ΔSF、ΔSM、ΔSS及ΔST越来越大。其中,当P 在递增区间2MPa→3MPa 变化时,对ΔSF、ΔSM、ΔSS及ΔST影响幅度最大。经计算,随着LHSV增加(0.5h-1→2.5h-1),当P由2MPa提高为6MPa时,(F)集总的脱硫率增量小 幅 增 加0.97% (0.5h-1) →1.23%(1.0h-1)→1.40%(1.5h-1)→1.53%(2.0h-1)→1.63%(2.5h-1)];(M)集总的脱硫率增量ΔyMHDS也大幅增加0.004%(0.5h-1)→1.63%(1.0h-1)→5.42%(1.5h-1)→7.54%(2.0h-1)→8.07%(2.5h-1)],(S)集总的 脱 硫 率 增 量则 大 幅 减 小12.28%(0.5h-1)→4.85%(1.0h-1)→2.51%(1.5h-1)→1.54%(2.0h-1) →1.04% (2.5h-1)]。这 说 明 在 高LHSV下,P 对较高脱除活性硫化物(F)集总、(M)集总的HDS反应影响较大,高压更加有利于高LHSV下较高脱除活性硫化物脱除,对低脱除活性硫化物(S)集总的影响弱一点;反之,在低LHSV 下,P对低脱除活性硫化物(S)集总HDS 反应影响较大,在低LHSV区间,低脱除活性硫化物HDS性能对P更加敏感。
由图6 还可发现,随着LHSV 增加(0.5h-1→2.5h-1),P 对产物中(M)集总硫含量的影响程度显著增加,对产物中(S)集总硫含量的影响逐渐减小。这是因为当LHSV>1h-1时,(M)集总硫化物脱除率随LHSV增加迅速降低(图5),通过提高P,可以一定程度上增加(M)集总硫化物在高LHSV下的HDS速率,进而提高其脱除率;而(S)集总硫化物由于本身HDS 活化能高,整体HDS 反应速率低,在较低的LHSV 下,P 对具有一定的促进作用;但在较高LHSV下,反应时间对(S)集总硫化物HDS 反应已有较大的抑制作用,因此P 对影响程度逐渐减小。随着LHSV 增加(0.5h-1→2.5h-1),当P 在6~4MPa 范围内时,其对(F)集总硫含量影响很小,当P由4MPa降到2MPa时,(F)集总硫含量相对快速增加。这说明过低的反应压力对高脱除活性硫化物HDS 反应具有一定程度的抑制作用。
图7 为 在LHSV=1.5h-1、V(H2)/V(Oil)=500 条 件下,VGO HDS产物中总硫(T)含量在不同的P下随T 的变化曲线。由图7 可知,在不同T 下,随着P减小(6MPa→2MPa),产物中总硫(T)含量明显增加,yTHDS相应减小;P 在递增区间(2MPa→3MPa)变化时,对ΔST影响幅度最大,这与前述转化规律相符。经计算,随着T 增加(653K→663K),当P 由2MPa 提高为6MPa 时,产物整体的脱 硫 率 增 量ΔyTHDS匀 速 小 幅 递 减,[ΔyTHDS:2.96%(653K)→2.74%(655K)→2.52%(657K)→2.30%(659K)→2.09%(661K)→1.89%(663K)]。这说明在一定LHSV下,相对于高温区,当处于低温区时P 对VGO HDS 反应影响更大一些,但影响幅度较小。
4 结论
(1)建立了VGO HDS 三集总动力学模型。该模型平均相对误差仅为5.18%,对产物硫含量预测准确,经过验证,其外推性良好,说明根据硫化物反应速率快慢进行集总划分所建立的HDS 集总动力学模型是可靠的。
(2)集总动力学模型参数表明,该VGO 中高脱除活性、中脱除活性、低脱除活性硫化物分别占到68.68%、22.71%、8.61%,反应速率依次降低。各集总硫化物活化能分别为73.66kJ/mol、144.08 kJ/mol、 184.73kJ/mol, 压 力 修 正 因 子 分 别 为0.1899、0.2000、0.4000,时间修正因子分别为0.1000、1.4999、1.7811。模型计算结果与加氢反应规律相符。
(3)得到了详细的VGO HDS反应规律:①中、慢反应速率集总硫化物需要更长反应时间才能达到理想的HDS 效果,而反应时间对快反应速率集总硫化物HDS 转化影响很小;②在高空速下,温度对较高脱除活性硫化物HDS 反应影响较大,高温有利于高空速下较高脱除活性硫化物脱除;在低空速下,温度对低脱除活性硫化物HDS 反应影响较大,在低空速区间,低脱除活性硫化物HDS 性能对温度更加敏感;③随着空速增加,温度对中反应速率集总硫含量影响程度显著增加,对快反应集总硫含量影响程度变化不大,对慢反应集总硫含量影响逐渐减小;④在高空速下,压力对较高脱除活性硫化物HDS 反应影响较大,高压更加有利于高空速下较高脱除活性硫化物脱除;在低空速下,压力对低脱除活性硫化物HDS 反应影响较大,在低空速区间内,低脱除活性硫化物HDS 性能对压力更加敏感;⑤在一定空速下,相对于高温区,当处于低温区时压力对VGO HDS反应影响更大。
符号说明

