真菌毒素免疫亲和柱的制备与评价
金晓林 张东升


[摘要]免疫亲和净化(IAC)是以免疫结合反应原理为基础的纯化和富集技术。IAC在食品安全、农业和生化等中的研究与应用已被色谱工作者接受和认同,展示了广阔的发展前景。本文旨在全面介绍IAC的工作原理、制备方法、评价指标,重点综述了IAC在真菌毒素分析领域的质量控制。
[关键词]免疫亲和;真菌毒素;制备;评价
中图分类号:TS207.5 文献标识码:A DOI:10.16465/j.gste.cn431252ts.202002
真菌毒素是由产毒真菌在适宜的环境条件下产生的有毒代谢产物,已经发现400多种真菌毒素,其中污染较严重的主要包括黄曲霉毒素B1(Aflatoxin B1,AFB1)、玉米赤霉烯酮(Zearalenone,ZEN)、脱氧雪腐镰刀菌烯醇(Deoxynivalenol,DON)、赭曲霉毒素(Ochratoxin A,OTA)及伏马菌素(Fomonisin,FB)等[1]。2017年百奥明公司的调查研究中发现[2],超过75%的样本被检出两种或更多的真菌毒素,其中ZEN、DON及FB的阳性率均超过了50%,DON污染浓度最高。当各种真菌毒素在农产品中同时出现,存在毒性加和或者叠加效应[3],对健康的威胁系数增大,因此有必要对多种真菌毒素同时进行检测。
国内外真菌毒素常用的仪器分析方法主要为免疫亲和层析(Immuno-affinity Column,IAC)结合液相色谱法(liquid chromatography,LC)及液相色谱-质谱联用(LC-MS)检测[4-5]等。与固相萃取柱(SPE)相比,IAC具有溶剂用量少、操作简便、特异性高、净化彻底等优点,这对于提高HPLC和LC-MS的检出限、消除背景干扰是非常必要的。针对生物毒素小分子净化和富集的IAC柱在国内外已经得到商品化并广泛应用[6]。本文在介绍IAC的工作原理、载体活化、抗体制备及偶联方式的基础上,重点阐述了IAC质量评价的必要性及评价要点。
1 免疫亲和层析
1.1 原理及优势
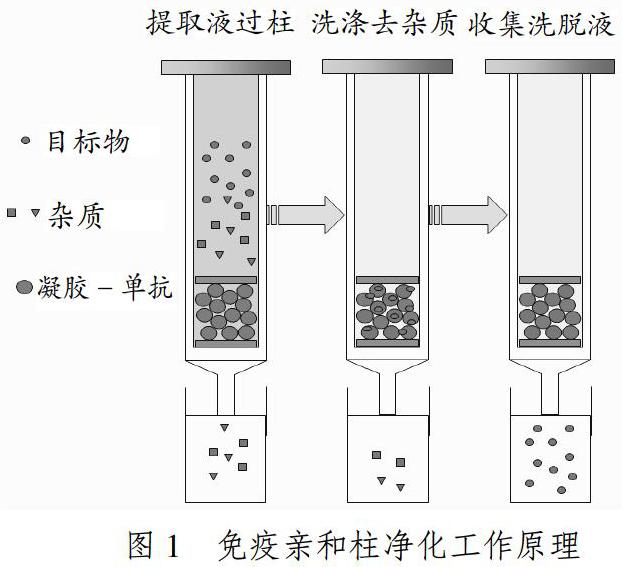
IAC是利用抗原抗体特异性可逆结合特性的亲和层析技术,将抗体与惰性载体共价结合物填入柱中制成的净化色谱小柱。IAC系统存在三个要素:目标物、抗体和惰性载体。当含目标物的样本提取液通过IAC柱时,固定于惰性载体上的抗体选择性地结合目标物,杂质流出,进一步洗涤除杂后将复合物解离,目标物被洗脱,样本得到净化。因抗体是其核心试剂,样品的免疫净化又称抗体介导的净化。其工作原理如图1所示 。
IAC较常规的SPE有许多优点:(1)IAC中抗体对目标物的高度选择性使样本前处理过程简化,分析质量得到改善。避免了反复萃取和浓缩,回收率高。(2)对目标物具有高效保留能力。在IAC柱容量范围内,IAC对于目标物的保留能力和净化能力不受样本体积和目标物浓度的影响。(3)多残留分析能力。固定有多种抗体或者簇特异性抗体的IAC柱可对多种目标物进行净化。(4)水相操作且IAC柱可重复使用,能够节约有机溶剂,保护环境。
1.2 载体分类及活化
IAC柱的绝大部分空间为载体基质所占据,其影响不可忽视。理想的基质必须既有优良的色谱性能,又能满足IAC的特殊要求[7],如高度的亲水性但不溶于水,适度的刚性、惰性、无非特异性吸附或者非常低,理化性质稳定,具有大量可供偶联的活性基团,疏松多孔结构,耐受酸、醇等洗脱作用。实际应用中的载体基质通常分为耐受低压的多糖类物质及耐受高压的聚合材料。多糖类物质除琼脂糖还有纤维素[8]等。代表性聚合材料有聚丙烯酰胺[9]、硅胶[10]等。纤维素及玻璃珠因非特异性吸附高使用受到一定的限制。
多糖基质的活化在IAC制备中占有重要位置。通常在骨架上引入强亲电基团,然后与抗体上的亲核基团如-NH2、-OH、-SH等发生取代反应,使抗体连接于载体上。如果需要使抗体通过间隔臂与基质连接,除可以选择适宜的活化试剂外,也可以首先将间隔臂(如SMCC)[11]与基质连接,再将抗体与间隔臂的活性基团偶联。常用的载体活化方式包括溴化氰活化(CNBr)[12]、碳酰二咪唑法(CDI)[13]等。
1.3 抗体的制备
依据抗体的来源可分为单克隆抗体(McAbs)和多克隆抗体(PcAbs),通过单克隆抗体生产途径不同又可以分为体内和体外,具体区别如表1所示。现阶段制备真菌毒素McAbs的主要途径依然是小鼠腹腔注射细胞诱导产生,受动物福利及抗体质量影响,细胞发酵生产单抗具有极大的发展空间[14]。
McAbs在建立IAC具有较多的优越性。其一,具有高度均一的亲和性和选择性,纯化后的单抗易于制备高容量的IAC柱。其二,制备IAC需要消耗大量的纯化抗体,如1支典型的DON-IAC柱所需要的抗體近乎1~2mg[15],杂交瘤技术的建立,可源源不断地提供性能均一的McAbs。其三,作为净化手段的IAC,具有交叉反应的单抗适宜制备处理多残留组分的Multi-IAC。综合各种因素,一般认为McAbs的突出优势是高度均一性,生产成本低,适于商业生产和推广应用。
1.4 偶联方式
使固定化的抗体维持高密度、高活性是制备一次性、大容量、低成本IAC柱的关键。但是,当抗体被固定在载体表面时,其活性通常比溶液中要低,活性降低的主要原因在于:一是高密度造成抗体分子的空间位阻;二是载体表面抗体的随机偶联。因此,抗体高度定向化的方法被陆续开发出来,主要有3种形式,如表2所示,其中通过蛋白结合单抗固定化应用最为广泛,但因同源交联剂无选择性反应而导致抗原结合域修饰,是其最大缺陷。
2 质量评价
IAC作为生化类产品,在分析领域逐步被推广应用,商业化的步伐加快,市场潜力巨大,至今国内外尚无商品化的免疫亲和柱质量标准或规范。产品生产、使用及评价体制尚不完善,其性能和质量控制尚不能满足检测需要。为了把好产品质量关,促进我国生化检测产业健康、有序地发展,急需建立一个关于IAC产品质量的指导性标准。
2.1 评价的必要性
(1)IAC已作为食品安全相关国家和行业标准检测方法中的关键生化试剂材料,应强化质量控制管理。目前已有专门针对抗生素[20-21]、农药[22]和真菌毒素[23-26]等的各类免疫亲和柱产品,尤其真菌毒素类亲和柱种类最为齐全。经检索采用IAC作为净化手段的测定方法标准共有20项,其中国家标准18项、行业标准2项,其质量直接影响我国食品安全监测和第三方检验结果的准确性和可靠性。
(2)IAC产品技术性能指标不统一、不规范。目前,IAC生产企业要为每一种IAC产品制定标准,且各类标准存在如下问题:一是同一企业、不同品种的标准,其内容仅是冠名的简单替换;二是不同企业IAC的制备方法不一致,在柱容量、非特异性吸附、柱空白等关键指标差异大,导致假阴/阳性测定结果;三是不同企业对IAC产品的重现性和稳定性等关键质量指标要求不一,产品市场混乱,检测单位无所适从,难以选择。
2.2 评价内容
2.2.1 建立原料质量的评价体系
(1)对于单抗的质量指标主要有亲和常数和交叉反应率。①抗体的亲和性(affinity)是抗体与半抗原间结合强度的量度,一般用结合反应的热力学参数平衡常数(Ka),又称亲和常数、结合常数,单位L/moL。Ka值越高,结合能力越强,一般抗原抗体反应的Ka值为106~1 012L/mol。②抗体的选择性或称特异性(specificity)是抗体对待测物的识别能力,是评价抗体与待测物间结合反应的专一性和对结构相近或相关物质的区分能力。在多数的免疫分析中对抗体的特异性有严格的要求,而单一IAC对于抗体的特异性没有完全的排他性,多组分IAC抗体及组合抗体对于类似物的交叉反应有一定的最低要求[27]。
(2)载体的粒径直接决定了样本的流速,载体的非特异性吸附率决定了洗脱率,这两个指标对于IAC的处理时间和回收率至关重要。同时载体的粒径也影响蛋白的结合能力,易建科[28]研究发现200目的氨基硅胶微球受比表面积大,单位体积内的活性基团多的原因,结合蛋白的能力比100目的微球大,对于制备大柱容量的IAC非常有益。①半抗原和抗体的初级结合反应可以在瞬间完成,一般IAC对于加样流速要求并不严格,0.5~3.0mL/min均有应用,一般常用的琼脂糖载体粒径为90?m,1mL层析小柱的尺寸径高比为0.55(同样凝胶体积为0.25mL时,3mL的层析柱径高比为1.78),径高比越大,重力流速越快。②载体非特异性吸附率是除抗体外对IAC质量影响最大的因素。多数活化与偶联过程引入的阴离子交换基团或阳离子交换基团成为非特异性吸附的重要来源。当亲和柱被过量上样时,样品中的待测物除可与特异性抗体结合外,还可与琼脂糖基质或杂蛋白发生非特异性吸附作用,通常用非特异性吸附率来表示,因为无法在亲和柱上直接测量待测物的非特异性吸附量,所以制备未偶联特异性单抗的琼脂糖凝胶柱(以下简称blank柱)对待测物的吸附作用,以非特异性吸附率来表示[29]。一般要求基质非特异性吸附率低于5%。
2.2.2 建立技术性能的评价体系
(1)柱空白,指商品化免疫亲和柱含分析物的含量,理应为0。董曼佳[30]等在制备DON及其乙酰化亲和柱时发现了空白柱含有一定的DON,研究发现其来自原料单抗,文献表明通过饲喂含有一定低剂量的真菌毒素饲料,其衍生物及本身会残留在动物的血液及组织液中,而腹腔中大量的抗体更是结合抗原最好的场所。
(2)柱体积,因IAC具有高效保留能力,所以IAC均采用较小的柱床体积,节约成本和减小非特异性吸附,通常不超过0.5mL;通常3~5倍柱体积的纯有机溶剂即可将待测物完全洗脱。
(3)柱容量,每毫升免疫吸附剂对分析物的最大吸附量(ng/mL),也称动态柱容量。动态柱容量与柱内免疫吸附劑体积的乘积即为单支柱最大吸附量(ng)。测定方法可通过超过理论容量的待测物使IAC柱饱和,经洗涤和洗脱后测定。为避免IAC样本超载而出现待测物流穿现象,需根据柱容量进行设计待测物的处理量。
(4)柱回收率,也称柱效,含分析物的基质提取液,被IAC吸附与解吸的过程,通过检测分析物的回收率来表示亲和柱对分析物捕获能力。该回收率不含标准物质的提取效率,仅反映的是样本基质对免疫结合反应的抑制效应,通过国标[31-32]可以推测理想柱效在90%~110%。
(5)柱稳定性,是指计量特性随时间不变化的能力,可以用计量特性随时间变化的关系来进行定量表征。选取3个不同批次适量的IAC柱,置37℃恒温加速试验1个月,测定柱容量及柱回收以评价稳定性[33]。
2.2.3 操作条件的标准化
(1)抗体抗原的最适反应温度是37℃,从冰箱中取出的IAC需平衡至室温25℃左右或室温下的缓冲液快速淋洗IAC,是确保其抗体免疫活性的重要措施。
(2)因不同的抗体耐受有机溶剂的浓度[34]和耐受酸碱的能力各不相同,所以上样缓冲液、冲洗液工作时的标准pH值一般使用具有缓冲能力的磷酸盐缓冲液,pH 值为7.0~7.4。
(3)淋洗液或者上样的有机相的浓度如甲醇一般不超过20%,乙腈不超过10%。
(4)过高的离子强度(NaCl>0.5mol/L )可能促使抗原抗体复合物的解离。
3 问题与展望
3.1 存在问题
传统IAC柱应用十多年来,问题依然存在,主要表现:(1)成本高。为避免重复使用和加快分析速度,一次性IAC柱成为趋势。(2)浪费大。国内外多采用溴化氰活化的琼脂糖为载体将抗体分子随机的固定在层析介质上,抗体的结合能力下降,造成抗体分子被低效利用。(3)产品不稳定、回收率高。国内外多通过小鼠腹腔诱导抗体,单位产量低,批间存在较大的差异,存在抗原污染的风险。(4)虽然产业化快,但是质量标准滞后。国内IAC的研发起步较晚,但发展迅速,基本改变依赖国外进口的局面。已出台的多项采用IAC净化的测定方法标准,虽然对IAC已有一些质量要求诸如柱容量、回收率,但不系统、不全面。
3.2 展望
标准化单克隆抗体生产和供应依然是IAC真正实现一次性IAC柱的前提;优化载体活化方法、定向偶联的方式,提高单抗的利用率是降低IAC使用成本的关键;开发全自动IAC纯化仪是避免人为操作不当、人为使用低效的有效途径;加快制定IAC通用技术评价规范,是满足检测结果准确性的客观需求。
参考文献
[1] 张宇昊,杨琳,马良.真菌毒素同时检测方法研究进展[J].中国粮油学报,2011,26(6):123-127.
[2] 王金勇,关舒.2017年百奥明原料与饲料霉菌毒素检测报告[EB/OL].(2018-02-08)[2018-02-05].http://www.sohu.com/a/221704058_676025.
[3] 易中华,吴兴利.饲料中常见霉菌毒素间的毒性互作效应[J].饲料研究,2009(1):15-18.
[4] 黎睿,谢刚,王松雪.高效液相色谱法同时检测粮食中常见8种真菌毒素的含量[J].食品科学,2015,36(6):206-210.
[5] 王瑞国,苏晓鸥,程芳芳,等.液相色谱-串联质谱法测定饲料原料中26种霉菌毒素[J].分析化学,2015,43(2):264-270.
[6] SenyuvaHZ,GilbertJ.Immunoaffinitycolumnclean-uptechniquesinfoodanalysis:Areview[J].Journalof ChromatographyB,2010,878(2):115-132.
[7] 肖付刚,赵晓联,汤坚,等.免疫亲和层析及其在真菌毒素检测中应用[J].粮食与油脂,2007(8):40-43.
[8] 邹长军.球型纤维素固定Anti-HBsAg单克隆抗体制备免疫吸附剂[J].化学与生物工程,2004,21(1):32-33.
[9] 杨春洪,李培武,张文,等.聚丙烯酰胺固相微球与黄曲霉毒素B1抗体偶联条件的研究[J].中国油料作物学报,2005,27(2): 62-65.
[10] 张灿,周婷,陆介宇,等.硅胶载体氯霉素免疫亲和柱的制备[J].食品科学,2012,33(24):352-355.
[11] 冯燕.SMCC法抗体定向偶联技术的优化与应用研究[D].武汉: 华中科技大学,2011.
[12] 王念跃,赵伟,李勇,等.两种pH条件下CNBr活化Sepharose4B偶联DSA方法的比较研究[J].中国生化药物杂志,2005,26(6): 356-358.
[13] 韦林洪,王莲,刘曙照.稻米中三唑磷残留免疫亲合色谱-高效液相色谱分析[J].中国农业科学,2006,39(5):941-946.
[14] 张权庚,张玉祥,丁卫,等.抗体制备与使用实验指南[M].北京:科学出版社,2010.
[15] 杨婷婷,吕轶,张东升,等.多合一真菌毒素免疫亲和柱的制备及其应用[J].分析化学,2016,44(8):1243-1249.
[16] Kim H,Kang DY,Goh HJ,et al.Analysis of direct immobilized recombinant protein Gonagold surface[J].Ultramicroscopy,2008,108(10):1152-1156.
[17] Ahmed SR,Lutes AT,Barbari TA.Specific capture of target proteins by oriented antibodies bound to tyrosinase-immobilized Protein Aona polyallylamine affinity membrane surface[J].Journal of membrane science,2006,282(1):311-321.
[18] Kang J H,Choi H J,Hwang S Y,et al.Improving immuno binding using oriented immobilization of anoxidized antibody[J].Journal of Chromato graphyA,2007,1161(1):9-14.
[19] Crivianu-GaitaV,ThompsonM.Immobilization of Fab fragment sontosubstrate surfaces:asurvey of methods and applications[J].Biosensorsand Bioelectronics,2015(70):167-180.
[20] 刘丽强,李寅,彭池方,等.环丙沙星免疫亲和柱的制备及优化[J].食品科学,2009,30(22):209-212.
[21] 李哲,胡擁明,张柳伟,等.庆大霉素免疫亲和柱的制备及测定[J].食品科学,2009,30(22):188-191.
[22] 刘曙照,韦林洪,徐维娜.克百威的免疫亲和色谱分析研究[J].色谱,2005,23(2):134-137.
[23] 龚燕,杨婷婷,莫晓嵩,等.基于蛋白A-琼脂糖凝胶黄曲霉毒素B1免疫亲和柱的制备[J].食品科学,2015,36(10):216-220.
[24] 孙兴荣,裴世春,柳家鹏.抗黄曲霉毒素M1免疫亲和柱的制备[J].现代食品科技,2011,27(3):306-309
[25] 章英,黄志兵,邓舜洲,等.抗玉米赤霉烯酮单克隆抗体免疫亲和柱的研究制备[J].中华预防医学杂志,2007,41(2):110-113.
[26] 章英,黄志兵,许杨.抗赭曲霉毒素A单克隆抗体免疫亲和柱的制备[J].中华预防医学杂志,2009,43(3):250-252.
[27] GB 5009.22-2016,中华人民共和国国家卫生和计划生育委员会/国家食品药品监督管理总局.食品安全国家标准食品中黄曲霉毒素B族和G族的测定[S].
[28] 易建科,李培武,张文,等.几种高分子微球与兔免疫球蛋白的偶联及偶联条件的优化[J].湖北大学学报(自然科学版), 2007,29(3):273-276.
[29] 张秀莉.免疫亲和萃取_LC_MS联用技术在痕量农残分析中的应用研究[D].大连:中国科学院大连化学物理研究所,2006.
[30] 董曼佳,杨婷婷,陆廷瑾,等.脱氧雪腐镰刀菌烯醇及其乙酰化衍生物免疫亲和柱的研制[J].粮食与食品工业,2018,25(2):73-79.
[31] GB 5009.111-016,食品安全国家标准食品中脱氧雪腐镰刀菌烯醇及其乙酰化衍生物的测定[S].
[32] GB 5009.24-2016,食品安全国家标准食品中黄曲霉毒素M族的测定[S].
[33] 杨梅,刘君君,牟晓然,等.阿伦尼乌斯方程在体外诊断试剂有效期预测中的应用[J].国际检验医学杂志,2013,34(12): 1586-1588.
[34] Stroka J, Petz M,Joerissen U,et al.Investigation of various extractants for the analysis of aflatoxin B1 in different food and feed matrices[J].Food AdditContam,1999(16):331-338.
收稿日期:2019-12-24
作者简介:金晓林,男,高级工程师,研究方向为食品安全与品控。
通信作者:张东升,男,副研究员,研究方向为食品安全与营养。

