猪瘟耐热活疫苗节能冻干曲线的优化研究
左晓昕 赵艳红 邓碧华 牟和平 胡来根 宋伟 吕芳 卢宇 侯继波


摘要: 猪瘟疫苗真空冷冻干燥工艺,可减少冻干对制品活性的影响,降低制品冻干过程的耗能,缩短冻干周期,故研制安全、耐热、节能的猪瘟减毒冻干疫苗极为重要。选用甘露醇、甘氨酸等成分设计猪瘟耐热保护剂配方,通过间接免疫荧光法比较制品在37 ℃、10 d的冻干和耐热损失,并用兔体热反应法复核。检测优化配方的共晶点和塌陷温度设计冻干程序,比较不同预冻方式对猪瘟耐热疫苗冻干的影响,调整冻干周期。猪瘟耐热保护剂配方A-4的冻干和耐热损失最小,分别为0.30 lg和0.45 lg。根据制品的共晶点-27.51 ℃,对预冻方式筛选,发现快冻冻干和耐热损失最小,分别为0.17 lg和0.38 lg,根据塌陷温度-24.3 ℃,成功将冻干曲线缩短至24 h。调整后的配方可使猪瘟活苗在 37 ℃ 保存 15 d、45 ℃保存7 d;内毒素和动物试验表明该疫苗安全、无副反应。上述结果表明,试验成功筛选出猪瘟耐热保护剂配方A-4,在保证疫苗质量的前提下优化冻干曲线,调整后的保护剂配方保证疫苗耐热性能,安全无副反应。
关键词: 猪瘟病毒;耐热保护剂配方;冻干工艺;耐热性能;安全性
中图分类号: S859.79+7 文献标志码: A
文章编号:1002-1302(2020)05-0156-06
猪瘟(classical swine fever,CSF)是由豬瘟病毒(classical swine fever virus,CSFV)引起的急性、接触性传染病,在各国均有暴发疫情,尤其是东南亚地区,呈散发性且流行范围广的特点[1]。猪瘟作为我国重大动物疫病,已经在国家中长期动物疫病防治规划中被列为优先防治的动物疫病[2]。
疫苗是控制猪瘟的重要手段,我国相继用4株猪瘟病毒诱导猪瘟发病,并成功筛选出能够减少对猪的致病能力但能保存免疫原性的猪瘟病毒,即猪瘟兔化弱毒疫苗C株。CSFV增殖方法多样,目前在生产上多在猪睾丸细胞和牛睾丸原代细胞上扩繁,生产工艺成熟。但是该疫苗的耐热性差,极易失活[3],在生产后期必须要添加一些保护剂,并进行真空冷冻干燥。但是,目前市场上的猪瘟冻干活疫苗在传输中仍无法脱离冷链环境,需要在 -15 ℃ 以下保存[4],现有疫苗的冻干工艺周期较长,一般在42~50 h,极大增加生产的成本[5]。在近期研究中,有报道指出,蔗糖、甘氨酸、表面活性剂等复合组方能够延长腺病毒在4 ℃和室温的保存期[6-7];使黄热病毒在4 ℃下可保存11周左右[8]。该复合组方在猪瘟活疫苗上也有应用,使用甘氨酸、聚乙烯吡咯烷酮、蔗糖等能够使疫苗在2~8 ℃保存2年,在37 ℃保存10 d耐热损失在0.9 lg,该复合组方安全、无副反应,避免了外源蛋白给动物带来的过敏反应[9-10],但目前这些配方对不同细胞培养的CSFV保护效果报道较少。
耐热保护剂配方与冷冻干燥工艺相互配套,保护剂是冻干工艺的基础,合理的保护剂配方和适宜的冻干曲线是制品顺利冻干的保证。在保证质量的前提下需要减少能耗、降低成本。冻干工艺主要分为预冻阶段和干燥阶段,在不同阶段需要通过参考制品的热参数,如共晶点、塌陷温度等进行设计。其中,塌陷温度是在真空冷冻的过程中测得的,能够真实反映制品的特性[11]。当温度超过塌陷温度会造成制品底部熔融、塌陷、萎缩,损害干燥制品的多孔结构,增加残余水分,降低生物制品的效价[12]。因此,以塌陷温度作为临界温度,可以提高升华干燥速度,缩短冻干时间。
本研究针对猪瘟冻干工艺周期长、耗能高及猪瘟耐热保护剂配方通用性等问题,以吕芳等的无明胶、无蛋白的猪瘟耐热保护剂配方[8]为基础,添加甘露醇、甘氨酸等成分,通过间接免疫荧光法筛选耐热保护组方。将筛选的配方分别和猪睾丸、牛睾丸细胞冻干,初步对配方的通用性进行探索。并根据共晶点和塌陷温度科学设计冻干程序,获得耗能低、冻干周期短的冻干曲线,研制安全、耐热、节能的猪瘟减毒冻干疫苗冻,为猪瘟耐热保护剂配方在实际生产上的应用提供科学依据。
1 材料与方法
1.1 试验材料
猪瘟兔化弱毒株(猪睾丸原代细胞毒)和ST细胞,均由成都天邦生物制品有限公司提供;猪瘟兔化弱毒株(牛睾丸原代细胞毒),由南京天邦生物制品有限公司提供;甘露醇、甘氨酸等,购自北京鼎国昌盛生物技术有限责任公司;DMEM培养基、谷氨酸钠等其他试剂耗材,均购自Sigma公司;鲎试剂盒、细菌内毒素标准品(0.25 EU/mL)和检查用水,均购自湛江安度斯生物有限公司。
1.2 试验仪器
冻干机(美国Virtis,Advantage Plus型号);37 ℃ 和45 ℃恒温干燥箱(上海新苗医疗器械制造有限公司);荧光显微镜(德国蔡司)、磁力搅拌器(金坛荣华仪器制造有限公司)、低温冻干显微镜(英国林肯,型号FDCS196)、DSC热分析仪(美国PerkinElmer公司)。
1.3 猪瘟耐热保护剂活疫苗配制
以无明胶、无蛋白的猪瘟耐热保护剂配方A为基础[8],添加甘露醇、甘氨酸等成分,设计出组方 A(1)~A(6)。配制时,根据配方成分的性质将其分为A、B部分制备,其中A为不耐热成分,超纯水溶解后用0.22 μm的滤膜过滤除菌;B为耐热成分,采用高温高压法灭菌。耐热保护剂配方与CSFV病毒液等比例混合,进行冷冻干燥,冻干程序参照文献[8]。
1.4 加速热稳定性试验
将不同配方配制的猪瘟耐热冻干活苗置于 37 ℃ 保存10 d,每组取5瓶样品进行加速耐老化试验。根据参考文献[13-14],通过间接免疫荧光法检测猪瘟TCID50,比较不同保护剂配方对猪瘟的耐热效果。为比较耐热保护剂配方对不同细胞下扩繁的猪瘟病毒的通用性,采用牛睾丸原代细胞培养的猪瘟兔化弱毒C株与筛选出来的耐热保护剂配方进行冻干,37 ℃保存10 d,采用《中国兽药典(2015年版)》兔体感染量(rabbit infection dose,RID)方法进行复核[15]。
1.5 耐热保护剂配方热参数的测定
将筛选的猪瘟耐热保护剂与猪瘟病毒等比例混合,测定混合液的共晶点和塌陷温度。共晶点采用DSC热分析仪测定,检测条件为:对液体状态疫苗以10 ℃/min升温速率,从-50 ℃升至30 ℃,通过记录热焓变化曲线,分析得到共晶点温度。
塌陷温度采用低温冻干显微镜测定,检测指标为:起始温度-45 ℃,真空为20.0 Pa,升温速率 2 ℃/s,最终温度20 ℃;由上海东富龙科技股份有限公司进行检测。
1.6 疫苗预冻方式的筛选
预冻环节是冷冻干燥的起始环节,也是冻干技术的基础,不同类型的药品成分其理化性质存在差异,在预冻方式上也存在差异[16]。根据“1.5”节方法测定的热参数指标,确定预冻温度和主干燥温度,并设计快速冷冻、慢速冷冻和退火3种方式对猪瘟耐热疫苗进行冻干。冻干样品采用“1.4”节方法进行加速耐老化试验,根据《中国药典》第3部通则0832检测残水分,残水率应不高于3%[17]。
1.7 疫苗冻干时长的优化
在保证猪瘟疫苗耐热性能的前提下,降低制品冻干过程的能耗,节约成本是冷冻干燥工艺研究生产中必须考虑的因素。物料的性质是影响冻干效率和时长的关键因素。需要提高一次干燥阶段疫苗的干燥速率,缩短冻干时长。根据“1.5节”检测的塌陷温度和“1.6”节筛选预冻方式,对冻干时长进一步优化,将缩短冻干程序至24 h。冻干样品采用“1.4”节方法进行加速耐老化试验。
1.8 猪瘟耐热活疫苗耐热性能检测
根据筛选出的猪瘟耐热保护剂配方和冻干程序,重新制备3批次猪瘟耐热冻干活苗,置于 37 ℃ 和45 ℃保存,在不同时间点取出,检测猪瘟耐热疫苗效价,以保存期内病毒滴度下降1.0 lg为判定终点。
1.9 内毒素含量检测
猪瘟耐热活疫苗中内毒素含量过高是引起动物产生过敏反应的主要原因之一,为检测猪瘟耐热配方和猪瘟耐热活疫苗的内毒素限制,试验参考《中国兽药典(2015年版)》[15]中的鲎试剂方法进行检测,根据参考文献[18],用内毒素标准用水分别将耐热保护剂和猪瘟耐热活苗稀释10、50、100倍,用标示灵敏度为0.25 EU/mL的鲎试剂进行比较。
1.10 猪瘟耐热活疫苗安全性能检测
参照《中国兽药典(2015年版)》对疫苗进行安全检验[15]。选用30日龄三元仔猪,将筛选的猪瘟耐热冻干活疫苗用灭菌生理盐水稀释成1 mL含20头份和30头份,1 mL/头,每个剂量组肌肉注射猪10头,对照组不免疫。接种后隔离观察,主要观察接种后仔猪的精神、采食、排泄等临床情况,按质量标准判定疫苗合格情况。
1.11 统计学处理
采用SPSS 17.0统计软件对数据进行单因素方差分析处理,以x[TX-*5]±s表示,P<0.05表示组间差异显著,P<0.01表示组间差异极显著。
2 结果与分析
2.1 耐热保护剂的初步筛选
将耐热保护剂配方A(1)~A(6)分别与猪瘟病毒混合后冻干,于37 ℃放置10 d进行加速耐老化试验。由表1可知,与基础配方A进行对比,在冻干损失方面,配方A(4)的冻干损失最小,仅为 0.3 lg,显著低于其他试验配方(P<0.05)。在耐热损失方面,配方A(4)的耐热损失为0.45 lg,显著低于基础配方A(P<0.05)。综合冻干损失和耐热损失2个指标,配方A(4)的冻干耐熱保护效果最好。将A和A(4)配方分别与牛睾丸原代细胞扩繁的CSFV冻干,通过兔体热试验检测耐热效果,结果发现,A(4)配方的耐热损失为0.44 lg,显著优于基础配方A(P<0.05)。A(4)配方对不同细胞培养的CSFV均具有耐热效果。
2.2 热参数
根据筛选出来的猪瘟耐热保护剂配方A(4)与猪瘟混合,进行热参数的测定。由表2可知,混合液的共晶点为-27.51 ℃,塌陷温度为-24.30 ℃。根据共晶点参数,将预冻的温度设置为-42.00 ℃,保证样品在该阶段充分冻实。在主干燥阶段,由于隔板温度比样品温度高10 ℃左右[19], 为防止样品发生熔融、塌陷、萎缩,要将制品温度控制在塌陷温度以下。
2.3 疫苗冻干程序筛选
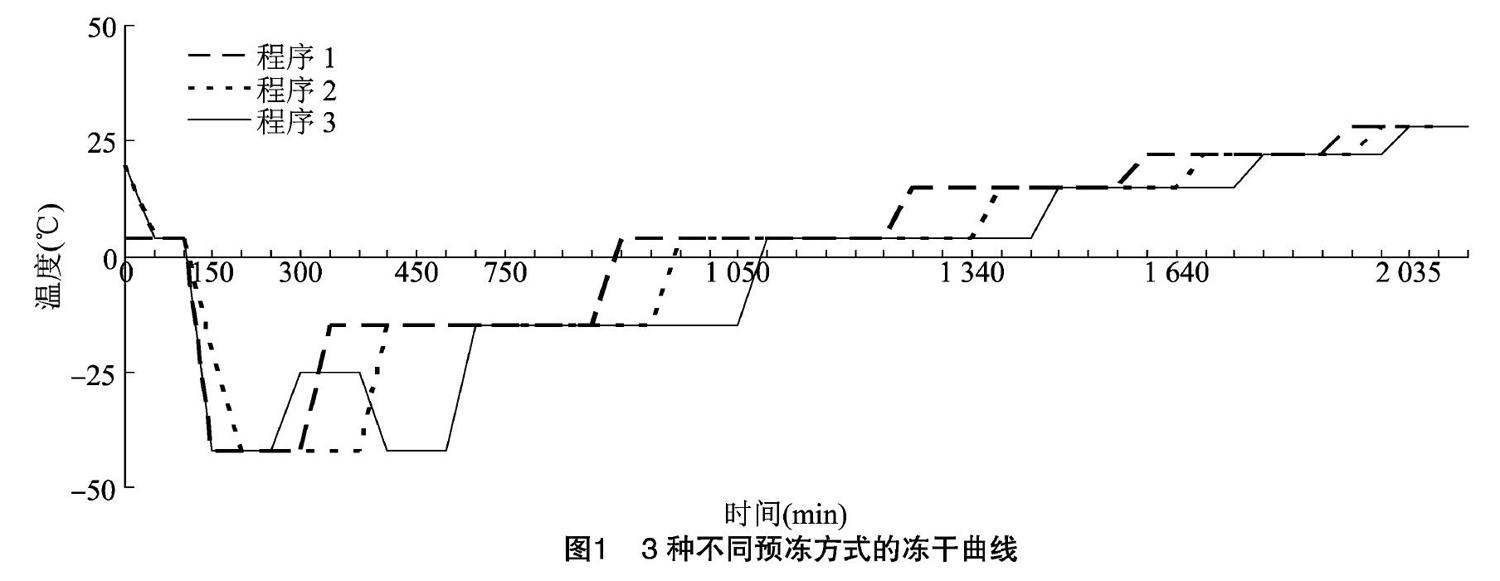
参考“2.2”节热参数性能指标,设定预冻温度为-42.00 ℃,主干燥温度为-15.00 ℃。在冻干过程中,预冻程序是影响冻干效率的关键步骤,物料不同,预冻的速率也存在差异,降温速度影响冻结快慢从而影响冰晶颗粒的大小和冻干时间。为筛选合适的预冻程序,分别采用快冻(图1-程序1),慢冻(图1-程序2)和退火(图1-程序3)对A(4)配制的猪瘟耐热疫苗进行冻干,冻干时长在32~35 h。
将3种程序冻干的疫苗在37 ℃放置10 d,进行加速热稳定试验。由表3可知,快冻和退火程序下猪瘟苗的冻干损失约0.2 lg,冻干效果显著优于慢冻程序(P<0.05)。由表3可知,快冻程序下的耐热损失为0.38 lg,极显著低于慢冻和退火程序(P<0.01)。在快冻程序下,猪瘟苗的冻干损失和耐热损失最小。因此,选择快冻方式作为猪瘟耐热配方A(4)的预冻方式,对冻干程序继续进行优化。
2.4 冻干时长缩短
作为冷冻干燥工艺研究的重要任务之一,需要对冻干时长进行缩短、降低能耗,以节约成本。根据制品的塌陷温度,程序4(图2-A)以程序1(图1-程序1)为基础,提高主干燥温度,将冻干时长缩短至24 h。在程序4中将主干燥温度提高,缩短主干燥时长,观察程序4的制品冻干实时曲线,发现在主干燥阶段,制品的温度仍维持在塌陷温度以下;在20 ℃左右,制品线与隔板重合,制品干燥完全,残水率检测合格。程序4在保证冻形同时提高缩干燥效率,缩短冻干时长(图2)。对程序4冻干的疫苗检测冻干损失和耐热损失,与原冻干程序2无明显差异(P>0.05),冻干损失在0.5 lg,耐热损失在 0.3 lg(表4)。
2.5 豬瘟冻干疫苗的耐热性能
将3批次猪瘟耐热冻干疫苗分别放置于37 ℃和45 ℃保存,在指定时间点取出,检测样品的耐热性能。图3-A显示,冻干苗在37 ℃放置15 d时耐热损失在0.8 lg左右;20 d时耐热损失在1.1 lg左右。图3-B显示,冻干苗在45 ℃保存7 d,耐热损失在1.0 lg左右。
2.6 猪瘟耐热保护剂活疫苗内毒素含量
内毒素是引起仔猪发生过敏反应的原因之一,本研究将内毒素含量作为判断配方副作用的指标。对耐热保护剂和耐热保护剂活疫苗进行10、50、100倍稀释后,在阴性和阳性对照组成立的条件下,各稀释倍数下的样品组均对灵敏度为0.25 EU/mL的鲎试剂无干扰(表5),说明其内毒素含量低于1 EU/mL,耐热保护剂和耐热保护剂活疫苗是安全的。
2.7 猪瘟耐热冻干疫苗的安全性
将筛选的猪瘟冻干活苗复溶,颈部肌肉注射,观察仔猪的采食、体温、精神状态等,发现所有仔猪均无不良反应,体温及精神状态正常,根据兽用生物制品质量标准判定疫苗对猪体是安全,筛选的配方无不良反应。
3 讨论
选用合适的保护剂对疫苗的质量和长期保存的稳定性至关重要。市场上现有的猪瘟活疫苗通常会添加蔗糖、脱脂奶粉和明胶等保护剂,组方简单、保护功能差,脱脂奶粉和明胶作为外源性蛋白容易引起猪,尤其是仔猪的过敏反应[20]。试验前期,吕芳等成功筛选出无明胶、无蛋白的耐热保护配方能够使猪瘟疫苗在37 ℃保存15 d,且安全无副反应,但是冻干耗时长在40~42 h[9]。本试验在该配方基础上进一步优化,缩短冻干时长,提高干燥效率[8]。
在对疫苗进行冷冻干燥处理时,起始环节是预冻阶段,在该阶段要保证制品充分冻实,制品温度要低于共晶点温度10 ℃左右。不同类型的药品成分理化性质不同,对预冻阶段程序的设定也存在差异。预冻速率是影响冰晶大小、兽用疫苗存活率和升华速率的关键因素[21]。根据预冻速率将其分为快冻、慢冻和退火。本次试验对预冻程序进行筛选优化,结果发现在快冻程序下猪瘟的冻干和耐热损伤最小。这可能是降温速率影响冰晶成核大小,快冻形成的冰晶颗粒更小,对病毒造成的机械损伤较轻[22]。
在冷冻过程中,一次干燥是整个冻干工艺中耗时最长的阶段,一次干燥周期与制品的塌陷温度有关。塌陷温度是指制品干燥过程中失去刚性,开始变黏,发生类似塌方的崩解、融化或产生发泡现象的临界温度,在冻干过程发生塌陷会严重影响冻干制品品质,因此制品在一次干燥的温度必须要低于塌陷温度。塌陷温度取决于制品本身的性质和保护剂的种类。制品的塌陷温度提高,有利于提高主干燥温度,提高干燥效率,节省冻干能耗和时长[23]。氨基酸是常用的蛋白保护剂之一,有研究指出,甘氨酸能提高生物制品的可塑性,提高制品的塌陷温度[24]。此外,甘露醇是常用的赋形剂,杨智等发现2%甘露醇在升华过程中未发生崩解,能够提高配方的塌陷温度[11]。本次试验通过添加甘露醇、甘氨酸等成分,将制品塌陷温度从-31 ℃提高至 -24 ℃。基于制品塌陷温度的提高,在一次干燥阶段,提高板层设置温度,提高干燥效率,将冻干时长缩短至 24 h,残水率合格,猪瘟耐热疫苗冻干损失0.5 lg,耐热损失0.3 lg,极大地减少了冻干能耗、时长,降低了经济成本。在耐热性能方面,研究报道的猪瘟活苗37 ℃能保存7~10 d[25],本研究中猪瘟活苗在37 ℃可保存15 d左右,在45 ℃可保存7 d左右。内毒素和动物试验均显示该配方是安全、无副反应的,本研究成功筛选出耐热性能好、无副作用、低耗能的猪瘟耐热保护剂配方,成功将冻干时长缩短至 24 h,初步探索了配方对不同细胞扩繁的猪瘟病毒的通用性,可为猪瘟耐热冻干保护剂配方在实际生产中的应用提供科学依据。
参考文献:
[1]夏铭崎. 猪瘟国内外流行新趋势[J]. 今日养猪业,2017(3):41-44.
[2]王元元. 规模化养猪场猪瘟流行特征、原因分析及疫苗研究进展[J]. 中国畜牧兽医文摘,2018(5):165.
[3]Chenut G,Saintilan A F,Burger C,et al. Oral immunisation of swine with a classical swine fever vaccine(Chinese strain)and transmission studies in rabbits and sheep[J]. Veterinary Microbiology,1999,64(4):265-276.
[4]Kartoglu U,Milstien J. Tools and approaches to ensure quality of vaccines throughout the cold chain[J]. Expert Review of Vaccines,2014,13(7):843-854.
[5]管清江,邹桂荣. 改进蓝耳病疫苗冻干工艺提高产品质量的工艺探索[J]. 中国农资,2013(28):139.
[6]Evans R K,Nawrocki D K,Isopi L A,et al. Development of stable liquid formulations for adenovirus-based vaccines[J]. Journal of Pharmaceutical Sciences,2004,93(10):2458-2475.
[7]Stewart M,Ward S J,Drew J. Use of adenovirus as a model system to illustrate a simple method using standard equipment and inexpensive excipients to remove live virus dependence on the cold-chain[J]. Vaccine,2014,32(24):2931-2938.
[8]Wiggan O,Livengood J A,Silengo S J,et al. Novel formulations enhance the thermal stability of live-attenuated flavivirus vaccines[J]. Vaccine,2011,29(43):7456-7462.
[9]吕 芳,赵艳红,张小飞,等. 猪瘟无明胶无蛋白耐热活疫苗的研制及冻干工艺[J]. 中国兽医学报,2016,36(12):2014-2018.
[10]邹立宏,何平有,翟含流. 猪瘟耐热保护剂活疫苗生产工艺研究[J]. 兽医导刊,2018,293(7):71-72.
[11]杨 智,李代禧,张 燕,等. 冷冻干燥过程中重要参数塌陷温度的研究[J]. 应用化工,2014(5):962-965.[HJ2.05mm]
[12]马兆堂,丁 敏. 浅谈药物冻干曲线的制定及常见问题分析[J]. 当代化工研究,2017(4):146-147.
[13]李晶梅,朱 薇,秦红刚,等. IFA和IPMA方法测定猪瘟兔化弱毒病毒含量[J]. 中国兽药杂志,2013,47(10):35-38.
[14]王遵宝,李俊辉,张先锋,等. 利用荧光定量RT-PCR法与间接免疫荧光法比较测定猪瘟兔化弱毒病毒含量[J]. 中国兽医学报,2017,37(3):410-414.
[15]中国兽药典委员会. 中华人民共和国兽药典:3部[M]. 北京:中国农业出版社,2015.
[16]贾立峰. 冷冻技术在制药工艺中的应用[J]. 中国新技术新产品,2018(8):37-38.
[17]国家药典委员会. 中华人民共和国药典[M]. 北京:化学工业出版社,2009.
[18]郭广君,吕素芳,苗立中,等. 猪瘟脾淋毒耐热保护剂活疫苗内毒素检测方法的建立与应用[J]. 中国动物检疫,2010,27(2):35-37.
[19]滕有寿,姜海艳. 制订生物制品冻干曲线的探讨[J]. 中国兽药杂志,2009,43(11):53-55.
[20]谭长江,孟宇航. 兽用疫苗耐热冻干保护剂的研究进展[J]. 中国畜禽种业,2011,7(6):16-18.
[21]Nakagawa K,Murakami W,Andrieu J,et al. Freezing step controls the mannitol phase composition heterogeneity[J]. Chemical Engineering Research & Design,2009,87(8):1017-1027.
[22]钱应璞. 制剂药品的冻结真空干燥技术[J]. 机电信息,2004(15):3-11.
[23]徐成海,张志军,张 斌. 冻干技术的几个热点问题[J]. 干燥技术与设备,2010(5):205-210.
[24]Flood A,Estrada M,McAdams D,et al. Development of a freeze-dried,heat-stable influenza subunit vaccine formulation[J]. PLoS One,2016,11(11):e0164692.
[25]汪宏才,楊 峻,杨 涛,等. 猪瘟活疫苗耐热保护剂研究[J]. 湖北农业科学,2009,48(11):2795-2797.
收 稿日期:2019-05-06
基金项目:国家重点研发计划(编号:2017YFD0500706-2);江苏省农业科学院探索性颠覆性创新计划[编号:ZX(17)2016]。
作者简介:左晓昕(1992—),女,江苏泰州人,硕士,从事兽用疫苗耐热剂型研究。E-mail:zuoxiaoxin08@163.com。
通信作者:吕 芳,硕士,副研究员,从事兽用疫苗耐热剂型研究。E-mail:lvfang31@163.com。

