海水中Mg2+和SO42-含量对电极表面钙质沉积层形成的影响
范旭文陈兴林邓会宁杜亚威
(1. 河北工业大学 化工学院,天津 300130; 2. 河北工业大学 海洋科学与工程学院,天津 300130)
阴极保护技术对于金属表面的缝隙腐蚀、应力腐蚀、均匀腐蚀等均有很好的防护作用,故该技术被广泛应用于海洋工程中的金属腐蚀防护[1]。然而,实际工程应用结果表明,阴极保护技术既有优点也有缺点[2]。在阴极保护过程中,金属表面会形成一层钙质沉积层,其主要成分多为CaCO3[3-4]。钙质沉积层会阻碍O2的扩散并且有效降低保护电流密度,从而增强阴极保护的效率[5]; 然而,垢层剥落会诱导金属表面发生点蚀,同时金属表面垢层覆盖区域会出现氧浓度差,导致局部区域形成氧浓度差电池,容易使基材受到缝隙腐蚀的影响[6]。因此,有必要研究阴极保护过程中钙质沉积层的形成过程以及阴极保护失效后钙质沉积层对金属基材的保护作用。
许多因素会影响钙质沉积层的表面形貌和微观结构,比如阴极保护电位﹑ 海水流速﹑海水温度等[7]。除了上述影响因素外,还有学者认为,海水成分也会对阴极保护中钙质沉积层的形成产生重要的影响[8]。
本工作研究了海水中Mg2+和SO42-含量变化对阴极保护过程中电极表面钙质沉积层沉积过程和微观结构的影响,应用计时电流法监测阴极保护过程中钙质沉积层形成的动力学过程,电极表面形成钙质沉积层后,在开路电位下进行电化学阻抗测试来模拟阴极保护失效后表面沉积层对金属基材的保护作用。以期为海洋环境中阴极保护的进一步应用提供理论支撑。
1 试验
将B30铜镍合金切割成尺寸为30 mm×15 mm×2 mm的试片,电极工作面积为1 cm2,非工作面经环氧树脂封装。电极表面用水磨砂纸(800~1 500 号)逐级打磨,在丙酮溶液中进行超声波清洗去除油污,用蒸馏水清洗并烘干,然后放在干燥器皿中备用。
电化学试验采用上海辰华公司生产的CHI600E电化学工作站完成,采用三电极体系,工作电极为制备的B30镍基合金试片,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极。文中电位若无特指,均相对于SCE。试验过程中,采用计时电流法模拟工程实际中的阴极保护过程,监测时间为86 400 s(24 h),初始电位为E= -1 V,高电位和低电位分别为-1 V和-1.01 V,阶跃次数为180,脉冲宽度为480 s,信号记录时间间隔为10 s,灵敏度为1×10-6A/V。对电极进行恒电位阴极保护24 h后,将电极静止30 min,然后在开路电位下进行电化学阻抗测试,设置测试频率范围为0.01 Hz~100 kHz,激励信号幅值为10 mV。阻抗测试完成后,将电极静止10 min再进行线性极化测试,通过线性极化电阻值来研究离子含量变化对金属表面钙质沉积层的孔隙率和密实度的影响。设定线性极化扫描速率为20 mV/min,电位范围为±20 mV(相对于开路电位)。测试完成后,采用蒸馏水冲洗去除金属表面盐分,吹干后采用扫描电子显微镜(SEM)观察钙质沉积层的形貌和晶体结构,并用X射线衍射仪对钙质沉积层进行XRD分析,扫描范围设置为30°~70°。
试验溶液采用人工海水,成分见表1,由分析纯药品和去离子水配制而成。为了研究离子含量的影响,试验溶液按照表1中离子质量浓度的0%、50%、100%和200%的标准改变Mg2+和SO42-的量并保持其他成分不变。为了避免沉积过程引起离子含量的变化,所有试验溶液的体积都固定为1 L,并且每次试验前都采用0.1 moL/L NaOH溶液调整试验溶液pH至8.2。
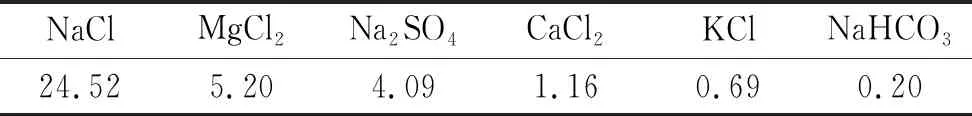
表1 人工海水的组成Tab. 1 Composition of artificial seawater g/L
2 结果与讨论
2.1 Mg2+含量对钙质沉积层的影响
2.1.1 计时电流曲线
图1中,J0代表电极在极化过程中的初始电流密度,J代表电极在极化过程中的瞬时电流密度。试验过程中,考虑到测试环境的稳定性因素,在极化3 min后开始采集J。试验通过观察J/J0的变化情况来表征电极在极化过程中钙质沉积层的沉积情况。

图1 在含不同量Mg2+的人工海水溶液中,试样的电流变化曲线Fig. 1 Current change curves of samples in artificial seawater solution containing different amounts of Mg2+
由图1可见:在极化初始阶段,极化电流出现了微弱的增大趋势,且J/J0值在极化2 h后达到最大。这主要是由于在极化初期,电极表面的氧化物薄膜逐渐溶解,使得电极表面的活化区域增大,导致瞬时电流增大。由图1还可见:Mg2+含量的变化会对钙质层的沉积过程产生明显影响,随着Mg2+含量的增大,钙盐的沉积过程变得缓慢。试验溶液中不含Mg2+条件下,J/J0值在极化7 h后达到0.2左右(如图1中a点处);试验溶液中Mg2+含量为标准人工海水的200%条件下,需要近24 h到达0.2(如图1中b点处)。图1结果表明:增加溶液中Mg2+的量对于阴极保护过程中钙质沉积层的形成
有明显的抑制作用。
2.1.2 表面形貌
由图2~4可见:随着溶液中Mg2+量的变化,试样表面钙质沉积层的微观形貌和晶体结构发生了明显的变化。在不含Mg2+的试验溶液中,经过24 h极化后,试样表面可以观察到含有微量菜花形态的大立方晶体,此时沉积层主要是方解石相的CaCO3晶体;随着试验溶液中Mg2+含量上升至标准人工海水的50%,试样表面形成了排列疏松的霰石相CaCO3晶体,结合图3可见,疏松的霰石相晶体底部具有排列规整的方解石相晶体,可以推断钙质沉积层中的霰石相晶体主要是由于Mg2+在方解石晶体表面的非均匀渗入,导致在方解石晶体表面发展了新的晶体,从而形成了霰石相晶体结构;当试验溶液中Mg2+含量上升至标准人工海水的100%和200%时,随着Mg2+的大量渗入,钙质沉积层中不再出现方解石相的CaCO3晶体,而是以霰石相CaCO3晶体为主。由此得出结论:Mg2+含量变化会引起钙质沉积层表面形貌和晶体结构的变化;随着Mg2+量的增大,电极表面钙质沉积层的覆盖面积逐渐变小,晶核数量和晶体大小也出现明显减小的趋势。造成这种现象的主要原因可能是随着溶液中Mg2+量的增加,影响了Ca2+和CO32-络合过程的活度系数,即减少了进一步沉积的可用离子,从而抑制了钙质沉积层晶体的成核和生长过程[9]。
2.1.3 电化学阻抗谱
通常以最低频率下阻抗模值的大小来表征沉积垢层对金属基材的保护作用[10]。由图5可见:随着溶液中Mg2+含量的增加,低频阻抗模值逐渐减小,当Mg2+含量为0时,阻抗模值比其他条件下的都大,这是由于Mg2+含量影响垢层的晶体结构,方解石相晶体结构的密实度和孔隙率相比于霰石相晶体结构的有明显改善,因此得出结论,垢层的密实度和孔隙率随着Mg2+含量的降低而逐渐得到改善。
2.2 SO42-含量对钙质沉积层的影响
2.2.1 计时电流曲线

(a) 0% Mg2+

(b) 50% [Mg2+]std

(c) 100% [Mg2+]std

(d) 200% [Mg2+]std图2 在含不同量Mg2+的试验溶液中,试样极化24 h后表面沉积层的SEM形貌Fig. 2 SEM morphology of surface deposit layers in test solutions containing different amounts of Mg2+ after 24 h of polarization

图3 图2(b)的局部放大图Fig. 3 Partially enlarged view of Fig. 2(b)

图4 在含不同量Mg2+的试验溶液中,试样极化24 h后表面沉积层的XRD图谱Fig. 4 XRD patterns of surface deposits layer in test solutions containing different amounts of Mg2+ after 24 h of polarization
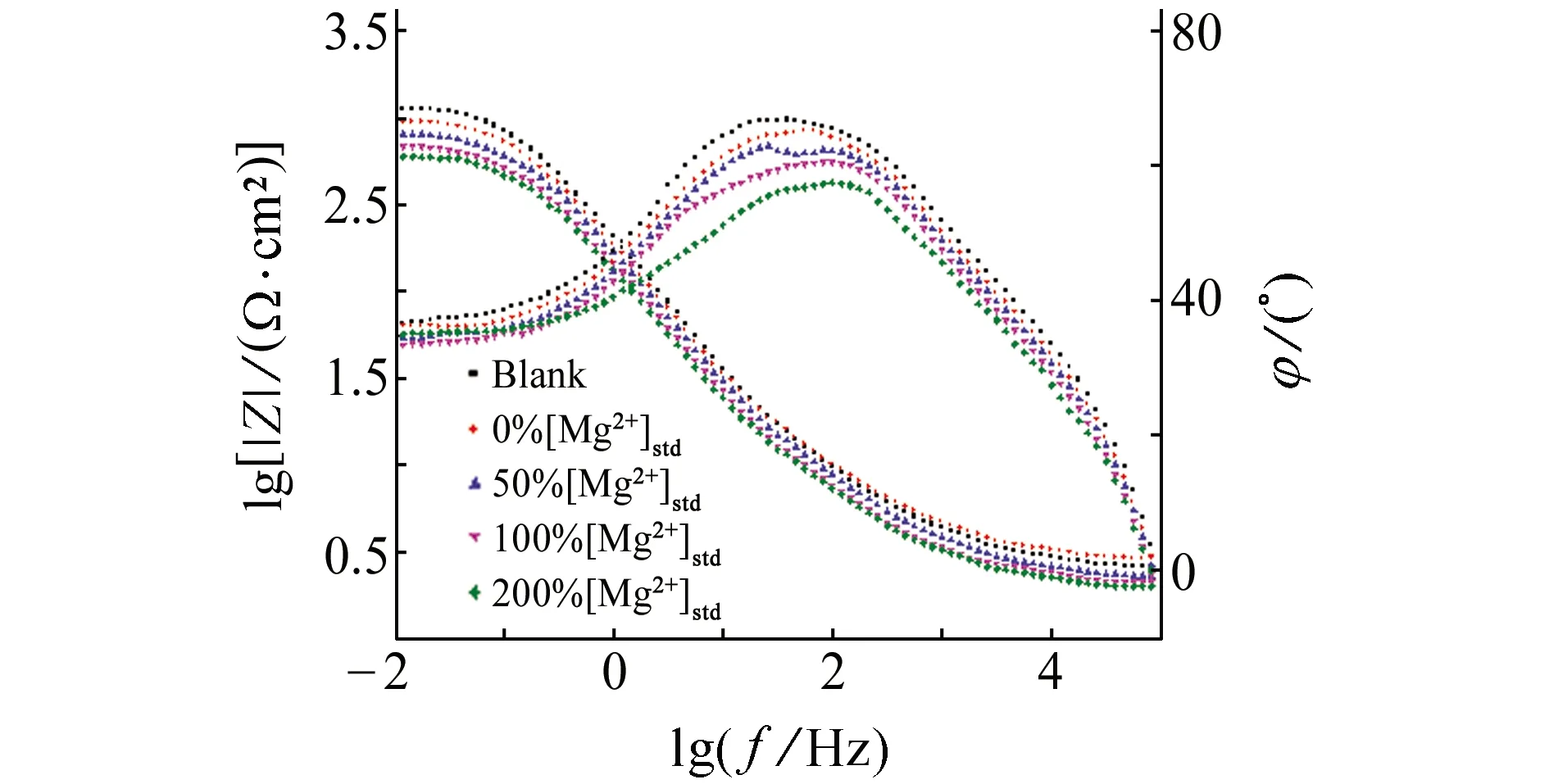
图5 在含不同量Mg2+的试验溶液中,试样极化24 h后的Bode图Fig. 5 Bode polt of samples in test solution containings different amounts of Mg2+ after 24 h of polarization
由图6可见:试样在含不同量SO42-的人工海水溶液中的计时电流曲线的变化趋势与图1类似,即随着SO42-含量的增大,电极表面钙质沉积层的沉积速率变慢,J/J0值也逐渐变大,这表明SO42-与Mg2+具有相同的作用,即阻碍钙质沉积层的形成。SO42-与Mg2+的不同之处在于极化初始阶段,在相同的试验条件下,SO42-含量为标准人工海水的200%时,电极的瞬时电流最大值相比于不含SO42-时的降低了接近20%,并且随着试验溶液中SO42-含量的增大,瞬时电流密度的最大值出现递减的现象。极化初期会引起电极表面氧化物的局部溶解,且极化初期不会形成钙质沉积层[11],因此可以排除以上两种因素的影响,故造成该现象的主要原因是极化初期试样表面形成了Mg2+的氢氧化物多孔沉积层。因此可以推断SO42-在阴极保护初期会促进Mg2+的氢氧化物沉积层的形成。

图6 在含不同量SO42-的人工海水溶液中,试样的电流变化曲线Fig. 6 Current change curves of samples in artificial seawater solution containing different amounts of SO42-
2.2.2 表面形貌
由图7和8可见:SO42-与Mg2+的作用相似,即随着SO42-含量的增加,钙质沉积层在电极表面的覆盖面积、晶核数量以及晶体尺寸都呈现减小的趋势。对于SO42-,产生这种现象的主要原因是SO42-的四面体结构体积较大,相比于CO32-的平面结构具有更大的表面能,这使得钙质层在沉积过程中的阻力较大[12]。SO42-与Mg2+最大的区别在于Mg2+改变了钙质沉积层的晶体结构和表面形貌,而SO42-仅改变了钙质沉积层的表面形貌。图7(d)中,电极裸露位置发现具有多孔性特征的Mg(OH)2沉积层,这与2.2.1节计时电流曲线的分析结果出现了矛盾,这主要是由于在恒电位极化过程中,极化初期具有较大的电流密度,且电极表面的活化区域较大,使得极化反应初期的吸氧反应进行较快,电极表面的pH很快达到Mg(OH)2沉积的临界值,但是随着极化反应的进行,垢层逐渐覆盖在电极表面,使得溶液中的氧气扩散到金属表面的过程受阻,导致吸氧反应被抑制,电极表面pH降低。CaCO3沉积层是稳定的,而Mg(OH)2沉积层并不稳定,当金属表面的pH低于9.5时,Mg(OH)2沉积层就会出现逆溶解现象[13]。
2.2.3 电化学阻抗谱
由图9可见:随着溶液中SO42-量的增加,阻抗模值呈现减小的趋势,这表明垢层对金属的保护效果减小。垢层的保护效果与垢层的多孔性有直接联系,SO42-含量增加,CaCO3垢层的沉积过程受到抑制,霰石晶体数量逐渐减少,钙质沉积层的覆盖面积和致密性均下降,并且垢层的多孔性变大,导致海水中的腐蚀性离子通过微观小孔渗透到电极表面的途径变多。综上可以得出结论,溶液中不含SO42-时,钙质沉积层多孔性最小,覆盖面积最大,对金属的保护作用也最好。

(a) 0% SO42-

(b) 50% [SO42-]std

(c) 100% [SO42-]std

(d) 200% [SO42-]std图7 在含不同量SO42-的试验溶液中,试样极化24 h后表面沉积层的SEM形貌Fig. 7 SEM morphology of surface deposit layers in test solutions containing different amounts of SO42- after 24 h of polarization
2.3 线性极化结果
在线性极化过程中,通常认为线性极化电阻与腐蚀电流密度成反比,较高的线性极化电阻表示自腐蚀速率较低,即电极表面钙质沉积层的密实度和孔隙率更好。对应用线性极化电阻来表征沉积层的密实度和孔隙率,李成杰[14]提出了保护因子概念,并得出如下公式:

(1)
式中:Fp为保护因子,其值的大小体现了沉积层的保护性能。Rp,0表示未极化时电极的线性极化电阻,Rp表示极化后的线性极化电阻,未极化时,Rp=Rp,0。
由图10可见:阴极保护过程中形成的钙质沉积层对于电极的保护作用随着海水中Mg2+和SO42-含量的增大而逐渐减小。当溶液中Mg2+和SO42-的含量为标准溶液的0%和50%时,Mg2+的保护因子明显大于SO42-的,随着溶液中离子含量的增加,SO42-的保护因子反而要大于Mg2+的。这主要是因为当Mg2+的含量为标准溶液的0%和50%时,电极表面钙质沉积层以方解石相晶体结构为主,有

图10 保护因子与离子含量的关系Fig. 10 Relationship between Fp and ion content
效增大了对金属基材的保护作用。而当Mg2+的含量为标准溶液的100%之后,电极的裸露面积明显大于SO42-含量为标准溶液的100%时的,从而使得钙质沉积层对金属基体的保护作用减弱。因此可以认为,当Mg2+和SO42-的含量为标准溶液的0%和50%时,增加Mg2+含量,生成垢层对金属基体的保护作用大于增大SO42-生成垢层的。当Mg2+和SO42-的含量为标准溶液的100%和200%时,增加SO42-含量,生成垢层对金属基体的保护作用大于增大Mg2+生成垢层的。由此可以推断,在恒电位阴极保护过程中,Mg2+和SO42-的含量为标准溶液的100%和200%时,Mg2+对于霰石相钙质沉积层形成过程中的抑制作用要大于SO42-的。
3 结论
(1) Mg2+和SO42-对于B30铜镍合金电极表面钙质沉积层晶核的形成和生长起到了明显的抑制作用,但增加SO42-含量会对Mg(OH)2沉积层的生成起到促进作用。
(2) Mg2+含量变化会引起电极表面钙质沉积层晶体结构和表面形貌发生变化,而SO42-含量变化仅改变钙质沉积层的表面形貌。
(3) 随着Mg2+和SO42-含量的增加,电极表面钙质沉积层的密实度和孔隙率逐渐恶化,同时对于电极的腐蚀防护能力也变差。
(4) Mg2+和SO42-的含量为标准溶液的100%和200%时,增加Mg2+含量,生成垢层对金属基体的保护作用大于增大SO42-生成垢层的。当Mg2+和SO42-的含量为标准溶液的100%和200%时,增加SO42-含量,生成垢层对金属基体的保护作用大于增大Mg2+生成垢层的,且在此条件下,Mg2+对于霰石相钙质沉积层形成的抑制作用明显大于SO42-的。

