碳氧化钼的制备及其氧还原性能研究
杨威威,丁 霞,董友珍
(盐城师范学院 化学与环境工程学院,江苏 盐城 224007)
随着石油燃料的能源消耗急剧增加以及相关的环境问题引起了人们对寻找清洁能源和可再生替代品的广泛研究关注。燃料电池是一种非常好的能量转换和储存装置,其中阴极氧还原反应(ORR)是限制质子交换膜燃料电池(PEMFC)和直接甲醇燃料电池(DMFC)性能的重要因素[1-3]。目前,铂(Pt)基催化剂仍然是适用最广泛和活性较好的催化剂材料,但是由于 Pt 价格昂贵,资源匮乏,严重阻碍了燃料电池的商业化进程[4-6]。同时甲醇渗透导致阴极 Pt 催化剂上发生电氧化,产生“混合电位”,且甲醇氧化产生的毒性中间体易使催化剂中毒,严重影响电池的输出性能[7-8]。因此,开发低成本、高性能和耐甲醇的阴极催化剂是 DMFC研究的重要课题。
过渡金属材料,如纳米金属,(氢)氧化物,硫化物,氮化物和碳化物,被认为是非贵金属电催化剂的良好选择[9-13]。其中,碳化钼材料因其类似Pt的d带电子结构,良好的化学稳定性和低成本而备受关注并具有特殊的前景。例如胡氏集团首次发现商业碳化钼表现出良好的HER活性[6]。为了提高钼的碳化物活性,进一步建立纳米级工程以暴露更多的催化活性位点,设计并确认具有各种纳米结构的碳化钼基材料是良好的HER催化剂。碳氧化钼在碱性介质中对HER和OER催化均具有优异的性能。CoMoC催化剂催化高活性,并显示出对HER和OER工艺进行电催化的长期稳定性。本文准备高温热解钼酸铵和三聚氰胺混合物制备碳氧化物,并用循环伏安和旋转圆盘电极测试其氧还原催化活性。
1 实验步骤
1.1 碳氧化钼催化剂的制备
称取16 mmol三聚氰胺和适量(NH4)6Mo7O24·4H2O(1 mmol、2 mmol和4 mmol)放置于研钵内研磨至全部混合均匀,去一定量于瓷舟内,再将装有样品的瓷舟放入管式炉内通氮气,以10 ℃/min的速度升温至700℃,并在700℃的氮气气氛下焙烧1.5 h,并对其结构和相关性能进行表征和测试。
1.2 修饰电极的制备
取上述样品在分析天平上称取0.0010 g加入1 mL 0.05 wt%的Nafion溶液超声震荡至均匀分散。在测试前将电极进行打磨处理,在打磨出加入少量Al2O3粉,将电极置于打磨处进行打磨,打磨完成后用蒸馏水冲洗并进行超声用N2气吹干,使用移液枪移6 μL配好的溶液滴至电极上方,带溶液干透即可进行测量。旋转圆盘电极(5 mm)处理方式同以上步骤,后使用移液枪移取20 μL的溶液滴在旋转圆盘电极上方,待干燥后进行测量。
2 结果与讨论
2.1 XRD谱图分析
图1是钼酸铵含量为2 mmol时合成碳氧化钼的X射线谱图。其中,34.49°、38.07°、39.55°、61.88°、69.77°、75.00°、76.71°归属于碳化钼Mo2C(PDF 65-8766),26.02°归属于二氧化钼MoO2(PDF 65-5787)。说明三聚氰胺和钼酸铵的热解后形成了Mo2C和MoO2的混合材料—碳氧化钼。

图1 Mo2C的X射线衍射谱图
2.2 扫描电镜图分析
通过图2可以看出,钼酸铵用量在1 mmol时合成的碳氧化钼大部分在2~5 μm左右大小,用量增加到2 mmol时,合成的碳氧化钼颗粒大小均匀,都在200~500 nm之间,当钼酸铵用量进一步增加到3 mmol时,合成的碳氧化钼又开始团聚,形成块状物,大小约是1~5 μm。

图2 钼酸铵在(A,B) 1 mmol、(C,D) 2 mmol和(E,F)4 mmol时合成样品的SEM图像
2.3 氧还原催化性能测试
图3是不同用量钼酸铵制备的样品在O2饱和KOH溶液中测试的循环伏安和线性扫描谱图。在图3A中可以看出,在氧气饱和的情况下,在0~0.7 V的电压范围内,都出现了明显的氧还原特征峰,而在氮气饱和的情况下则没有此峰,说明碳氧化钼样品对氧气有还原作用,且活性较好。钼酸铵用量为1、2和4 mmol时合成样品的还原峰电流密度和峰电压分别是0.310 mA·cm-2,-0.348 V;0.549 mA·cm-2,-0.377 V 和 0.387 mA·cm-2,-0.362 V。由此可以看出当钼酸铵含量为2 mmol时合成的碳氧化钼效果最好,这可能和此样品颗粒均匀有关。通过图3B可以看出,当转速为1600 r/min时,钼酸铵用量为2 mmol的样品的极限电流密度最大,其次是钼酸铵用量为2 mmol,用量为4 mmol时阻值最小。此结果和循环伏安结果一致,说明钼酸铵含量为2 mmol的样品氧还原活性最好。
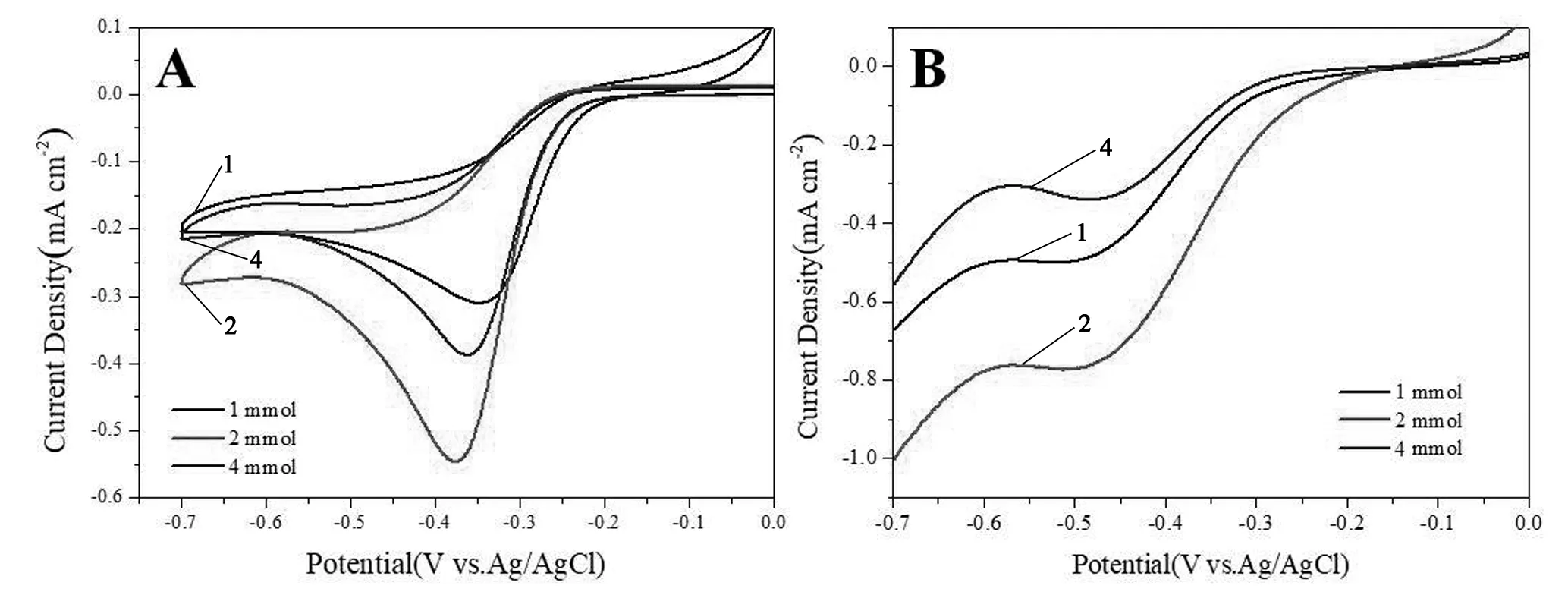
图3 钼酸铵在1 mmol、2 mmol和4 mmol时合成的样品在饱和O2的0.1 mol/L KOH溶液中的(A)循环伏安,扫描速度5 mV·s-1和(B)线性扫描谱图,转速1600 r/min
通过交流阻抗曲线来测量催化剂的界面电荷传输性能,得到图4。阻抗谱图中曲线的半径对应着阻抗数值的大小,半径越大,阻值越大。在图中可以看出当钼酸铵用量为2 mmol,半径最小,即样品的阻值最小,界面电荷传输性能最好。其次是钼酸铵用量为2 mmol,用量为4 mmol时阻值最大。这与循环伏安结构一致。
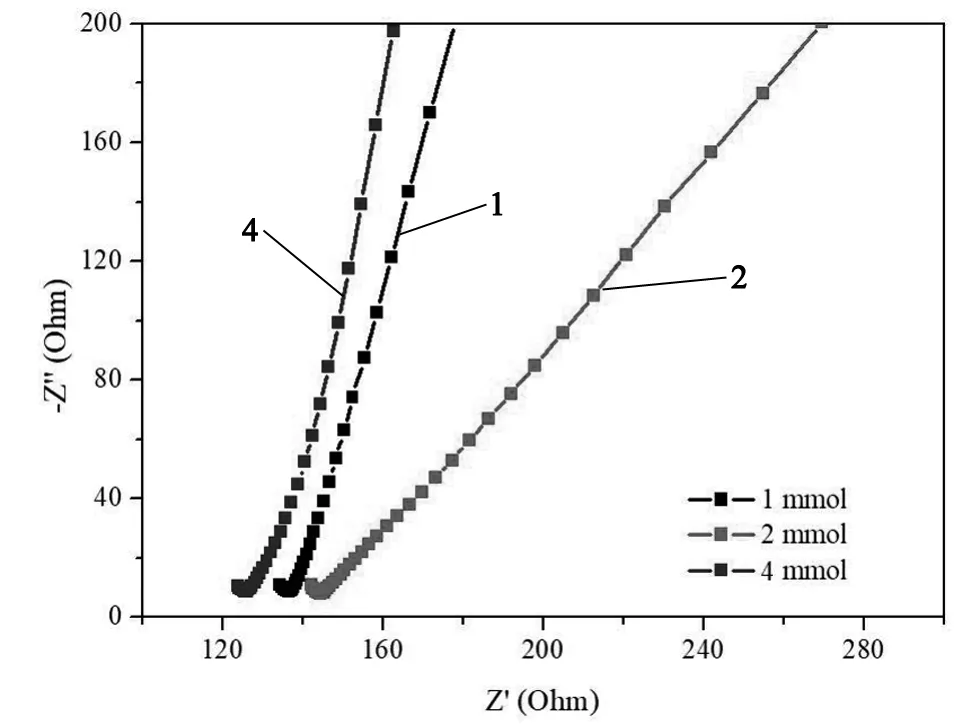
图4 钼酸铵在1 mmol、2 mmol和4 mmol时合成样品的交流阻抗Nyquist谱图
为了进一步对催化剂的氧还原反应的动力学进行研究,使用了旋转圆盘电极(RDE)。这种方法是将电极放置于氧气饱和的0.1 mol/L KOH溶液中,通过改变转速测得的数据。从图5可以发现当转速增大时,极限扩散电流密度也随之增大。且通过其对应的K - L曲线中也可以发现,K - L曲线内的数据有良好的线性关系,说明在不同的电压下,碳氧化钼的电子转移数相类似,符合一级反应动力学。此外,其他比例的图谱也有相同的特征。说明了用量为2 mmol的钼酸铵在700℃下退火生成的CoMoC的稳定性最好,且氧还原活性最好。

图5 钼酸铵在(A,B)1 mmol、(C,D)2 mmol和(E,F)4 mmol时合成的样品在饱和O2的0.1 mol/L KOH溶液中不同转速下的线性扫描曲线和对应的K-L曲线
2.4 抗甲醇性能测试
催化剂在用于燃料电池时,能否拥有良好的耐甲醇渗透性是判断催化剂的一个最重要的指标。我们通过在氧气饱和0.1 mol/L KOH溶液中加入3 mol/L甲醇,测试其抗甲醇能力,如图6所示。当钼酸铵的用量为2 mmol时,催化剂在有甲醇存在的情况下与没有甲醇的情况下没有明显的差别,而商业铂碳在有甲醇时几乎没有氧还原催化活性。说明碳氧化钼拥有较好的抗甲醇性能,在甲醇环境下有良好的应用前景。
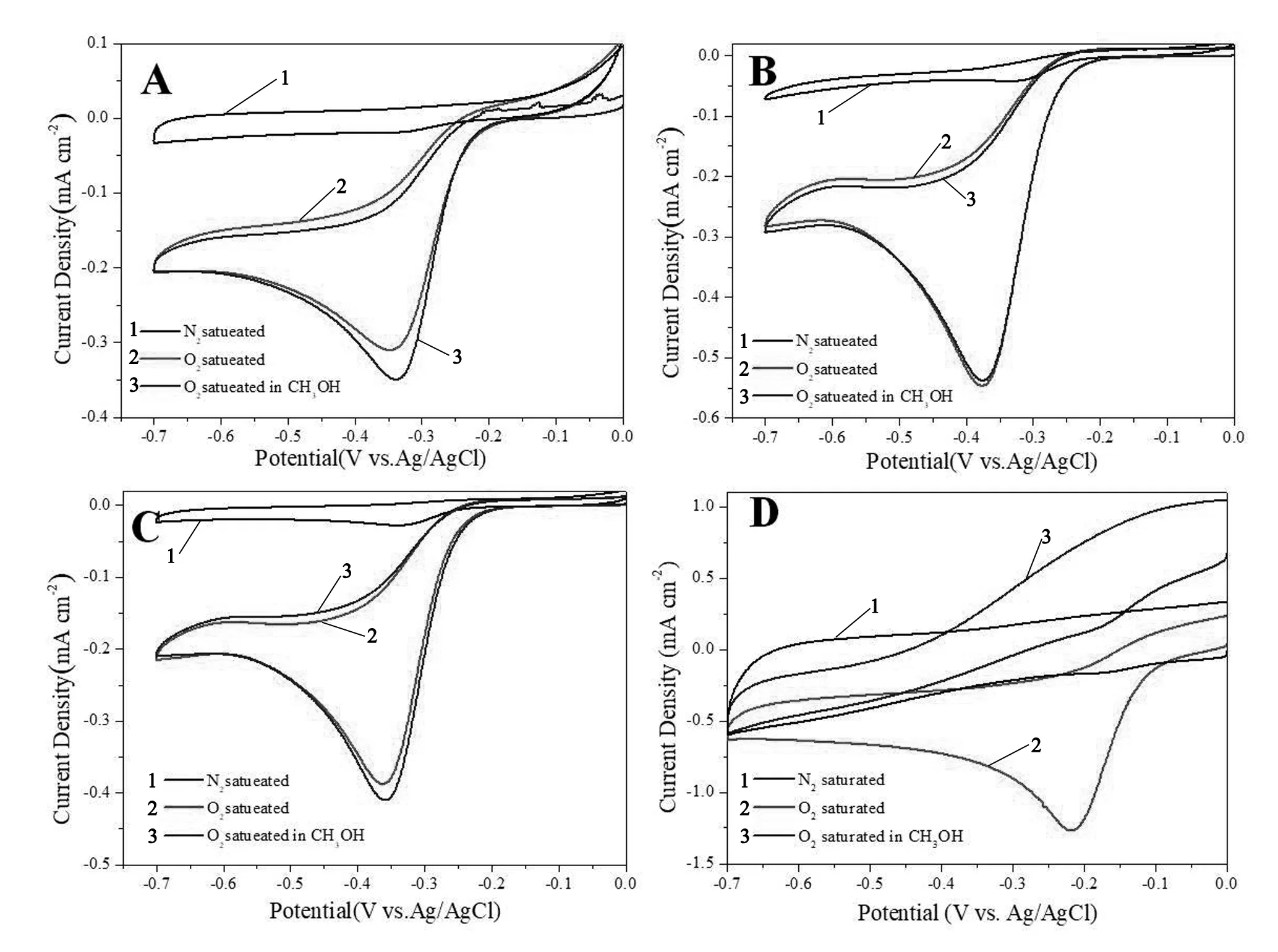
图6 钼酸铵在(A)1 mmol、(B)2 mmol、(C)4 mmol时合成的样品和(D)商业铂碳在饱和N2、O2和3 mol/L 甲醇的0.1 mol/L KOH溶液中循环伏安曲线,扫描速度5 mV·s-1
3 结论
本文以钼酸铵和三聚氰胺为原料,在氮气气氛中700℃高温热解得到碳氧化钼。通过改变钼酸铵的用量,得到不同的样品。经过一系列电化学测试可知用量为2 mmol时得到的碳氧化钼氧还原性能最好。

