添加剂作用下铁粉协同还原酸性硫脲浸金液中金的研究
郭学益 张磊 田庆华 李栋 衷水平











摘要:以酸性硫脲浸金液为原料,考察了添加剂作用下各因素对酸性硫脲浸金液中金还原率的影响,并确定了最优条件;同时开展了添加剂作用下铁粉还原酸性硫脲浸金液中金的动力学研究,考察了反应温度对金还原率及还原动力学的影响。结果表明:采用铁粉-亚硫酸钠体系协同还原酸性硫脲浸金液中的金,在最优条件下,金还原率达100.00 %;该体系不会引入新的杂质,可有效降低铁粉消耗,提高金回收率,尾液可循环使用;铁粉置换硫脲金的反应过程符合一级动力学模型,反应过程的速率控制步骤为扩散过程。
关键词:金;硫脲;铁粉;亚硫酸钠;还原;动力学
中图分类号:TF831 文章编号:1001-1277(2020)09-0081-05
文献标志码:Adoi:10.11792/hj20200913
引 言
黄金是一种非常重要的贵金属,具有很高的耐腐蚀和耐久性,可以作为战略储备,制造耐腐蚀的高精度产品[1]。一个多世纪以来,氰化浸出一直是黄金提取的主导工艺。近年来,由于氰化提金存在污染严重、周期长等问题,众多学者开展了非氰提金的研究[2-3]。硫脲作为众多非氰浸出剂中的一种,具有浸金速度快、清洁环保等优点,是一种理想的替代氰化物的浸金剂,如何从硫脲浸金液中高效回收金是推动硫脲提金工业化应用的重要一步[4]。
从含金溶液中回收金的方法主要有置换法、活性炭吸附法、树脂吸附法、胶结法、电沉积法等[5-8]。在酸性硫脲体系中,活性炭易吸附酸性硫脲溶液中铁、铜等杂质离子,导致其解吸困难、產品纯度低,同时活性炭存在易磨损和再生困难等缺点。溶剂萃取法和电沉积法不适合处理金浓度低的溶液,离子交换法的树脂存在选择性差、吸附容量低等问题。置换法具有经济高效、流程短、成本低等优点,常见的金属置换剂有锌、铁、铝、铜等;但在酸性硫脲浸金液中,锌粉还原性强,易与氢离子发生剧烈反应,不适合作为酸性硫脲体系的还原剂;而铜粉存在耗量大、成本高等缺点。考虑酸性硫脲体系元素组成和铁粉适中的还原性,铁粉更适宜作为酸性硫脲体系的还原剂,但单独使用铁粉还原酸性硫脲浸金液中的金仍存在金回收不彻底、铁粉耗量大等问题[9-10]。
基于此,本文首次创新性提出了以亚硫酸钠作为添加剂与铁粉协同还原酸性硫脲浸金液中金的方法,揭示铁粉-亚硫酸钠协同作用机理,系统开展铁粉-亚硫酸钠体系还原金的因素试验,确定最优参数,实现金的高效回收;同时对还原过程动力学进行研究,明确铁粉还原过程的动力学控制步骤,构建铁粉还原动力学模型。研究结果不仅为酸性硫脲浸金液中金的回收提供了一条高效、清洁、环保的途径,而且该技术原理具有一定的普适性,可以运用于其他领域的金属置换回收工艺中,同时该技术的提出丰富了置换回收工艺。
1 试验部分
1.1 试验原料与试剂
试验用硫脲浸金液为某黄金企业金精矿采用酸性硫脲浸金后所得滤液,金质量浓度为14.5 mg/L,其主要元素采用ICP-AES法测定,结果见表1。试验所用还原铁粉、亚硫酸钠均为分析纯试剂。
1.2 试验原理
铁是一种活泼金属,具有较强的还原性,可以将金属活泼性比铁弱的金属离子还原成单质。在酸性硫脲浸金液中,铁粉还原硫脲金的反应过程可用以下化学反应式表示:
由于Au[SC(NH2)2]+2/Au的标准电极电势E0=0.38 V, 远大于Fe2+/Fe的标准电极电势(E0=-0.44 V),所以在酸性硫脲溶液中,铁粉可以将Au[SC(NH2)2]+2/Au 中金的配合物还原成单质金。
1.3 试验方法
取250 mL硫脲浸金液于500 mL烧杯中,将烧杯置于恒温水浴中,加入一定量的还原铁粉和亚硫酸钠反应一段时间,溢出的二氧化硫可与碳酸钠溶液反应制备亚硫酸钠循环使用。反应结束后过滤,滤液用原子吸收光谱法分析其中的金,根据式(1)计算金还原率(α)。
式中:ρ0为硫脲浸金液中金质量浓度(mg/L);ρ1为还原后溶液中金质量浓度(mg/L)。
2 结果与讨论
2.1 亚硫酸钠用量
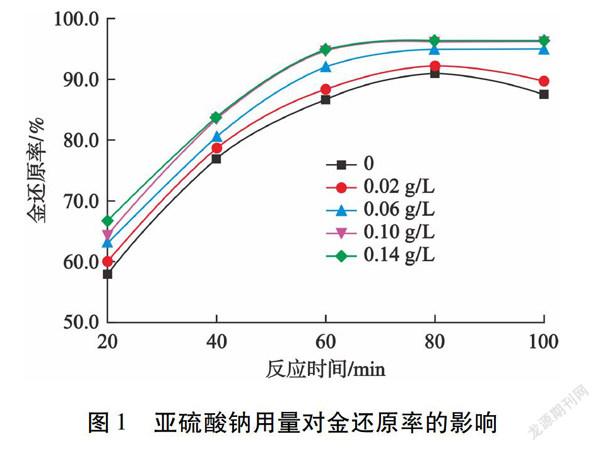
在铁粉用量0.2 g/L,反应温度25 ℃,搅拌转速400 r/min的条件下,考察亚硫酸钠用量对金还原率的影响,结果见图1。
由图1可知:加入亚硫酸钠可有效提高金还原率,当亚硫酸钠用量增加至0.10 g/L,反应时间为60 min时,金还原率可达94.9 %;继续增加亚硫酸钠用量,金还原率基本不再变化。当不添加亚硫酸钠和添加0.02 g/L亚硫酸钠时,出现金返溶现象。亚硫酸钠本身是一种还原性较强的还原剂,加入到还原体系中后,一方面能够和铁粉起到协同还原的作用,促进金的还原,使得在相同铁粉用量下,金还原率随着亚硫酸钠用量的增加而提高;另一方面,还原剂亚硫酸钠能够有效降低体系的氧化还原电位,从而降低溶解氧和三价铁离子对还原反应的影响,进而抑制金的重新溶解[11]。亚硫酸钠的加入能够有效提高金还原率,但当亚硫酸钠用量达到0.10 g/L以上时,继续增加亚硫酸钠用量,金还原率不再提高,且亚硫酸钠用量过高,在酸性溶液中易产生二氧化硫气体,因此亚硫酸钠用量为0.10 g/L较适宜。
2.2 反应温度
在铁粉用量0.2 g/L,亚硫酸钠用量0.10 g/L,搅拌转速400 r/min的条件下,考察反应温度对金还原率的影响,结果见图2。
由图2可知:适当升高反应温度有助于铁粉还原金,当反应温度升高至45 ℃,反应时间为80 min时,金还原率达99.5 %;继续升高反应温度至55 ℃ 时,金还原率呈现先增加后降低趋势。适当升高反应温度可加快溶液传质,硫脲金更容易迁移到铁粉表面与之反应,提高反应速率。但是,反应温度过高,亚硫酸钠在酸性溶液中的稳定性降低,部分二氧化硫逸出致使体系中亚硫酸钠质量浓度过低,出现金返溶现象。此外,较高反应温度下部分硫脲易氧化分解生成单质硫,其附着在铁粉表面阻碍还原反应进行[12]。综合考虑金还原率等因素,选取反应温度45 ℃较为合适。
2.3 搅拌转速
在铁粉用量0.2 g/L,亚硫酸钠用量0.10 g/L,反应温度45 ℃的条件下,考察搅拌转速对金还原率的影响,结果见图3。
由图3可知:金还原率随反应时间的延长而增加,搅拌转速对金还原反应速率的影响较还原率明显;当反应时间达到80 min时,不同转速条件下金还原率均达到100.0 %。提高搅拌转速可加速溶液中各离子的传质速度,利于反应的正向进行,反应速率更快[13]。综合考虑金还原率及生产成本等因素,选取搅拌转速300 r/min為最佳条件。
2.4 铁粉用量
在亚硫酸钠用量0.10 g/L,反应温度45 ℃,搅拌转速300 r/min的条件下,考察铁粉用量对金还原率的影响,结果见图4。
由图4可知:在不同铁粉用量下,金还原率都随反应时间的延长而提高。反应40 min后,铁粉用量分别为0.16 g/L、0.20 g/L和0.24 g/L时的金还原率差别较小;反应80 min后,金还原率均接近100.0 %。但是,当铁粉用量为0.12 g/L,反应至100 min时,金还原率相对较低。综合考虑生产成本等因素,选取铁粉用量0.16 g/L,反应时间80 min为最佳反应条件。
2.5 综合条件试验
通过条件试验研究,确定了铁粉-亚硫酸钠体系协同还原酸性硫脲浸金液中金的优化条件为:亚硫酸钠用量0.10 g/L,反应温度45 ℃,搅拌转速300 r/min,反应时间80 min,铁粉用量0.16 g/L。在此优化条件下,开展了铁粉-亚硫酸钠协同还原酸性硫脲浸金液中金的综合试验,共进行3组平行试验,结果见表2。
由表2可知:在优化条件下,3组试验中金还原率都接近100.00 %,还原效果较理想。在优化条件下,铁、金质量比仅为10.8,在保证金彻底回收的同时进一步降低了铁粉消耗,表明铁粉-亚硫酸钠协同还原体系可实现酸性硫脲浸金液中金的高效回收。
2.6 铁粉还原硫脲金动力学曲线
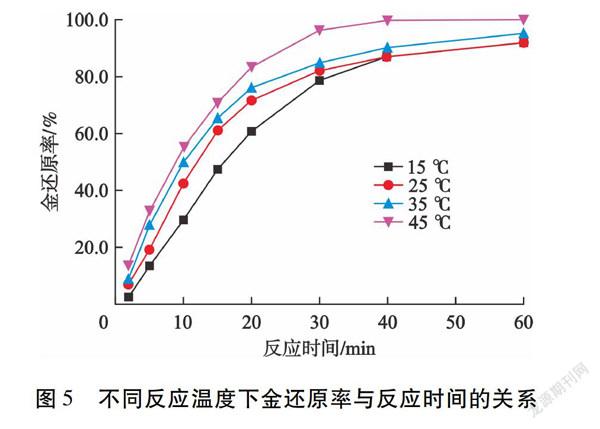
按照综合条件试验所述试验方法开展铁粉还原酸性硫脲浸金液中金的动力学研究,在铁粉用量0.16 g/L,搅拌转速300 r/min的条件下,分别考察了反应温度15 ℃、25 ℃、35 ℃和45 ℃对金还原过程的影响,得到了不同反应温度下金还原率随反应时间的变化关系,见图5。
由图5可知:随着反应时间的延长,不同反应温度下金还原率的变化趋势基本一致,金还原率随反应时间延长呈先升高后平缓的趋势。Greg Power等[14]研究表明,置换反应氧化还原电位相差大于0.36 V时,该置换反应可被认为受扩散过程控制,符合扩散控制动力学模型。Au[SC(NH2)2]+2/Au的标准电极电势E0=0.38 V, 而Fe2+/Fe的标准电极电势E0=-0.44 V,其差值远大于0.36 V,故推断铁粉置换酸性硫脲浸金液中的金受扩散过程控制。由于硫脲金在溶液中的扩散可通过加强搅拌消除,所以硫脲金扩散通过反应边界层到达铁粉表面的过程成为反应速率控制步骤。因此,铁粉置换硫脲金的反应速率与铁粉的比表面积及硫脲金在铁粉表面与溶液之间的边界层中的浓度梯度有关,故可用质量传递方程来描述置换反应的反应速率,见式(2)[15]。
式中:J为物质传输速率(mol/(L·s));M为摩尔质量(g/mol);V为溶液体积(L);c为在t时刻溶液中金浓度(mol/L);k1为具有t-1的量纲;A为铁粉表面积(m2/g);cs为铁粉表面反应界面处金浓度(mol/L)。
由于铁粉置换金热力学趋势大,扩散到铁粉表面的硫脲金立即与铁粉发生置换反应,故认为铁粉表面反应界面处金浓度为零,即认为式(2)中cs=0,所以金的置换反应过程可用式(3)的一级反应速率方程式来描述。
在置换反应过程中,认为铁粉表面积和溶液总体积随着反应的进行变化很小,即V和A是定值,而溶液中金浓度随着反应的进行不断减小,故将式(3)进行积分和变形后可得到式(4)和式(5)。
利用图5中的数据,采用式(5)的一级动力学模型进行拟合,每组反应温度下取反应前20 min时间段内溶液中金浓度对数与反应时间的关系进行拟合,结果见图6。
由图6可知:在不同的反应温度下,ln c关于反应时间都呈线性关系,且拟合直线的线性相关性很显著,相关系数均在0.989~0.999,可认为该反应遵循一级动力学反应,其他的金置换体系动力学研究也得到了类似的结果[16-18]。在反应温度15 ℃~45 ℃内,铁粉置换硫脲金体系中ln c
与反应时间t的线性回归方程见表3。
2.7 表观活化能和控制步骤
根据式(5),图6中不同反应温度下ln c关于反应时间的拟合直线的斜率绝对值就是反应的速率常数,速率常数(k)与反应温度之间的关系可用阿仑尼乌斯经验公式表示,见式(6)[18]。
式中:B为频率因子;E为表观活化能(kJ/mol);R为摩尔气体常数(J/mol·K);T为反应温度(K)。
将式(6)两边取对数,可得到直线方程式(7)。
根据式(7),利用表3中的各回归方程的斜率绝对值取对数得到ln k,并对1/T作图,可得到阿仑尼乌斯图,见图7。
由图7可知:各温度下的ln k与1/T拟合的线性关系较好,其回归方程为y=2.899-1.685x。根据回归方程和式(7)可计算得出,铁粉置换酸性硫脲浸金液中金的反应活化能为14.01 kJ/mol,其值小于20 kJ/mol, 故可认为该置换反应受扩散过程控制,硫脲金从溶液中迁移到铁粉表面的过程是置换反应的速率控制步骤[19]。因此,通过加强搅拌、提高温度、加入添加剂等能够促进溶液中离子的迁移,从而有效促进铁粉还原硫脲金的过程。
3 结 论
1)铁粉-亚硫酸钠体系可实现硫脲浸金液中金的高效还原。铁粉-亚硫酸钠体系协同还原酸性硫脲浸金液中金的最优条件:亚硫酸钠用量0.10 g/L,反应温度45 ℃,转速300 r/min,反应时间80 min,铁粉用量0.16 g/L。在此优化条件下,金还原率接近100.00 %。
2)通过进行动力学曲线拟合,确定了该置换反应过程符合一级动力学模型,反应过程的速率控制步骤为扩散过程;通过阿仑尼乌斯公式,计算出铁粉置换硫脲金的反应活化能为14.01 kJ/mol。
[参 考 文 献]
[1] 雷永康,李青,万宏民,等.微细粒含砷难处理金矿石提金工艺研究[J].黄金,2017,38(1):56-60.
[2] 郭学益,张磊,田庆华,等.氧压渣非氰体系浸金及其机理[J].中国有色金属学报,2020,30(5):1 131-1 141.
[3] 李骞,董中林,张雁,等.含硫砷含碳金精矿提金工艺研究[J].黄金,2016,37(11):41-45.
[4] GUO X Y,ZHANG L,TIAN Q H,et al.Stepwise extraction of gold and silver from refractory gold concentrate calcine by thiourea[J].Hydrometallurgy,2020,194:105330.
[5] 叶跃威,杨建国.用锌粉从高铜铅含氰贵液中置换金银[J].湿法冶金,2007(3):150-153.
[6] KARAVASTEVA M.Kinetics and deposit morphology of goldcemented on magnesium,aluminu,zin,iron and copper from ammonium thio-sulfate-ammonia solutions[J].Hydrometallurgy,2010,104(1):119-122.
[7] 余洪,胡显智,字富庭,等.置换法回收硫代硫酸盐浸金液中金的研究进展[J].稀有金属,2015,39(5):473-480.
[8] 王为振,王云,常耀超,等.铁粉还原法从含金滤液中回收金银铜[J].有色金属(冶炼部分),2016(11):43-44,56.
[9] 杨坤,梁可.金平和巍山精金矿氰化液中金的回收方案比选[J].有色金属设计,2014,41(3):26-29.
[10] 吳永胜.金置换率下降原因分析及对策[J].有色金属科学与工程,2011,2(5):36-40.
[11] 刘建.表面活性剂对金属置换硫脲金络离子溶液中金的影响[J].稀有金属,2001(6):448-451.
[12] 马方通,高利坤,董方,等.硫脲浸金及置换法从硫脲溶液中回收金研究现状[J].湿法冶金,2017,36(4):257-261,270.
[13] 李永芳.置换法回收硫脲和硫代硫酸盐中的金[D].新乡:河南师范大学,2012.
[14] POWER G,RITCHIE I M.A contribution to the theory of cementation(metal displacement)reactions[J].Australian Journal of Chemistry,1976,29(4):699-709.
[15] ZHANG H G,DOYLE J A,KENNA C C,et al.A kinetic and electrochemical study of the cementation of gold onto mild steel from acidic thiourea solutions[J].Electrochimica Acta,1996,41(3):389-395.
[16] WANG Z K,CHEN D H,CHEN L.Gold cementation from thiocyanate solutions by iron powder[J].Minerals Engineering,2007,20(6):581-590.
[17] ESMAEIL J,AHMAD G.Challenges with elemental sulfur removal during the leaching of copper and zinc sulfides,and from the residues:a review[J].Hydrometallurgy,2017,171(1):333-343.
[18] WANG Z K,LI Y F,YE C L.The effect of tri-sodium citrate on the cementation of gold from ferric/thiourea solutions[J].Hydrometallurgy,2011,110(1/2/3/4):128-132.
[19] WANG Z K,CHEN D H,CHEN L.Application of fluoride to enhance aluminum cementation of gold from acidic thiocyanate solution[J].Hydrometallurgy,2007,89(3/4):196-206.
Synergistic reduction of gold in acidic thiourea leaching
solution by iron powder under the effect of additives
Guo Xueyi1,2,Zhang Lei1,2,Tian Qinghua1,2,Li Dong1,2,Zhong Shuiping3
(1.School of Metallurgy and Environment,Central South University;
2.Cleaner Metallurgical Engineering Research Center,China Nonferrous Metals Industry Association;
3.Zijin Mining and Metallurgy Research Institute)
Abstract:The experiment uses acidic thiourea leaching solution as raw material,and investigates the effects of various factors on gold reduction rate in acidic thiourea leaching solution under the effect of additives and the optimal conditions are determined.At the same time,the kinetic study on the reduction of gold in acidic thiourea gold leaching solution by iron powder under the effect of additives is carried out,and the effects of reaction temperature on gold reduction rate and reduction kinetics are investigated.The result shows that synergistic system of iron power-sodium sulfite for gold reduction in acidic thiourea leaching solution can achieve 100.00 % reduction of gold under optimal conditions;the system will not introduce new impurities,can effectively reduce iron powder consumption,improve gold recovery rate while the tail solutions can be recycled;the reaction process of gold thiourea replacement by iron powder conforms to the first-order kinetic model and the rate control step of the reaction process is the diffusion process.
Keywords:gold;thiourea;iron powder;sodium sulfite;reduction;kinetics
收稿日期:2020-07-30; 修回日期:2020-08-20
基金项目:湖南省环保厅环境保護科研课题;国家优秀青年科学基金项目(51922108);湖南省杰出青年基金项目(2019JJ20031)
作者简介:郭学益(1966—),男,湖南长沙人,教授,博士生导师,博士,研究方向为有色金属资源循环及先进材料制备等;主持完成包括国家及省部级科技计划项目、国家自然科学重点/面上基金等数十项课题,在有色金属资源循环及先进材料制备等领域拥有系列原创性成果;获国家科技进步奖3项,省部级科技进步奖15项;授权发明专利90余项,发表SCI论文130余篇,EI论文240余篇;长沙市岳麓区麓山南路932号,中南大学冶金与环境学院,410083;E-mail:xyguo@csu.edu.cn
*通信作者,E-mail:qinghua@csu.edu.cn,0731-88876255

