某医院静脉用药调配中心工作人员抗肿瘤药物职业暴露评估研究
尹红梅


[摘要]目的 评估某医院静脉用药调配中心工作人员的抗肿瘤药物职业暴露情况,旨在进一步优化静脉用药调配中心抗肿瘤药物调配工作流程及管理。方法 选取某医院静脉用药调配中心2019年3月1~25日工作人员34例,根据是否接触抗肿瘤药物分为暴露组(18例)和控制组(16例),收集各工作环节中物体表面和个人防护用物的擦拭样本及人员生物样本,以环磷酰胺(CP)和阿糖胞苷(CAR)为标志物,进行环境监测和生物监测,比较污染程度。结果 环境监测显示,静脉用药调配中心各工作环节中物体表面均存在不同程度的CP和CAR污染,最为严重的是生物安全柜操作台面,CP和CAR的平均残留浓度分别为(3.303±0.701)ng/cm2、(0.838±0.247)ng/cm2;其次为混合调配间门把手,CP和CAR的平均残留浓度分别为(1.629±0.142)ng/cm2、(0.108±0.026)ng/cm2。生物监测显示,暴露组人员淋巴细胞凋亡率高于控制组,差异有统计学意义(P<0.05);暴露组人员高剂量尿液浓缩致TA98与TA100突变阳性率高于控制组,差异有统计学意义(P<0.05)。结论 静脈用药调配中心各工作环节的环境存在不同程度抗肿瘤药物污染,可能会对工作人员造成一定的损伤。
[关键词]静脉用药调配中心;抗肿瘤药物;职业暴露;环境监测;生物监测
[中图分类号] R979.1 [文献标识码] A [文章编号] 1674-4721(2020)6(c)-0179-04
Study of occupational exposure risk in workers to anticancer drugs in pharmacy intravenous admixture service of a hospital
YIN Hong-mei
Pharmacy Intravenous Admixture Service, Qilu Hospital of Shandong University, Shandong Province, Ji′nan 250012, China
[Abstract] Objective To evaluate occupational exposure risk in workers to anticancer drugs in pharmacy intravenous admixture service (PIVAS) of a hospital, and to further optimize the admixture workflow and management of anticancer drugs in PIVAS. Methods A total of 34 workers in PIVAS of a hospital from March 1 to 25 of 2019 were selected and divided into the exposed group (18 cases) and the control group (16 cases) according to whether they were exposed to antitumor drugs. Wiping samples were collected from the surface of the object in the work environment and personal protective materials, and biological samples were collected from the selected workers. To investigate the level of contamination, environmental and biological effects were monitored with cyclophosphamide (CP) and cytarabine (CAR) as markers. Results Environmental monitoring results suggested that different pollution levels of CP and CAR existed in the surface of different objects in the work environment of PIVAS. The most polluted place was the countertop of biosafety cabinets with CP residual concentration of (3.303±0.701) ng/cm2 and CAR residual concentration of (0.838±0.247) ng/cm2, followed by the doorknobs of deploy rooms with CP residual concentration of (1.629±0.142)ng/cm2 and CAR residual concentration of (0.108±0.026)ng/cm2. Biological monitoring results indicated that the total apoptosis rate of lymphocytes in the exposed group increased compared with the control group with statistical significance (P<0.05). The positive rate of TA98 and TA100 mutations caused by high-dose urine concentration in the exposed group was higher than that in the control group with statistical significance (P<0.05). Conclusion Different levels of anticancer drug contamination exist in the work environment of PIVAS, which may cause certain damage to workers.
[Key words] Pharmacy intravenous admixture service; Anticancer drugs; Occupational exposure; Environmental monitoring; Biological monitoring
近年来,随着各类肿瘤发病率的持续升高,越来越多的抗肿瘤药物被开发出来并应用于临床[1-2]。此类药物大多是细胞毒性药物,在杀伤和抑制癌细胞的同时,对正常组织也有一定损伤,可通过皮肤接触或吸入等方式造成包括生殖系统、泌尿系统、肝肾系统的毒害,具有致癌、致畸及致突变等毒性作用[3-5]。医院静脉用药调配中心(pharmacy intravenous admixture service,PIVAS)的工作人员每天在进行摆药、混合调配、复核包装时不可避免地暴露于各类抗肿瘤药物。长期接触抗肿瘤药物的人员随着时间延长可导致体内有一定蓄积,对机体产生某些损伤,如骨髓抑制、白细胞下降、脱发、消化道症状、角膜损害、皮膚过敏、肾功能损害、细胞遗传物质染色体和脱氧核糖核酸损伤等[6-8]。目前,国内越来越多的医院已经建立了PIVAS,但抗肿瘤药物调配工作流程缺乏统一的规范,防护管理体制不成熟,工作人员正面临着较大的职业暴露风险[9-12]。本研究通过探索某医院PIVAS工作人员抗肿瘤药物职业暴露情况,旨在进一步优化PIVAS抗肿瘤药物调配工作流程及管理,为加强工作人员的防护提供依据。
1资料与方法
1.1一般资料
选取某医院PIVAS 2019年3月1~25日工作人员34例,根据接触抗肿瘤药物的情况分为两组,接触抗肿瘤药物人员共18例为暴露组,非接触抗肿瘤药物人员共16例为控制组。所有工作人员统一接受问卷调查。纳入标准:①工作年限>3年;②无严重吸烟史、饮酒史;③饮食习惯健康,不经常食用油炸或烟熏食品。排除标准:本人拒绝参加调研。暴露组中,男6例,女12例;年龄22~32岁,平均(24.8±1.4)岁;工作年限4~15年,平均(6.8±1.7)年。控制组中,男5例,女11例;年龄25~35岁,平均(27.5±1.1)岁;工作年限6~16年,平均(9.8±1.6)年。两组受试者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审核批准,且所有参与研究的工作人员在项目开始前均已签署知情同意书。
1.2擦拭样本收集
选择PIVAS使用频率较高且具有较高挥发性及渗透性的环磷酰胺(cyclophosphamide,CP)和阿糖胞苷(cytarabine,CAR)作为环境监测标记物,所有环境擦拭样本均在抗肿瘤药物调配结束后且未进行清场前取样。每个取样点共取样3次(选择不同3天的同一时间与同一地点取样)。使用乙腈-0.1%甲酸溶液(80∶20,v/v)10 ml为预湿溶液。
1.2.1环境擦拭样本收集 用一次性洁净的平头镊子夹取滤纸(采用面积为2 cm×2 cm的滤纸),对指定区域进行定面积的擦拭(10 cm×10 cm,以预先制作好的塑料框架确定),擦拭顺序为从上至下、从左至右擦拭一遍。指定区域是指PIVAS调配抗肿瘤药物的生物安全柜操作台面、混合调配间治疗车、靠近生物安全柜20 cm处的地面、摆药盒。不易计算面积的地点如传递门把手、混合调配间门把手、冰箱门把手、电话则直接用预湿的滤纸进行擦拭,并估算各处面积。
1.2.2个人防护用物擦拭样本收集 留取抗肿瘤药物相关操作使用后的最内层、最外层手套和口罩,做好标记并记录佩戴时间。用滤纸对手套的内侧进行擦拭,擦拭顺序为从上至下、从左至右擦拭一遍,采样过程注意避免交叉污染。
1.3生物样本收集
1.3.1血液样本 暴露组采血时间为早晨上班前10 min,控制组采血时间与暴露组同时进行。采集血样2 ml,置于抗凝采血管中,处理后用于后续测定。血液样本收集完成后注意将采血时间与完成流式测定之间的时间控制在12 h内。
1.3.2尿液样本 暴露组与控制组成员留取尿液样本150 ml置于一次性塑料瓶中,随后定量量取120 ml经XAD-2树脂进行浓缩,用于尿液浓缩致突变性的测定。当第一次留取的尿液≥120 ml时,量取120 ml用于尿浓缩物致突变实验,不足的人员可合并后一次的尿液。留取尿液样本时间从上班开始计时,留取至12 h,记录每人每次留尿的时间及尿液体积。
1.4样本测定方法
1.4.1擦拭样本测定方法 采用超高效液相串联质谱法(ultra-high performance liquid chromatography-tandem mass spectrometry, UPLC-MS/MS)测定擦拭样本中CP和CAR的残留浓度[13-14],定量下限浓度为0.625 ng/ml。
1.4.2生物样本测定方法 血液样本采样后立即进行淋巴细胞的提取,提取方法见淋巴细胞提取试剂盒说明书,淋巴细胞试剂盒处理染色后经流式细胞仪检测凋亡率[15]。尿液样本采用XAD-2树脂进行浓缩[16],采用UPLC-MS/MS法测定CP浓度,设定下限浓度为20 pg/ml。采用酶联免疫吸附测定检测8-羟基脱氧鸟苷(8-hydroxydeoxyguanosine,8-OHdG)水平。采用细菌(鼠伤寒杆菌TA98和TA100菌株)通过微量波动试验进行回复突变实验,检测尿液浓缩物的致突变性[17]。
1.5观察指标及评价标准
比较PIVAS各工作环节中物体表面CP和CAR的平均残留浓度;比较个人防护用物CP和CAR的平均残留量;比较两组受试者淋巴细胞凋亡率、尿液8-OHdG浓度和尿液浓缩物的致突变性。尿液致突变试验中,低剂量:100 μl尿浓缩液含原尿2.5 ml;中剂量:100 μl尿浓缩液含原尿5 ml;高剂量:100 μl尿浓缩液含原尿10 ml。
1.6统计学方法
采用SPSS 19.0統计软件建立数据库并进行统计学处理,计量资料以均数±标准差(x±s)表示,组间比较采用t检验;计数资料采用Fisher确切概率法进行统计分析,以P<0.05为差异有统计学意义。
2结果
2.1环境监测
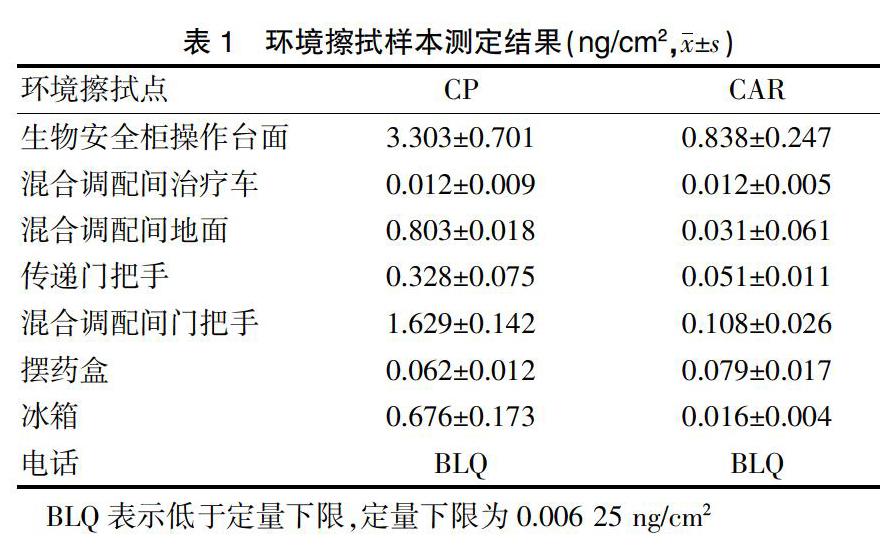
2.1.1环境擦拭样本测定结果 环境擦拭样本测定结果显示,PIVAS生物安全柜操作台面、混合调配间治疗车、摆药盒、混合调配间地面、混合调配间门把手、传递门把手、冰箱把手、电话等均存在不同程度的CP和CAR污染。污染程度最为严重的是生物安全柜操作台面,CP和CAR平均残留浓度分别为(3.303±0.701)ng/cm2、(0.838±0.247)ng/cm2;其次是混合调配间门把手,CP和CAR的平均残留浓度分别为(1.629±0.142)ng/cm2、(0.108±0.026)ng/cm2(表1)。
2.1.2个人防护用物测定结果 个人防护用物测定结果显示,抗肿瘤药物相关操作使用后的口罩和手套内侧均检测到不同程度的CP和CAR残留(表2)。
2.2生物监测
2.2.1两组研究对象淋巴细胞凋亡率和尿液8-OHdG 浓度的比较 暴露组淋巴细胞凋亡率和尿液8-OHdG 浓度均高于控制组,差异有统计学意义(P<0.05)(表3)。
2.2.2两组研究对象不同剂量尿浓缩液致突变率的比较
两组低剂量、中剂量尿液浓缩致TA98与TA100突变阳性率比较,差异无统计学意义(P>0.05);暴露组高剂量尿液浓缩致TA98与TA100突变阳性率高于控制组,差异有统计学意义(P<0.05)(表4)。
3讨论
抗肿瘤药物可通过皮肤接触或吸入方式进入体内,对调配人员造成潜在的健康损害,因此职业防护受到越来越多的关注[18-19]。本研究根据国内外相关文献报道,结合抗肿瘤药物在PIVAS的使用现况,选取挥发性和渗透性较强的CP和CAR作为监测标记物,对PIVAS各工作环节的物体表面开展了环境监测,结果提示抗肿瘤药物的污染已经不仅仅局限在混合调配区域,也有向其他区域扩散的趋势。抗肿瘤药物由于本身存在一定的挥发性,在混合调配过程中会从生物安全柜飘散出来,与空气中的灰尘或颗粒吸附混合,分布在工作环境中,存在转移性污染的风险。混合调配工作结束后,周围环境的清场、清洁、消毒工作不容忽视,必须严格的按照规范执行到位,加强日常的监督管理。
在PIVAS现有的防护措施下,大部分工作人员的口罩和手套的内侧均能够检测到不同程度的抗肿瘤药物的残留。这与工作人员的操作规范性、更换个人防护用物的时间等有密切关系,因此提高混合调配人员的个人防护意识至关重要。在进行抗肿瘤药物混合调配前,工作人员应先进行个人防护用物规范使用的培训,考核合格后再上岗,在操作过程中应最大程度地减少意外事件的发生,避免抗肿瘤药物溢出。
发达国家对抗肿瘤药物调配工作的职业防护很重视,相关研究表明在工作中长期接触抗肿瘤药物的医务人员被检测出某些生物学指标改变[20]。本研究生物监测结果显示,暴露组人员淋巴细胞凋亡率较控制组要高(P<0.05),尿液8-OHdG浓度显著升高(P<0.05);尿液浓缩致突变率较控制组也有增高趋势,且高剂量时差异有统计学意义(P<0.05)。PIVAS工作人员由于长期频繁地接触抗肿瘤药物,可能会对身体产生一定的影响,但是至今仍然没有导致疾病发生的生物学指标临界值。
综上所述,很多的职业暴露风险是可以避免的,这需要管理人员对PIVAS抗肿瘤药物的调配工作流程进一步优化,混合调配结束后做好清场、清洁、消毒工作,避免抗肿瘤药物转移性污染,提高工作人员的个人防护意识,加强个人防护用物的规范使用,尽最大限度的减少抗肿瘤药物的暴露,使工作人员的职业损伤降到最低。
[参考文献]
[1]Siegel RL,Miller KD,Jemal A.Cancer statistics,2018[J].CA Cancer J Clin,2018,68(5):7-30.
[2]王奎鹏.某院2014-2016年抗肿瘤药物应用分析[J].黑龙江医学,2018,42(6),599-601.
[3]Kroschinsky F,St■lzel F,von Bonin S,et al.New drugs, new toxicities:severe side effects of modern targeted and immunotherapy of cancer and their management[J].Critical Care,2017,21(1):89.
[4]Tewari D,Rawat P,Singh PK.Adverse drug reactions of anticancer drugs derived from natural sources[J].Food Chem Toxicol,2019,123:522-536.
[5]Apostoli P,Catalani S,Bergonzi R,et al.Carcinogenicity of antineoplastic drugs:classification,protection and prevention,use and evidence[J].G Ital Med Lav Ergon,2014,36(1):5-16.
[6]Yanagawa C.Measures for the disposal of non-regulated alternative medical wastes safe handling of eytotoxie drugs[J].Rinsho Byori,2000,112:120-128.

