浮选-消解法提取土壤中的微塑料
陈娴 顾轩宁 包丽婧 马璇 潘亚男 马闪闪 穆瑛慧
摘 要:土壤作为微塑料(MPs)最重要的“汇”开始逐渐受到关注,但是,由于土壤基质的复杂性,目前尚未建立土壤MPs监测的标准化方法。探讨浮选-消解法提取土壤中两种典型MPs-聚乙烯(PE)和聚苯乙烯(PS)的效果,重点考察5种消解体系: KOH、H2O2、HNO3、H2O2+H2SO4和H2O2+HNO3。结果显示,H2O2的消解效果最佳,其他消解方法会造成土壤有机质去除不完全或引起MPs颗粒表观形貌和表面微观特征的变化。采用饱和NaCl溶液浮选和H2O2消解联用,可有效提取土壤中两种粒径(0.85 mm和0.075 mm)的PE和PS,回收率在83%~94%,且大粒径MPs的回收率更高。
关键词:土壤;微塑料;浮选;消解;提取
中图分类号:X55 文献标识码:A 文章编号:2095-7394(2020)04-0001-07
作为一种新型污染物,微塑料(MPs<5 mm,包含纳米塑料NPs<0.1 μm)污染已成为第二大环境和生态问题。相比于海洋,目前对于土壤MPs的研究还很匮乏。事实上,土壤是一个比海洋更大的MPs“储存库”,也是海洋MPs的主要来源[1]。污泥施用、农用膜使用和土地填埋等造成了土壤中MPs的普遍污染。但是,目前仅有少数研究报道了土壤MPs的污染状况,其颗粒丰度范围在1.3~42 960个 /kg[2-6],在工业区土壤中甚至检出了高达7%的MPs[7]。有证据显示,MPs能通过陆地食物链传递,从而增加人类暴露的风险[8]。因此,有必要开展对土壤MPs污染状况的调查,以明确其潜在环境风险。
由于受到土壤质地、有机质及团聚体结构的影响,从土壤中分离和鉴定微塑料要比水和沉积物中更加困难,这也是限制土壤MPs污染研究的主要原因。由于MPs的密度较小,一般在0.8~1.4 g/cm3,所以密度分离法是最常用的提取方法。常用的浮选液有饱和NaCl (密度为1.2 g/cm3 )、ZnCl2(1.5~1.7 g/cm3)和NaI(1.6 ~1.8 g/cm3)以及水[9-10]。因此,分离效果的好坏主要取决于MPs和杂质的密度差。但是,当从富含有机质的土壤中分离MPs时,由于土壤有机质和MPs的密度相近(1.0~1.4 g/cm3),所以采用密度提取无法有效分离出有机质,需要进一步去除有机质。在水、底泥和生物样品中常用酸(如HNO3)、碱(如KOH)和氧化(如H2O2)及酶(如蛋白酶)进行消解[11]。对于这些技术的处理效率还没有系统评价。相比于浮选-消解法,直接提取技术,如加压液体萃取[7]、快速加熱法[5]和热解[12]等虽然省略了分离等样品前处理,却破坏了MPs的颗粒信息[13]。因此,土壤MPs污染调查的首要问题是探索MPs的分析检测方法,以保证较高的回收率和准确率。
笔者选用浮选-消解法分离和提取土壤样品中的典型MPs,重点考察不同消解体系对土壤基质的去除效果和对MPs表观特征的影响。拟探讨一种操作简单、经济、准确度高且对环境影响小的土壤MPs提取方法。
1 材料和方法
1.1 供试土壤
供试土壤采自常州市武进区农田表层(0~20cm),位于N31°41'26''、E119°51'37''。土壤经自然风干后,去除碎石、砂砾及动植物残体等杂质,研磨后过10目(2 mm)孔径尼龙筛。土壤基本理化性质如下:pH 6.53(0.01M CaCl2 :土= 5 : 1),阳离子交换量21.4 cmol(+) kg-1,有机质1.04%,壤土(黏粒、粉沙粒和沙粒含量分别为14.3%、42.3%和43.4%)。
1.2 供试MPs
选择了两种类型的MPs,聚乙烯(PE)和聚苯乙烯(PS),粒径大小包括20目(0.85 mm)和200目(0.075 mm),均购自南京卡佛科学仪器有限公司。供试MPs的选择依据是:土壤MPs污染调查发现,PE是土壤中最主要的MPs类型[2, 3, 14];PS占了塑料总需求量的90%,并且在环境中被普遍检出,在很多研究中被用作MPs的代表[15];土壤中检测到的MPs大小主要集中在<1 mm的范围[2, 4, 14]。
1.3 重力浮选
在50 mL离心管中加入0.1 g PE或PS和10.0 g土壤,混合均匀后加入40 mL的饱和NaCl溶液,超声(40 kHz)10 min,室温下以150 r/min振荡30 min,5 000 r/min离心20 min后将上清液和悬浮物倒入烧杯中。将上述提取过程重复2次,合并提取液,真空抽滤至孔径10 μm的尼龙膜上,并用去离子水冲洗烧杯内壁和布氏漏斗。
1.4 消解
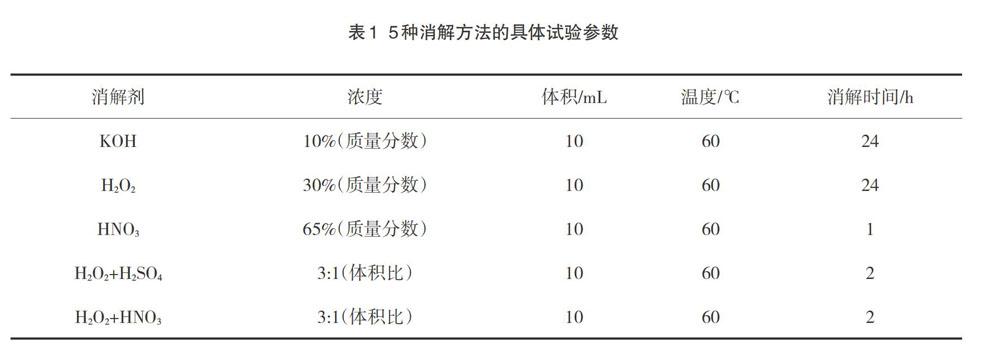
将滤渣转移至50 mL的带盖消解管中,加入10 mL的消解液,将消解管置于SH230N石墨消解仪中进行消解,具体试验条件见表1。消解后,用去离子水进行稀释和冲洗管壁,真空抽滤至孔径10 μm尼龙膜上,随后将滤膜放入铺有锡箔纸的玻璃培养皿中,于60 ℃烘箱中干燥。将消解后的MPs进行电镜扫描(SEM,Hitachi S-3400N扫描电子显微镜),观察MPs的表面微观特征。消解体系对比实验选用20目MPs作为研究对象。
1.5 数据分析
回收率结果均用平均值 ± 标准偏差(n = 3)表示。采用独立样本t检验用于评价两种粒径MPs的回收率差异。显著性水平P设定为0.05。所有统计分析在微软IBM SPSS 19.0软件上进行。
2 结果与讨论
2.1 土壤中MPs的提取
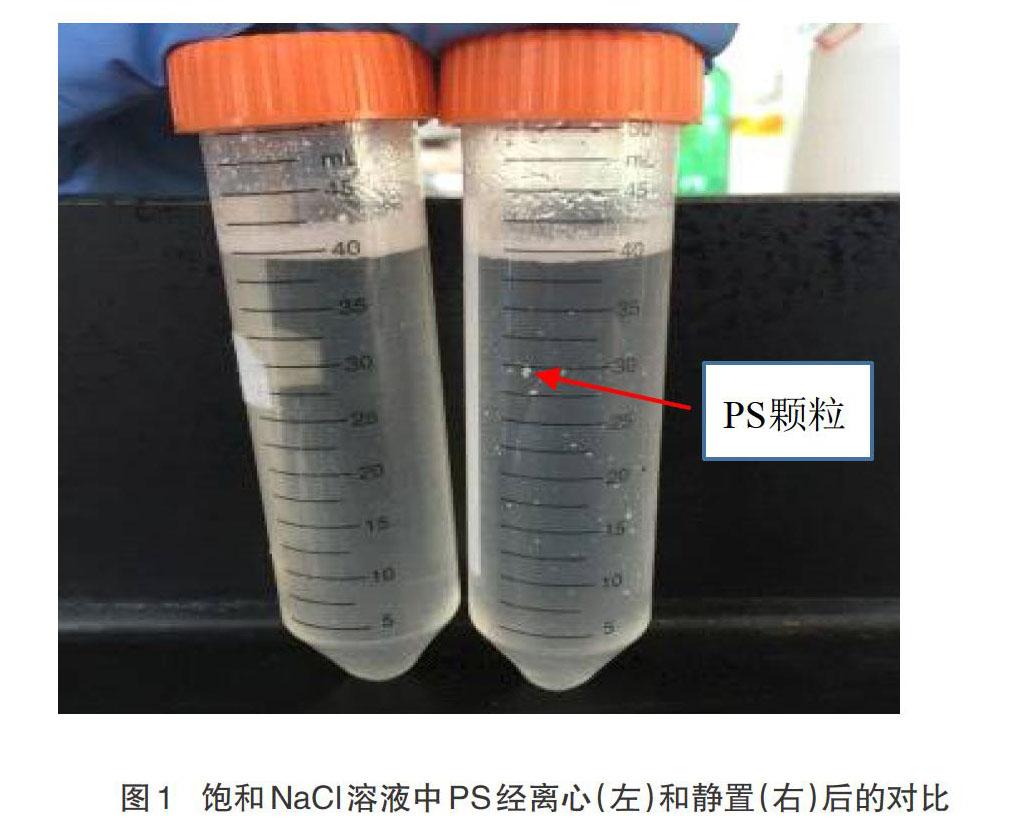
浮选法被认为是分离MPs的有效方法,并且采用的盐溶液度越高则可以收集的MPs种类范围越广,但也可能造成更多的土壤杂质被一起浮选出来。海洋战略框架指令海洋废弃物技术组推荐使用价格低廉且环境友好的NaCl作为MPs的浮选试剂[16]。同时,饱和NaCl溶液密度(1.2 g/cm3)大于PE(0.92 g/cm3)和PS(1.04 g/cm3),可以实现土壤中这两种MPs的提取。为了提高回收率,将浮选过程重复3次,结果显示,第3次浮选过滤后,滤膜上未见MPs,表明两次浮选即能提取完全。浮选后的重要过程就是土壤和MPs的分离,通常采用静置[2, 8, 17]或离心[4, 18]。为了达到较好的分离效果,静置通常需要24 h以上,且密度较小的土壤组分难以分离;离心所需时间短,上清液澄清,但可能造成部分MPs沉淀。预试验比较了静置和离心对分离饱和NaCl溶液中PE或PS的效果,其中,PE经静置和离心后均能完全分离,但PS易沾壁,经离心处理后沾壁现象消失,但静置无法完全消除沾壁,见图1。两种分离方式均未见MPs沉淀。经比较,试验选择离心处理。经离心后,上清液中的MPs采用真空抽滤分离。但滤膜材质也会影响结果的准确度。Li等比较了石英、玻璃纤维、聚四氟乙烯(PTFE)和尼龙4种材质的滤膜,结果显示,石英和玻璃纤维滤膜在冲洗过程中容易掉落纤维,PTFE膜因其疏水性难以过滤水相,尼龙膜效果最佳。因此,本试验选择了尼龙膜进行过滤。
2.2 不同消解体系的比较
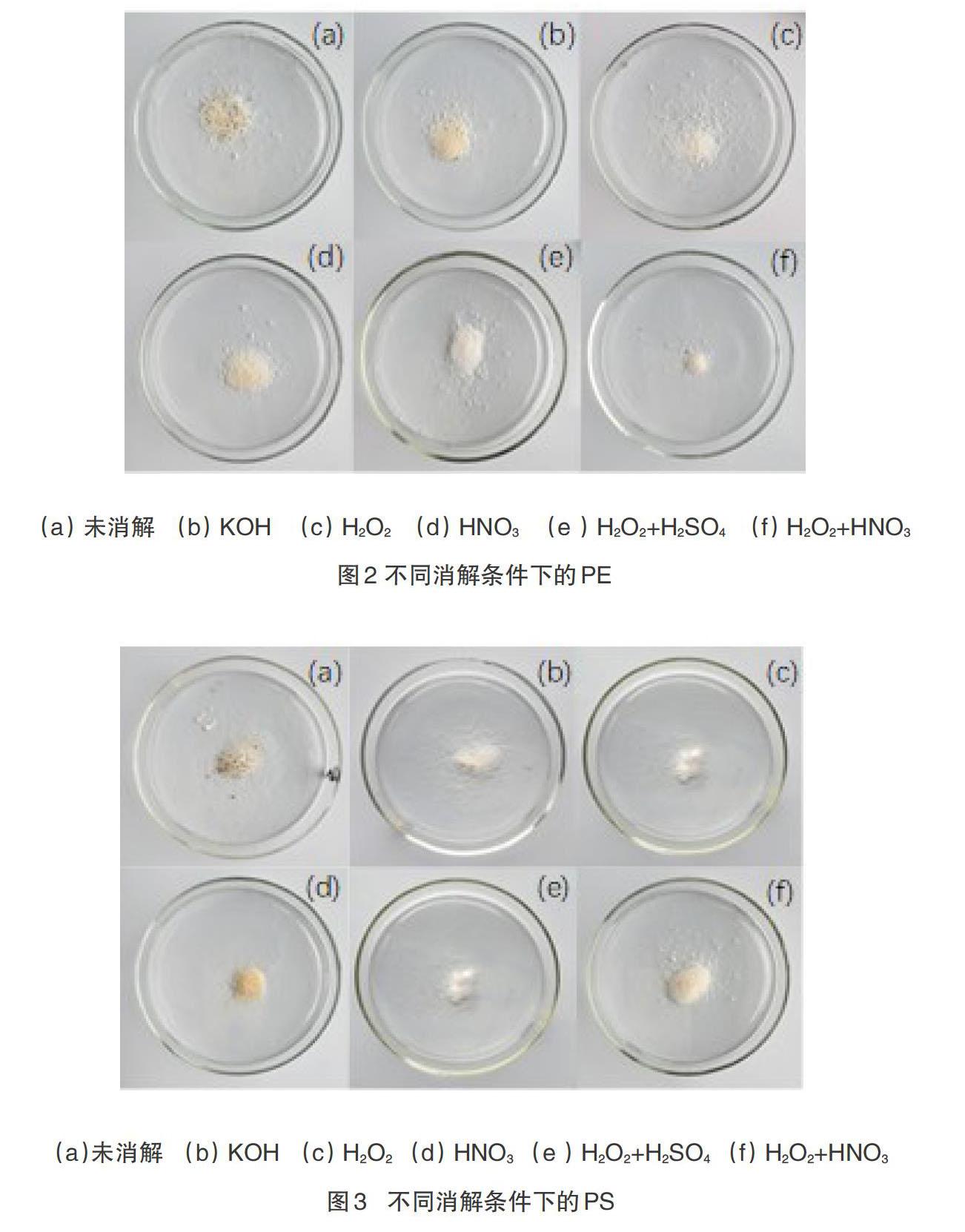
土壤组成复杂,特别是含有各种有机质。一方面,MPs与有机质结合被包裹在土壤团聚体中,MPs难以从土壤颗粒中分离;另一方面,土壤有机质密度较小,浮选法无法将其和MPs分离。因此,浮选和消解联用可以提高MPs的分离效率,但消解体系的选择还应保证MPs的颗粒信息,如数量、形状和大小不受影响。He等综述了各种土壤有机质的去除方法,其中H2O2是最常用的消解液,但可能会轻微改变PE和PP的形状,酸会消解塑料自身,碱会引起塑料表面降解。[11]但是消解的影响也与MPs的类型相关。Hurley等评价了4种主要的有机质去除方法(H2O2氧化、Fenton试剂、NaOH和KOH碱消解)对8种MPs颗粒完整性的影响,其中H2O2在70℃消解对多数MPs无影响[13]。笔者比较了5种消解体系对浮选后滤渣的消解效果,见图2和图3。消解前滤渣中存在大量杂质,主要为植物残体,总体呈淡黄色(见图2a和3a)。KOH的消解效果最差,仍残留部分大颗粒有机质,对PS无显著影响,但是PE变黄(见图2b和3b)。H2O2和H2O2+H2SO4的消解效果最好,有机质消解完全,MPs表观未见明显变化(见图2c、2e和3c、3e)。HNO3和H2O2+HNO3消解速度快且消解完全,但是造成了MPs不同程度的变黄,单一HNO3消解的影响大于二元体系,且对PS的影响大于PE(见图2d、2f和图3d、3f)。此外,HNO3和H2SO4对尼龙滤膜有腐蚀作用,会造成回收率的降低。
综合上述分析,H2O2以及含有H2O2的二元消解体系(H2O2+H2SO4和H2O2+HNO3)的消解对MPs的整体表观影响较小,为了进一步了解对MPs的表面微观特征的影响,对这3种消解体系下的MPs进行电镜扫描,其SEM图见图4和图5。PE颗粒间会互相吸附,形成较大的团聚体,初始PE颗粒表面虽然不平整但较光滑(见图4a)。与初始PE颗粒相比,H2O2消解损伤最小,无明显腐蚀痕迹(见图4b)。但H2O2与酸的混合体系造成PE颗粒表面出现了不同程度的损伤,H2O2+H2SO4消解后PE表面出现少量剥落及裂痕(见图4c),而H2O2+HNO3的消解造成PE表面严重腐蚀甚至降解(见图4d)。新鲜的PS表面较光滑,研磨过程造成了表面的轻微磨损(见图5a)。而经消解后的PS仍处于均匀分散状态,颗粒分明,未出现Claessens等研究中出现的融合现象(见图5b、5c、5d)。这是由于本试验消解温度较低,未达到PS的玻璃化轉化温度(95 ℃)。在含酸的消解体系中,PS颗粒表面损伤严重,特别是HNO3的存在造成了颗粒表面溶解而大量剥落(见图5c、5d)。这可能是因为强酸具有强氧化性和腐蚀性。相比之下,单一H2O2消解后的PS与新鲜的PS没有明显差别(见图5b)。Li等比较了这3种消解体系在70 ℃下对6种塑料(PE、PP、PS、PA、ABS和PET)的影响,发现H2O2+ H2SO4和H2O2+HNO3对PA表面有少量溶解,但未对其他塑料形态产生影响[14],这可能是由于该文献采用的是大颗粒(1~2 cm)塑料,并用体视显微镜在较大视野下观察;并且还发现仅有H2O2+HNO3氧化改变了PE的FT-IR光谱[14]。虽然H2O2的氧化能力较弱,但是对本试验中土壤有机质的去除效果良好,因此,采用该消解液用于后续试验。
2.3 不同粒径MPs的回收
根据上述回收条件的优化结果,采用饱和NaCl溶液浮选、30%H2O2消解提取和分离土壤中不同粒径的PE和PS,回收效率见图6。PE和PS的回收率分别在83%~91%和90%~94%。之前的研究显示,浮选法可以有效地分离MPs。采用不同分离装置,如直接浮选法、分液漏斗法、容量瓶法和连续流动-气浮法等对潮滩沉积物中MPs的回收率在60%~99%[20]。但很多回收试验中采用了沙粒作为基质和大颗粒MPs作为研究对象,且未经过消解步骤[6,20]。本试验采用真实土壤为基质,所选MPs粒径在环境中MPs的主要粒径范围内,因此,所得结果具有较好的代表性。相对于PS,PE的回收率较低,这是由于PE颗粒具有较强的吸附性,易聚集成团并在转移过程中粘附在瓶壁上,造成部分损失。从粒径来看,200目的MPs回收率显著(P<0.05)低于20目的MPs。由于对小粒径MPs回收困难,在MPs的污染调查中可能会低估了MPs的污染程度。
3 结论
本试验采用浮选-消解法提取土壤中的PE和PS。浮选采用饱和NaCl为浮选剂,并通过离心和尼龙膜过滤,实现MPs和土壤颗粒的分离。综合比较了5种消解体系10%KOH、30%H2O2、65%HNO3、H2O2+HNO3(3:1)和H2O2+H2SO4(3:1)對土壤有机质的去除效果和对MPs的表观影响。由于30%H2O2能完全消解土壤中的有机质,且对MPs的表面微观特征无明显影响,可作为消解液。采用本试验的分离方法,MPs的回收率高达94%,其中,PS的回收效果优于PE,大粒径(0.85 mm)比小粒径(0.075 mm)MPs更易回收,是一种操作简单、经济、准确度高且对环境影响小的土壤MPs提取方法。在后续的方法优化中将考虑对更多MPs类型和土壤类型的适用性。
参考文献:
[1] ROCHMAN C M. Microplastics research from sink to source[J]. Science, 2018,360(6384):28-29.
[2] LIU M, LU S, SONG Y, et al. Microplastic and mesoplastic pollution in farmland soils in suburbs of Shanghai, China[J]. Environ Pollut, 2018,242:855-862.
[3] PIEHL S, LEIBNER A, L?DER M G J, et al. Identification and quantification of macro- and microplastics on an agricultural farmland[J]. Sci Rep, 2018,8(1):17950.
[4] ZHANG G S, LIU Y F. The distribution of microplastics in soil aggregate fractions in southwestern China[J]. Sci Total Environ, 2018,642:12-20.
[5] ZHANG S, YANG X, GERTSEN H, et al. A simple method for the extraction and identification of light density microplastics from soil[J]. Sci Total Environ, 2018,616-617:1056-1065.
[6] 周倩, 章海波, 周阳, 等. 滨海潮滩土壤中微塑料的分离及其表面微观特征[J]. 科学通报, 2016,61(14):1604-1611.
[7] FULLER S, GAUTAM A. A procedure for measuring microplastics using pressurized fluid extraction[J]. Environ Sci Technol, 2016,50(11):5774-5780.
[8] HUERTA L E, MENDOZA V J, KU Q V, et al. Field evidence for transfer of plastic debris along a terrestrial food chain[J]. Sci Rep, 2017,7(1):14071.
[9] 王昆, 林坤德, 袁东星. 环境样品中微塑料的分析方法研究进展[J]. 环境化学, 2017,36(1):27-36.
[10] CHAE Y, AN Y. Current research trends on plastic pollution and ecological impacts on the soil ecosystem: A review[J]. Environ Pollut, 2018,240:387-395.
[11] HE D, LUO Y, LU S, et al. Microplastics in soils: Analytical methods, pollution characteristics and ecological risks[J]. TrAC Trends in Analytical Chemistry, 2018,109:163-172.
[12] ELERTA M, BECKER R, DUEMICHEN E, et al. Comparison of different methods for MP detection: What can we learn from them, and why asking the right question before measurements matters?[J]. Environ Pollut, 2017,231:1256-1264.
[13] HURLEY R R, LUSHER A L, OLSEN M, et al. Validation of a method for extracting microplastics from complex, organic-rich, environmental matrices[J]. Environ Sci Technol, 2018,52(13):7409-7417.
[14] LI Q, WU J, ZHAO X, et al. Separation and identification of microplastics from soil and sewage sludge[J]. Environ Pollut, 2019,254:113076.
[15] LIU J, MA Y N, ZHU D Q, et al. Polystyrene nanoplastics-enhanced contaminant transport: role of irreversible adsorption in glassy polymeric domain[J]. Environ Sci Technol, 2018,52(5):2677-2685.
[16] ROCHA-SANTOS T, DUARTE A C. A critical overview of the analytical approaches to the occurrence, the fate and the behavior of microplastics in the environment[J]. TrAC Trends in Analytical Chemistry, 2015,65:47-53.
[17] LV W, ZHOU W, LU S, et al. Microplastic pollution in rice-fish co-culture system: A report of three farmland stations in Shanghai, China[J]. Sci Total Environ, 2019,652:1209-1218.
[18] RILLIG M C, ZIERSCH L, HENPEL S. Microplastic transport in soil by earthworms[J]. Sci Rep, 2017,7(1):1362-1366.
[19] CLEASSENS M, VAN C L, VANDEGEHUCHTE M B, et al. New techniques for the detection of microplastics in sediments and field collected organisms[J]. Mar Pollut Bull, 2013,70(1-2):227-233.
[20] 劉凯,冯志华,方涛,等. 3种典型潮滩沉积物微塑料分离方法研究[J]. 水生态学杂志, 2017,38(4):36-42.
责任编辑 张志钊

