液相色谱-串联质谱法测定木瓜发酵饮料中的三种α-二羰基化合物
陈荣祥,顾雯,罗敏,何婷,尹考,罗春燕
1(遵义医科大学,分析测试中心,贵州 遵义,563000)2(遵义医科大学 药学院,贵州 遵义,563000)3(遵义医科大学 检验医学院,贵州 遵义,563000)
木瓜是我国广泛分布的木本植物,作为药食两用作物其应用和研究有数千年之久。木瓜中含有苹果酸、酒石酸、柠檬酸、琥珀酸等有机酸,同时含有丰富的单宁,其含糖量相对较低,口感酸涩,不宜生吃[1]。因此,木瓜作为食品多采用加工后食用,例如在黔北地区通常采用加糖、加水后自然发酵3个月左右,发酵生产的饮料口感明显改善,在当地很受欢迎[2-3]。
然而,与其他发酵产品类似,木瓜发酵饮料在发酵过程中可能通过美拉德反应产生乙二醛、丙酮醛、丁二酮等α-二羰基化合物。这些化合物是在焦糖化反应逆醛醇缩合、自氧化和美拉德反应中形成的活性中间体[4]。在发酵饮料中,α-二羰基化合物是苹果酸-乳酸发酵的结果,可在酒精发酵后或同时发生,广泛存在于蜂蜜、啤酒、咖啡、食用油、醋和酱油中[5]。它们是食品中风味和颜色的重要前体物质,可与酯类物质相互作用,促进酯类物质的挥发,使发酵产物具有特殊的复合风味和口感。但是,如果α-二羰基化合物的含量过高,会对发酵产品的风味产生负面影响。同时,过量摄入这些化合物也会影响人体健康,导致蛋白质糖基化并诱导糖基化终产物的形成,造成细胞损伤和炎症[6-7]。还可能引起淀粉样蛋白的积累,诱发阿尔茨海默症[8-9]。因此,发酵饮料中的α-二羰基化合物含量的准确、灵敏的检测方法对于正确评价其质量具有重要意义和应用价值。
α-二羰基化合物早期检测多采用分光光度法,但该法灵敏度低,只能测定α-二羰基化合物的总量,不能测定单个化合物的浓度[10]。目前最常用的方法是用衍生试剂与之反应,然后用气相色谱或液相色谱法进行检测[11-13]。常用的衍生试剂有2,4-二硝基苯肼、氨基胍、甲基羟胺、吉拉德T试剂、邻苯二胺类等[14-15]。其中邻苯二胺类衍生试剂如邻苯二胺(o-phenylenediamine, OPD)[16]、4,5-亚甲二氧基-1,2-邻苯二胺[17]、4-硝基邻苯二胺[18],3,3-二氨基联苯胺[19]等最为常用,衍生产物采用紫外、荧光检测[20-21]。然而光学检测器存在灵敏度不高、选择性较差等问题。相对于光学检测器,串联质谱灵敏度更高,选择性更好。例如,有文献采用邻苯二胺进行衍生化,进一步采用固相萃取净化,液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)测定乳制品中的α-二羰基化合物[22]。也有文献首先进行固相萃取净化,后采用邻苯二胺衍生化的方式测定碳酸饮料中的α-二羰基化合物[23]。然而,这些方式均需要复杂的固相萃取净化,前处理步骤繁琐,成本较高。超滤离心是一种简单的前处理净化方式,可以有效去除样品中的蛋白质、核酸等大分子成分,适合乳制品、血浆等蛋白含量较高的样品的净化[24-25]。木瓜中含有丰富的木瓜蛋白酶、超氧化物歧化酶等多种蛋白质,然而目前还没有针对木瓜发酵饮料中α-二羰基化合物的测定方法。本研究采用离心超滤的方式对木瓜发酵饮料进行净化,进一步采用邻苯二胺进行衍生化,建立了柱前衍生-高效液相色谱-串联质谱法测定3种α-二羰基化合物的方法,并应用该方法测定不同发酵时间下木瓜饮料中的α-二羰基化合物的含量。
1 材料与方法
1.1 仪器和试剂
I-class-TQ-S超高效液相色谱-三重四级质谱仪,美国Waters公司;SB-800DTD超声波清洗仪,宁波新芝;Microfuge-20高速离心机,美国Beckman Coulter公司;Purelab Chorus2超纯水系统,英国Elger公司;ME-104电子天平、FE-28 pH计,瑞士Mettle-Toledo公司;超滤离心管(截留分子质量为10、50、100 kDa),美国Millipore公司。
OPD(99.5%)、乙二醛(40%)、丙酮醛(40%)、丁二酮(≥99%),上海阿拉丁生化科技股份有限公司;乙腈(质谱纯),霍尼韦尔贸易(上海)有限公司;其他试剂均为分析纯;木瓜发酵饮料,正安天楼食品有限公司。
1.2 标准储备液和衍生试剂的制备
标准储备液的制备:准确移取乙二醛、丙酮醛、丁二酮溶于超纯水中,定容至100 mL,制备质量浓度为1 mg/mL的储备液,4 ℃下储存备用。
衍生溶液的配制:称取邻苯二胺10 mg,用水溶解并定容至10 mL,配成质量浓度为1 mg/mL的邻苯二胺溶液。
1.3 样品处理和衍生化反应
移取1 mL待测样品,加水稀释至10 mL。取1 mL加入超滤管中(截留分子质量10 kDa),5 000 r/min离心10 min。吸取滤液0.5 mL加入0.5 mL OPD 衍生试剂和0.1 mL 0.1 mol/L NaHSO4溶液,涡旋混匀,室温下反应15 min后,进行LC-MS/MS测定。OPD与3种α-二羰基化合物的反应方程式如图1所示。
1.4 色谱条件
色谱柱:Waters Xbridge BEH C18(100 mm×2.1 mm,1.7 μm); 流动相:0.2%乙酸水溶液(A)-乙腈(B),梯度洗脱:0~5 min,25%B, 6 min,80%B, 7 min,80%B, 7.5 min,25%B;体积流量0.2 mL/min;柱温40 ℃;进样量1 μL。

图1 α-二羰基化合物与OPD的衍生化反应Fig.1 Derivative reaction of α-compounds with OPD
1.5 质谱条件
电喷雾电离源,正离子模式下采用多反应监测模式检测。毛细管电压3.5 kV;脱溶剂温度500 ℃;脱溶剂气体(N2)流量750 L/h,离子源温度150 ℃,碰撞气为Ar。为防止过量的衍生试剂及难挥发缓冲盐污染质谱,2 min之前的色谱洗脱成分不经质谱直接排入废液。
2 结果与分析
2.1 超滤管截留分子质量的选择
木瓜中含有丰富的木瓜蛋白酶、超氧化物歧化酶等多种蛋白质,此外还含有丰富的多糖。这些大分子化合物不仅会污染色谱柱,影响色谱分离,还可能导致较强的基质效应影响离子化效率。食品检测中大分子化合物通常可以采用有机溶剂沉淀、固相萃取、超滤等方式去除[26-28]。其中离心超滤的方式操作简单,不需要额外有机溶剂及吸附剂等,绿色环保[25]。因此,本研究选择超滤离心的方式去除此类大分子化合物。
将3种化合物对照品储备液稀释成质量浓度为0.5 mg/L混合溶液,分别向截留分子质量10、50、100 kDa的超滤管内室加入3种化合物溶液2 mL,5 000 r/min下离心10 min,收集滤液。将超滤离心前后的3种化合物溶液衍生化之后进样测定,计算不同截留分子质量的超滤管对3种化合物回收率的影响,结果表明使用10、50、100 kDa超滤管离心过滤后,3种化合物的回收率均>95%,说明不同规格超滤管对于3种化合物均无显著性吸附作用。考虑到截留分子量越低,去除杂质效果越好,选择10 kDa超滤管用于净化。
2.2 衍生化反应条件的优化
2.2.1 反应体系pH优化
通常,反应体系的酸度、温度和反应时间对反应效果有直接影响。邻苯二胺类衍生试剂的衍生化反应条件的优化有文献进行了大量的研究,反应条件为弱酸性[14]、中性[23]、弱碱性[13]均有报道。我们分别采用不同浓度的NaHSO4溶液(0.05, 0.1, 0.2, 0.3, 0.5 mol/L)、pH 3~10的缓冲溶液(pH 3.0, 5.0, 7.0, 8.5, 10.0),在40 ℃反应15 min,结果表明,所有条件下的产物峰面积无显著性的差异(峰面积差异<10%),均可用于OPD的衍生化反应。考虑配制和操作方便,采用0.1 mol/L NaHSO4作为衍生试剂的添加剂。
2.2.2 反应体系的温度和反应时间的优化
在本实验中研究了不同反应温度(室温、40、50、60、70、80、90 ℃)对衍生物峰面积的影响。结果表明,随着反应温度的升高,衍生物的峰面积保持不变,可以在室温下进行反应。随后,在室温下研究了反应时间(5、15、30、60 min)对衍生物峰面积的影响。结果表明,当反应时间为15 min时,产物的峰面积已达最大,且随着反应时间的延长,产物的峰面积保持稳定。因此,选择反应时间为15 min。
2.2.3 衍生试剂用量的优化
按照样品和衍生试剂的体积比为1∶1,比较不同浓度的OPD衍生试剂对于衍生产物的影响。结果表明,在OPD质量浓度为0.05~5 mg/mL,乙二醛、丙酮醛、丁二酮衍生产物的峰面积随着OPD质量浓度的增加而增加,初始增加较快,当衍生试剂的质量浓度>1 mg/mL时,其峰面积增加缓慢(图2),因此,选择衍生试剂的质量浓度为1 mg/mL。

图2 衍生试剂OPD质量浓度的优化Fig.2 Optimization of OPD concentration for the derivative reaction
2.3 色谱条件优化
在本次试验中,我们比较了乙酸和乙酸铵溶液作为流动相添加剂对目标化合物色谱峰和电离度的影响,结果表明,在2种流动相条件下其分离效果均较好。但在ESI+模式下,酸性环境有利于目标化合物的离子化,提高灵敏度,所以选择0.2%(体积分数)乙酸作为流动相添加剂。
2.4 质谱条件优化
将乙二醛、丙酮醛、丁二酮用超纯水配制成质量浓度为0.5 mg/L混合标准溶液,加入OPD衍生化后进样,进行质谱条件的优化。通过全扫描模式确定3种衍生产物的母离子,在选择离子监测模式下优化锥孔电压。进一步通过产物离子扫描模式确定其产物离子,选择峰度最高的产物离子用于质谱多反应监测(multiple reaction monitoring,MRM),并优化其碰撞能量。优化后的最佳质谱条件如表1所示,衍生产物的二级质谱如图3所示。
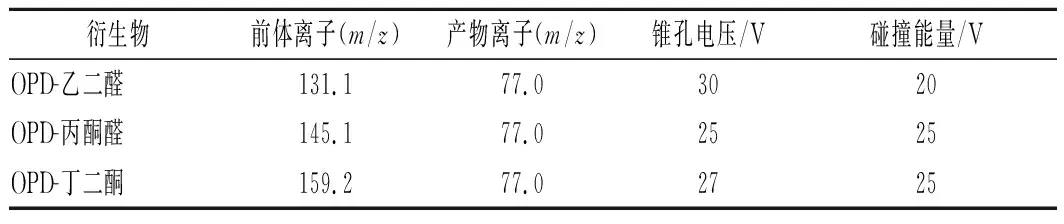
表1 α-二羰基化合物衍生产物的质谱分析参数Table 1 MRM parameters of the α-dicarbonyl compound derivative products

a-OPD-乙二醛;b-OPD-丙酮醛;c-OPD-丁二酮图3 三种α-二羰基化合物衍生产物的二级质谱图Fig.3 Mass spectrograms of the 3 kinds of α-dicarbonyl compounds
2.5 方法验证
2.5.1 标准曲线及检出限
将乙二醛、丙酮醛、丁二酮标准溶液配置成质量浓度为0.012、0.030、0.120、0.300、0.600、0.900 mg/L的混合标准品溶液,与OPD衍生试剂按1∶1的体积比均匀混合,在室温下反应15 min,然后用LC-MS/MS进行检测,重复3次,以峰面积y作为纵坐标,样品质量浓度x(mg/L)作为横坐标,进行线性回归。结果表明,3种化合物在0.012~0.900 mg/L线性关系良好,相关系数r2>0.99,并以3倍信噪比计算检出限。结果如表2所示。

表2 三种α-二羰基化合物的回归方程、线性范围和检测限Table 2 Regression equation, liner range and LODs of the 3 α-dicarbonyl compounds
2.5.2 稳定性
乙二醛、丙酮醛、丁二酮与OPD溶液混合衍生化在室温下放置12 h,每隔2 h进行测定,结果表明衍生物的峰面积RSD<5%(n=6),说明衍生产物稳定性较好。
2.5.3 回收率
在已测定浓度的实际样品中进行3个不同质量浓度水平的加标回收试验,重复6次。结果表明,乙二醛、丙酮醛、丁二酮的回收率为86.26%~95.29%,RSD为2.49%~7.31%(表3)。该方法回收率良好,可用于乙二醛、丙酮醛、丁二酮的准确测定。
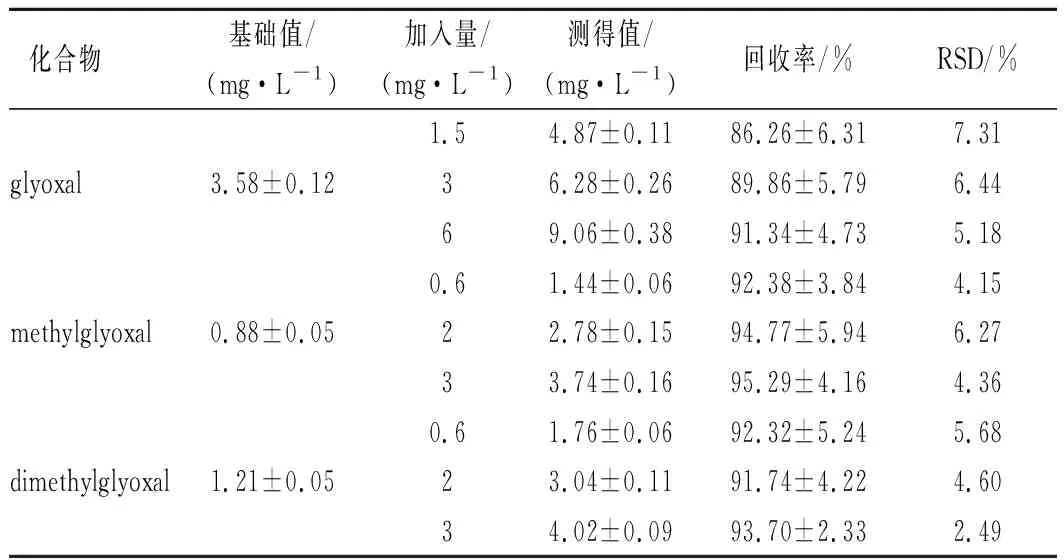
表3 木瓜发酵饮料中3种α-二羰基化合物的回收率(n=6)Table 3 Recovery of the α-dicarbonyl compounds in Fructus Chaenomelis fermented beverage
2.5.4 基质效应
木瓜发酵饮料中含有大量的蛋白、多糖、多酚等化合物,均可能影响其离子化。本实验分别以水和待测样品(稀释10倍)为溶剂,分别配制不同质量浓度的3种待测化合物溶液,衍生化后测定,通过比较二者的斜率来评价基质效应,基质效应计算如公式(1)所示:

(1)
本研究中乙二醛、丙酮醛、丁二酮的基质效应分别为107.1%,111.8%,108.9%。通常认为在85%~115%范围内无显著基质效应[29]。本研究通过离心超滤以及衍生化处理后,3种衍生产物无显著的基质效应。
2.6 实际样品的检测
取不同发酵时间木瓜果汁1 mL,用水稀释至10 mL。按照1.3方法处理后进样,测定乙二醛、丙酮醛、丁二酮的含量。标准品和样品的色谱如图4所示。
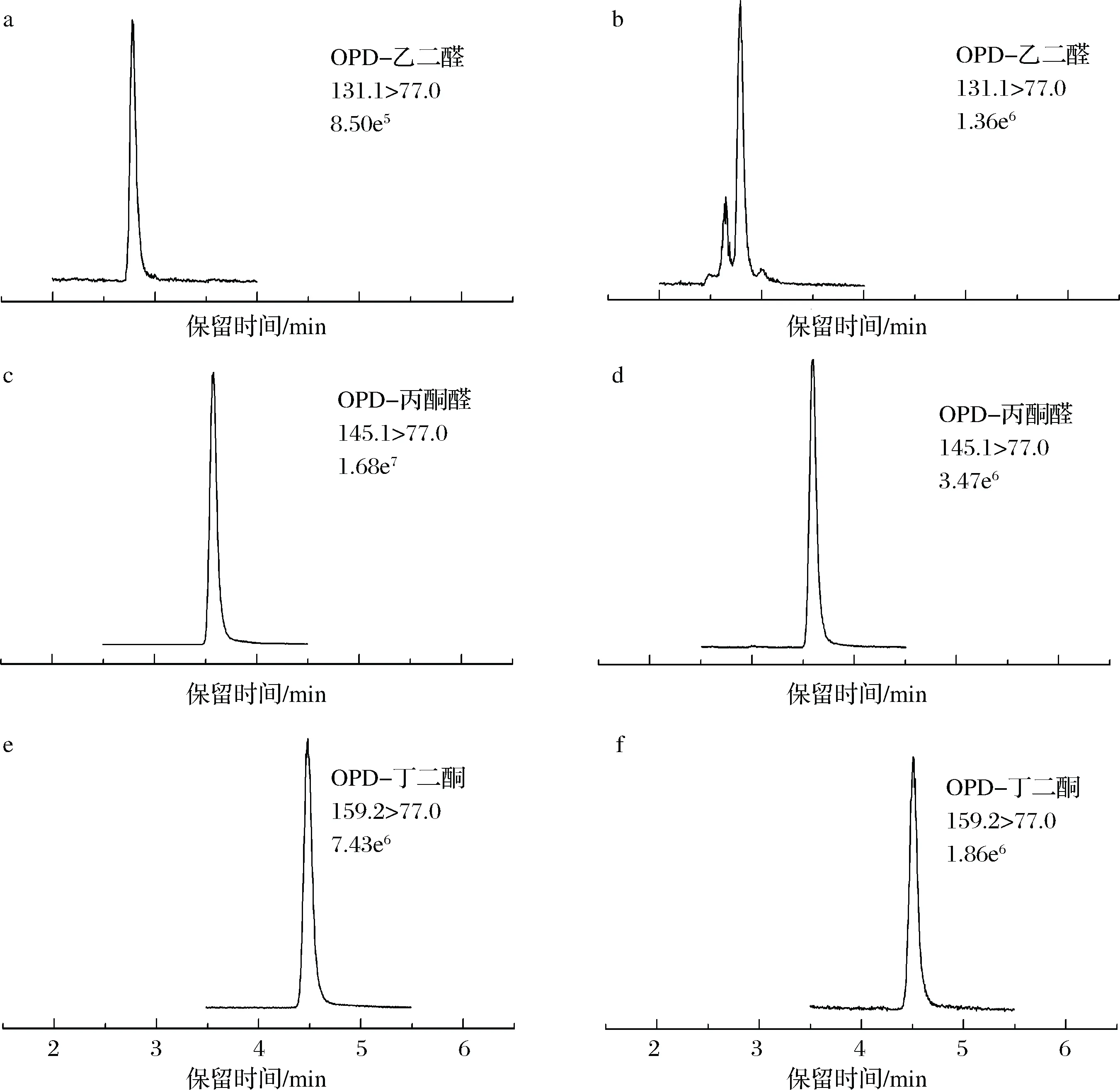
a-标准品OPD-乙二醛;b-样品OPD-乙二醛;c-标准品OPD-丙酮醛;d-样品OPD-丙酮醛;e-标准品OPD-丁二酮;f-样品OPD-丁二酮图4 木瓜发酵饮料中3种α-二羰基化合物衍生产物的标准品和样品色谱图Fig.4 Chromatograms of the 3 kinds of α-dicarbonyl compounds in standard solution and Fructus Chaenomelis fermented beverage
对不同发酵时间(0、0.25、0.5、1、2、4个月)的木瓜发酵饮料进行测定,结果表明,3种α-二羰基化合物的质量浓度随着发酵时间延长而增加。其中乙二醛质量浓度最高,丙酮醛最低。当发酵时间达到0.5个月时,乙二醛的质量浓度达到峰值,发酵时间为1个月时,丙酮醛、丁二酮的质量浓度达到峰值,继续增加发酵时间3种化合物的质量浓度基本保持稳定(图5,表4)。
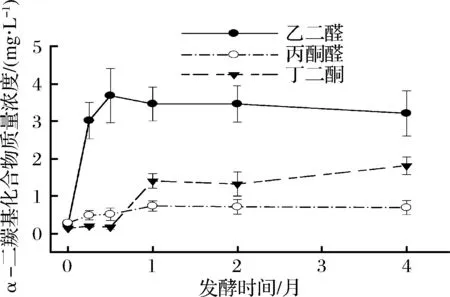
图5 三种α-二羰基化合物质量浓度随发酵时间的变化(n=3)Fig.5 Concentration of three α - dicarbonyl compounds with different fermentation time

表4 不同发酵时间下3种α-二羰基化合物浓度(n=3)单位:mg/L
3 结论
建立了以OPD为衍生试剂的柱前衍生-超高效液相色谱-串联质谱法测定木瓜发酵饮料中乙二醛、丙酮醛、丁二酮含量的方法,并用于木瓜发酵饮料中这3种化合物含量的快速准确测定。结果表明,发酵时间为1个月时,α-二羰基化合物的质量浓度即达到最高值,继续增加发酵时间其含量保持稳定。该方法线性范围宽,重复性好,准确度高,可以为产品的质量控制提供方法依据。

