腹腔镜胆囊切除术转开腹预测模型的建立与分析
唐 浩,梁 平,周亚龙,赵晓彪,曾 凯
自1987年首例腹腔镜胆囊切除术(laparoscopic cholecystectomy, LC)开展以来,相比于传统的开腹胆囊切除术(open cholecystectomy, OC),LC凭借其创伤小、恢复快的优势,迅速在肝胆外科中普及[1]。据统计,目前LC已占胆囊良性疾病手术治疗的90%以上[2]。然而在实际工作中,由于各种因素的影响,常导致LC术中转开腹。根据不同的报道,胆囊炎症水肿严重、Calot三角解剖结构不清、意外胆囊癌(unsuspected gallbladder carcinoma, UGC)及胆囊颈部结石嵌顿等因素是LC转开腹的主要危险因素[3]。但由于上述报道所纳入的研究样本为国外患者,并且样本筛选标准不同,其结果并不一定适用于国人。同时,上述研究报道对LC转开腹的危险因素仅做了定性研究,对于临床工作的指导意义有限。尽管已有少数学者[4]建立了预测LC转开腹的数学模型,但在实际应用中需要医生记忆大量数据,操作繁琐,在临床中普及率较低。由此可见,建立简便、可视化的术前预测LC转开腹的模型,将有助于外科医生在术前对患者进行评估,有利于加强医患沟通。基于以上,本研究回顾性分析了LC患者术中转开腹的危险因素,利用R软件建立可视化的列线图预测模型,并近一步评估该模型预测模型对LC患者术中转开腹的预测价值,现将研究报道如下。
1 资料与方法
1.1 一般资料 选择2015年1月至2018年2月期间解放军第一八七医院肝胆外科收治的LC患者132例作为研究对象,其中,术中转开腹的患者18例作为转开腹组(open cholecystectomy group, OCG),另外114例患者作为对照组(laparoscopic cholecystectomy group, LCG)。纳入标准:(1)我院肝胆外科收治的LC患者:经影像学和病理诊断为良性胆囊病变,同时具有上腹部不适等临床症状。(2)手术方式为LC,并具有相应的手术指征,患者可耐受手术并同意行LC手术。(3)患者年龄≥18岁,性别不限。(4)术者均为我院高年资医师,具有相应的LC手术经验,采用“4孔”法或“3孔”法入腹。(5)患者一般资料、临床资料完整。排除标准:(1)排除合并胆囊外疾病,需要开腹手术患者。(2)排除不适合实施气腹的患者。(3)排除临床资料不完整患者。(4)排除其他不适合纳入研究的患者,如:因器械原因术中转开腹、因家属要求术中转开腹等。
1.2 资料收集 利用“住院病人信息管理系统”,收集医院肝胆外科2015年1月至2018年2月期间收治的所有患者,根据纳入标准和排除标准,选择研究样本。记录患者一般资料:性别、年龄、体质量指数(BMI)等,临床资料:疾病类型、影像学检查结果、术中转开腹原因、既往病史、血压、血糖、血常规、肝肾功等。其中,以血清总胆红素>22.2 μmol/L记为血清总胆红素增高,以胆囊壁厚度≥0.4 cm记为胆囊壁增厚,以胆囊横纵径≤4.5 cm×1.5 cm记为胆囊萎缩。
1.3 统计学处理 应用SPSS 19.0和R 3.5.0软件对数据进行统计分析。符合正态分布的计量资料用均数±标准差(x±s)表示,组间比较采用t检验。计数资料以百分比表示,组间计数资料比较采用χ2检验或Fishers确切概率法。将具有统计学意义的变量纳入二元Logistic回归模型,确定LC术中转开腹的独立危险因素。再将得出的独立危险因素引入R软件,应用rms程序包建立LC术中转开腹的列线图预测模型。根据列线图模型结果绘制列线图模型的ROC曲线,通过计算曲线下面积(AUC)和Hosmer-Lemeshow检验,评估其对LC术中转开腹的预测价值。P<0.05表示差异有统计学意义。
2 结果
2.1 一般资料比较 OCG组中,伴有糖尿病、上腹部手术史、胆囊萎缩、胆囊壁增厚、胆囊颈部结石嵌顿、总胆红素升高、急性胆囊炎的患者比例高于LCG组,差异具有统计学意义(P<0.05),见表1。
2.2 LC术中转开腹危险因素Logistic回归分析 以是否术中转开腹作为因变量(1:发生;0:未发生),将具有统计学意义的临床资料(糖尿病、上腹部手术史、胆囊萎缩、胆囊壁增厚、胆囊颈部结石嵌顿、总胆红素升高、急性胆囊炎)作为自变量进行二元Logistic回归分析,结果显示糖尿病、上腹部手术史、胆囊萎缩、胆囊壁增厚、胆囊颈部结石嵌顿、总胆红素升高、急性胆囊炎是LC术中转开腹的危险因素(P<0.05),见表2。

表1 LCG组和OCG组一般资料比较
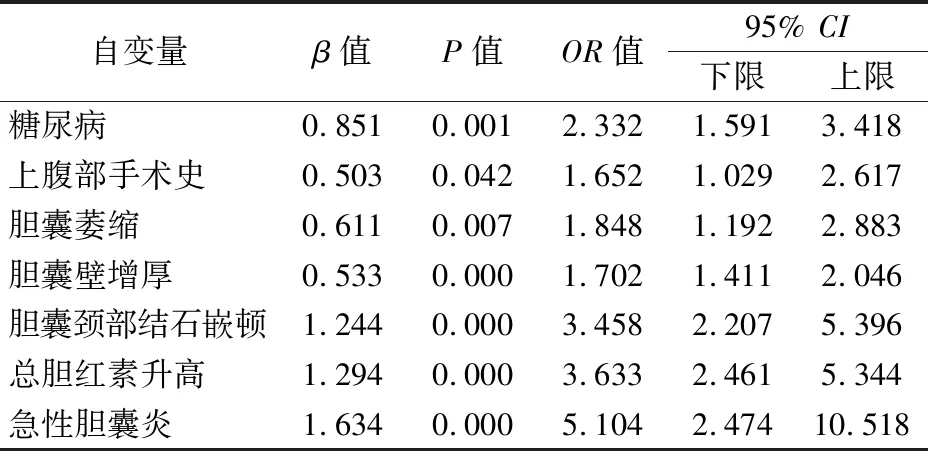
表2 腹腔镜胆囊切除术(LC)中转开腹危险因素Logistic回归分析
2.3 LC术中转开腹发生风险列线图模型建立与验证 将得出的独立危险因素引入R软件,应用rms程序包的lrm函数建立LC术中转开腹的列线图预测模型。根据列线图模型,伴有糖尿病、上腹部手术史、胆囊萎缩、胆囊壁增厚、胆囊颈部结石嵌顿、总胆红素升高、急性胆囊炎的患者,其列线图模型相应评分也增高,对应发生术中转开腹的风险上升,见图1。
2.4 列线图模型对LC术中转开腹的预测价值 Hosmer-Lemeshow检验结果显示,预测效能为93.94%,说明模型拟合良好(P<0.05),见表3。ROC曲线分析显示,列线图模型预测发生的AUC为0.937(95%CI:0.895~0.980),特异性为88.68%,敏感性为82.98%,见图2。

表3 Hosmer-Lemeshow检验结果(例)

图2 列线图模型的ROC曲线
3 讨论
目前研究认为,LC转开腹的主要原因包括:胆囊炎症水肿严重导致Calot三角解剖结构不清,术中发现胆囊癌,胆道损伤等[5]。而LC转开腹的危险因素则包括众多。
本研究结果中,糖尿病、上腹部手术史、胆囊萎缩、胆囊壁增厚、胆囊颈部结石嵌顿、总胆红素升高、急性胆囊炎是LC转开腹的危险因素,这一结果与文献报道相一致[6],但同时也与部分报道不符[7]。其中,有学者认为,男性患者可能存在较女性更长的胆囊结石病史,使得胆囊解剖结构不清[7]。高龄患者多由于反复发作的胆囊结石,使得Calot三角粘连严重。本研究未发现性别和年龄是LC转开腹的危险因素,这可能与纳入样本量较小有关。而糖尿病患者由于对炎症的抵抗能力降低,当发生胆囊炎时,疾病进展更为迅速,更易给LC手术带来难度[8]。上腹部手术史患者,由于接受过上腹部的手术,腹腔内脏器存在不同程度的粘连,也为LC手术分离胆囊带来了挑战[9]。胆囊萎缩与胆囊壁增厚均为胆囊炎症病史较长或已导致胆囊纤维化的表现,此类患者往往在术中会发现Calot三角粘连严重,迫不得已转为开腹[10]。胆囊颈部结石嵌顿患者,胆囊壁往往存在炎性瘢痕,术中转为开腹几率明显增加[11]。总胆红素升高总胆红素升高患者常预示着胆囊炎已经影响到肝脏,或患者合并胆总管结石,或存在Mirizi综合征,病情较为复杂,LC术野不清,是LC转开腹的危险因素[12]。急性胆囊炎患者胆囊多存在严重水肿,急性炎症使胆囊与周围其他脏器粘连,术中容易伤及肝外胆管或胆囊动脉[13]。在开展LC的早期,急性胆囊炎曾被认为是LC的相对禁忌证,尽管随着手术技术的进步,急性胆囊炎也可行LC切除,但其转开腹的几率仍居高不下。
随后,本研究根据多因素Logistic回归分析结果建立列线图模型,结果显示,伴有糖尿病、上腹部手术史、胆囊萎缩、胆囊壁增厚、胆囊颈部结石嵌顿、总胆红素升高、急性胆囊炎的患者,其列线图模型相应评分也增高,对应的并发症发生风险上升。列线图又称诺莫图(Nomogram plot),可以将Logisitic回归分析的结果可视化、直观化,更易于临床推广[14]。研究证实列线图可以用于肿瘤预后、术后并发症等风险的定量预测[15]。通过建立的列线图模型,有利于临床医生直观分析患者发生相关风险的权重。接下来,为了验证列线图的预测效能,本研究进行了Hosmer-Lemeshow检验和ROC曲线分析,结果显示,该列线图预测效能为93.94%,这说明,模型拟合良好。列线图模型预测发生的AUC为0.937,特异性为88.68%,敏感性为82.98%。这说明,该列线图模型对于预测LC转开腹的风险具有较好的价值。
综上所述,基于LC手术患者临床资料建立预测LC转开腹发生风险的列线图模型,具有良好的特异性和敏感性,模型拟合良好,临床价值较高。

