微波活化玉米秸秆生物质炭对水中亚甲基蓝的吸附研究
来雪慧,闫晋宏,郭睿铭,吴 丹,史航宇
1.太原工业学院环境与安全工程系,山西 太原 030008
2.山西大学环境与资源学院,山西 太原 030006
近年来,染料逐渐被广泛应用于如纺织、造纸和皮革等工业企业中,而印染废水造成的环境污染问题也日益严重[1]。印染废水排放到水体中,可以减弱水生植物的光合作用,影响水生生物的生长[2]。同时,大多数染料还具有潜在的高毒性,致癌致畸作用,对水生动物和人体的健康造成威胁[3]。亚甲基蓝作为一种典型的阳离子有机染料,其分子结构稳定,可长期存在于环境中,难以降解[4]。
目前去除亚甲基蓝的方法包括生物降解、光电催化、臭氧氧化和吸附法等[5]。其中,吸附法因其去除效果好,操作方便成为有效处理亚甲基蓝的主要方法[6]。当前使用较多的吸附材料,如活性炭的吸附性能较好,但其成本高且制备复杂。生物质炭是生物质在厌氧或者绝氧条件下经过高温热解后产生的固体碳产物,它来源广泛,制备过程简单,同时还可以还田改良土壤肥力,属于环境友好型的吸附材料[7,8]。
现有的研究表明生物质炭作为吸附材料,对于亚甲基蓝的吸附容量较低[9]。目前,通常采用磷酸活化、二氧化碳活化和氢氧化钾活化等方法提高生物质炭的吸附量[10]。本研究选用玉米秸秆为原料制备得到生物质炭,通过磷酸将其活化,考察对溶液中亚甲基蓝的吸附性能,以期为我国印染废水的处理提供科学依据,同时为农业废弃物的资源化利用提供一种新的选择。
2 材料与方法
2.1 材料与试剂
试验所用试剂为亚甲基蓝、盐酸、氢氧化钠和磷酸,均为分析纯,用水为去离子水,玉米秸秆取自山西省太原市尖草坪区南寨玉米种植区。
2.2 仪器
所用到的仪器主要有FA224 型电子分析天平,M1-L2138 型微波炉,DHG-9070 型电热恒温鼓风干燥箱,HZQ-X100 双层气浴恒温振荡器,微型植物粉碎机,UV-1800 型紫外可见分光光度计,PHS-3C型酸度计,Kubo-X1000 比表面及孔径分析仪,80 目和100 目筛。
2.3 生物质炭的制备
将收集的玉米秸秆晾干,剔除残留的玉米叶,清洗,切成10 cm~20cm 的小段。在105 ℃下烘干至完全,再将干燥后的玉米秸秆通过植物粉碎机进行粉碎。过0.18 mm(80 目)筛,取筛下部分,再过0.15 mm(100 目)筛,取未筛过的部分,得到粒径为0.15 mm~0.18 mm 的玉米秸秆粉末。将其与14.7 mol·L-1的浓磷酸H3PO4分别按照1:1,1:2 和1:3 的浸渍比进行混合,于25 ℃、150 r/min条件下振荡0.5 h,反复振荡3 次,充分混匀,放置24 h,同时应注意避免光照。之后将浸渍后的混合物在105 ℃条件下于恒温烘箱中进行预炭化一定时间。将预炭化后的固体物质置于微波炉中,在700 W 的微波功率条件下微波活化,然后用0.1 mol·L-1的稀盐酸HCl 和去离子水清洗数次,直至pH>6.0。清洗之后的样品在105 ℃下烘干至恒重,即得到玉米秸秆生物质炭,备用。
2.4 亚甲基蓝的吸附实验
取50 mL 一定质量浓度的亚甲基蓝溶液置于100 mL 的具塞三口烧瓶中,加入0.1 g 生物质炭,室温下于恒温振荡箱中以275 r/min 振荡120 min,静置沉淀后,吸取上清液。在665 nm 波长下测定滤液的浓度Ce,按照下式计算生物质炭对亚甲基蓝的平衡吸附量Qe:Qe=(C0-Ce)V/W。
式中:C0和Ce为亚甲基蓝溶液的初始浓度和吸附后浓度(mg·L-1);V为亚甲基蓝溶液的体积(L);W为生物质炭的质量(g)。
3 结果与讨论
3.1 制备条件对吸附性能的影响
3.1.1 单因素试验 研究不同玉米秸秆与浓磷酸的浸渍比(1:1、1:2 和1:3)、预炭化时间(2 h、4 h、6 h、8 h 和10 h)和微波活化时间(2 min、5 min、8 min、12 min 和15 min)条件下制得的生物质炭对亚甲基蓝的吸附量。在一定条件下(浸渍比1:1,预炭化时间6 h,微波活化时间8 min),考察单因素对吸附性能的影响,如图1 所示。可以看出,当玉米秸秆粉末与浓H3PO4的浸渍比为1:1 时,亚甲基蓝的吸附量最大,为49.94 mg·g-1,高于浸渍比为1:2 和1:3。亚甲基蓝的吸附量在预炭化6 h时达到最大值(图2);当预炭化时间超过6 h 后,碳损失率随着时间延长而增加,导致吸附量减少。微波功率为700 W 时,活化时间为2 min 时,对亚甲基蓝的吸附量仅为42.65 mg·g-1;当微波活化时间为5 min 时,亚甲基蓝的吸附量达到最大值51.26 mg·g-1(图2)。因此,单因素条件下,生物质炭制备的适宜浸渍比为1:1,预炭化时间为6 h,微波活化时间为5 min。

图1 浸渍比对吸附量的影响Fig.1 Effect of impregnation ratio on absorbance

图2 预炭化时间和微波活化时间对吸附量的影响Fig.2 Effects of precarbonization and microwave activation time on absorbance
3.1.2 正交试验设计 表1 为正交试验设计和结果。在不同的浸渍比、预炭化时间和微波活化时间条件下,制得的生物质炭对亚甲基蓝的吸附量不同。在浓磷酸浸渍比(玉米秸秆:浓磷酸)为1:1,预炭化时间为6 h,微波活化时间为5 min 时,对亚甲基蓝的吸附量最大,为71.26 mg·g-1。吸附量随着浸渍比和预炭化时间的增加而降低,这主要是因为破坏了生物质炭的内孔隙结构,同时孔隙结构中由于残留过多的磷酸浸渍残留物,会进一步减少孔隙数量,并导致生物质炭的内表面积减小。因此,在亚甲基蓝的吸附研究中,选择此条件下制得的玉米秸秆生物质炭。

表1 正交试验设计和结果Table 1 Orthogonal experimental design and results
3.1.3 比表面积测定 选取活化前以及最佳条件制备的活化后生物质炭,进行氮气吸附-脱附等温线的测定,计算得出生物质炭活化前后的比表面积和孔结构参数,如表2 所示。

表2 生物质炭活化前后的比表面积和孔隙结构参数Table 2 The parameters of specific surface area and pore structure for biochar before and after activation
由表2 可以看出,活化后生物质炭的比表面积和孔隙结构与活化前相比均有明显的增加,说明生物质炭经过浓磷酸活化之后,生物质具有更高的比表面积和更为发达的孔隙结构。微波活化后,秸秆表面出现了许多孔,吸附容量增加,与实验结果吻合。活化前的生物质炭比表面积只有18 m2·g-1,极少量大孔;活化后比表面积增大到589 m2·g-1,且孔径增大,孔数量增多。
3.2 吸附影响因素分析
3.2.1 生物质炭用量对亚甲基蓝吸附效果的影响 在室温(25±0.5 ℃)及初始浓度为150 mg·L-1的亚甲基蓝溶液中,初始溶液pH=6.0 及振荡120 min 条件下,玉米秸秆生物质炭用量对吸附效果的影响如图3 所示。可以看出,用量在0.2~2 g·L-1时,随着生物质炭投加量增加,其表面提供的吸附活性点位增多,对亚甲基蓝的吸附量逐渐增加,最大达到74.29 mg·g-1。当生物质炭用量增加到2~5 g·L-1时,吸附量缓慢减小,但仍高于71 mg·g-1。这说明玉米秸秆生物质炭用量为2 g·L-1时,对亚甲基蓝的吸附量达到饱和。
3.2.2 pH 对亚甲基蓝吸附效果的影响 在室温(25±0.5 ℃)及初始浓度为150 mg·L-1的亚甲基蓝溶液中,生物质炭用量为2 g·L-1及振荡120 min 的条件下,pH 值对亚甲基蓝吸附的影响如图3 所示。结果表明,pH 在2~6 条件下,玉米秸秆生物质炭对亚甲基蓝的吸附随着pH 值的增加而增多。玉米秸秆中的纤维素和木质素含有羟基和羧基等,可以为亚甲基蓝提供有效的吸附点位。但同时,亚甲基蓝是一种阳离子染料,酸性条件下,溶液中H+和H3O+与亚甲基蓝染料之间发生吸附竞争,导致吸附量变化不大,在74.82~75.00 mg·g-1之间变化。当pH 在6~10 之间,H+和H3O+的竞争吸附作用减弱,生物质炭对亚甲基蓝的静电吸引作用增强。而此时的pH 范围内,溶液中H+和OH-浓度相近,生物质炭表面的质子化/去质子化效应不显著,导致亚甲基蓝的吸附量增加缓慢。

图3 生物质炭用量和pH 值对亚甲基蓝吸附的影响Fig.3 Effects of biochar dosage and pH on methylene blue adsorption
3.3 吸附等温线
在初始溶液pH=6.0,生物质炭用量2 g·L-1及振荡120 min 条件下,不同温度(20 ℃,30 ℃和40 ℃)下对不同浓度亚甲基蓝(75 mg·L-1,100 mg·L-1,125 mg·L-1,150 mg·L-1,200 mg·L-1,250 mg·L-1及300 mg·L-1)吸附等温线如图4 所示。可以看出,20 ℃时生物质炭对亚甲基蓝的最大吸附量为77.64 mg·g-1;温度上升到30 ℃时,最大吸附量为80.92 mg·g-1;温度上升到40 ℃时,亚甲基蓝的最大吸附量达到84.89 mg·g-1,这表明玉米秸秆生物质炭对亚甲基蓝的吸附为吸热过程。

图4 生物质炭对亚甲基蓝的等温吸附Fig.4 Isothermal adsorption of methylene blue by biochar
通过Langmuir,Freundlich,Dubinin-Radushkevich (D-R)和Temkin 四个模型对吸附量进行拟合,拟合方程如下

式中,Qe和Qmax分别表示平衡吸附量(mg·g-1)和最大吸附量(mg·g-1);Ce为吸附平衡时的溶液平衡浓度(mg·L-1);KL和KF为Langmuir 常数(L·mg-1)和Freundlich 常数[(mg·g-1)·(L·mg-1)1/n];Qm为D-R 模型中的理论饱和吸附量(mg·g-1);为Polanyi 势能,A和B表示Temkin常数;T为热力学温度(K)。
四种等温吸附模型的拟合参数如表3 所示。Langmuir 方程的拟合度最好(图5),线性相关系数分别为0.9884(20 ℃)、0.9908(30 ℃)和0.9905(40 ℃),这表明吸附过程是单层吸附。由Freundlich模型拟合得到的相关系数为0.8814(20 ℃)、0.9327(30 ℃)和0.9517(40 ℃),拟合效果也较好(图5)。由图6 可以看出,Temkin 模型拟合得到的线性相关系数为0.8650(20 ℃)、0.9240(30 ℃)和0.9432(40 ℃),表明该模型也适用于解释玉米秸秆生物质炭吸附亚甲基蓝的行为。同时也说明吸附能量在生物质炭表面均匀分配,直至达到最大吸附[11]。D-R 模型的吸附拟合度最小,但相关系数R2为0.8458~0.9151,拟合效果也较好。

表3 不同等温吸附模型的参数统计Table 3 Parameter statistics of different isothermal adsorption models

图5 不同温度下生物质炭对亚甲基蓝的Langmuir 和Freundlich 吸附等温线Fig.5 Langmuir and Freundlich adsorption isotherms for methylene blue by bichar at different temperatures

图6 不同温度下生物质炭对亚甲基蓝的D-R 和Temkin 吸附等温线Fig.6 D-R and Temkin adsorption isotherms for methylene blue by biochar at different temperatures
3.4 吸附动力学
在室温(25±0.5 ℃),初始溶液pH=6.0 及生物质炭用量2 g·L-1条件下,生物质炭对不同初始浓度亚甲基蓝(150 mg·L-1、200 mg·L-1和250 mg·L-1)的吸附量随时间的变化如图7 所示。可以看出,在60 min 内不同浓度的亚甲基蓝溶液基本达到吸附平衡,达到总吸附量的89.35%~92.37%。这可能是因为吸附前期主要发生在生物质炭外表面,具有较快的吸附速率;当吸附由外表面过渡到微孔时,吸附容量缓慢增加,直至达到吸附平衡。
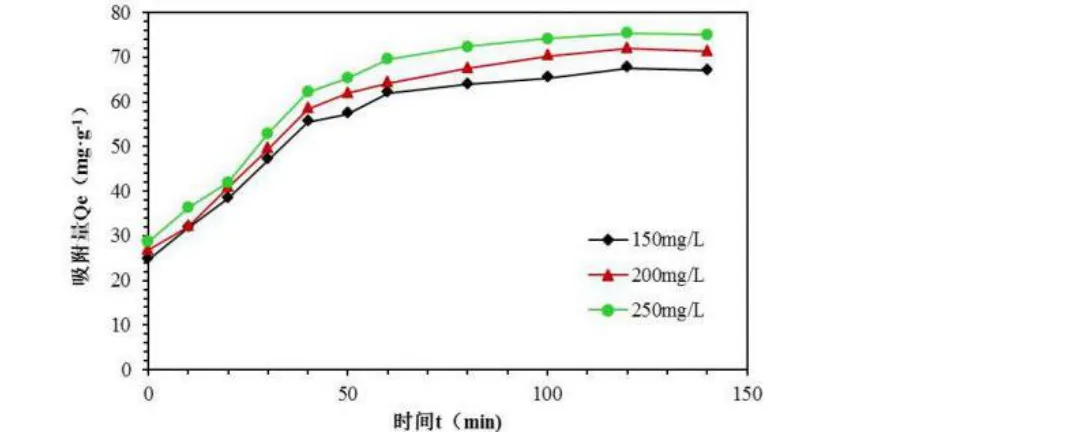
图7 生物质炭对亚甲基蓝溶液的吸附动力学曲线Fig.7 Adsorption kinetics curve of biochar to methylene blue solution
通过Lagergren 准一级动力学模型(式5)和准二级动力学模型(式6)对生物质炭吸附亚甲基蓝的动力学过程进行拟合:

式中,Qe和Qt分别表示平衡吸附量(mg·g-1)和反应时间为t时的吸附量(mg·g-1);K1和K2为准一级速率常数(min-1)和准二级速率常数(g·mg-1·min-1)。
图8 为通过准一级和准二级动力学模型拟合玉米秸秆生物质炭对亚甲基蓝的吸附参数。不同浓度溶液的一级动力学方程相关系数为0.9708、0.9797 和0.9669;二级动力学方程相关系数为0.9503、0.9503 和0.9454,相关系数均大于0.9。但是,二级动力学方程计算所得的平衡吸附量与实测值非常接近,说明生物质炭对亚甲基蓝的吸附符合准二级动力学模型。二级吸附速率常数K2随着亚甲基蓝溶液浓度的增加而减小,从150 mg·L-1的0.0018 g·mg-1·min-1降低到250 mg·L-1的0.0016 g·mg-1·min-1。吸附过程可以认为,吸附初期由于生物质炭存在大量的吸附点位,导致对亚甲基蓝吸附速率快,随着表面吸附点位逐渐饱和,吸附动力下降[12]。
3.5 吸附机理
3.5.1 Weber-Morris 模型 为评估扩散作用对生物质炭吸附亚甲基蓝过程产生的影响,通过Web-Morris颗粒内扩散模型(式7)对动力学结果进行分析[13]:
式中,Qt为t时刻的亚甲基蓝吸附量(mg·g-1),Kw表示吸附颗粒内扩散速率常数(mg·g-1·min0.5),与边界层厚度(mg·g-1)成正比关系。

图9 Webber-Morris 和Boyd 模型拟合曲线及参数Fig.9 Webber-Morris and Boyd models fitting curves and parameters
有研究表明,如果Qt与t1/2呈现线性关系,且直线没有截距,通过原点,说明吸附过程中完全受吸附颗粒内扩散控制[13]。本研究中通过Webber-Morris 模型模拟曲线(图9(a)),可知不同浓度的亚甲基蓝溶液拟合曲线的截距为24.119~27.143 mg·g-1,表明吸附过程由膜扩散和颗粒内扩散的共同作用而控制。
3.5.2 Boyd 模型 通过Boyd 模型评估生物质炭吸附亚甲基蓝过程中的实际速率控制步骤,主要包括膜扩散和孔扩散,分析模式如式(8)和(9)所示[14]:
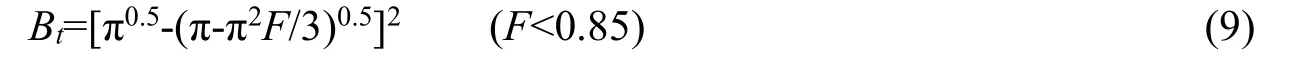
式中,F=Qt/Qe为反应t时刻的亚甲基蓝吸附量占平衡吸附量的比例,Bt是F的函数。图9(b)为Bt-t曲线,可以表明生物质炭吸附亚甲基蓝的吸附机理。有研究表明,如果曲线是过原点的直线,则吸附速率由颗粒内扩散控制,反之为膜扩散控制[15]。由图可以看出,Boyd 模型的模拟曲线相关性为0.9805~0.9821,截距为0.0241~0.1513,存在截距,这说明吸附速率由膜扩散控制。在玉米秸秆生物质炭对亚甲基蓝的吸附过程中,膜扩散起主导作用,与国内外诸多研究结果一致[13,16]。
4 结论
以浓H3PO4为活化剂,通过微波活化将玉米秸秆制备成生物质吸附剂,考察对亚甲基蓝的吸附性能。结果表明:(1)当玉米秸秆与浓磷酸浸渍比为1:1,预炭化时间为6 h,微波活化时间为5 min时,制备的生物质炭对亚甲基蓝的吸附量最大;(2)生物质炭吸附亚甲基蓝的最佳投加量为2 g·L-1;pH 在2~6 的范围内,随pH 值的增大,对亚甲基蓝的吸附量越多;(3)对亚甲基蓝的吸附为吸热过程,四种等温吸附模型拟合度最好的是Langmuir 模型,属于单分子层吸附;(4)吸附动力学符合准二级动力学模型,最大吸附量为75.19 mg·g-1。吸附速率由膜扩散控制,在吸附过程中起主导作用。

