频繁急性加重的慢性阻塞性肺疾病继发肺动脉高压的危险因素分析
王潇,许爱国
(郑州大学第一附属医院 呼吸与危重症医学科,河南 郑州 450000)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种呼吸系统常见病,以持续气流受阻为特征,严重危害人类健康,10 a后将成为全球第三大死因[1],慢性阻塞性肺疾病急性加重(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)及并发症均会严重影响患者预后。频繁急性加重的COPD指:每年COPD急性加重≥2次[2]。肺动脉高压(pulmonary arterial hypertension,PAH)是COPD的严重并发症之一,右心导管检查是PAH诊断的金标准,但因该检查项目昂贵、有侵入性,导致其使用受到限制。多普勒超声心动图(Doppler echocardiography,DE)具有无创、经济的优点,成为可疑PAH的首选检查[3],但对可疑PAH者的密切随访和预测能力不足。因此,越来越多的研究者致力于寻找能够协助诊断COPD继发PAH的无创且容易获得的生物标记物。研究表明COPD的进展与炎症反应密切相关,N端脑钠肽前体(N-terminal brain natriuretic peptide,NT-pro BNP)是公认的心衰指标[4]。目前对于频繁急性加重的COPD并发PAH的研究甚少。本研究采用DE测定患者的肺动脉压,收集多项生物标记物并进行分析,探讨频繁急性加重的COPD并发PAH的危险因素,分析NLR、NT-pro BNP对频繁急性加重的COPD继发PAH的预测价值。
1 资料与方法
1.1 研究对象回顾性分析于郑州大学第一附属医院2018年4月至2020年4月住院的频繁急性加重的122例COPD患者的病历资料,男90例,女32例,年龄40~90岁。纳入标准:符合《慢性阻塞性肺疾病诊治指南》[2]的诊断标准。排除标准:(1)合并肺癌、肺栓塞、哮喘等疾病;(2)患先天性心脏病;(3)患风湿结缔组织疾病;(4)合并严重的肝肾功能不全;(5)合并血液系统疾病。
1.2 研究方法收集所有纳入对象的临床资料,包括年龄、性别、吸烟指数、COPD病程。收集多项血清学检验结果。血常规项目:白细胞计数(white blood cell,WBC)、中性粒细胞计数(neutrophil,NEUT)、淋巴细胞计数(lymphocytes,LY)、中性粒细胞/淋巴细胞比值(neutrophil/lymphocyte ratio,NLR)。血生化项目:白蛋白、NT-pro BNP。炎症指标:C反应蛋白(C-reactive protein,CRP)、血沉(erythrocyte sedimentation rate,ESR)、降钙素原(procalcitonin,PCT)。记录所有纳入对象的肺动脉压和右室径。
1.3 分组根据DE测得的肺动脉压将研究对象分为两组:将PAP<35 mmHg(1 mmHg=0.133 kPa)的患者纳入非PAH组(60例)和将PAP≥35 mmHg的患者纳入PAH组(62例)。
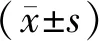
2 结果
2.1 一般资料两组性别、年龄、病程、吸烟指数比较,差异无统计学意义(P>0.05)。见表1。
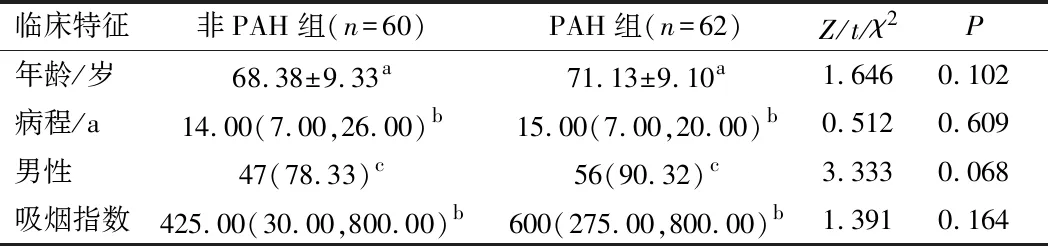
表1 两组患者一般资料比较
2.2 实验室指标PAH组NEUT、NLR、NT-pro BNP水平高于非PAH组,LY、白蛋白水平低于非PAH组,右室径大于非PAH组,差异有统计学意义(P<0.05)。两组WBC、ESR、CRP、PCT水平比较,差异无统计学意义(P>0.05)。见表2。

表2 两组实验室指标比较[M(P25,P75)]
2.3 NEUT、LY、NLR、NT-pro BNP及白蛋白截断值水平的确定分别绘制NEUT、LY、NLR、NT-pro BNP、白蛋白诊断频繁急性加重的COPD并发PAH的ROC曲线,得出各个指标的最佳临界值及相应的灵敏度与特异度。见表3。
2.4 频繁急性加重的COPD继发PAH的危险因素NLR>5.61、NT-pro BNP>590.61 ng·L-1是频繁急性加重的COPD继发PAH的独立危险因素(P<0.05)。见表4。
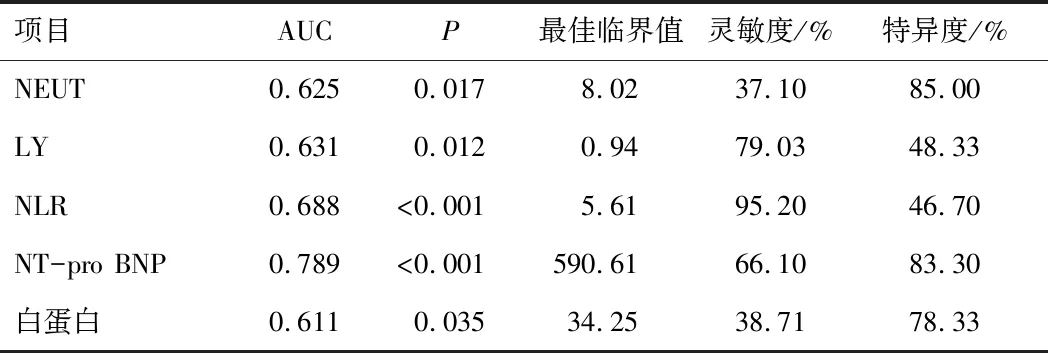
表3 NT-pro BNP、NLR对频繁急性加重的COPD继发 PAH的预测效能

表4 频繁急性加重的COPD并发PAH的logistic回归分析
3 讨论
COPD患者因长期缺氧可导致肺血管收缩甚至重塑,进而继发PAH。AECOPD常常存在严重的感染、缺氧、炎症反应,这些因素均可加快PAH的形成,导致心功能不全,又因机体高代谢状态、胃肠道淤血等因素导致营养不良,严重影响预后[5-6]。频繁急性加重的COPD继发PAH对患者的生活质量威胁更严重。因此,对频繁急性加重的COPD继发PAH早发现、早治疗显得尤其重要,但因早期PAH无特异的临床表现难以识别[7],故需寻找可靠的生物标记物协助频繁急性加重的COPD继发PAH的预测。
Humbert等[8]发现PAH患者肺血管重塑除了内皮细胞功能的病理损伤外,还有炎症细胞在血管周围过度浸润,炎症细胞的血管周围浸润通常先于结构性肺血管重构,表明炎症和免疫系统的紊乱有促进肺血管重塑的作用。陈康勰等[9]指出,急性加重的COPD 患者处于应激状态,糖皮质激素及儿茶酚胺水平升高,进而导致淋巴细胞计数下降。本研究发现,PAH组NEUT较非PAH组高,LY水平低,与既往研究结果[8-9]相符。近年来NLR受到广泛的关注,NLR是一个可以反映机体NEUT与LY的平衡状态的综合指标,目前已有很多其与炎症相关疾病的研究,例如恶性肿瘤[10]、溃疡性结肠炎[11]和ANCA相关性脉管炎[12]等。Zuo等[13]对AECOPD合并PAH患者的研究发现,PAH组NLR高于非PAH组,本研究也发现频繁急性加重的COPD继发PAH组NLR较非PAH组高。NT-pro BNP是公认的心衰标志物,而频繁急性加重的COPD继发PAH后可导致右心室前负荷增加,严重者将发生右心功能衰竭,因此有较多的研究者探讨NT-pro BNP与COPD及PAH之间的关系。王娜娜等[14]通过研究发现NT-pro BNP与肺动脉高压的严重程度呈正相关。本研究结果显示,PAH组NT-pro BNP高于非PAH组,与既往多个研究[15-18]结果相符。
Nursalim等[19]研究表明单一检测NEUT或LY评估患者的临床预后价值较低,与之结论大致相符,本研究发现NEUT及LY并非频繁急性加重的COPD继发PAH的独立危险因素,表明单一的NEUT或LY并不能作为其重要的预测指标。Zuo等[13]对AECOPD合并PAH研究发现,NLR的ROC曲线AUC为0.701,最佳临界值取4.65时灵敏度为81.2%,特异性为59.5%,然而NLR并非AECOPD合并PAH的独立危险因素。本研究结果显示,NLR在预测频繁急性加重的COPD继发PAH的ROC曲线中AUC为0.688,当NLR取最佳临界值5.61时,灵敏度为95.2%,特异度为46.7%,与之不同的是,本研究进行多因素logistic回归分析发现,NLR>5.61是频繁急性加重的COPD继发PAH的独立危险因素。结合既往的研究及本研究结果,表明NLR作为一种炎症的综合指标,对频繁急性加重的COPD继发PAH有值得肯定的临床预测价值。此外,NLR通过血常规计算NEUT与LY的比值即可获得。因此,对于医疗机构相对落后的社区医院来说,NLR对于预测频繁急性加重的COPD继发PAH具有很高的临床价值。李湘荣[17]研究发现NT-pro BNP可对COPD合并慢性呼吸衰竭的严重程度进行预测。Jin等[20]研究表明BNPrs198389基因座G等位基因、rs6668352基因座A等位基因和rs198388基因座T等位基因是COPD患者继发PAH的高风险因素。本研究通过ROC曲线分析显示,当NT-pro BNP取最佳临界值590.61 ng·L-1时,灵敏度为66.1%,特异度为83.3%,AUC为0.789,多因素logistic回归分析发现NT-pro BNP>590.61 ng·L-1是频繁急性加重的COPD继发PAH的独立危险因素。因此,对于临床疑似PAH患者可结合NT-pro BNP水平评估是否进行多普勒超声心动图或右心导管检查来进一步明确诊断,在一定程度上也减少了医疗资源的浪费。
综上所述,频繁急性加重的COPD患者继发PAH者NEUT、NT-pro BNP、NLR明显升高,LY、白蛋白明显降低。NLR>5.61、NT-pro BNP>590.61 ng·L-1是频繁急性加重的COPD继发PAH的独立危险因素,在PAH的预测上有一定的价值。因此,临床上关注NT-pro BNP、NLR指标水平,有助于早期识别频繁急性加重的COPD继发的PAH,以更好地协助临床医生诊疗。

