两种中药酊剂微生物限度方法适用性研究
杨群,肖文涛
九江市食品药品检验所,江西 九江 332000
酊剂系指将原料药物用规定浓度的乙醇提取或溶解而制成的澄清液体制剂,微生物污染情况是重要的药品质控指标[1,2]。按照《中华人民共和国药典》(2015年版)四部规定,非无菌产品需做微生物限度检査,且需采用通过方法适用性试验的检查方法。本研究中两种酊剂复方补芷酊、养血首乌酊由不同中药原料经乙醇提取制成,由于提取溶剂为75%的乙醇,以及中药原料固有成分的复杂性,存在不同程度的抑菌作用。依据《中华人民共和国药典》2015年版四部通则1105、1106、1107 要求,制剂进行微生物限度检查前应先消除其抑菌活性,避免试验干扰。本文对两种酊剂需氧菌、霉菌和酵母菌及控制菌进行试验,通过适用性试验研究,消除制剂的抑菌性,建立准确可靠的微生物限度检查方法。
1 仪器与试剂
1.1 仪器
LMQ.C型高压蒸汽灭菌器(山东新华仪器有限公司);YP1002N型电子天平(上海菁海仪器有限公司);BSC-1304IIB2型生物安全柜(苏净安泰空气技术有限公司);LRH-150型细菌培养箱(上海一恒科学仪器有限公司);SPX-150型霉菌培养箱(扬州慧科科学仪器有限公司);GHP-9162型生化培养箱(扬州慧科科学仪器有限公司)。
1.2 试剂、试药及培养基
复方补芷酊(批号:20200110、20200122、20200205)、养血首乌酊(批号:20200106、20200117、20200203),均由景德镇市皮肤病医院提供。胰酪大豆胨液体培养基(批号:190329),胰酪大豆胨琼脂培养基(批号:190518),沙氏葡萄糖琼脂培养基(批号:190402),pH 7.0 氯化钠缓冲蛋白胨水(批号:200319),均为北京陆桥技术股份有限公司生产;溴化十六烷基三甲胺琼脂(批号:1073801),甘露醇氯化钠琼脂(批号:3102307)均为广东环凯微生物科技有限公司生产。
1.3 工作菌株
枯草芽孢杆菌CMCC(B)63501(批 号:200411),金黄色葡萄球菌 CMCC(B)26003(批号:200305),铜绿假单胞菌CMCC(B)10104(批号:200317),白色念珠菌CMCC(F)98001(批号:201108),黑 曲 霉CMCC(F)98003 (批号:200514),均由北京三药技术开发公司生产。
2 方法与结果
复方补芷酊和养血首乌酊均为皮肤给药制剂,其微生物限度标准如下:需氧菌总数不超过100 cfu/mL(1 mL或1 g可接受的最大菌数为200 cfu),霉菌和酵母菌总数不超过10 cfu/mL(1 mL或1 g可接受的最大菌数为20 cfu),不得检出金黄色葡萄球菌、铜绿假单胞菌(1 mL)。
2.1 菌液制备
取枯草芽孢杆菌、金黄色葡萄球菌、铜绿假单胞菌、白色念珠菌、黑曲霉冻干物,分别吸取复溶液1 mL加入菌株西林瓶中,盖上瓶盖,静置5~10 s,涡旋震荡5~10 s。吸取1 mL加入9 mL无菌生理盐水,混匀,逐级进行10倍稀释,最终使其含菌数约5 000~10 000 cfu/mL。
2.2 供试液制备
取供试品10 mL,置锥形瓶中,加无菌生理盐水至100 mL,震荡混匀,作为1∶10供试液。
2.3 回收测定(平皿法)
2.3.1 需氧菌总数计数实验组:取供试液9.9 mL,加入适宜浓度的试验菌液0.1 mL,混匀,使每1 mL供试品中含菌量不大于100 cfu。取1 mL注入平皿,立即注入胰酪大豆胨琼脂培养基,置35 ℃培养箱培养24~72 h逐日观察结果。
供试品对照组:取上述供试液,以稀释液代替菌液,同实验组操作,测定供试品本底菌数。
菌液对照组:取相应稀释液替代供试液,按试验组操作加入试验菌液并进行微生物回收试验。
2.3.2 霉菌和酵母菌总数计数实验组:取上述试液9.9 mL,加入适宜浓度的试验菌液0.1 mL,混匀,使每1 mL供试品中含菌量不大于100 cfu。取1 mL注入平皿,立即注入沙氏琼脂培养基,置25 ℃培养箱培养24~120 h逐日观察结果。供试品对照组:取上述供试液,以稀释液代替菌液,同实验组操作,测定供试品本底菌数。菌液对照组:取相应稀释液替代供试液,按试验组操作加入试验菌液并进行微生物回收试验。
2.4 回收计算
按如下公式计算试验组的加菌回收比例:
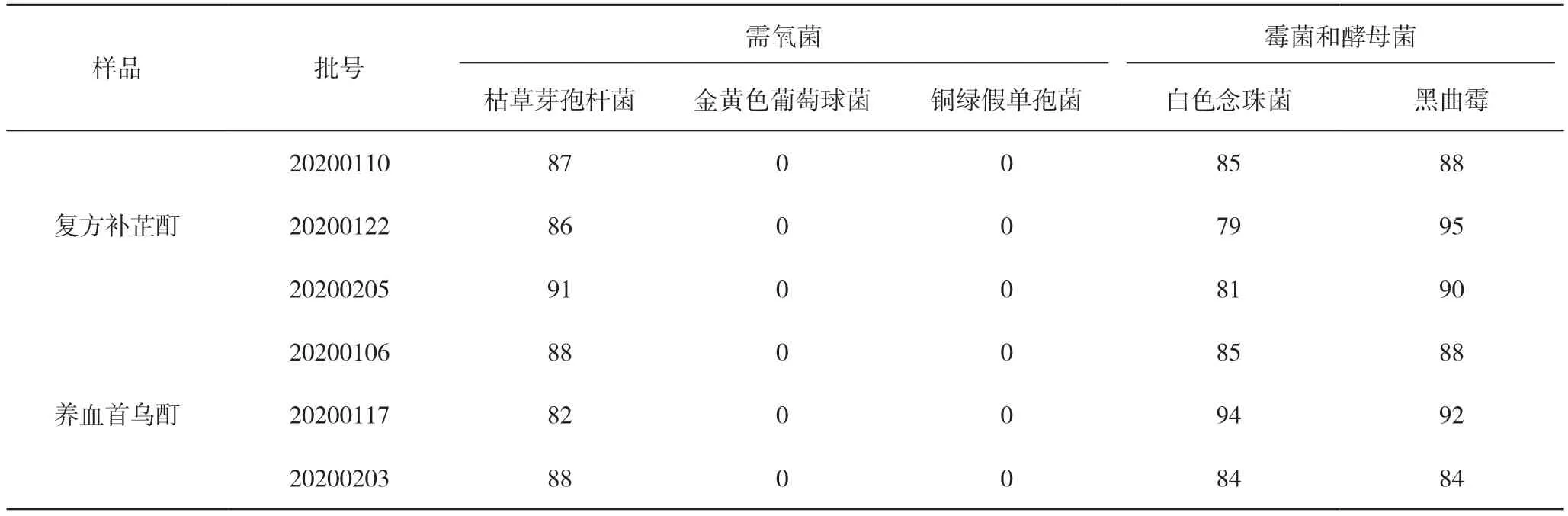
表1 试验组加菌的回收率 %
由表1可见,平皿法对金黄色葡萄球菌和铜绿假单孢菌有极强的抑制作用,选用薄膜过滤法对需氧菌进行试验。
2.5 回收测定(薄膜过滤法)
2.5.1 实验组取供试液1 mL,采用薄膜过滤法,每筒用pH7.0无菌氯化钠-蛋白胨缓冲液300 mL分3次冲洗,在最后一次冲洗液中加入不大于100 cfu的试验菌,滤干,立即贴膜与胰酪大豆胨琼脂培养基,置35 ℃培养箱培养24~72 h逐日观察结果。
2.5.2 供试品对照组取上述供试液,以稀释液代替菌液,同实验组操作,测定供试品本底菌数。
2.5.3 菌液对照组取相应稀释液替代供试液,按试验组操作加入试验菌液并进行微生物回收试验。
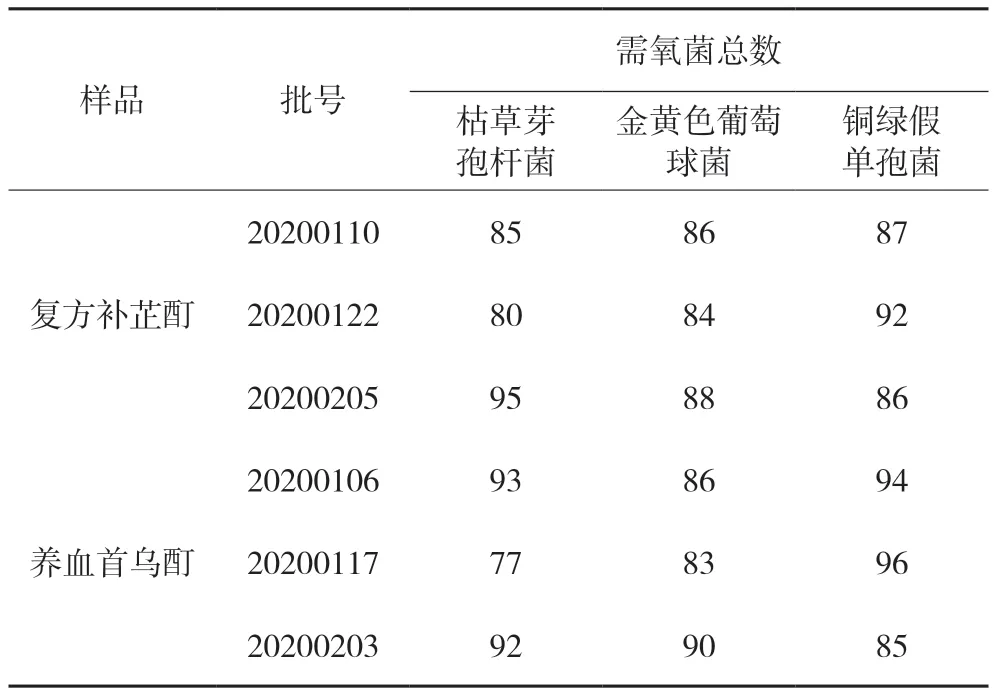
表2 试验组加菌的回收率 %
由表2可见,薄膜过滤法可消除制剂的抑菌作用,选用薄膜过滤法对需氧菌进行试验。
2.6 样品细菌、霉菌和酵母菌检查结果
取复方补芷酊和养血首乌酊各3批,需氧菌总数按照薄膜过滤法操作步骤,霉菌和酵母菌总数按照平皿法操作步骤,对6批样品进行微生物限度检查,结果显示,样品中需氧菌总数均小于10 cfu/mL、霉菌和酵母菌总数均小于10 cfu/mL,符合相关规定。
2.7 控制菌检查结果
取复方补芷酊和养血首乌酊各3批,金黄色葡萄球菌和铜绿假单孢菌按照薄膜过滤法操作步骤,结果显示,样品中金黄色葡萄球菌和铜绿假单孢菌均未检出。
3 讨论
两种制剂采用平皿法检验时,对需氧菌有明显抑菌作用,金色葡萄球菌和铜绿假单孢菌回收率远低于70%,对霉菌则无影响。该两种医院制剂由75%乙醇提取制成,经测定制剂乙醇实际浓度60%~70%,乙醇溶剂20%即具有不同程度的抑菌作用。同时中药成分复杂,自身也存在不同程度的抑菌作用,其抗菌作用不仅体现在方剂有效成分对细菌直接抑杀,同时还表现在方剂中各味药多种成分相互作用的综合效应上[3]。考虑两种制剂均有一定的抑菌性,且易溶于水,采用薄膜过滤法可快速、有效地去除药品中所含有的抑菌性,提高检验的效率和结果的准确性[4],而平皿法相对简单经济,微生物检验时可根据实际情况采用不同稀释级的平皿法或薄膜过滤法检测[5]。
本研究根据其对不同菌种的抑菌特性,可采用薄膜过滤法测定需氧菌,平皿法测定霉菌及酵母菌,结果可靠,回收率均达到0.5~2.0。建立了可靠的微生物检查方法,消除干扰,为含抑菌成分的外用制剂的微生物限度检查方法适用性试验的研究提供参考和研究思路,进一步保证制剂的检测可靠性和科学性。

