水杨酸分子印迹聚合物整体柱合成及其固相微萃取应用
余小芳,曹逸非,张珊珊,彭帆,陈怀侠
(湖北大学化学化工学院,湖北 武汉 430062)
0 引言
水杨酸(邻羟基苯甲酸,salicylic acid,2-HBA)是重要的医药中间体和精细化工原料,常用于制备阿司匹林、抑氮磺胺、水杨酸钠、水杨酸偶氮磺胺二甲嘧啶、二氟苯水杨酸、水杨酰胺、乙氧酰苯氨、扑炎痛、水杨酸萘酯、罗匹宁、乙酰水杨酰胺、沙利芬、芬胺呋和醋醚水杨胺等医药产品.水杨酸具有去角质和清理毛孔的作用,广泛用于医疗保养品,有很好的淡化色素斑、缩小毛孔、去除细小皱纹及改善日晒引起的老化等效果,安全性较高,对皮肤的刺激低.因此,作为典型的药物与个人日用品,水杨酸成为环境水体中的新型微污染物.而人体摄入过量的水杨酸会刺激消化道而产生食道的黏膜和内膜的毒副作用,并能与机体组织中的蛋白质发生反应,产生腐蚀作用,从而引起腹泻、呕吐、腹痛、酸中毒、呼吸频促等症状[1].所以,环境水体中的水杨酸残留会造成人类的健康危害[2].因此,建立一种简便快速、高灵敏度的方法进行环境水体中水杨酸的测定尤为重要[3-5].
水杨酸的检测方法主要有气相色谱法[6]、液相色谱法[7]、气质联用法[8]、液质联用法[9]等.其中,液相色谱法具有对分析物热稳定性、沸点和分子量没有限制的特点而得到广泛应用,但是选择性灵敏度有限.而样品前处理可以有效提高该方法的灵敏度和选择性.分子印迹聚合物能够对模板选择性的吸附富集,满足分析的需要,在样品前处理中的应用得到了迅速发展.分子印迹技术具有高选择性[10-14],与整体柱材料[15-17]相结合即成为分子印迹整体柱,合成简单,省去了研磨、过筛、填料等一系列复杂过程,重复性好,柱压低,为快速传质提供了便利.S.G.Dmitrienko等考察了分子印迹聚合物对水杨酸及其酯类的选择性吸附能力,获得了较好的结果[18],但目前还鲜见水杨酸分子印迹有机聚合物整体柱固相微萃取研究的报道.
本研究以水杨酸为模板分子,采用原位聚合法,在移液枪小枪头中合成了水杨酸分子印迹整体微柱,并对分子印迹聚合物进行了表征和固相微萃取应用研究.考察了合成条件和萃取条件,建立了环境水样中水杨酸的SPME-HPLC定量分析方法.该方法简单方便、选择性好、灵敏度高,分离富集效果好,适用于环境样品中水杨酸残留的分析测定.
1 实验部分
1.1 仪器与试剂Dionex ultimate 3000型高效液相色谱仪(美国Dionex公司);PDA-3000 光电二极管矩阵检测器(美国Dionex公司);Amethyst-C18(4.6 mm×250 mm,5 μm)色谱柱(美国Sepax Technologies,DE);BS210S分析天平(北京赛多斯天平有限公司);超声清洗仪(美国Branson公司);100~1 000 μL可调式移液器(上海热电仪器有限公司);兰格LSP01-1A型注射泵(保定兰格恒流泵有限公司);X-650 扫描电子显微镜(日本日立电子电气公司);WH-3 微型漩涡混合仪(上海沪西分析仪器厂有限公司);DZF-6021 型真空干燥箱(上海一恒科学仪器有限公司);AWJ1-0501-U 型超纯水机(艾科浦公司);移液枪枪头(4*49,200 μL).
水杨酸(2-HBA,分析纯)购自广州化学试剂厂;对羟基苯甲酸(PHBA,分析纯)购自北京化工厂;甲硝唑(MNZ,分析纯)购自中国生物药品制品检验所;甲苯和十二醇(分析纯)均购自天津市富晨化学试剂厂(分析纯,使用前减压蒸馏处理);4-乙烯基吡啶(4-VP,95%)购自美国Acros公司;丙烯酰胺(AM)购自武汉市华顺生物技术有限公司(使用前重结晶);乙二醇二甲基丙烯酸酯(EGDMA)购自美国Acros公司(先用5%NaOH溶液萃取3次,再用超纯水洗去多余的NaOH,最后用无水MgSO4干燥后使用);偶氮二异丁腈(AIBN,化学纯)购自上海试剂四厂(使用前用无水乙醇重结晶);甲醇和乙腈(色谱纯)均购自美国Tedia公司;超纯水.
标准储备液的配制:配制1.0 mg/mL的水杨酸的甲醇溶液,4 ℃冷藏储存.
标准溶液的配制:用超纯水稀释水杨酸储备液而制得,现配现用.
样品溶液的配制:分别取自来水、长江水和沙湖水,用0.22 μm的滤膜过滤两次后于4 ℃冰箱冷藏储存.
1.2 聚合物整体柱的合成水杨酸分子印迹聚合物整体柱(MIP)的合成:7.2 mg(0.05 mmol)水杨酸充分溶解于360 μL十二醇和45 μL甲苯中,加入21 μL(0.2 mmol)4-VP,超声预聚合4 h,加入170 μL(0.9 mmol)EGDMA和8 mg AIBN,溶解均匀后超声脱气10 min,立即转至200 μL规格的移液枪头中并将两端密封,置于真空干燥箱60 °C反应24 h.反应完成后,用甲醇将洗尽模板分子和杂质,用超纯水平衡后备用.
非印迹聚合物整体柱 (NIP)的合成:除不加入水杨酸外,其他步骤同上.
1.3 MIP-PMME过程用5 mL甲醇清洗印迹柱,以1 mL超纯水活化.取5 mL样品溶液以0.15 mL/min的流速上样后,用500 μL超纯水清洗,再用80 μL乙腈∶水(90∶10)混合液洗脱,洗脱液直接进行HPLC分析.
1.4 分子印迹整体柱选择性的考察2 mL 400 ng/mL水杨酸、对羟基苯甲酸和甲硝唑混合水溶液,以0.10 mL/min的流速分别用印迹柱和非印印迹柱进行萃取,经500 μL超纯水清洗后,用100 μL甲醇洗脱后直接进行HPLC分析,通过比较印迹柱和非印迹柱对目标物及非类似物的富集能力来评价分子印迹柱的选择吸附性.
1.5 色谱条件色谱柱:Amethyst C18柱(5 μm,4.6 mm×250 mm);流动相:甲醇∶ 0.05%甲酸水溶液为70∶30 (V∶V);流速:1.0 mL/min;柱温:30 ℃;进样量:100 μL;检测波长:2-HBA为235 nm、PHBA为256 nm、MNZ为320 nm.
2 结果与讨论
2.1 合成条件的优化合成条件改变影响着合成的分子印迹聚合物的形态特征和选择性吸附能力.本文中主要研究以水杨酸为模板分子合成时选择不同的功能单体的影响并优化了模板分子与功能单体比例.
2.1.1 功能单体的选择 由于水杨酸为酸性化合物,为了使分子印迹整体柱获得较好的识别选择性,所以选择碱性或中性功能单体.本实验分别考查了AM、4-VP为功能单体时聚合物整体柱的选择性和富集能力.
0.05 mmol水杨酸、0.2 mmol不同的功能单体,360 μL十二醇和45 μL甲苯为致孔剂,170 μL (0.9 mmol)交联剂EGDMA、8 mg引发剂AIBN置于真空干燥箱60 ℃反应24 h.分别比较不同功能单体对印迹柱选择性和富集效果的影响,结果如表1.显然,当4-VP为功能单体时,水杨酸印迹整体柱选择性好,而AM为功能单体时,整体柱富集能力较强,综合考虑,后续实验选择4-VP为功能单体.

表1 2-HBA的功能单体对MIP整体印迹因子的影响
2.1.2 模板分子与功能单体比例的优化功能单体的选择 功能单体与模板分子的比例直接影响印迹聚合物整体柱的识别性能,当功能单体的量过多而模板分子过少时,聚合物的识别位点数量减少,识别能力差,选择性差,同时非特异性吸附严重;相反,若功能单体偏少而模板分子过多,也不能形成丰富的分子识别位点,同时会造成模板分子的浪费,所以必须对模板分子与功能单体的比例进行优化.
本研究根据模板分子水杨酸与功能单体4-VP的结构推出反应的大致比例,然后选取了水杨酸与4-VP摩尔比分别为1∶2和1∶4进行了比较,结果见表2.可见,当模板分子与功能单体为1∶4时,印迹柱的印迹因子更大,这可能是由于功能单体的量增多时,能与模板分子充分预聚合,识别位点增加.但功能单体过多,印迹柱的非特异性吸附将相应增加,选择性会下降,故后续实验选择模板分子与功能单体的比例为1∶4.

表2 模板与功能单体的摩尔比对2-HBA MIP单体印迹因子的影响
2.2 聚合物整体柱结构表征及选择性考察水杨酸分子中的羧基和羟基氢均能够与4-VP分子中的N原子形成氢键,加入交联剂将这种作用记忆下来,合成结束,去除模板水杨酸分子,聚合物整体柱中就形成了与水杨酸分子空间尺寸和化学结构相匹配的位点空穴,从而对水杨酸具有选择性的分子识别,其作用机理见图1.

图1 MIP的印迹工艺示意图


图2 2-HBA、4-VP、MIP和NIP的FT-IR光谱
用扫描电镜对水杨酸分子印迹聚合物整体柱的形貌特征进行了表征,见图3.显然,聚合物中存在着较多不同尺寸的微孔,这些微孔相互连通形成整体柱的双连续结构,从而具有很好的渗透性,为整个萃取过程快速顺利的完成提供了有利条件.

图3 MIP整体的SEM图像(放大倍数5 000倍)
为了表征分子印迹整体柱的选择性,将印迹柱和非印迹柱作比较,同时考察了他们对模板分子水杨酸及其类似物对羟基苯甲酸和非类似物甲硝唑的吸附作用.结果如图4所示,和非印迹柱相比,印迹柱对模板及其类似物具有良好的吸附性,且对模板具有更高的吸附能力,而印迹柱和非印迹柱对非类似物的吸附能力相当,即该印迹柱对水杨酸具有很好的选择性和富集能力.

图4 MIP、NIP对2-HBA、4-HBA和MNZ富集倍数(5 mL 50 ng/mL样品溶液,80 μL 90∶10的乙腈∶水混合液洗脱)
2.3 MIP-PMME条件的优化对于分子印迹聚合物整体柱微萃取来说,影响萃取效率的因素主要有样品pH、体积和流速,以及洗脱剂种类和体积等.使用 100 ng/mL 的水杨酸标样对上述因素进行了优化.
目前还没有环境水样中水杨酸残留量的标准出台,本方法的选择性很高,检测限达到ng/mL数量级,满足环境微污染物定量分析的要求.
2.3.1 上样pH的影响 恒定样品体积为5 mL,分别用磷酸调节样品pH为2~6,上样后用100 μL甲醇进行洗脱进样,结果如图5(A).可见,溶液pH增大时,回收率降低,这可能是由于水杨酸的pKa为2.98,当pH小于3时,水杨酸以分子形态存在,更容易被印迹位点识别,故后续的实验选择pH=2为最佳酸度条件.
2.3.2 上样体积的影响 分别上样5、6、7、8、9 mL,考察样品体积对提取效率的影响,见图5(B).可见,随着上样体积的增大,回收率不断下降,选择5 mL为合适的样品体积.
2.3.3 萃取流速的影响 上样5 mL,流速在0.05~0.30 mL/min之间变化时,提取效率见图5(C).可见,当流速为0.15 mL/min时萃取效率最好,故后续实验中上样流速均选择为0.15 mL/min.
2.3.4 洗脱剂种类的影响 将5 mL 100 ng/mL pH=2的水杨酸水溶液以0.10 mL/min的流速通过分子印迹整体柱,然后用500 μL的水清洗,再用100 μL的不同洗脱剂洗脱.考虑到与高效液相色谱流动相的一致性,考察了甲醇和水、乙腈和水为洗脱剂时的回收率.如图5(D),5(E)无论是使用甲醇和水或者乙腈和水混合液做洗脱剂,回收率都随着水比例的增加先上升后下降,而且乙腈比甲醇有更好的洗脱能力,当洗脱剂为乙腈和水为9∶1时,回收率达到最高,最终选择洗脱剂为乙腈和水为9∶1(V∶V).
2.3.5 洗脱剂体积的影响 将5 mL 100 ng/mL水杨酸水溶液以0.15 mL/min通过水杨酸分子印迹整体柱,用500 μL的水清洗,再分别用50、70、80、100和150 μL的洗脱液洗脱.结果如图5(F).显然,随着洗脱液体积的增加,回收率增加,当洗脱液体积增加到80 μL后,回收率变化不大,所以选择80 μL的乙腈和水(9∶1)为合适的洗脱剂.

图5 上样条件及洗脱条件优化
2.4 方法评价图6为空白自来水样品分析、样品添加350 ng/mL的水杨酸直接HPLC分析与MIP-PMME-HPLC分析的色谱图,显然,该印迹柱对水杨酸有很好的分离富集效果.
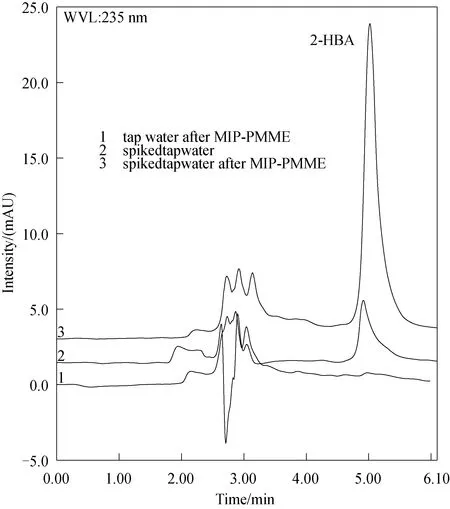
图6 自来水中2-HBA的HPLC色谱图2-HBA样品溶液添加到350 ng/mL;HPLC条件∶流动相,MeOH- 0.05%甲酸(70∶30,V/V)(1) MIP-PMME后的自来水;(2)添加了杂质的自来水;(3) MIP-PMME后添加的自来水
分别以3倍和10倍信噪比计算检出限和定量限,得到自来水、长江水和沙湖水中水杨酸的检出限为1.2 ng/mL,定量限为4.0 ng/mL.该方法的重现性如表3,日间精密度为连续4 d分别对添加含量为10、100、350 ng/mL自来水、长江水和沙湖水样品进行萃取所得.日内精密度为同一天内分别对同上述浓度样品3次测定所得.结果表明,方法重复性良好,日内小于8.1%,日间小于9.8%,满足常规分析要求.
2.5 实际样品分析对本实验室自来水、长江水和沙湖水进行MIP-PMME-HPLC分析,均未检出水杨酸.为了考察MIP-PMME-HPLC方法对检测水样中水杨酸的适用性和可靠性,分别对空白样品中加入高、中、低3种浓度的水杨酸,空白水样中的加标浓度分别为10、100、350 ng/mL,结果见表3.该方法对水杨酸在水样中的加标回收率分别为92.1%~105.8%.

表3 MIP-PMME-HPLC法测定自来水、长江水和沙湖水中2-HBA的回收率、准确度、LODs和LOQs
3 结论
优化合成条件,以水杨酸为模板分子,4-VP为功能单体,在模板分子∶功能单体∶交联剂为1∶4∶18的最佳条件下,运用原位聚合法在移液枪头中合成了水杨酸印迹聚合物整体柱,是良好的吸附传质介质.而且,材料合成步骤简单,对水杨酸有较强的选择性吸附能力.优化上样溶液pH、体积、萃取流速、洗脱剂种类、体积等萃取条件后,建立了SPME-HPLC定量分析方法,对环境水样进行了测定,水样中水杨酸在5~500 ng/mL浓度范围内线性关系良好,检出限(LOD)为 1.2 ng/mL,回收率的范围在 92.1%~105.8% 之间,日内、日间精密度(RSD)均小于 9.8%.该方法简单快速、选择性高、灵敏度高,适合于环境水样中水杨酸的分离分析.

