云南白药活性肽牙膏成分有效性研究及牙膏临床验证
张秋霞 刘 萍 宁科功 伍 鹏 蔡 英 李劲峰 李黎仙 陈 邈 孔祥烨 高 鹰
(云南白药集团股份有限公司,云南 昆明 650217)
引言
云南白药散剂创始于1902年,主要功能为化瘀止血,活血止痛,解毒消肿。用于跌打损伤,瘀血肿痛,吐血,咳血,便血,疮疡肿毒及软组织挫伤,溃疡病出血,以及皮扶感染性疾病。迄今为止在众多的临床研究中显示,对于多种出血性疾病都有明显的疗效,可以加速止血、缩短病程。其机理主要是缩短出血时间和凝血时间,云南白药能使凝血酶原时间缩短,增加凝血酶原含量[1],并能诱导血小板的聚集和释放[2]。对于创伤出血、消化道出血、呼吸道出血、出血性脑病,妇科、小儿科、五官科出血性疾病都有很好的治疗效果;同时云南白药通过抑制组胺和PG炎症物质的释放,有效减弱炎性介质所引起的肿胀和毛细血管渗透性;改善微循环,促进组织生长因子增殖[3],使炎症组织得到良好修复。
美洲大蠊(Periplanetaamericana)提取物主要化学成分为肽类、多种氨基酸、核苷类、信息素类、多元醇、蛋白质、糖类、生物碱类、有机酸 以及脂肪酸等化合物[4,5]。在临床主要应用于消化科、口腔科、外科、耳鼻喉科等创面修复的治疗中。功能为促进组织修复,调节免疫功能等[6-8],外用特别对烧伤、烫伤、压疮等修复效果显著。
利用云南白药提取物和美洲大蠊提取物组合成更有效的活性组合物,并用于牙膏产品中使其发挥良好的保护口腔组织、减少口腔问题的作用。
1 实验材料
1.1主要试药
云南白药活性肽组合物(云南白药美洲大蠊组合物BYPA)由云南白药集团股份有限公司提供。氯化钠,二甲苯,丙酮,甲醛,苯酚,冰醋酸,水合氯醛,乙醇,30%过氧化氢为常规分析纯试剂。依文思蓝:深蓝色粉末,规格5g/瓶,批号M3474,MP Biomedicals,LLC,法国。白砂糖:耿马三山牌白砂糖。亚甲蓝:北京化工厂,批号860522。
1.2实验动物
ICR小鼠,SPF级,26~30g,雄性,动物合格证号SCXK(川)2013-24,购自成都达硕生物科技有限公司。
KM小鼠,SPF级,26~30g,雄性,动物合格证号SCXK(川)2013-24,购自成都达硕生物科技有限公司。
SD大鼠,SPF级,200~220g,雄性,动物合格证号SCXK(川)2013-24,购自成都达硕生物科技有限公司。
Hartley豚鼠:健康一级,雄性,200~300g,动物合格证号SCXK(川)2013-14,购自四川省动物管理委员会养殖场。
日本大耳白兔:健康一级,雄性,2.0~3.0kg,动物合格证号SCXK(川)2013-14,购自四川省实验动物专委会养殖场。
1.3动物饲养
动物常规饲养于四川大学华西药学院动物房,实验动物设施使用许可证号:SYXK(川)2013-113号。饲养条件:笼养,小鼠、大鼠、豚鼠5只/笼;家兔2只/笼。自然照明,自由觅食及摄水。室温23±1℃;湿度50%~60%。动物饲料购自四川大学实验动物中心。饮水为高压灭菌蒸馏水。
2 实验方法与结果
2.1组合物对二甲苯所致ICR小鼠耳壳急性炎症反应的影响
雄性SPF级ICR小鼠,禁食12小时后称重,挑选体重26~30g合格动物,按体重随机分组,随机均分为3组:空白正常组、模型组、受试品组,每组10只。除正常组小鼠右耳给予50μl/只生理盐水外,其余各组小鼠右耳在给予50μl/只二甲苯刺激后,分别于15分钟、30分钟、45分钟耳廓局部给予不同受试品溶液70μl/只,溶媒对照组给予等体积生理盐水,60分钟时颈椎脱臼处死动物,沿耳廓基线剪下两耳,盲法用打孔器(直径7mm)分别在相同部位打下圆耳片、1/万电子天秤称重。以左右两耳片重量之差作为耳肿胀度。
肿胀抑制率=(模型组肿胀度-给药组肿胀度)/ 模型组肿胀度×100%
实验结果用均数±标准差表示,采用SPSS19.0软件One-Way ANOVA分析进行组间差异的显著性检验。结果见表1。
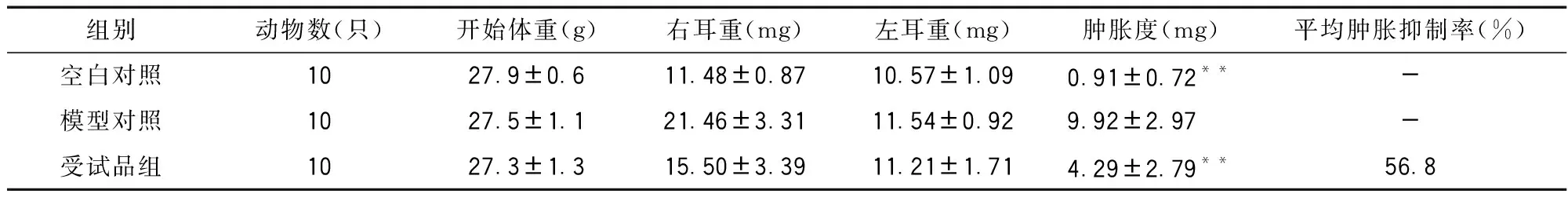
表1 受试品对二甲苯所致ICR小鼠耳壳急性炎症的影响
由表1可见,在本实验条件下,二甲苯作用1小时后,肉眼可见模型组小鼠左耳红肿、增厚明显;在二甲苯作用1小时期间,间隔三次给药后,与模型组(给予生理盐水)比较,受试品组对二甲苯所致小鼠耳壳炎性肿胀有56.8%的抑制作用,肿胀度与模型对照组比较有显著统计学差异(P<0.01)。
2.2组合物对小鼠断尾出血的止血作用比较研究
取SPF级雄性ICR种小鼠,挑选体重22~25g合格动物,按体重随机分组,随机均分为2组:空白对照组、受试品组,每组10~12只。以尾部浸泡接触法给药,将小鼠固定于小鼠筒中,尾尖部2cm浸泡于400μl的受试品溶液或生理盐水中,给药时间30分钟,间隔4小时后,重复给药1次。末次给药30分钟后,以利剪在小鼠距尾尖1.5cm处剪断,待血液自然流出时开始计录出血时间,每隔10s用事先已称重的棉球吸取血滴,直至出血自然停止(棉球吸时无血),1/万天平上称量带血棉球重量。按下式计算各组动物出血量:
出血量=带血棉球重量-初始棉球重量 (毫克)
实验结果用均数±标准差表示,采用SPSS19软件One-Way ANOVA分析进行组间差异的显著性检验。结果见表2。

表2 受试品对清醒小鼠断尾出血的影响
由表2可见,与空白溶媒对照组比较,受试品对清醒小鼠断尾出血时间有明显缩短(P<0.05),受试品对清醒小鼠断尾出血量均值有减少的倾向。
2.3组合物对豚鼠口腔溃疡的治疗作用比较研究[9-11]
取健康雄性豚鼠,适应性喂养5天后挑选体重200~300g合格动物,用乙醚将豚鼠麻醉后,用内径0.6cm、长3cm的塑料管垂直固定于豚鼠口腔粘膜表面,在管内放入充分浸润了40%冰醋酸的棉签,60秒后将棉签和塑料管取出,并迅速用水冲洗创面1分钟。于造模24小时后,测量动物口腔溃疡面积,并按随机分为空白溶媒组、受试品组。用医用棉签分别浸润受试样品后、充分涂抹每只动物口腔溃疡局部、并保持药棉与溃疡面接触60秒,每天上下午各给药1次, 连续给药直至每只动物口腔溃疡完全愈合。空白溶媒组同法给予生理盐水。实验中前5天期间,每天盲法测量动物口腔溃疡面积,按下式计算给药后溃疡面积变化百分率:
溃疡面积变化百分率=Sx/ S0×100%
其中,S0为给药前溃疡面积(mm2),Sx为给药后各天溃疡的面积(mm2)。
实验结果用均数±标准差表示,采用SPSS19.0软件One-Way ANOVA分析进行组间差异的显著性检验。
本实验观察发现:40%冰醋酸可致豚鼠口腔面颊侧粘膜急性炎症反应,在粘膜局部可见明显的红肿、黄白色假膜、继而粘膜坏死、脱落,形成溃疡面。口腔溃疡造模后,每日2次局部给予不同受试品,每日观察动物口腔溃疡面积的变化情况,并记录每只豚鼠口腔溃疡的愈合时间。结果见表3。

表3受试品对豚鼠实验性口腔溃疡的治疗作用
由表3可见,药后1~4天期间,受试品组口腔溃疡面积与同期溶媒对照组比较有相应减小,第4天减小明显(P<0.01);同时受试品组口腔溃疡完全愈合时间也明显小于溶媒对照组(P<0.01)。结果表明受试品对豚鼠口腔腔溃疡具有明显的治疗作用。
2.4组合物对家兔口腔溃疡的治疗作用比较研究[12]
取健康雄性家兔,适应性喂养5天后挑选体重2~3kg合格动物,用乙醚将其麻醉后,用内径为0.7cm,长为3cm的塑料管垂直固定于家兔口腔粘膜表面,在管内放入充分浸润了90%苯酚溶液的棉签,于造模后24小时,测量动物口腔溃疡面积并随机分为空白溶媒组、受试品组。用医用棉签分别浸润受试样品后、充分涂抹每只动物口腔溃疡局部、并保持药棉与溃疡面接触60秒,每天上下午各给药1次,连续给药直至每只动物口腔溃疡完全愈合。空白溶媒组同法给予生理盐水。实验中前5天期间,每天盲法测量动物口腔溃疡面积、观察溃疡感染程度并参照表4标准评分。

表4 口腔溃疡表面感染情况评分标准
按下式计算给药后溃疡面积变化百分率:
溃疡面积变化百分率=Sx/S0×100%
其中, S0为给药前溃疡面积(mm2),Sx为给药后各天溃疡的面积(mm2)。
实验结果用均数±标准差表示,采用SPSS19软件One-Way ANOVA分析进行组间差异的显著性检验。
在本实验中,苯酚所致家兔口腔溃疡模型中,溃疡周围充血严重、溃疡表面可见明显感染情况。口腔溃疡造模后,每日2次局部给予不同受试品,每日观察动物口腔溃疡面积及感染程度的变化情况,并记录每只家兔口腔溃疡的愈合时间。结果见表5。

表5 受试品对日本大耳白兔口腔溃疡的治疗作用
由表5可见,药后1~4天期间,受试品组口腔溃疡面积与同期溶媒对照组比较均有明显的减小(P<0.05或P<0.01)。给药前,溶媒对照组与给药组的口腔溃疡感染程度评分均为最高值4.0,组间没有差异(P >0.05);局部给药治疗4天后,受试品组的口腔溃疡感染程度有非常显著改善(P<0.01)。此外,由表5可见,与溶媒对照组比较,受试品组的口腔溃疡愈合时间有明显缩短(P<0.01),受试品组与溶媒对照组比较有显著差异。本结果表明受试品对家兔口腔溃疡具有明显的治疗作用。
2.5组合物对大鼠牙周炎治疗效果的研究[13-17]
2.5.1大鼠牙周炎模型制作
22只大鼠,腹腔注射10%水合氯醛麻醉、固定于鼠板上,用正畸钢丝缠绕在M2磨牙颈部并尽量使其陷入牙周袋,术后饲养,造模动物自由饮用10%高糖水(称取白砂糖若干,按计量用超纯水溶解即得),使其形成牙周炎。 空白对照组,不造模自由饮用纯水。造模组在确认大鼠已形成牙周炎后,按规定进行给药。
2.5.2模型确认及给药方法
造模4周后,经牙周炎临床指标检测,确认牙周的探诊深度大于1mm的动物为模型建立成功动物,挑选18只模型动物,麻醉后取出钢丝、SD雄性大鼠SPF级,8周龄,体重210±10g,随机分2组,加上最初选入的空白对照组,共计3组:受试品组每日上、下午牙龈局部涂抹给药(给药剂量同上述实验受试品组),空白对照与模型对照组动物同法给予纯水。连续给药5周。给药前、给药2周和5周时,水合氯醛麻醉大鼠后,由牙医检测大鼠牙周临床指标,包括动物牙周的探诊深度( probing depth,PD)、龈沟出血指数( sulcus bleeding index,SBI)、牙龈指数(gingival index,GI)、菌斑指数( plaqueindex, PLI)。
2.5.3探诊深度( probing depth,PD)
探诊深度是重要的牙周临床指标,使用牙周探针测定牙周袋的深度,龈缘至龈沟底的距离即探诊深度。
检查方法:用牙周探针与牙长轴平行检查大鼠牙周袋深度,探察麻醉大鼠的左上颌M2磨牙近中、腭、远中三个位点的深度,取其平均数。结果见表6。

表6 受试品对大鼠牙周探诊深度的影响
2.5.4龈沟出血指数 ( sulcus bleeding index,SBI)
在患有牙龈炎时牙龈一般有红肿、出血现象发生,龈沟出血是牙龈炎活动期的表现,根据龈沟出血情况对牙龈进行评价,能反应牙龈炎的活动状况,龈沟出血情况用龈沟出血指数表示。
检查方法:用牙周探针轻轻探至龈缘下方并滑动,观察牙龈出血程度,按下述评分标准计分。检查时探察大鼠的左上 M2近中、腭、远中3个位点,取均数。评分标准:0=用牙周探针轻探不出血,牙龈外观健康无红肿;1=用牙周探针轻探不出血,牙龈略红肿,有轻度炎症;2=用牙周探针轻探牙龈呈点状出血,牙龈外观有颜色改变和水肿;3=用牙周探针轻探牙龈出血沿龈缘扩展,牙龈有明显肿胀;4=用牙周探针轻探牙龈出血溢出龈缘,呈重度炎症,牙龈有明显肿胀;5=自动出血,牙龈有颜色改变和明显肿胀,有时有溃疡。结果见表7。

表7 受试品对大鼠龈沟出血指数的影响
2.5.5牙龈指数(gingival index,GI)
牙龈指数是观察牙龈状况,检查牙龈颜色和质的改变以及出血倾向的评定指数。
检查方法:使用钝头牙周探针,检查左上颌M2磨牙周围牙龈的近中唇(颊)乳头、正中唇(颊)缘、远中唇(颊)乳头和舌侧龈缘,分别按下述评分标准评分并取其平均数。评分标准:0=牙龈健康,无红肿、出血;1=有轻度炎症,探针轻探不出血。牙龈有颜色改变和轻度水肿;2=有中度炎症,探针轻探出血,牙龈红肿;3=有重度炎症,有自动出血倾向,牙龈明显红肿或有溃疡。结果见表8。
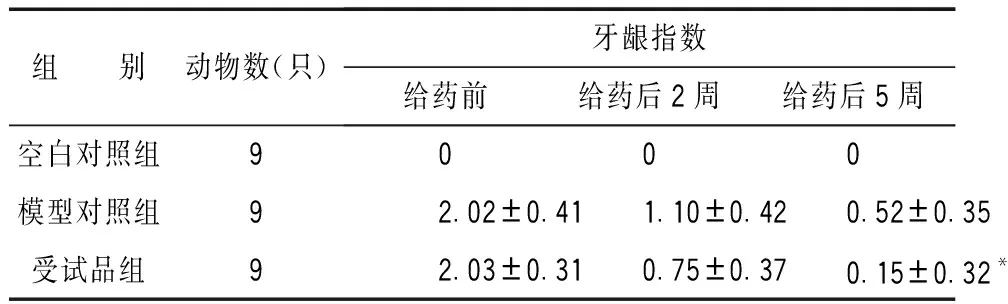
表8 对大鼠牙龈指数的影响
2.5.6菌斑指数 ( plaqueindex , PLI)[18]
根据牙菌斑的情况衡量牙周病的治疗和预防效果,根据菌斑的厚度作为记分依据。操作方法:先用棉球蘸纯水轻擦拭大鼠牙齿以清洁口腔,再用棉球蘸取碱性品红染色剂擦拭左上颌M2磨牙,染色后再用干燥棉球吸干牙面多余染液。染色完成后使用牙科探针在大鼠的左上颌M2磨牙龈沟内、龈缘及邻近牙面轻轻划过检查是否能刮出菌斑。依照此法对左上颌M2磨牙,做近中、远中、颊和舌四个面的检查并按照下述评分标准计分,取其平均值。评分标准:0=龈缘及邻近牙面无菌斑;1=肉眼视诊龈缘及邻近牙面无菌斑,探针尖划过时可刮出菌斑;2=龈缘及邻近牙面有中等量的菌斑;3=龈沟内和龈缘及邻近牙面有大量菌斑。结果见表9。
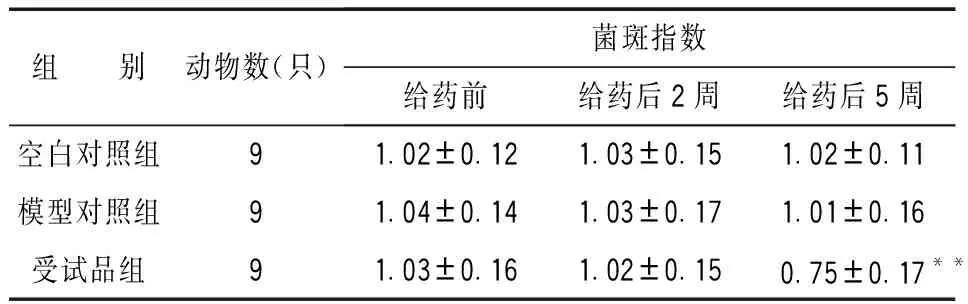
表9 对大鼠菌斑指数的影响
上述实验结果表明,受试品对牙周炎大鼠,牙周探诊深度、牙龈出血指数、牙龈指数、牙菌斑指数均有良好的改善效果,各项指标均有显著性差异(P<0.05或P<0.01,)说明该组合物对大鼠牙周炎的缓解和治疗是有效的。
依据中华人民共和国卫生行业标准WS/T326.1-2010要求,对云南白药活性肽牙膏进行了临床观察试验,本试验参加人数共计73人,其中5人因没能参加定期的检查,退出试验观察,68人参加完成整个临床试验。其中年龄分布为18~70岁,30~55岁人员占比为85%。
3 临床试验观察方案[19]
3.1试验设计
试验采用盲法、随机、对照观察的临床研究方法。试验样品分别为云南白药活性肽牙膏、不含云南白药提取物和美洲大蠊提取物相同基质的牙膏(空白对照牙膏)。
3.2试验期限
3.2.1在试验前医生需先对受试者进行口腔状况检查,筛选出符合试验要求的患者进入试验。
3.2.2试验用产品使用期限为3个月。
3.2.3每名受试对象共需接受3次口腔检查,第1次为筛选受试者并进行刷牙方法指导,对受试者各项观察指标进行记录并进行随机分组,开始使用牙膏进入试验观察;产品按要求使用一个月后进行第2次检查并对各项指标进行记录;第3次检查为使用牙膏3个月后并对各项指标进行记录。
3.2.4每次复查后发给受试对象2-3支优质软毛牙刷和足量的试验样品牙膏;要求受试对象每天至少用该牙膏刷牙2次,每次一分钟以上,并用所发牙刷刷牙。要求所有受试者必须进行巴氏刷牙法的指导。
3.3试验对象
受试者为符合纳入及排除标准的患有牙龈炎或慢性牙周炎(轻度及中度)的成年男性和女性,一般情况试验人群每组数量应不少于30人。
3.4纳入标准
牙龈炎或慢性牙周炎轻度及中度患者。
全身健康状况良好、无重要的全身系统性疾病、有20颗以上可检测的牙齿。
年龄在18~70周岁。
如果为女性,不得处于妊娠期和哺乳期内。
受试者应具有适当程度的菌斑或牙龈炎。
没有同时参加其他类似试验研究。
签署知情同意书,能按要求完成临床试验。
3.5排除标准
对试验产品成份有过敏史。
现在服用对试验结果有影响的药物。
在参加研究之前一个月使用抗生素。
口腔内有开放性龋齿或口腔粘膜病变。
患严重的牙周炎。
3.6检查内容
3.6.1检查指标:①牙龈指数(GI),②龈沟出血指数(BI),③菌斑指数(PLI),社区牙周指数(CPI)。
3.6.2检查器械 检查器械使用WHO推荐的CPI探针,探针尖端为一小球,直径为0.5mm,在距顶端3.5~5.5mm处为黑色涂布区域,距顶端8.5mm和11.5mm处有两条环带。
3.6.3检查方法
确定指数牙正常情况下,将口腔中分为6个区段,10颗指数牙,分别是上下颌8个磨牙加右上左下各一个中切牙,即17、16、11、26、27、37、36、31、46、47。
3.6.4牙龈指数(GI)
使用钝头牙周探针,对目标牙龈进行检查,分别按下述评分标准评分并取其平均数。
评分标准:0=牙龈健康,无红肿、出血;1=有轻度炎症,牙龈颜色轻度改变,轻度水肿,探针轻探不出血;2=有中度炎症,牙龈红肿,探针轻探出血;3=有重度炎症,明显发红,水肿,溃疡,有自动出血倾向。
3.6.5龈沟出血指数(BI)
对目标牙齿的颊、舌面进行菌斑的评价计分,用牙周探针轻轻探至龈缘下方并滑动,观察牙龈出血程度,按下述评分标准计分。
评分标准:0=龈缘和龈乳头外观健康,用牙周探针轻探龈沟不出血;1=有轻度炎症,牙龈略红肿,用牙周探针轻探不出血;2=牙龈呈轻度炎症,牙龈外观有颜色改变和水肿,用牙周探针轻探牙龈呈点状出血;3=牙龈呈中度炎症,牙龈有颜色改变,轻度水肿,用牙周探针轻探牙龈出血沿龈缘扩展;4=牙龈呈重度炎症,不但有颜色改变,且有明显肿胀,用牙周探针轻探牙龈出血溢出龈缘;5=牙龈有颜色改变,明显肿胀,有时有溃疡,探诊后出血或自动出血。
3.6.6菌斑指数(PLI)
受试者使用菌斑指示剂后,对目标牙齿的颊、舌面进行菌斑的评价计分,所有牙面菌斑记分的总和除以受检牙面数,得出该个体牙齿的菌斑分值,再将10颗指标牙菌斑指数相加,除以牙齿数,即为每一受试者菌斑指数的均值。采用 Quigley-Hein 改良Turesky菌斑指数评价龈上菌斑。典型病例进行拍照留样。
评分标准:0=无菌斑 ;1=牙颈部边缘存在散在的菌斑 ;2=牙颈边缘可见连续的薄菌斑带(达1mm 宽);3=牙颈部菌斑带大于1mm 但少于牙面的1/3;4=菌斑覆盖牙面的1/3~2/3;5=菌斑覆盖牙面2/3以上。 计算每一受试者菌斑指数的均值。典型病例进行拍照留样。
3.6.7社区牙周指数(CPI)
以探诊为主,结合视诊。检查时以执笔式握持CPI探针,无名指为支点,将探针轻缓地插入龈沟或牙周袋内,探针与牙长轴平行,紧贴牙根。沿牙齿颊(唇)、舌(腭)面龈沟从远中向近中移动,作上下短距离的提插式移动,以感觉龈下结石。同时查看牙龈出血状况,并根据探针上的刻度观察牙周袋深度,CPI探针使用时所用的力不超过20g。
评分标准:0=牙龈健康;1=牙龈炎,探诊后出血;2=牙石,探诊可见牙石,但探针黑色部分暴露在龈袋外;3=早期牙周病,龈缘覆盖部分探针黑色部分,龈袋深度在4~5mm;4=晚期牙周病,探针黑色部分被龈缘完全覆盖,牙周袋深度大于6mm;X=除外区段(少于两颗功能牙);5=无法检查。
3.7临床试验结果
试验组和对照组分别统计试验开始时基线、1个月及3个月检查的①牙龈指数(GI),②龈沟出血指数(BI),③菌斑指数(PLI),社区牙周指数(CPI)。并进行统计学分析,采用统计学方法,双侧t检验,显著性水准a=0.05,p<0.05,结果显示连续使用产品三个月指标存在统计学显著性差异。
临床试验结果见表10。

表10 临床试验结果
3.8临床试验观察结论
试验观察结果分析表明:① 使用牙膏1个月后,云南白药活性肽牙膏和空白对照牙膏,各项指标均有一定好转,其中云南白药活性肽牙膏在牙龈指数(GI),龈沟出血指数(BI), 牙周社区指数(CPI)与试验开始时对比有非常显著性差异P≤0.001,菌斑指数(PLI)也有显著性差异P≤0.01;空白对照牙膏在牙龈指数(GI),牙周社区指数(CPI)与试验开始时对比有显著性差异P≤0.01,龈沟出血指数(BI)有显著性差异P≤0.05;但云南白药活性肽牙膏和空白对照牙膏相比,组间没有显著性差异。二者之间的差异无统计学意义。
② 使用牙膏3个月后,云南白药活性肽牙膏在牙龈指数(GI),龈沟出血指(BI)方面与空白对照牙膏相比较有非常显著性差异P≤0.01,牙周社区指数(CPI)也有显著性差异P≤0.05,组间比较差异具有统计学意义。
其中牙龈指数(GI)减少百分比:(空白牙膏组-云南白药活性肽牙膏组)/空白牙膏组=(1.04-0.80)/1.04≈23%,满足标准WS/T326.1-2010(对照-试验)/对照≥12%的要求。
龈沟出血指数(BI)减少百分比:(空白牙膏组-云南白药活性肽牙膏组)/空白牙膏组=(1.07-0.81)/1.07≈24.3%,满足标准WS/T326.1-2010(对照-试验)/对照≥12%的要求。
牙周社区指数(CPI)减少百分比:(空白牙膏组-云南白药活性肽牙膏组)/空白牙膏组=(1.46-1.20)/1.46≈17.7%,满足标准WS/T326.1-2010(对照-试验)/对照≥12%的要求。
云南白药活性肽牙膏在牙龈指数(GI),龈沟出血指数(BI),菌斑指数(PLI),牙周社区指数(CPI)与试验开始时对比有非常显著性差异P≤0.001;空白对照牙膏在牙龈指数(GI),龈沟出血指数(BI),菌斑指数(PLI)方面,与试验开始时对比有非常显著性差异P≤0.001;牙周社区指数(CPI)与试验开始时对比有显著性差异P≤0.01。
本临床试验观察结果经统计学分析表明:云南白药活性肽牙膏,通过3个月的连续使用,对牙龈炎相关指标(牙龈指数,龈沟出血指数),有非常明显的改善,表明产品对牙龈炎有很好的减轻和改善作用;通过对牙周社区指数的统计学差异表明,产品对牙周不健康问题有相应的改善和修复作用。
试验同时表明通过掌握正确的刷牙方式,养成良好的刷牙习惯,及每天两次认真刷牙,牙龈炎各项指标及牙菌斑指数均有明显减少,其减少数量也具有统计学意义。
3.9不良反应情况
在整个实验过程中未见不良事件和副作用发生。
4 总结
通过建立相应的动物模型,验证了云南白药提取物和美洲大蠊提取物构成的组合物(BYPA)有良好的抗炎、止血、促进溃疡组织愈合的作用,并对牙周炎大鼠牙周探诊深度、龈沟出血指数、牙龈指数、牙菌斑指数均有良好的改善作用,说明BYPA对大鼠牙周炎的缓解和改善是有效的。含有BYPA的云南白药活性肽牙膏,在临床观察中通过患有牙龈炎或慢性牙周炎(轻度及中度)患者3个月的连续使用,对牙龈指数、龈沟出血指数有非常明显的改善,表明牙膏对牙龈炎有很好的减轻和改善作用;对牙周社区指数的好转表明牙膏对牙周不健康问题有相应的改善和修复作用。
关于云南白药提取物复配美洲大蠊提取物,对口腔组织良好的改善和修复作用机制,希望在进一步的研究中进行深入探讨。

