CS/PVA微球的制备及其对重金属离子吸附研究
郑学成,颜玉如,罗 维,唐 嘉
(西南石油大学化学化工学院,四川 成都 610500)
随着社会的工业化发展,各种工业废弃物排放到环境中,特别是对人类活动和生活环境造成严重危害的重金属,已成为全球关注的问题之一。去除废水中重金属的处理方法主要有化学沉淀法、离子交换法、电解法、絮凝法、生物法和吸附法等。与其他传统方法相比,吸附法具有能耗低、效率高、无二次污染等优点,在废水处理领域具有很大的优势。常用的吸附剂有沸石、活性炭、分子筛、壳聚糖等。其中,壳聚糖作为一种新型高效可回收吸附剂在重金属废水处理中得到了广泛的应用。但由于壳聚糖作为吸附剂时其耐化学性和机械强度较差,通过壳聚糖的交联改性能有效改善这些性能,因此人们在对改性壳聚糖吸附废水中重金属方面做了大量的研究工作。如Jin等通过间歇式吸附试验,利用傅里叶红外光谱和X射线光电子光谱研究了溶液pH值对交联壳聚糖/聚乙烯醇(CS/PVA)微球吸附废水中Pb的影响机制,不同pH值下交联壳聚糖/聚乙烯醇微球对废水中Pb的吸附机制为壳聚糖/聚乙烯醇微球吸附废水中重金属离子的研究提供了方法指导;Kumar等制备了在酸性介质中具有化学稳定性的交联壳聚糖/聚乙烯醇微球,其能有效回收废水中的Cd,为交联壳聚糖/聚乙烯醇微球去除废水中重金属离子的应用提供了理论依据;Laus等使用环氧氯丙烷和三磷酸通过共价键和离子键与壳聚糖进行交联,研究了其对废水中重金属离子Cu、Pb和Cd的吸附容量;Liu等研究了纳米纤化壳聚糖作为螯合剂吸附废水中重金属离子Cu、Pb、Cd、Zn、Ni的吸附过程,发现其吸附过程符合Langmuir等温线和准二阶动力学模型;Kandile等首次以1,3-(二氧异吲哚啉-2-氨基)为改性基团,制备了新型壳聚糖水凝胶,并将其应用于吸附废水中重金属离子Co、Hg、Cu、Zn和Pb,结果发现其只对Co和Hg具有较好的吸附效率;张慧敏等制备了壳聚糖/聚乙烯醇纳米纤维膜,发现其对废水中重金属离子Cu、Pb和Ni的吸附性能较好,为开发高效 CS/PVA 纳米纤维膜吸附剂及其在吸附废水中重金属的应用提供了理论依据;Shen等采用水热碳化法合成了HTC-壳聚糖,其对废水中Cr的吸附效率可达92%以上;Khawar等研究了由壳聚糖、磷酸氢二铵、乙二胺四乙酸合成的吸附剂对废水中Pb的吸附性能。
由于壳聚糖/聚乙烯醇共混体系具有良好的机械和化学性能,因此本研究以壳聚糖、聚乙烯醇为原料,戊二醛为交联剂,制备了低含水量的CS/PVA微球,探究了生物可降解材料CS/PVA微球对废水中重金属离子Cu、Fe、Pb、Cd的吸附性能,阐明了CS/PVA微球对重金属的吸附机理,以期为含有重金属离子废水的处理提供有效信息和理论依据。
1 实验部分
1. 1 试验材料与仪器
试验材料与试剂:壳聚糖(脱乙酰度90%),聚乙烯醇,吐温-80,丙酮、25%戊二醛、甲苯、氯苯、乙酸、氢氧化钠均为分析纯,用来制作CS/PVA微球;铜标准液、铁标准液、铅标准液、镉标准液均符合国家标准GSB 04-1721—2004,三氯化铁、五水硫酸铜、硝酸铅、硝酸镉均为分析纯,用来配制作为吸附试验的重金属离子溶液。所有化学药品均从成都科龙化学试剂公司购买。
试验仪器:WQF-520傅里叶变换红外光谱(北京瑞利分析仪器有限公司,China);X Pert PRO MPD X射线衍射仪(荷兰帕纳科公司,Nederland);Quanta 450扫描电子显微镜(美国FEI公司,America)。
1.2 CS/PVA微球的制备
首先用100 mL质量分数为2%乙酸溶解已知量的壳聚糖粉,用去离子水制备质量分数为12.5%聚乙烯醇溶液250 g,再按质量比2∶1的比例混合聚乙烯醇与壳聚糖-乙酸溶液,搅拌得到均匀溶液,用盐酸调节共混溶液的pH值;然后在含有一定量吐温-80的180 mL甲苯-氯苯中加入180 mL壳聚糖-聚乙烯醇共混溶液,以130 r/min持续搅拌,直至温度逐渐升高至90℃,当共混体系几乎不含水分时,停止搅拌,将共混体系冷却至室温(25℃);最后再加入质量分数为25%的戊二醛6.552 mL,连续搅拌10 h,得到CS/PVA微球。由于微球是在酸性条件下得到的,故用0.1 mol/L NaOH溶液中和至弱碱性,再用气泵过滤,丙酮洗涤,用去离子水清洗,于70℃的烘箱放置24 h。
1. 3 吸附试验
1.3.1 重金属离子溶液的制备
分别称取0.393 g 五水硫酸铜、0.289 g三氯化铁、0.159 g硝酸铅、0.210 g硝酸镉,分别加入纯水,配成100 mL溶液,再分别吸取1 mL、2 mL、3 mL、4 mL、5 mL的溶液配成50 mL溶液,最后配成浓度分别为20 mg/L、40 mg/L、60 mg/L、80 mg/L、100 mg/L的Cu、Fe、Pb、Cd重金属离子溶液,作为吸附试验的基础液。
绘制重金属离子溶液的标准曲线:通过测定浓度分别为0.5 mg/L、1.0 mg/L、1.5 mg/L、2 mg/L、3 mg/L的标准Cu溶液的吸光度,利用最小二乘法拟合直线,得到Cu溶液的标准曲线。Fe、Cd、Pb溶液的标准曲线绘制方法与Cu溶液一致。
1.3.2 初始pH值对CS/PVA微球吸附性能的影响
在pH值为3、5、7、9、11的条件下,研究初始pH值对CS/PVA微球吸附效果的影响。配制初始浓度为60 mg/L的 Cu、Fe、Pb和Cd溶液各50 mL,用0.1 mol/L HCl或0.1 mol/L NaOH溶液调节溶液pH值,再加入0.4 g CS/PVA微球置于30℃恒温振荡器中在130 r/min条件下连续振荡吸附24 h后取样,测定溶液中Cu、Fe、Pb和Cd离子浓度。
1.3.3 吸附时间对CS/PVA微球吸附性能的影响
在吸附动力学试验中,时间间隔分别设置为1 h、3 h、5 h、7 h、9 h、11 h,研究吸附时间对CS/PVA微球吸附效果的影响。配制初始浓度为60 mg/L 的Cu、Fe、Pb和Cd溶液各50 mL,初始pH值为7,再加入0.4 g CS/PVA微球置于30℃恒温振荡器中在130 r/min条件下进行连续振荡吸附,按吸附时间取样测定溶液中Cu、Fe、Cd和Pb离子浓度。试验结果用吸附动力学模型拟合。
1.3.4 重金属离子溶液初始浓度对CS/PVA微球吸附性能的影响
为了研究不同重金属离子溶液初始浓度对CS/PVA微球吸附效果的影响,设计试验重金属离子溶液初始浓度分别为20 mg/L、40 mg/L、60 mg/L、80 mg/L、100 mg/L,配制不同初始浓度重金属离子溶液各50 mL,初始pH值为7,加入0.4 g CS/PVA微球置于30℃恒温振荡器中在130 r/min条件下连续振荡吸附24 h后取样测定溶液中Cu、Fe、Cd和Pb和离子浓度。
1. 4 吸附机理
1.4.1 吸附动力学
CS/PVA微球的吸附能力可以通过吸附动力学得到合理阐释,吸附动力学主要包括准一级动力学和准二级动力学。吸附容量的计算公式为
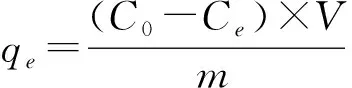
(1)
准一级动力学的方程可表示为
ln(q
-q
)=lnq
-k
t
(2)
准二级动力学的方程可表示为

(3)
上式中:q
为吸附平衡时的吸附容量(mg/g);C
为溶液中吸附质的初始质量浓度(mg/mL);C
为吸附平衡时溶液中吸附质的剩余质量浓度(mg/mL);V
为吸附质溶液的体积(mL);m
为CS/PVA微球的质量(g);q
为时间t
时刻的吸附容量(mg/g);k
为准一级动力学模型的速率常数(min);k
为准二级动力学模型的速率常数(g/mg·min);t
为吸附时间(min)。1.4.2 吸附等温线
利用吸附等温线来描述吸附达到平衡时的吸附量与溶液中吸附质浓度间的定量关系,可为吸附机理的研究提供依据。
(1) Langmuir等温吸附模型。Langmuir吸附等温线模型是Langmuir在1916年提出的单分子层吸附理论。该理论应用的假设条件是单分子层吸附即吸附达到饱和后不能发生进一步吸附,固体表面均匀,被吸分子相互间无作用力。Langmuir等温吸附模型可表示为
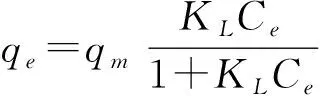
(4)
线性形式为

(5)
上式中:q
为吸附平衡时的吸附容量(mg/g);C
为吸附平衡时溶液中吸附质的剩余质量浓度(mg/mL);K
为吸附平衡常数;q
为吸附剂的最大吸附容量(mg/g),与吸附位点有关,一般与温度无关。(2) Freundlich等温吸附模型。Freundlich等温吸附模型为经验模型,它假设的吸附能量呈指数型衰减,通过包括多种吸附能的不同位点进行吸附且呈非均匀分布。Freundlich等温吸附模型可表示为
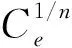
(6)
线性形式为

(7)
一般认为,1/n
的数值在0~1之间时,其数值越小,吸附性能越好;1/n
的数值在0.1~0.5之间时,则易于吸附;1/n
的数值大于2,则难以吸附。K
值为单位浓度时的吸附量,该值一般随温度的升高而降低。2 结果与讨论
2.1 壳聚糖和CS/PVA微球的表征
2.1.1 FTIR表征
壳聚糖和CS/PVA微球的红外光谱图,见图1。
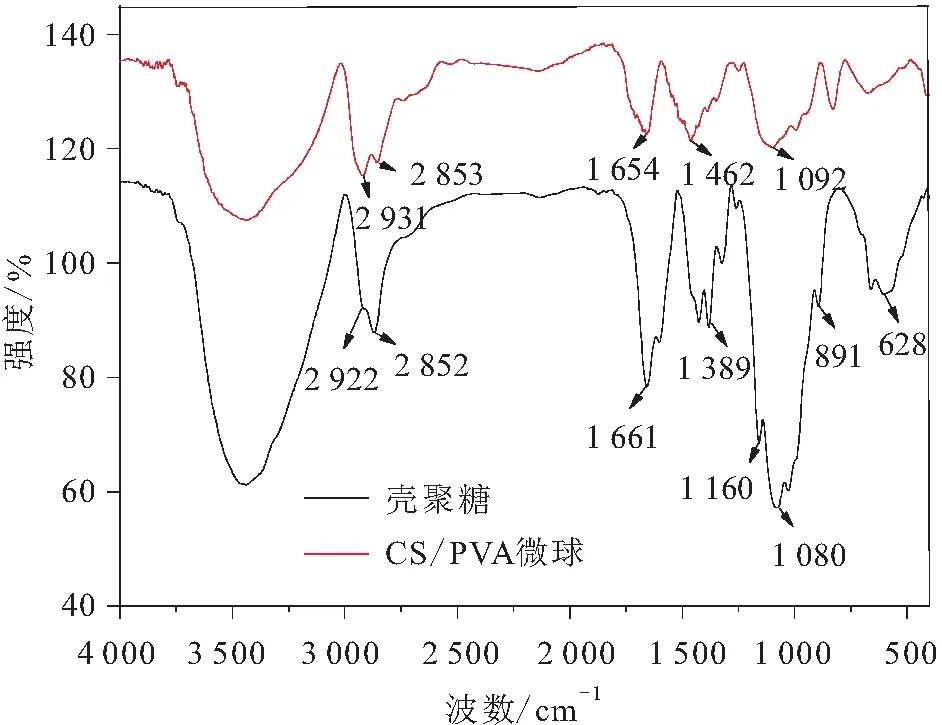
图1 壳聚糖和CS/PVA微球的红外光谱图Fig.1 FTIR of chitosan and CS/PVA microspheres

2.1.2 XRD表征
壳聚糖和CS/PVA微球的X射线衍射谱图,见图2。
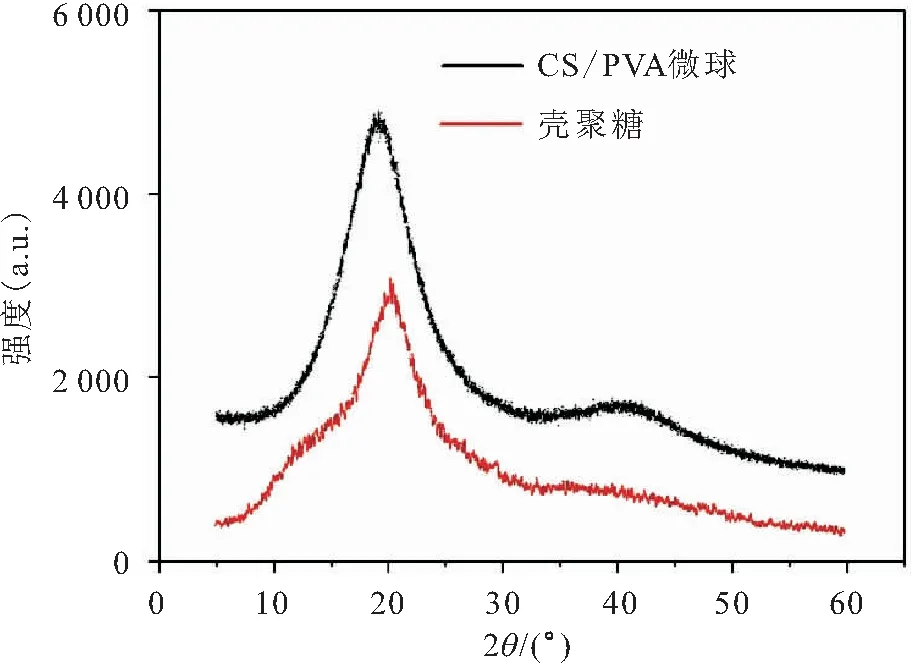
图2 壳聚糖和CS/PVA微球的X射线衍射谱图Fig.2 XRD of chitosan and CS/PVA microspheres
由图2可以观察到,当2θ
为20°时,两种物质都有一处明显的衍射峰,是壳聚糖的分子链规整排列结晶引起产生的衍射峰。在2θ
为20°处壳聚糖的特征吸收峰成因是壳聚糖分子本身带有的—OH和—NH之间可以形成较强的分子间氢键和分子内氢键,因而壳聚糖具有良好的溶解性;而CS/PVA微球的衍射峰变得尖锐,可能是由于交联过程影响了壳聚糖链段自由度,使链段的规整性下降,导致其结晶度下降;在2θ
为42°处CS/PVA微球的特征吸收峰生成的原因是戊二醛与壳聚糖的—NH之间发生了反应,导致壳聚糖分子链内或壳聚糖分子链间所存在的较强氢键被破坏。当壳聚糖加入至溶液中时,由于其内含有的—NH发生了氨基质子化,从而使得壳聚糖变为带电荷的聚电物质。此外,壳聚糖的分子内及分子间氢键易遭受破坏,因此壳聚糖会溶于酸中。合成改性后壳聚糖的氨基和聚乙烯醇的羟基的分子内氢键作用减弱了CS/PVA微球的结晶程度,表明了CS/PVA微球的非晶体性质。2.1.3 SEM表征
壳聚糖和CS/PVA微球的SEM微观形貌图,见图3和图4。

图3 壳聚糖的SEM微观形貌图Fig.3 SEM of chitosan

图4 CS/PVA微球的SEM微观形貌图Fig.4 SEM of CS/PVA microspheres
由图3和图4可见,壳聚糖表面无孔隙,且大多数呈现块状且大小不一,分散性不均匀;壳聚糖经过戊二醛和聚乙烯醇交联改性后形成的CS/PVA微球,其粒径分布较均匀,粒径约为150~200 μm,粒子均呈球体状,分散性良好,这是由于戊二醛的交联作用和吐温-80致孔剂的加入,使CS/PVA微球表面具有相对均匀的孔隙度,说明该改性微球具备吸附能力。
2.2 初始pH值对CS/PVA微球吸附性能的影响
吸附试验中溶液的初始pH值是影响吸附剂表面电荷、吸附剂官能团活性以及金属离子的离化程度的重要因素之一。CS/PVA微球对重金属离子的吸附主要以化学络合作用为主,主要是通过分子链中性基团—NH与金属离子发生螯合作用,因为N原子具有孤对电子,能进入金属离子的空轨道中形成配位键而与之结合。
不同pH值条件下CS/VPA微球对溶液中重金属离子的吸附效率曲线,见图5。
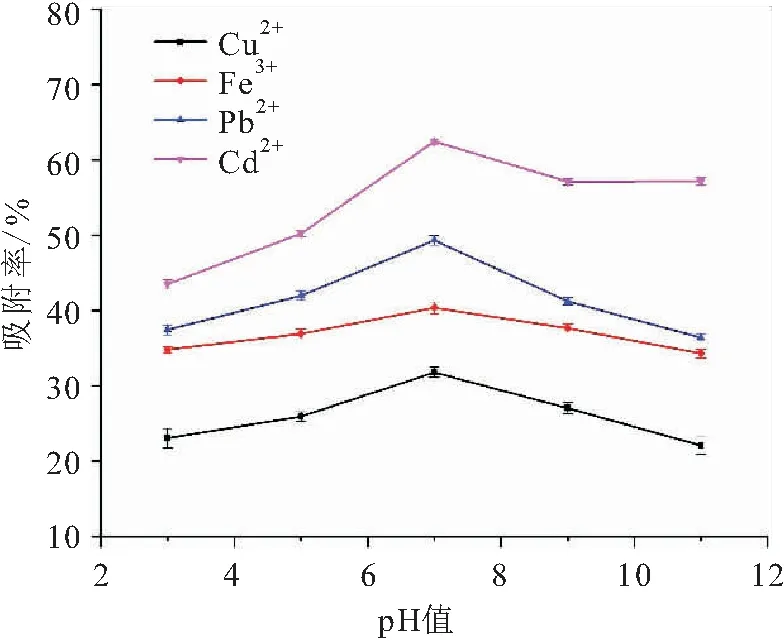
图5 不同pH值条件下CS/PVA微球对溶液中 重金属离子的吸附效率曲线Fig.5 Adsorption efficiency curves of CS/PVA microspheres for heavy metals ions in solution under different pH conditions

2.3 吸附时间对CS/PVA微球吸附性能的影响
吸附时间是研究吸附动力学的主要变量因素。不同吸附时间条件下CS/PVA微球对重金属离子的吸附效率曲线,见图6。
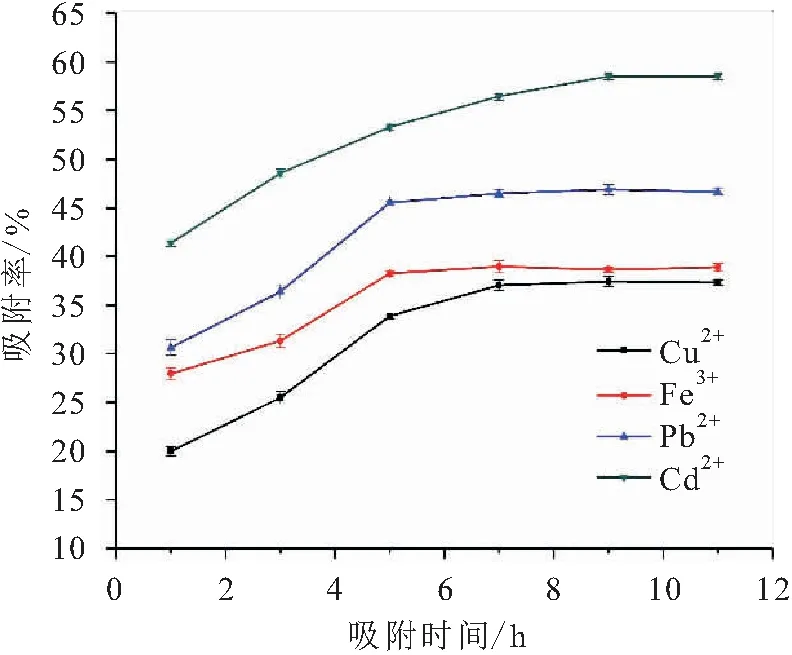
图6 不同吸附时间条件下CS/PVA微球对溶液中 重金属离子的吸附效率曲线Fig.6 Adsorption efficiency curves of CS/PVA microspheres for heavy metals ions under different time conditions
由图6可见,当吸附时间为2 h时,CS/PVA微球对溶液中Cu、Fe、Pb、Cd的吸附率分别为10.5%、28.1%、30.5%、35.7%;随着吸附时间的增加,吸附速率加快,在7 h时CS/PVA微球对溶液中Cu、Fe、Pb、Cd的吸附率分别为37.1%,38.3%、46.1%、62.1%;7 h以后,溶液中剩余重金属离子浓度几乎无变化,表明在7 h时吸附已经达到饱和状态。
2.4 重金属离子溶液初始浓度对CS/PVA微球吸附性能的影响
不同重金属离子溶液初始浓度条件下CS/PVA微球对溶液中重金属离子的吸附效率曲线见图7。

图7 不同重金属离子溶液初始浓度条件下CS/PVA 微球对溶液中重金属离子的吸附效率曲线Fig.7 Adsorption efficiency curves of CS/PVA microspheres for heavy metals in solution under different initial concentration of heavy metel ion solution conditiions
由图7可见,当重金属离子溶液浓度为20 mg/L时,溶液中Cu、Fe、Pb、Cd的吸附率均达到最高,其中Cd的吸附率为94.5%;随着重金属离子溶液初始浓度的增加,吸附率逐渐降低并趋于平衡,这表明吸附剂的大多数位点已经被占据,吸附剂对于一定浓度重金属离子的去除已达到了饱和;当重金属离子溶液初始浓度为100 mg/L时,溶液中Cu、Fe、Pb和Cd的吸附率分别为22.6%、25.1%、34.1%和42.9%,说明CS/PVA微球对Cd的吸附量最大,即表明CS/PVA微球对Cd具有较高的选择性,而对Cu的选择性较低。
2. 5 吸附动力学研究
表1显示了不同吸附时间时CS/PVA微球对溶液中重金属离子的吸附容量。
由表1可知,当吸附时间为7 h时,CS/PVA微球对溶液中Cu、Fe、Pb和Cd的吸附达到平衡;当吸附时间为9 h时,CS/PVA微球对溶液中Cu、Fe、Pb和Cd的最大吸附容量分别为27.69 mg/g、28.88 mg/g、34.73 mg/g、43.50 mg/g。

表1 不同吸附时间时CS/PVA微球对溶液中重金属离子的吸附容量
本文对CS/PVA微球吸附溶液中重金属离子的过程进行了准一级动力学和准二级动力学线性拟合,其拟合直线见图8。
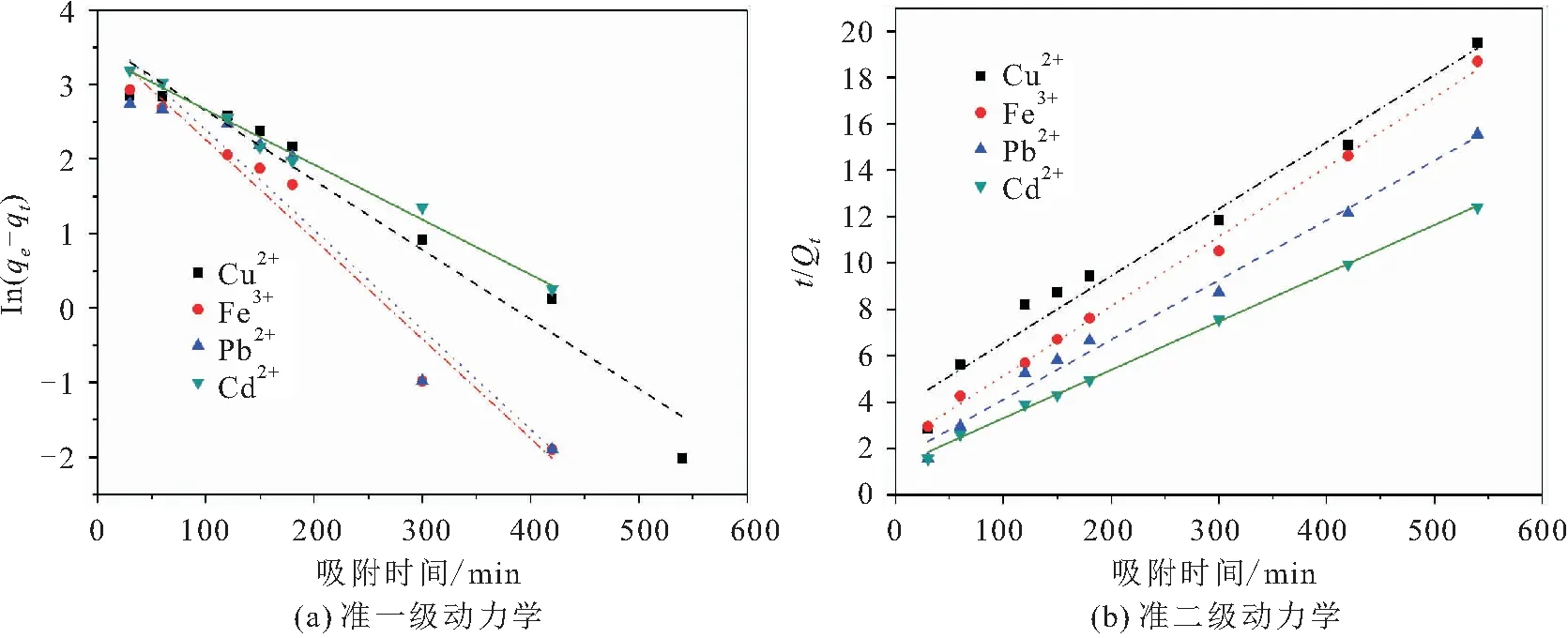
图8 CS/PVA微球对溶液中重金属离子吸附过程的准一级动力学和准二级动力学拟合曲线Fig.8 Fitting lines of pseudo-first order kinetic and pseudo-second-order kinetic of CS/PVA microspheres for adsorption of heavy metal ions in solution
表2和表3列出了CS/PVA微球对溶液中重金属离子吸附过程的准一级动力学和准二级动力学模型拟合参数和相关系数(R
)。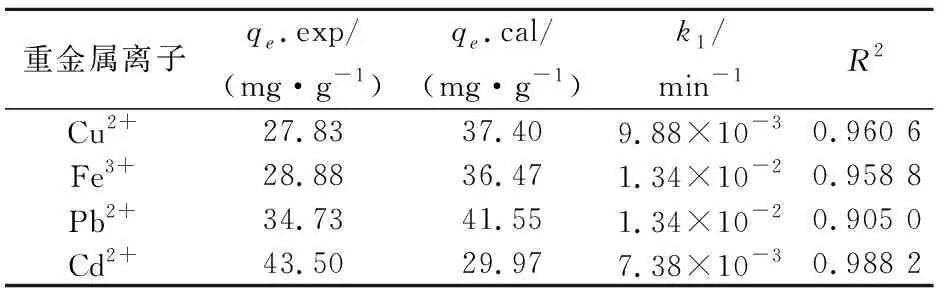
表2 CS/PVA微球对溶液中重金属离子吸附过程的准一级动力学模型拟合参数和相关系数
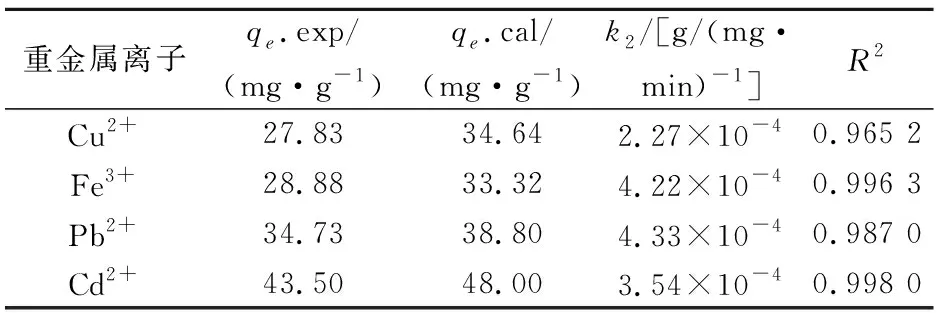
表3 CS/PVA微球对溶液中重金属离子吸附过程的准二级动力学模型拟合参数和相关系数
由表2可知,准一级动力学模型速率常数的范围为9.88×10至1.34×10,相关系数(R
)的范围为0.905 0至0.988 2;而Pb与Fe的相关系数(R
)分别为0.905 0和0.958 8,说明两者均不符合准一级动力学模型;4种重金属离子的q.exp与q.cal的差值均大于7 mg /L,表明准一级动力学拟合效果不理想。由表3可知,准二级动力学模型速率常数的范围为2.27×10至4.33×10,低于准一级动力学模型速率常数;4种重金属离子的q.exp与q.cal接近,且相关系数范围为0.965 2至0.998 0,表明4种重金属离子的吸附过程更符合准二级动力学模型,表明其吸附过程是以化学反应为主导的,如离子交换、螯合反应等。
CS/PVA微球对溶液中重金属离子吸附过程的Langmuir等温吸附模型和Freundlich等温吸附模型的拟合曲线,见图9。
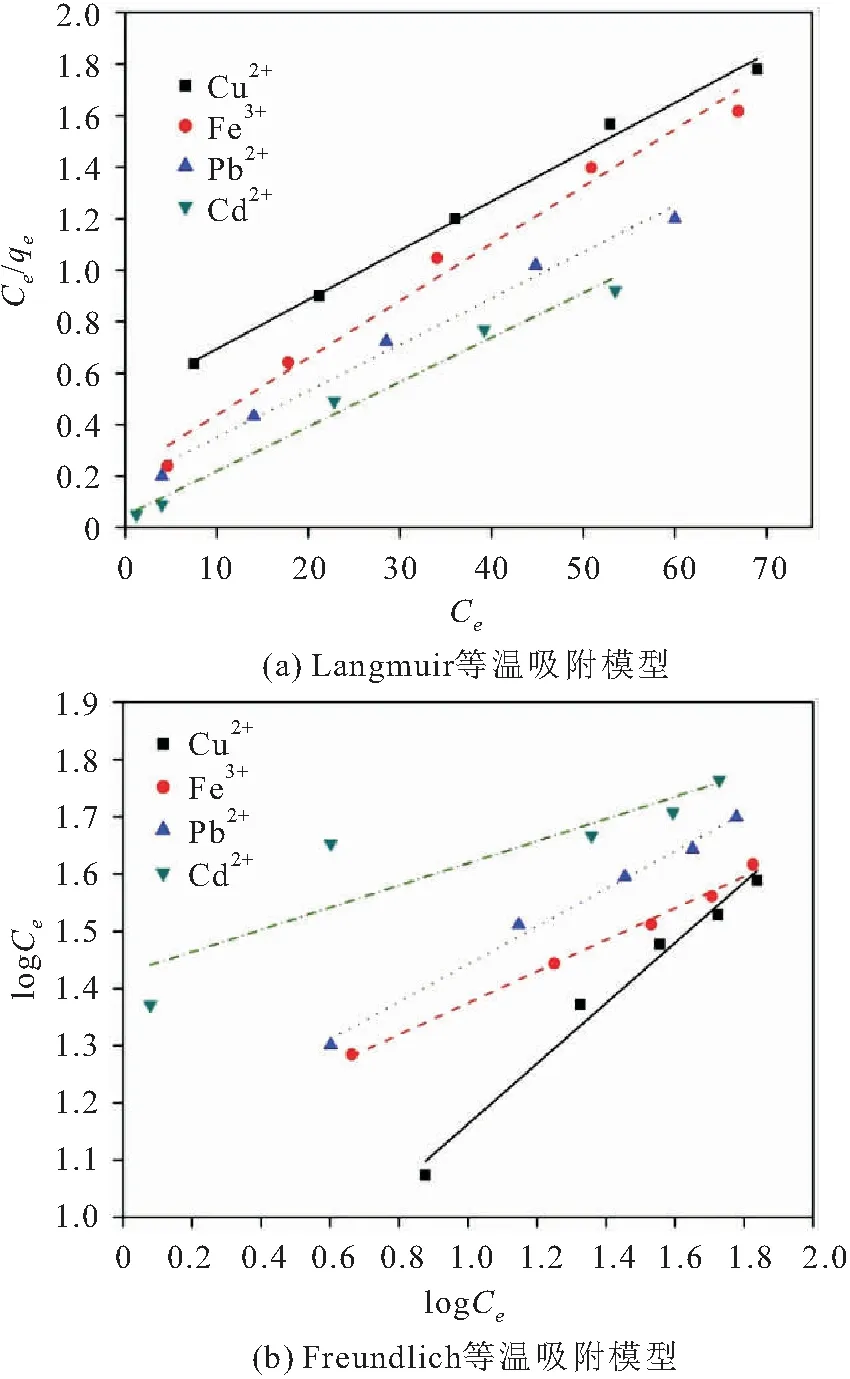
图9 CS/PVA微球对溶液中重金属离子吸附过程的 Langmuir等温吸附模型和Freundlich等温吸附 模型拟合曲线Fig.9 Fitting curves of Langmuir adsorption isotherms and Freundlich adsorption isotherm of CS/PVA microspheres for adsorption of heavy metal ions in solution
由图9可见,CS/PVA微球对溶液中Cd的吸附容量最大,对Cu的吸附容量最小。
表4给出了CS/PVA微球对溶液中重金属离子吸附过程的等温吸附模型参数。
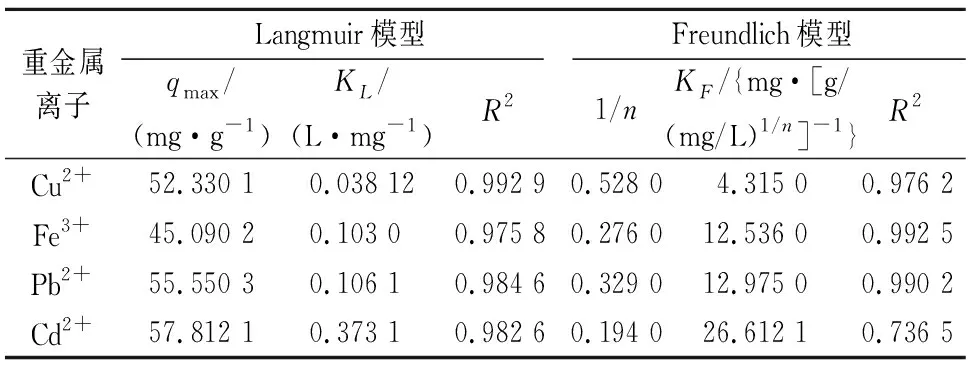
表4 CS/PVA微球对溶液中重金属离子吸附过程的等温吸附模型参数
由表4可知,CS/PVA微球对溶液中Fe和Pb的吸附过程与Freundlich等温吸附模型一致,且Fe的1/n
值小于Pb的1/n
值,说明Fe更容易被吸附;而CS/PVA微球对溶液中Cu和Cd的吸附过程更符合Langmuir等温吸附模型,表明Cu和Cd的吸附为单层吸附,CS/PVA微球对溶液中Cu和Cd的最大吸附容量分别为52.33 mg/g和57.81 mg/g,其中Cd的K
值约为Cu的10倍,说明CS/PVA微球对Cd的吸附能力大于Cu。3 结 论
本试验合成的CS/PVA微球被证明是有效的重金属离子吸附剂,并得出以下结论:
(1) 在pH值为7的条件下,CS/PVA微球对溶液中重金属离子的吸附效果最佳,吸附达到饱和的时间为7 h。
(2) CS/PVA微球对溶液中Cd的吸附率最大,可达到94.5%。
(3) 动力学模型表明,CS/PVA微球对溶液中重金属离子的吸附过程符合准二级动力学模型,吸附过程主要以化学络合作用为主,通过分子链中性基团—NH与金属离子发生螯合作用。
(4) CS/PVA微球对溶液中Cu和Cd的吸附更符合Langmuir等温吸附模型,表明Cu和Cd的吸附为单层吸附,CS/PVA微球对溶液中Cu和Cd的最大吸附容量分别为52.33 mg/g和57.81 mg/g。
(5) CS/PVA微球对溶液中Fe和Pb的吸附过程与Freundlich等温吸附模型一致,说明Fe更容易被吸附。

