妊娠期接种百白破联合疫苗安全性的Meta 分析
张学,左伟伦
中国医学科学院北京协和医学院医学生物学研究所
云南省重大传染病疫苗研发重点实验室,云南昆明650118
百日咳是一种可通过疫苗预防的细菌性呼吸道感染疾病,婴幼儿发病率高。西方国家虽然儿童百日咳疫苗接种率较高,但其百日咳疾病负担仍较重[1]。WHO 估计,2008 年全球约有 1 600 万百日咳病例,95%发生在发展中国家,近20 万儿童死亡[2];2013 年约 6.3 万名 5 岁以下儿童死亡[3];2015 年WHO 报道了142 512 例百日咳病例[4]。成人和青少年虽不是百日咳发病率和死亡率最高的群体,却是该病的主要传播媒介,大部分重症和死亡病例均是3 个月以下的婴儿(未完成基础免疫)[5-6]。为减轻疾病负担,一些国家对儿科医护人员、产后孕妇、与12 个月以下婴儿密切接触人群进行百日咳疫苗接种和青少年加强免疫等策略来避免婴幼儿感染百日咳[7-8],但这些策略均未能对6 个月以下的婴儿群体产生实质性的保护效果。有研究表明,在妊娠期接种含百日咳成分的疫苗不仅能保护孕妇本身,还能通过胎盘传递抗体给新生儿,从而提供被动免疫[9]。2011 年,美国疾病预防与控制中心免疫咨询委员会推荐未接种过百日咳疫苗的孕妇于怀孕27 ~36 周时应接种百白破联合疫苗(etanus toxoid,reduced diphtheria toxoid,and acellular pertussis combined vaccine,TdaP),至 2012 年,规定所有孕妇均需接种TdaP[10-11]。目前,关于妊娠期接种TdaP 安全性的研究结果不尽相同[12-15],有些系统综述对其安全性进行评价[13,16-18],均以队列研究为主、收集的数据不够全面、评价的结局指标少。
Meta 分析是按照严格的纳入和排除标准全面收集某个医疗卫生问题的研究,对纳入的研究进行质量评价和定量或定性分析,对研究的问题进行系统、真实、客观的评价。Meta 分析克服了传统综述依赖于作者的主观分析、缺乏共同遵守的原则、步骤等缺点,可有效提高分析的样本量,改善研究的统计效能。本研究通过妊娠期接种TdaP 疫苗对孕妇和胎儿不良结局影响进行全面的Meta 分析,以期为妊娠期接种TdaP 疫苗提供循证医学证据。
1 资料与方法
1.1 文献检索方法 检索中国知网(China National Knowledge Infrastruture,CNKI)、中国生物医学文献数据库(China Biology Medicine disc,CBM)、万方数据库(WangFang Database,WF)、美国国家医学图书馆数据库(PubMed)、EMbase、Cochrane 协作网图书馆数据库,并结合文献追溯法查找建库至2020 年4 月关于孕妇接种TdaP 疫苗的文献。检索采用主题词与自由词相结合的方式,根据各数据库的特点对检索式进行调整。检索词为Pregnancy、Tetanus,Diphtheria and Acellular Pertussis or TdaP、safety,并用逻辑连接词“OR”和“AND”进行连接。同时辅以手工检索的方法进行检索及追溯纳入文献的参考文献。
1.2 纳入及排除标准
1.2.1 纳入标准 研究对象为孕妇;研究设计为随机对照试验(randomized controlled trial,RCT)[试验组是TdaP 疫苗组,对照组是安慰剂或其他疫苗,如破伤风类毒素(tetanus toxid,TT)疫苗、破伤风类毒素联合白喉类毒素(tetanus toxoid and DiPheria toxoid,Td)疫苗],无论是否进行分配隐藏、盲法和失访;安全性指标应至少包含下文定义的其中一项,根据预防用疫苗临床试验不良反应分级标准指导原则和全球妊娠免疫接种安全评估(Global Alignment of Immunization Safety Assessment in Pregnancy,GAIA)定义不良反应[19-20];语言为英文。
1.2.2 排除标准 研究方法不是RCT 及无对照研究;未标明接种人数或只有监测人数;无安全性数据或数据不全;综述、会议记要、讲座类文献、信;重复文献。
1.3 文献筛选方法及方法学质量评价 根据纳入和排除标准,由2 名研究者独立阅读文题、摘要和关键词对文献进行初筛,确定进入第2 轮筛选的文献;通过全文阅读确定最终纳入的文献[14-15,21-24];2名研究者汇总文献,若有不同意见,讨论或请第3 名研究者进行判定。参照修改后的Jadad 量表,对纳入文献进行以下4 方面的评价:随机分配、分配隐藏、盲法、失访和退出。Jadad 量表总分为7 分,4 ~7分为高质量,1 ~3 分为低质量。
1.4 数据提取 提取数据内容包括:文献基本信息(作者、发表年份、实施地区、干预措施、研究人数、孕妇年龄、接种时间、纳入的结局指标)、结局指标、局部不良反应(疼痛、肿胀、红斑)、全身不良反应(头疼、乏力或萎靡、发热、肌肉酸疼)、孕妇严重不良反应(妊娠高血压、肺栓塞、肾结石等)、早产、新生儿先天性异常和畸形、新生儿严重不良反应(脑膜炎、高胆红素血症等)。
1.5 统计学分析 应用Excel 2013 软件建立数据库,Revman 5.3 软件进行Meta 分析和图形制作。本研究Meta 分析结局指标均为二分类变量,采用风险比(risk ratio,RR)进行数据合并分析,以95%置信区间(95% confidence intervals,95% CI)表示。合并效应量采用Z 检验,设定检验水准α 为0.05,以P <0.05 为差异有统计学意义。用I2评估研究间的异质性,当I2>50%时,表明各研究间有异质性,采用随机效应模型进行分析;I2≤50%时,采用固定效应模型进行合并分析。异质性采用亚组分析或敏感性分析进行处理。采用Egger′s 法进行发表偏倚的检测,以α = 0.05 为检验水准,P <0.05 为有发表偏倚。
2 结 果
2.1 文献检索结果 共检索出相关文献391 篇,通过逐层筛选后,有6 篇RCT 纳入研究,包括文献[14-15,21-24],3 篇对照组是安慰剂,3 篇对照组是 TT /Td(评估TdaP 中百日咳成分在孕妇中的安全性),共计1 324 名受试者。纳入的6 篇RCT 研究中,高质量研究 5 篇,包括文献[14-15,21-22,24],得分为 4 ~ 7分);低质量研究 1 篇,为[23],得分为 3 分。纳入研究文献的基本特征见表1。
2.2 Meta 分析结果
2.2.1 孕妇局部不良反应发生率Meta 分析 局部不良反应包括疼痛(相应文献[15,22,24]),肿胀(相应文献[15,22])、红斑(相应文献[15,22,24])。纳入报告疼痛的各研究具有重度异质性(I2= 72%),采用随机效应模型进行合并分析;纳入报告肿胀、红斑的各研究均具有较好的同质性(I2均 = 0%),采用固定效应模型进行合并分析。TdaP 疫苗组的疼痛、肿胀、红斑不良反应发生率均高于TT / Td 和 安慰剂组(P < 0.01),见表2。
2.2.2 孕妇全身不良反应发生率的Meta 分析 全身不良反应包括发热(相应文献[14-15,22])、头疼(相应文献[15,22,24])、肌肉酸疼(相应文献[15,21,24])、乏力(相应文献[15,21-22,24])。纳入报告发热、头疼、肌肉酸疼的研究均具有同质性(I2分别为0%、0%、50%),采用固定效应模型进行合并分析;纳入报告乏力的研究具有异质性(I2= 61%),采用随机效应模型进行合并分析。TdaP 疫苗组与TT/Td 和安慰剂组的发热、头疼、肌肉酸疼、乏力发生的差异无统计学意义(P > 0.05),见表3。
2.2.3 其他严重不良反应发生率比较的Meta 分析纳入报告早产、孕妇严重不良反应事件、新生儿先天异常和畸形的研究同质性较好(I2均= 0%),采用固定效应模型进行合并分析。TdaP 疫苗组与TT / Td和安慰剂组早产、孕妇严重不良反应事件、新生儿先天异常和畸形发生率差异无统计学意义[RR 分别为1.48、0.98、0.74,95%CI 分别为 0.74 ~ 2.98、0.71 ~1.34、0.37 ~ 1.50,Z 分别为 1.10、0.13、0.83,P 分别为0.27、0.90、0.40)。纳入报告新生儿严重不良反应的研究具有异质性(I2= 55%),采用随机效应模型进行合并分析。TdaP 疫苗组与TT / Td 和安慰剂组的新生儿严重不良反应发生率差异无统计学意义(RR=0.83,95%CI:0.51 ~ 1.35,Z=0.74,P=0.46)。见图1。

表1 纳入研究的基本特征Tab.1 Basic characteristics of literatures included in this study
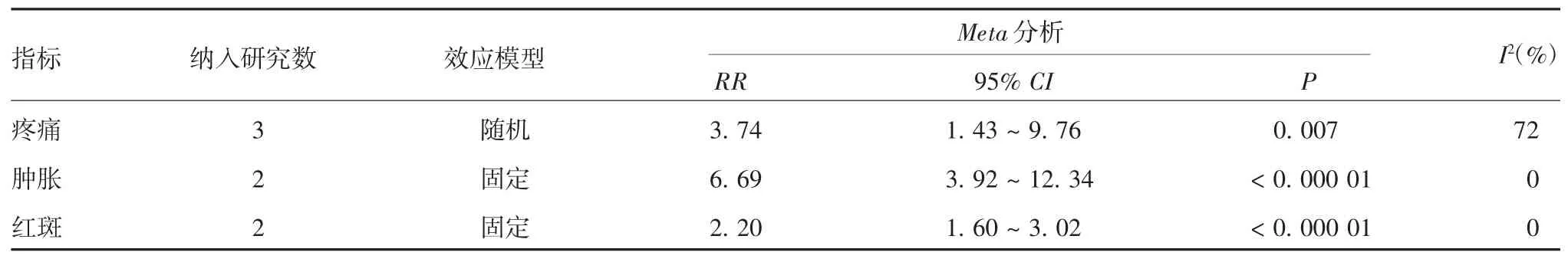
表2 TdaP 疫苗组与TT / Td 和安慰剂组局部不良反应发生率比较的Meta 分析Tab.2 Meta-analysis of incidences of local adverse reaction in TdaP vaccine and TT / Td and placebo groups
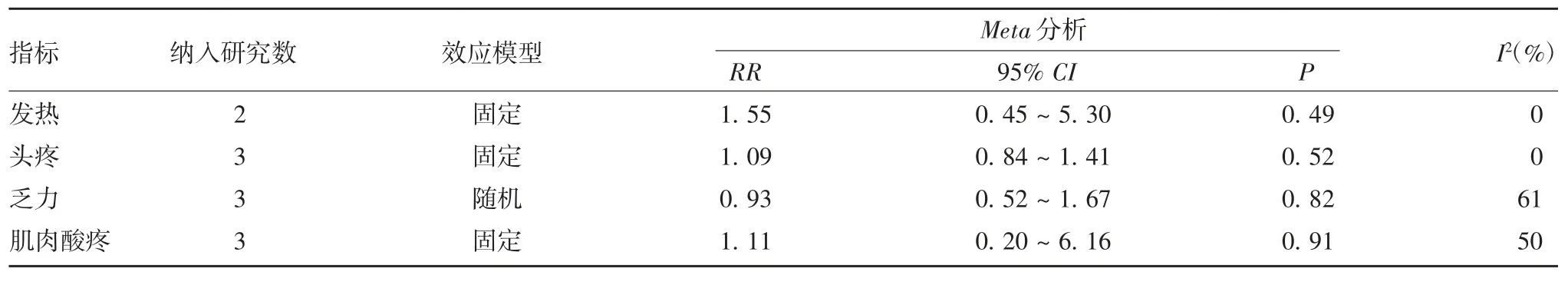
表3 TdaP 疫苗组与TT / Td 和安慰剂组全身性不良反应发生率比较的Meta 分析Tab.3 Meta-analysis of incidences of systemic adverse reaction in TdaP vaccine and TT / Td and placebo groups
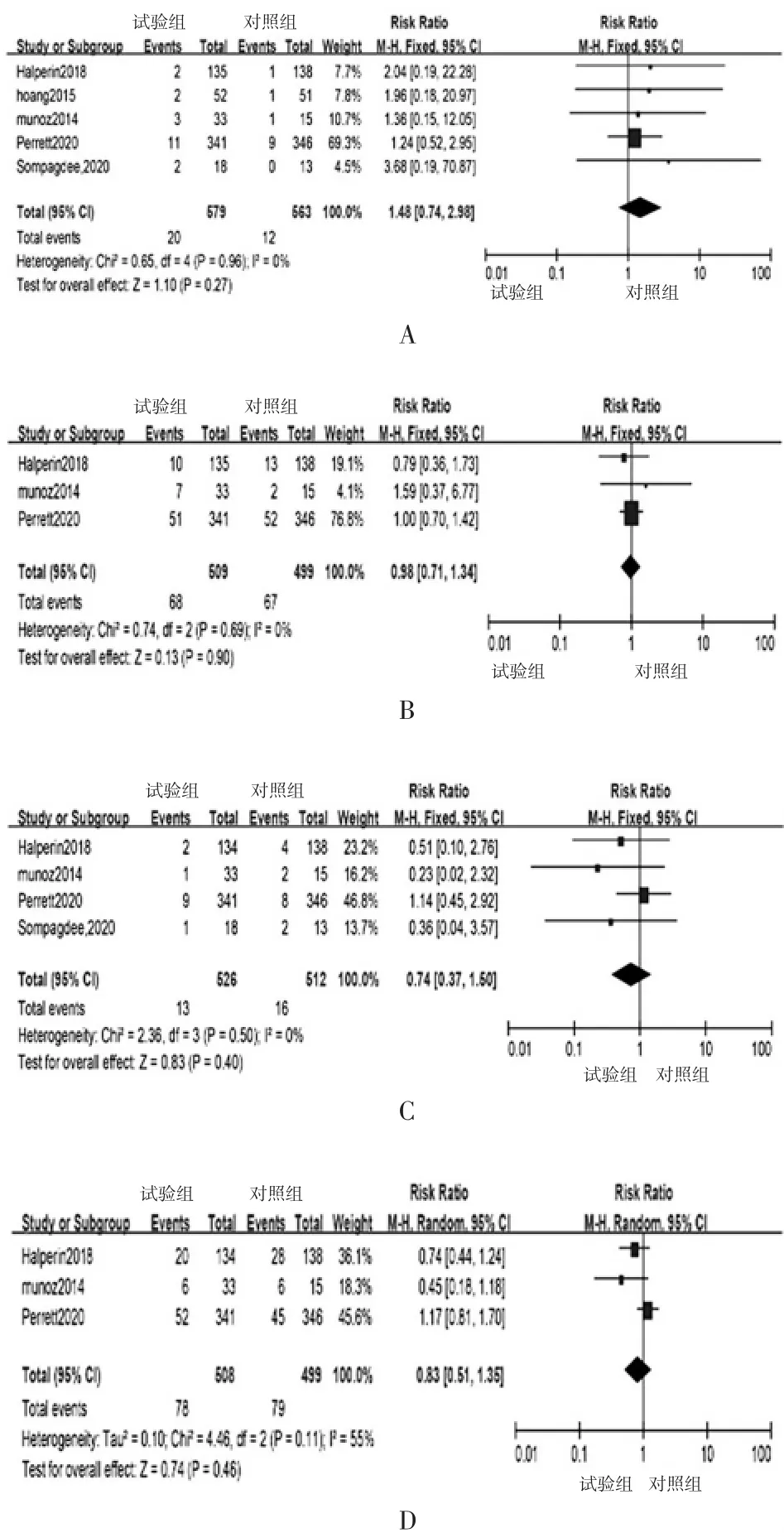
图1 妊娠期接种TdaP 疫苗与不良反应关系的Meta 分析森林图Fig.1 Forest plot for Meta-analysis of relationship between TdaP vaccination and adverse reactions during pregnancy
2.3 亚组分析 根据接种人群所在地区对疼痛进行亚组分析显示,北美地区和包含其他地区的合并效应量分别为 I2=0%(RR=1.28,95%CI:0.32 ~ 5.22)和 I2= 85%(RR = 0.87,95% CI:0.42 ~ 1.80),提示地区不是异质性来源。根据不同对照组对早产进行亚组分析显示,对照组TT / Td 和安慰剂的合并效应量分别为 I2=0%(RR=2.38,95%CI:0.56 ~ 10.18)和 I2=0%(RR=1.26,95%CI:0.56 ~ 2.81),提示对照组注射TT / Td 或安慰剂均不会对结果有影响。
2.4 敏感性分析 疼痛、乏力、新生儿严重不良反应中分别剔除文献[24]、文献[21]或[22]、文献[22],异质性消失(I2= 0%),合并效应量无明显变化。
2.5 发表偏倚 新生儿先天异常和畸形存在发表偏倚(t = 8.74,P = 0.015),早产、孕妇严重不良反应、新生儿严重不良反应、疼痛、红斑、头疼、乏力、肌肉酸疼、发热无发表偏倚(t 分别为-0.35、0.00、2.93、3.26、8.76、0.97、-1.42、0.36、0.21,P 分别为0.753、1.000、0.206、0.189、0.072、0.509、0.291、0.781、0.524)。
3 讨 论
3 月龄以下婴儿易被百日咳感染并引发危及生命的并发症(肺炎、癫痫、脑损伤等)。妊娠期接种TdaP 疫苗是预防婴幼儿感染百日咳最有效的手段[9]。一些国家推荐妊娠期接种TdaP 疫苗[25-27],但接种率不同,2014 年英国接种率为 60%[28],2013 —2014 年美国接种率为50%[29]。低接种率的主要原因是临床医生或女性对妊娠期接种TdaP 疫苗安全性的担忧[30-31]。本研究通过归纳汇总相关随机对照试验,应用Meta 分析的方法评价妊娠期接种TdaP疫苗对孕妇自身和新生儿安全性的相关结果,数据表明,妊娠期接种TdaP 会有明显的接种部位局部反应,不会增加全身不良反应、早产、孕妇严重不良反应、新生儿畸形、新生儿严重不良反应发生的风险。该结果可为国内外研究者、医务工作者及政策制定者提供参考,从而促进孕妇接种TdaP 疫苗,减轻疾病负担。
本研究纳入的6 个研究均为随机对照研究,且对妊娠期接种TdaP 与TT / Td 和安慰剂进行了安全性比较,结果显示,TdaP 疫苗组发生局部不良反应(疼痛、红斑、肿胀)的风险高于对照组。NASSER 等[13]研究显示,TdaP 疫苗组与对照组无差异,该研究仅纳入了4 篇RCT 文献,本研究纳入了6 篇,因此论证因果关系能力更强,其他安全性指标合并效应值无差异。VYGEN-BONNET 等[18]研究显示,妊娠期接种TdaP 疫苗会增加发热的风险,本研究结果显示,发热的风险无统计学意义(P >0.05),其原因可能是本研究纳入发热的样本量小,导致可信区间变大,有待今后开展大样本的RTC 研究进行进一步证实。本研究未发现妊娠期接种TdaP 对早产、孕妇严重不良反应、新生儿先天异常和畸形、新生儿严重不良反应的发生有影响,该结果与NASSER 等[13]研究结果相符,本研究还根据对照组是TT / Td 或安慰剂对早产指标进行了亚组分析,结果显示,效应量与原合并效应量一致,因此结论更具说服力。敏感性分析是研究单个文献是否影响整体的效应量,通过逐一剔除单个研究后重新进行合并效应分析。在对妊娠期接种TdaP 疫苗与新生儿严重不良反应的敏感性分析中发现,去除异质性较大的文献[22]后,妊娠期接种TdaP 疫苗不会增加新生儿严重不良反应发生的风险,与原分析结果相同,表明结果稳定性好。
鉴于本研究纳入文献仅有6 篇,因此采用Egger′s法进行定量评价发表偏倚,结果显示,新生儿先天异常和畸形存在发表偏倚,表明存在无统计学意义的小样本文献未被发表,其他结果无发表偏倚。由于肿胀的纳入文献仅有2 篇,未能进行发表偏倚检测。
本研究广泛且全面地收集了关于妊娠期接种TdaP 疫苗的文献,共6 篇RCT,增加了代表性;纳入了校正混杂因素的文献,重要指标纳入的研究同质性较好,对有异质性的指标进行敏感性分析后,合并效应量并未发生改变,结果可靠;纳入的不良指标更为全面;纳入研究在实验设计、干预措施、研究对象选择方面差异较小。但本研究尚存在一定局限性:纳入研究数量较少,最多的为5 篇,最少的为2 篇,使论证强度受到一定影响;各研究间指标定义不完全相同,可能会增加临床异质性;不同孕期和不同疫苗生产厂家的研究较少,导致未能按孕期及疫苗厂家进行亚组分析。
综上所述,妊娠期接种TdaP 疫苗,虽然局部不良反应发生风险较对照组高,但多为短暂、轻微的,且不会增加其他严重不良反应发生的风险,因此总体上认为,妊娠期接种TdaP 疫苗是安全的。但由于本研究所纳入原始文献的数量偏少,部分证据的引用需谨慎。今后将采用扩大样本量、完善试验设计、统一指标定义、允许阴性结果发表等策略来提高研究的质量和论证的强度。

