蛇葡萄素对结肠癌细胞增殖抑制、自噬诱导及自噬对增殖的影响研究
李晨红, 宋长丰, 林志康, 赵宇侠,2*
(1.上海中医药大学 研究生院,上海200120; 2.上海健康医学院 医学技术学院,上海201138;3.华东理工大学 药学院,上海200237)
结肠癌是胃肠外科常见的消化道恶性肿瘤,在我国的发病率和死亡率均排在前五,且呈逐年上升趋势[1-2],包括结肠癌在内的肿瘤是一种细胞凋亡过少而增殖过多的疾病,若能抑制肿瘤细胞的增殖并诱导其凋亡,肿瘤细胞就有可能停止生长[3],从而控制肿瘤的发生发展,因此有效抑制癌细胞增殖和促进凋亡是治疗的关键,寻找合适的靶点来调控肿瘤成为抗肿瘤药物关注的热点问题.
最近研究证实自噬与多种肿瘤细胞的恶性转化和生长相关[4].随着研究的不断深入,发现自噬相关分子例如Beclin1与肿瘤的发展有着密不可分的关系[5],一定程度的细胞自噬可以抑制肿瘤的增殖及转移[6-7],同时,自噬过程被证明能够通过调控肿瘤细胞凋亡及细胞增殖过程等形式抑制肿瘤[8-10].关于自噬蛋白作为抗肿瘤靶点的研究也已经进入临床前研究[11-12],探讨自噬与肿瘤细胞增殖关系具有积极的临床应用意义.
中药抗肿瘤作用的深入研究成为中药现代化推进的一项主要内容,AMP作为被广泛报道有抗肿瘤作用的中药单体,对于其抗肿瘤机制的研究也有大量报道,包括诱导细胞凋亡、抑制肿瘤侵袭转移、抑制细胞增殖[13-16]等.而且,AMP也被报道可以诱导细胞自噬[13-15],那么AMP是否能够通过自噬作用实现对细胞增殖过程的调控进而起到促进肿瘤细胞增殖抑制的作用值得研究,这将为自噬靶点的临床应用提供可行依据.
目前关于AMP诱导结肠癌HCT116细胞自噬且自噬对结肠癌细胞增殖的影响报道较少,本研究通过慢病毒感染法构建HCT116-RFP-GFP-LC3重组细胞株,体外实验将不同浓度AMP作用于HCT116及重组细胞株,初步探索AMP对结肠癌细胞的增殖活力、自噬诱导作用及阻断自噬晚期降解过程对结肠癌细胞增殖的影响,为深入研究其抗肿瘤机制提供一定依据,以期为结肠癌的治疗提供新思路.
1 材料与方法
1.1 实验材料 人结肠癌HCT116细胞来源于中国科学院细胞库;自噬慢病毒由上海吉凯基因化学技术有限公司构建,感染所用感染试剂(Polybrene,Enhanced Infection Solution)均由其提供.RPMI 1640培养基,质量分数1%青链霉素购自上海生工生物工程有限公司;胎牛血清、胰酶购自美国Gibco公司;嘌呤霉素(puromycin),巴佛洛霉素(Baf A1),质量分数4%多聚甲醛均购自北京建强伟业科技有限公司;蛇葡萄素(Ampelopsin,AMP)购自曼斯特生物科技有限公司;预染蛋白Marker购自美国Thermo公司;CCK-8检测试剂盒,Bradford蛋白定量试剂盒,SDS-PAGE凝胶制备试剂盒均购自上海碧云天生物技术有限公司;兔抗人β-actin、LC3B、P62抗体,山羊抗兔抗体均为美国Proteintech Group产品;ECL超敏发光液购自美国Bio-Rad公司;其他试剂均为国产分析纯级别试剂.
1.2 实验方法
1.2.1 细胞培养 使用RPMI 1640培养基(含质量分数10%FBS+质量分数1%青链霉素)于37℃、体积分数5%CO2培养箱中培养,根据细胞密度进行传代.
1.2.2 慢病毒感染 将HCT116细胞按5×103个/mL接种于96孔板中,细胞密度约30%开始感染,操作严格按照吉凯基因公司提供的说明书进行,以感染复数(MOI)为20设置实验分组,按照不同感染条件将实验分为4组:正常培养基组、含质量浓度5μg/mL Polybrene的正常培养基组、Enhanced Infection Solution组和含质量浓度5μg/mL Polybrene的Enhanced Infection Solution组.感染72 h后激光共聚焦显微镜观察细胞荧光蛋白表达情况,选取MOI为20、含质量浓度5μg/mL Polybrene的Enhanced Infection Solution条件扩大培养,每2~3 d换含puromycin(终质量浓度3μg/mL)的完全培养液一次,至不感染筛选对照组细胞被puromycin杀光,将感染并筛选后的细胞进行传代,并继续施加puromycin进行维持性筛选培养,连续筛选并传3代后,冻存保种稳定细胞株.
1.2.3 激光共聚焦观察结肠癌细胞荧光表达 将HCT116-RFP-GFP-LC3重组细胞按5×105个/mL接种于6孔板爬片中,待细胞贴壁后弃培养基,用PBS洗2次,加入适量质量分数4%多聚甲醛溶液固定10 min,PBS洗3次,封片剂封片,通过激光共聚焦显微镜在200×下观察并记录绿红色荧光表达,确认构建重组细胞株成功.
将重组细胞按5×104个/mL接种于24孔板中,分别用AMP(质量浓度0、50、75μg/mL)组及AMP(质量浓度0、50、75μg/mL)+Baf A1组处理24 h,检测AMP诱导HCT116-RFP-GFP-LC3重组细胞自噬情况.弃培养基,PBS洗2次,用1 mL DAPI溶液覆盖细胞染色15 min,PBS洗3次,加入适量质量分数4%多聚甲醛溶液固定10 min,PBS洗2次,封片剂封片,通过激光共聚焦显微镜(630×)随机观察3个视野并记录,LC3自噬点的计算方法参照Popp等[17]研究方法,采用Image J软件中“Threshold”和“Analyze Particles”功能进行图像分析.
1.2.4 CCK-8法检测细胞增殖活力 将HCT116细胞按1×104个/mL接种于96孔板中,用AMP(质量浓度0、25、50、75、150、300μg/mL)处理24 h,每孔加质量分数10%CCK-8溶液反应1 h.酶标仪检测每孔在450 nm处的吸光度(OD值),计算

设置3个重复实验测定AMP对HCT116细胞增殖影响.
1.2.5 细胞形态学观察 将HCT116细胞按5×105个/mL接种于6孔板中,用AMP(质量浓度0、25、50、75、150、300μg/mL)处理24 h,用PBS洗2次,质量分数4%多聚甲醛固定5 min,PBS洗2次,倒置显微镜(100×)下观察并记录细胞形态学变化.
1.2.6 蛋白质印迹法检测自噬相关蛋白表达 将HCT116细胞按5×105个/mL接种于6孔板中,AMP(质量浓度0、50、75μg/mL)组及AMP(质量浓度0、50、75μg/mL)+Baf A1组处理24 h,用预冷的PBS(含质量分数5%PMSF)洗涤3次后,加入RIPA裂解液,冰上裂解30 min,4℃12 000 g条件下离心取上清,采用Bradford法定量蛋白浓度.随后取40μg蛋白进行质量分数15%SDS-PAGE电泳,250 mA、0.5 h条件下PVDF膜转膜1 h,质量分数5%脱脂奶粉封闭2 h,分别加入一抗兔抗人的β-actin、LC3B、P62抗体(稀释比例为1∶1 000)后4℃孵育过夜;次日TBST液洗膜后加入山羊抗兔的二抗(稀释比例为1∶2 000),室温孵育2 h,充分洗膜后ECL发光液避光孵育1 min显影,用Image Lab软件分析每组目的蛋白和相对应的内参蛋白条带灰度值.
1.2.7 统计学方法 所有研究结果均采用SPSS 17.0软件进行统计学分析,计量资料呈正态分布,以均数±标准差±s)表示,两组间比较采用独立样本t检验,多组间比较采用单因素方差分析,进一步两两比较采用LSD法,P<0.05表示差异有统计学意义.
2 结果
2.1 稳定表达RFP-GFP-LC3蛋白的细胞系鉴定结果 HCT116-RFP-GFP-LC3重组细胞由携带有LC3、RFP、GFP全基因的重组慢病毒感染,其中RFP、GFP和LC3作为一个重组基因组同步共表达,荧光检测捕捉到的RFP或GFP荧光蛋白表达则标志为LC3表达,反之亦然;载体结构中包含嘌呤霉素(puromycin)抗性,采用puromycin(3μg/mL)持续筛选细胞,得到感染效率100%的HCT116-RFP-GFP-LC3重组细胞株.激光共聚焦显微镜下观察经感染和嘌呤霉素筛选获得稳定表达RFP-GFP-LC3蛋白的重组细胞,可以看到RFP或GFP荧光蛋白表达的阳性细胞,且细胞状态较好(图1,其中(a)为白光下重组细胞;(b)为红色荧光LC3蛋白细胞;(c)为绿色荧光LC3蛋白细胞;(d)为(b)和(c)的荧光蛋白细胞merge图),可以作为检测细胞自噬标志性蛋白LC3表达的细胞模型.

图1 重组细胞的RFP-GFP-LC3荧光蛋白表达情况Fig.1 RFP-GFP-LC3 fluorescent protein in recombinant cells
2.2 AMP对HCT116细胞毒性作用 CCK-8法检测结果(图2(A)为AMP对HCT116细胞增殖影响)显示,不同浓度的AMP(质量浓度为0、25、50、75、150、300μg/mL)作用于HCT116细胞24 h后,在低质量浓度(0~75μg/mL)范围内对HCT116细胞增殖抑制不显著(P>0.05).形态学上观察无明显差异(图2(B)为AMP对HCT116细胞形态影响,其中a、b、c、d、e、f分别指代AMP质量浓度为0、25、50、75、150、300μg/mL处理后HCT116细胞形态图),但高质量浓度AMP(150、300μg/mL)抑制HCT116细胞增殖活力,细胞形态发生变化,表明AMP具有抗肿瘤作用.

图2 AMP对HCT116细胞毒性的影响Fig.2 The effect of AMP on the cytotoxicity of HCT116 cells
2.3 AMP诱导结肠癌细胞自噬的结果
2.3.1 激光共聚焦法观察自噬体形成情况 在本实验中,选用AMP(质量浓度0、50、75μg/mL)组及AMP(质量浓度为0、50、75μg/mL)+Baf A1组作用HCT116-RFP-GFP-LC3细胞24 h后,激光共聚焦显微镜结果如图3所示,其中图3(a)为各组细胞自噬发生情况,图3(b)为各组自噬荧光蛋白表达统计图,Baf A1为自噬晚期抑制剂,正常对照组的绿色或红色荧光在细胞中呈散在分布,自噬水平较低,自噬发生率5.15%,AMP(质量浓度50、75 μg/mL)处理组的细胞出现绿色或红色荧光点状聚集的自噬体,自噬发生率分别为26.72%、19.47%,说明AMP能够诱导HCT116-RFP-GFP-LC3细胞发生自噬.
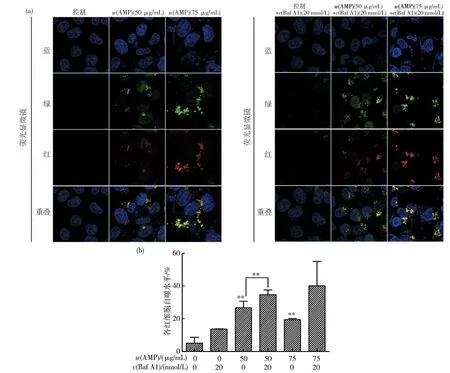
图3 激光共聚焦检测AMP-AMP+Baf A1处理组的HCT116-RFP-GFP-LC3细胞自噬点Fig.3 The fluorescent spot of recombinant cells in the AMP-AMP+Baf A1 groups were observed by laser confocal microscopy(X630)
一般把自噬过程分成3个阶段.第一阶段:自噬诱导信号刺激细胞,细胞质中形成杯状具双层膜结构的自噬前体;第二阶段:自噬前体在一些自噬蛋白的作用下不断延伸,如伴随此过程的LC3不断被聚集到自噬前体上,对自噬前体的延伸起着关键的调节作用,进而包裹一些胞浆成分形成自噬泡;第三阶段:自噬泡通过胞内运输系统到达溶酶体,溶酶体、自噬体两者融合,并在溶酶体的水解酶作用下降解包裹物[18-20].
实验中HCT116-RFP-GFP-LC3重组细胞中红绿色荧光均能代表LC3蛋白的表达,区别在于自噬后期,自噬后期溶酶体与自噬体融合形成自噬溶酶体,环境pH值发生改变,而绿色荧光蛋白对酸性环境敏感.当环境pH<5时,绿色荧光发生淬灭,不能用来表征LC3表达,只能检测到红色荧光点状聚集,因此绿色荧光只能用来检测自噬前两个阶段.第三阶段溶酶体降解过程,绿色荧光猝灭,红色荧光可以持续表达表征LC3表达,红绿荧光共定位复合为黄色荧光,绿色荧光的淬灭证明自噬晚期降解过程完成,红绿色同时存在则说明自噬处于前两阶段或晚期溶酶体降解过程阻断,自噬过程没有完成[4,18,20].
自噬晚期抑制剂Baf A1通过抑制H+-ATP酶,从而阻止自噬体和溶酶体融合,LC3Ⅱ蛋白就会聚集在自噬体膜上不被降解,绿色荧光蛋白不发生淬灭,红绿色荧光均能被检测到,此时能观察到更多细胞的LC3Ⅱ蛋白荧光自噬点,因此,自噬荧光亮点的细胞数增加表明自噬晚期降解过程被阻断.换言之,加入Baf A1后,若观察到自噬点增加证明了自噬晚期降解过程被成功阻断,而不是自噬诱导增强.本研究中,相对于control组,control+Baf A1组绿色荧光较暗,红色荧光较多,此时绿光淬灭,红光正常表达,表明自噬过程完整;同时,相对于AMP(质量浓度0、50、75μg/mL)组,AMP(质量浓度0、50、75μg/mL)+Baf A1组的自噬发生率分别为13.78%、34.69%、40.10%,红色或绿色点状聚集的细胞数量分别增多了168%、30%、106%,说明Baf A1有效阻断AMP诱导的结肠癌细胞自噬晚期降解过程.
2.3.2 蛋白质印迹法检测自噬相关蛋白表达结果通过蛋白质印迹法对AMP(质量浓度0、50、75μg/mL)及AMP(质量浓度0、50、75μg/mL)+Baf A1组进行了验证,结果如图4所示,其中图4(a)为自噬相关蛋白印迹图,图4(b)为对应自噬蛋白表达量统计图.相对于空白对照组,AMP(质量浓度50、75μg/mL)组细胞的LC3II蛋白表达水平上调,AMP(质量浓度50μg/mL)组变化不显著(P>0.05),表明AMP诱导结肠癌HCT116细胞自噬,同时AMP(质量浓度50μg/mL)组的P62蛋白被降解,表明自噬流晚期自噬溶酶体降解过程完成.
加入Baf A1后,自噬晚期降解过程阻断,相对于AMP(质量浓度0、50、75μg/mL)组,AMP+Baf A1组的LC3II蛋白表达上调,其中AMP(质量浓度0、75μg/mL)+Baf A1组虽然LC3II蛋白表达数值上调,但变化不显著(P>0.05);相对于AMP组,AMP+Baf A1组的P62蛋白表达数值上调,其中AMP(质量浓度0、50μg/mL)+Baf A1组数值增大但不显著,表明Baf A1加入后阻断溶酶体降解过程,从而LC3II和P62蛋白未被降解表达上调,侧面证明AMP诱导HCT116细胞发生自噬流.
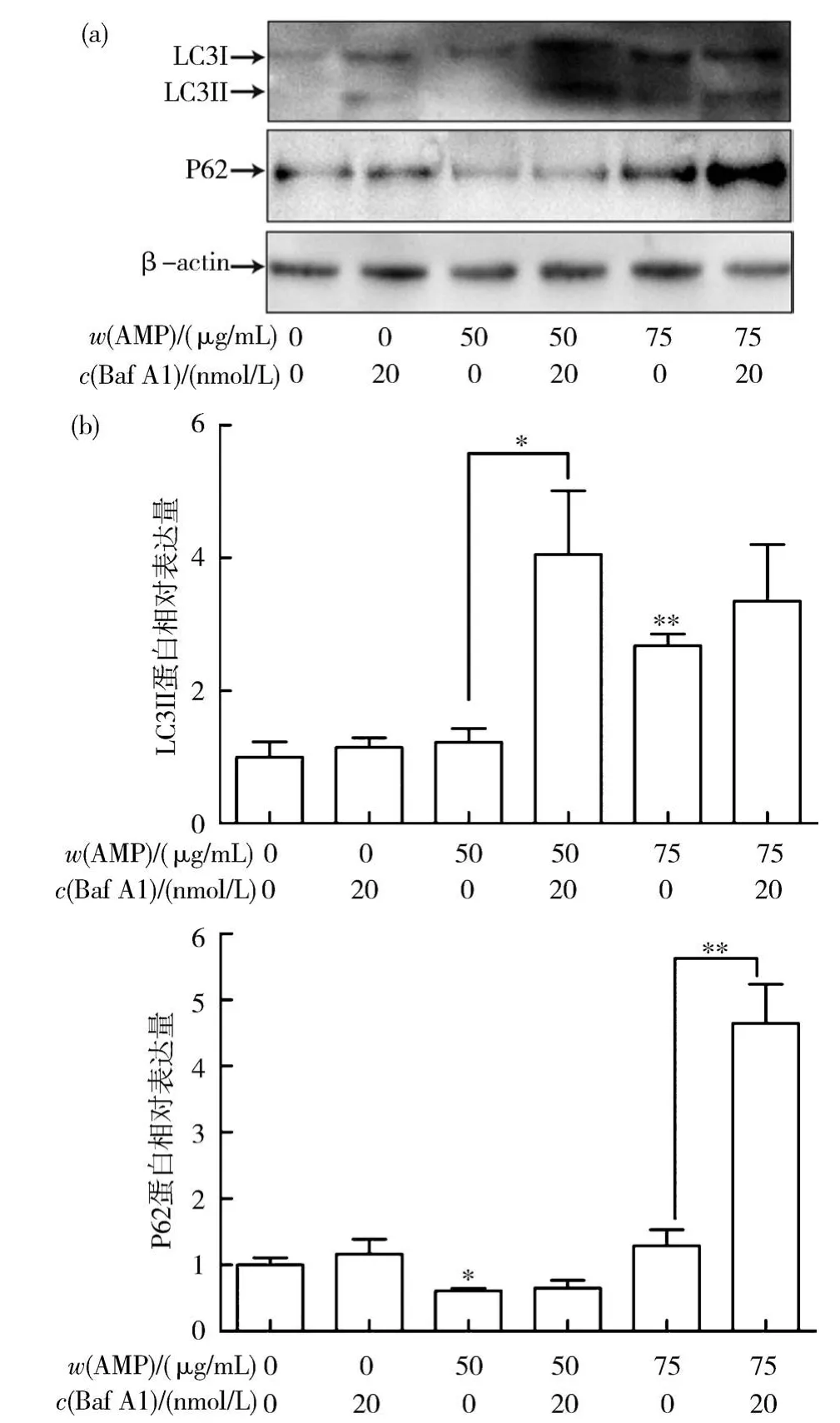
图4 AMP-AMP+Baf A1组诱导的HCT116细胞自噬相关蛋白LC3I/II和P62的表达量Fig.4 The expression of the autophagy-related proteins of LC3I/II and P62 in the AMP-AMP+Baf A1 groups
2.4 阻断自噬晚期降解过程对HCT116细胞增殖的影响 根据CCK-8实验结果,选取有显著性差异的细胞增殖抑制浓度AMP(质量浓度0、75、150、300μg/mL),加入Baf A1后,自噬晚期降解过程阻断,AMP与AMP+Baf A1组间细胞增殖活力影响不显著(P>0.05)(图5),结果表明AMP(质量浓度0~300μg/mL)范围内,自噬晚期溶酶体降解过程阻断对细胞增殖活力无影响.
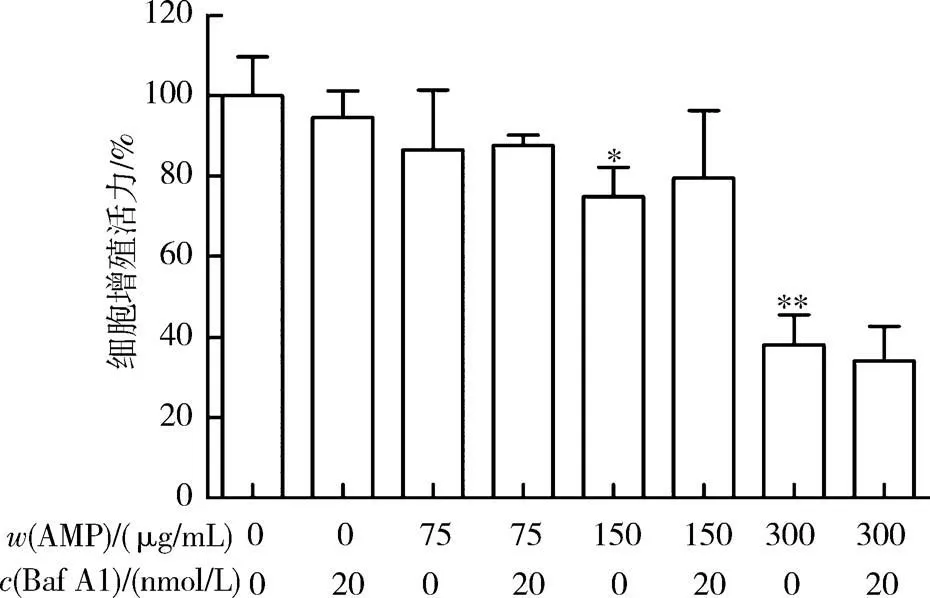
图5 Baf A1对AMP诱导的HCT116细胞增殖活力影响Fig.5 The effect of Baf A1 on AMP-induced proliferation in HCT116 cells
3 讨论
细胞增殖是生物体的重要生命特征,细胞以分裂的方式进行增殖,增殖是生物体生长、发育、繁殖和遗传的基础[21].肿瘤是一种细胞周期疾病,肿瘤的发生发展与细胞生长周期的失调直接相关,诸多研究表明通过药物干预抑制肿瘤细胞的周期进程可以抑制肿瘤细胞增殖[22].本研究中,AMP(0~300μg/mL)作用于结肠癌HCT116细胞24 h后,高浓度下细胞增殖活力受到抑制,细胞形态变化,但低浓度范围内对HCT116细胞增殖影响不大,细胞形态影响较小,说明AMP具有潜在抗肿瘤的临床应用价值,这与AMP能够抑制肺癌、卵巢癌和胃癌的增殖,还能增强奥沙利铂抗结肠癌的活性[16]报道相一致.
大量报道表明,哺乳动物雷帕霉素靶蛋白(Mammalian Rapamycin Target of Rapamycin,mTOR)是细胞增殖和自噬的中心调节器,因此自噬可能参与并影响细胞增殖过程[23-24],成为调控细胞增殖的靶点.研究表明,AMP能够诱导乳腺癌细胞[14]和人胶质瘤细胞[15]自噬,也有报道称褪黑素通过自噬增强神经干细胞增殖[25],双氢青蒿素通过诱导细胞自噬抑制HepG 2.2.15细胞增殖[26].本研究通过AMP对细胞自噬的诱导以及自噬晚期降解过程阻断检测细胞增殖,来探索AMP抑制HCT116细胞增殖的作用是否通过自噬作用调控和实现.
细胞自噬是真核生物中进化保守的对细胞内物质进行周转的重要过程,利用溶酶体吞噬并降解自身受损蛋白或细胞器并得以循环利用[4,18].本论文通过构建RFP-GFP-LC3双荧光自噬指示细胞系作为检测细胞自噬标志性蛋白LC3表达的细胞模型,选取AMP(质量浓度0、50、75μg/mL)作用于重组株24 h后,激光共聚焦观察正常对照组细胞中绿色或红色荧光呈散在分布,自噬发生率为5.15%,AMP(质量浓度50、75μg/mL)组的细胞出现绿色或红色荧光点状聚集的自噬体,自噬发生率分别为26.72%、19.47%,说明AMP能够诱导HCT116-RFP-GFP-LC3细胞发生自噬,这与中药雷公藤甲素诱导结肠癌细胞自噬的研究相一致[27].自噬体与溶酶体融合时,与膜表面偶联的LC3Ⅱ荧光蛋白被降解,自噬荧光颗粒减弱或细胞自噬数目减少,而这个过程被Baf A1阻断,因此LC3Ⅱ蛋白进入溶酶体后,就会聚集在自噬体膜上不被降解,此时观察到更多细胞的LC3Ⅱ蛋白荧光自噬颗粒点或更多数量的细胞自噬.实验中,相对于AMP(质量浓度0、50、75μg/mL)组,AMP+Baf A1组的自噬发生率分别为13.78%、34.69%、40.10%,红色或绿色点状聚集的细胞数量分别增多了168%、30%、106%,说明Baf A1能够有效阻断AMP诱导的结肠癌细胞的自噬溶酶体降解过程,侧面证明发生自噬流过程.
LC3是自噬活性标志物,可直观反应自噬表达水平,目前最为广泛的检测方法是通过蛋白质印迹法检测LC3蛋白表达水平,SQSTM1/P62是选择性自噬最重要的货车蛋白,也被称为选择性自噬受体,它是连接LC3与待降解泛素化底物的桥梁,通常选择P62结合LC3蛋白翻转实验评价自噬流[19-20].蛋白质印迹法对AMP(质量浓度0、50、75μg/mL)组及AMP+Baf A1组进行了验证,其LC3蛋白表达结果与自噬点检测的LC3荧光表达观察结果一致,对应自噬诱导和自噬降解过程阻断的P62的低表达与未降解蓄积的高表达相呼应,这与AMP能够促进头颈部鳞状细胞癌(HNSSC)自噬的结果一致[13],以上结果均能证实AMP诱导细胞自噬.
本论文在探索自噬对细胞增殖影响中,采用自噬抑制剂Baf A1人工干预,在AMP(质量浓度0~300μg/mL)剂量范围内,加入Baf A1,自噬晚期溶酶体降解阶段阻断,图5结果显示阻断自噬晚期降解过程对AMP组与AMP+Baf A1组间细胞增殖活力影响不显著(P>0.05),这说明阻断自噬降解过程对结肠癌HCT116细胞增殖无影响.
目前讨论AMP诱导的结肠癌HCT116细胞自噬影响增殖的研究还很少,本研究证实AMP可抑制细胞增殖,发挥抗肿瘤作用,诱导结肠癌HCT116细胞发生自噬,Baf A1阻断AMP(质量浓度0~300μg/mL)诱导的自噬晚期降解过程,且图5结果证明阻断自噬晚期降解过程不影响细胞增殖(P>0.05),但自噬参与机体多种途径,是否影响凋亡或抑制细胞周期蛋白D1(CyclinD1)表达等调控抗肿瘤作用还需进一步实验探索,以期为临床治疗结肠癌提供有效的实验依据与理论基础,并揭示了细胞自噬是调控结肠癌治疗的潜在靶点.
致谢 上海健康医学院种子基金(E1-0200-19-201132)和上海健康医学院百人库项目(B1-0200-19-311133)对本文给予了资助,谨致谢意.

