宫颈癌后装治疗中基于U-net的自动施源器分割
胡海 黎杰 王培 唐斌 王先良 杨强
宫颈癌是女性常见的恶性肿瘤,根据2018年对185个国家36种癌症的统计结果显示,全球宫颈癌新发患者达到了569 847例,死亡患者达到了311 365例[1]。标准的宫颈癌放射治疗模式是在进行外照射治疗之后,通过后装治疗进行补量[2-3]。图像引导的三维后装是后装治疗技术的主流,施源器重建是三维后装治疗计划设计的关键一步,现阶段施源器重建都依靠物理师人工完成,存在着重建精度受物理师主观因素影响大,重建速度慢的缺点。施源器重建的精度、患者从扫完定位CT到治疗期间长时间的等待都会影响到患者的剂量分布[4-6],从而影响患者的治疗效果。自动后装治疗计划设计是未来发展的方向之一,在后装治疗计划制定中,自动、精确、快速地重建施源器是尚未解决的问题。本文基于U-net网络建立了一种用于分割三维CT图像中施源器的深度学习模型,并通过戴斯相似性系数(DSC)、95百分位豪斯多夫距离(HD95)、相关体积差异(RVD)、精确率和召回率等参数对模型分割结果进行了评估,现报道如下。
1 材料和方法1.1 数据和数据标注
本文回顾性研究了2019年12月—2020年10月间27例四川省肿瘤医院已完成治疗的宫颈癌患者的CT数据,CT图像的分辨率为0.1 cm×0.1 cm×0.3 cm。27例患者使用的均为金属管柱施源器(Elekta applicator,no.084.350),CT层数范围是70~94层,平均值为84层。施源器的标注是由经验丰富的物理师在核通(Elekta AB,Stockholm,Sweden)治疗计划系统中进行,在每层CT中用直径6 mm的圆圈勾画出施源器的轮廓,进行标注。患者含施源器标注的CT层数在37~65层,平均为54层。最终得到规模为512×512×(54×27)的含有CT图像和对应施源器标注图像(以下称真值图)的数据集,按15∶2∶10将数据集划分为训练集、验证集和测试集。在标注时考虑到施源器连接端(下段)和顶端(上段)不同的结构特征,选择施源器的连接端(图1a)和顶端(图1b)进行标注展示,图1c和图1d为其对应的真值图。

图1 施源器标注和对应的标注图像(真值图)
1.2 数据预处理
对训练集和验证集中的CT图像进行直方图均衡化操作,增强图像中施源器和背景之间的对比度,使施源器的特征更加明显。由于施源器通常位于CT图像的中间部位,为加快训练速度,对CT图像及其对应的真值图进行裁剪处理,裁剪是每层图像的几何中心,上下左右裁剪尺寸均为128,得到规模分别为256×256×(58×15),256×256×(59×2)的训练集和验证集,其中256×256为裁剪后CT图像和真值图的尺寸,15例训练集患者平均样本数为58,2例验证集患者的平均样本数为59。对CT图像和真值图进行归一化处理,使其所有数据落在0~1之间。通过Keras的数据增强接口,对训练集CT图像和真值图进行相同的旋转、放大和平移等操作,完成数据增强。最终得到训练集和验证集的规模分别为256×256×(116×15),256×256×(59×2),116为经过数据增强后训练集每例患者的平均样本数量。
1.3 U-net网络模型的构建
1.3.1 模型的构建 模型基于经典U-net网络结构建成[7],总共由10个部分组成。模型输入为256×256×1的CT图像,前5层为下采样层,每层包含两次卷积操作和一次最大池化操作。6~9层为上采样层,每层在反卷积操作后通过跳跃连接层(Skip connection)将底层信息和高层信息融合,接着进行两次卷积操作。卷积核的大小为3×3,反卷积核的大小和最大池化核的大小为2×2,步长均为1,激活函数为Relu。第10层通过1×1卷积核将跨通道的特征进行整合,激活函数为sigmoid,最后输出256×256×1的二维预测图(图2)。
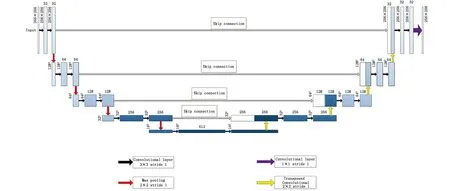
图2 U-net网络结构
1.3.2 模型的编译 模型编译中优化器选择Adam(Adaptive Moment Estimation)[8],利用梯度的一阶矩估计和二阶矩估计动态调整每个参数的学习率,经过偏执校正,每次迭代后学习率都有确定范围,使得参数比较完整。监测(Metrics)选择DSC,定义如下:
公式中A为预测图,B为真值图,λ则为Laplace平滑因子。为了减少过拟合和避免出现分母为0的情况,本研究λ=1。
损失函数(Loss function)选择Ls(Dice loss),Ls定义如下:
Ls=1-DSC
1.4 网络的训练及分割
将预处理过后的训练集和验证集放入网络中进行训练,训练在一台intel Core i7-7700HQ CPU @ 2.80GHz,GPU NVIDIA GeForce GTX 1050ti,8GB RAM的计算机上完成,批处理(Batch size)为8,轮次(Epoch)为200次,初始学习率(Learning rate)为0.0001,通过监测学习过程对学习率进行动态调整。训练结束后,将测试集的数据输入网络进行分割,得到相应患者的分割结果并对其进行评估(图3)。

图3 U-net训练预测流程
1.5 分割效果的评估
1.5.1 DSC 施源器的重建精度取决于施源器的分割精度。因此为了评估分割效果,采取五种方式进行评估[9-11]。模型的编译部分已对DSC进行了定义,它用于度量两个样本的相似性,取值范围为[0,1]。0代表基本不相似,1代表两个样本相似度高,分割结果非常好。在实际预测中,每例患者有70~90层CT图像,因此对DSC求均值及标准差(以下评估方式均采取相同处理)。
1.5.2 豪斯多夫距离(Hausdorff distance,HD)
由于DSC预测图内部填充比较敏感,故还得计算对边界比较敏感的HD来评估模型。给定欧式空间中的两样本A和B,HD用来衡量这两个样本间的距离,计算公式如下:
HD(A,B)=max(D(A,B),D(B,A))
式中:
D(A,B)=maxa∈Aminb∈B||a-b||
式中A为预测图,B为真值图,a,b分别为A,B里面的元素。为了消除预测图和真值图之间离群值的影响,计算HD的95个百分位得到HD95。
1.5.3 RVD RVD定义如下:
λ为Laplace平滑因子,λ在评估过程中取1,避免出现分母为0的情况。
1.5.4 精确率和召回率 精确率是在被所有预测为正的样本中实际为正样品的概率,公式如下:
召回率为实际为正的样本中被预测为正样本的概率:
2 结果
2.1 模型的训练结果
模型在25个轮次之后,训练集和验证集上损失函数已收敛到较低水平。在200轮次后,训练集损失函数降到0.07,验证集上损失函数降到0.1,训练集上DSC达到了0.93,验证集上DSC达到了0.90,表明该模型对施源器特征的学习效果较好。训练总共用时7小时。训练过程中训练集、验证集损失曲线在200个轮次之后的结果显示模型已收敛(图4)。

图4 训练和验证损失曲线
2.2 模型的分割结果
将训练模型对测试集10例患者进行分割。以第1、2例患者为例,两例患者施源器连接端和顶端的分割结果较佳(图5)。
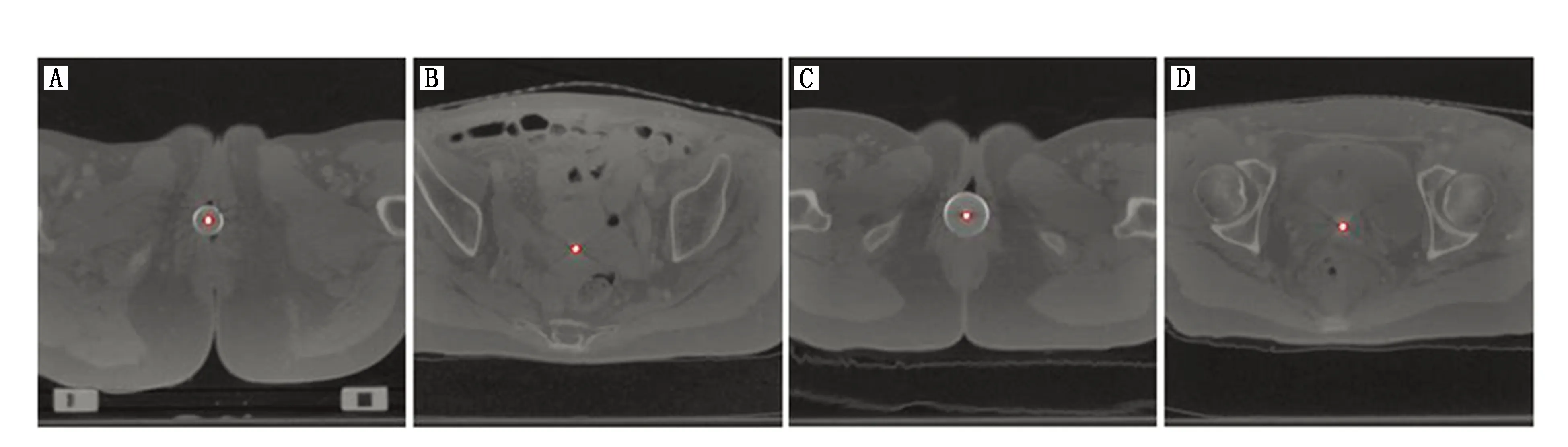
图5 预测分割结果
测试集10例安有金属管柱施源器的患者分割效果评估参数都较理想,DSC平均为0.90,HD95最大为2.85 mm,最小为0.86 mm,平均为1.26 mm,RVD、准确率和召回率平均则分别为-0.06,0.94和0.88。患者分割预测时间最长为6 s,最短时间为4 s,平均为5 s(表1)。
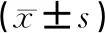
表1 10例患者的评估结果
3 讨论
施源器作为患者和放射源之间的纽带,在后装治疗中的重要性不言而喻。施源器的重建质量对整个治疗计划起着关键性的作用[12]。本研究基于U-net框架构建模型,将CT图像和真值图进行预处理后输入模型,让模型学习施源器的特征信息,再将特征信息应用到新的患者上。通过对模型分割结果的多重评估,证明该方法可行可靠,可以快速准确的分割出施源器。通过模型分割施源器仅需要5 s左右,DSC精度也可达到0.90。
近年来随着计算机硬件的发展,深度学习逐渐在不同的领域大放光彩,不同的网络被开发出来解决各种问题。2015年Ronneberger等[7]首次提出了U-net网络,适合小数据集的图像分割,针对于像素级分类,整个网络分为编码和解码部分,通过跳跃连接(Skip connection)进行特征融合。由于U-net的特点,U-net网络模型被广泛应用于医学图像分割领域[13],因此本研究选择U-net网络。通过将深度学习技术与三维后装技术结合起来,完成计划制定中施源器的快速精确重建,降低物理师在重建过程中产生的人为误差,使得制作的计划更为精准,也为患者的治疗提供更好的保障。
目前国内外对后装治疗中施源器分割的研究还比较少。国内,朱琳等[14]采用基于灰度值的自动跟踪算法重建施源器,在保证正确重建施源器的前提下,平均节省了1/2的施源器重建时间。国外,Zhang等[15]构建了Attention网络将其应用到超声引导的高剂量率前列腺后装治疗中,成功地分割定位出插值针在超声图像中的位置,本研究借助了其思路,完成了在宫颈后装中对管柱施源器的分割。Zaffino等[9]通过构建三维U-net网络,完成了核磁引导的宫颈癌后装中的插值针的重建,最后的DSC达到了0.6左右。本研究与之相比,DSC更高,且本研究根据医院的实际情况,由于管柱施源器使用频率高,故针对性的对其进行分割重建,为治疗效果的提升添砖加瓦。
后装治疗计划制定的自动化是未来发展的方向,计划制定流程包括器官勾画、施源器重建、剂量计算、剂量优化和计划评估等。前期课题组已经完成了器官勾画、剂量计算与剂量优化的工作[16-19]。本研究可与前期工作进行整合,实现计划制定的自动化,提升工作效率。
本研究还有少量的不足之处,具体体现在以下几个方面:(1)只对金属管柱施源器进行了研究。临床中的施源器种类繁多,核磁三管和金属三管施源器等应用也较为广泛,该模型不一定适用于其他施源器。但是在具备了本研究基础的情况下,可以很快开展其他不同种类施源器的分割工作;(2)当前患者数据量较少,仅有15例患者的数据用来训练,可以进一步搜集数据,完善当前工作,使得分割效果更加精确;(3)施源器重建的目的是为了确保在临床中的可用性,然而本研究目前只进行了施源器的分割工作,还未进行施源器的重建验证。但是通过对比施源器分割的精度,推测施源器重建的精度足以满足临床需求。临床中施源器的自动重建、重建偏差对患者剂量的影响和施源器重建模型的评估是本课题组正在开展的工作。
综上所述,本文通过构建U-net模型,研究后装治疗计划中施源器重建工作,现阶段成功完成金属管柱施源器的分割,并对分割结果通过不同方式进行了评估。结果显示该模型分割效果较好,分割的各种评估参数都较佳,满足临床上施源器的重建。施源器的精准分割是能否精确重建最为关键的一步,该模型完成的施源器精确分割对后面实现治疗计划制定自动化流程中的施源器重建具有重大意义。

