初中化学微粒观的层级、内涵与策略
成素萍

摘要:分析有关发展学生“宏观辨识与微观探析”素养的文献特点,尝试对比、分析三个版本教科书中“宏观辨识与微观探析”的发展层级、内涵,基于“证据推理与模型认知”,通过从微观视角建构认识微粒的知识框架、建构原子水平上的分子模型、分析质量守恒定律的微观实质、构建物质溶解的微观模型和反应类型等实践策略,使化学核心素养的培养具有可操作的实际意义。
关键词:初中化学;宏观辨识与微观探析;内涵解析;实践策略
文章编号:1008-0546(2021)07-0002-05 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.07.001
一、问题的提出
普通高中化学课程标准(2017版)指出:“化学是在原子、分子水平上研究物质的组成、结构、性质、转化及其应用的一门基础自然科学,其特征是从微观层面认识物质,以符号形式描述物质,在不同层面创造物质[1]”。义務教育化学课程标准(2011版)中有关原子、分子的学习标准,注重控制难度,除“认识物质的微粒性、初步认识核外电子在化学反应中的作用”外,认知目标水平的行为动词都是“知道”,认知性学习目标的最低水平[2]。
梳理有关发展初中学生“宏观辨识与微观探析”素养的代表性文献发现,鲜有从初中化学的整体发展脉络出发,深入研究如何分阶段、有层次地促进和发展初中生的“宏观辨识与微观探析”思维水平。有的从分子、原子视角[3-4],有的以离子或复分解反应条件教学的视角,通过实验探究、模型运用、理论建立等教学策略,运用微粒观建构概念,理解化学反应的本质,帮助学生构建微粒观[5-6]。虽有一定的效果,但在一定程度上割裂了“宏观辨识与微观探析”发展的层级,表现为碎片化、片面化,不利于发展学生的化学学科核心素养。
本文在对比、分析义务教育化学课程标准(2011版)指导下的3个版本教科书[7-9]中“宏观辨识与微观探析”知识内容的选择、编排体系和目标取向的基础上,梳理出适合发展初中学生微粒观的层级。就初中化学教学中如何落实微粒观作微观思考,欲起抛砖引玉之作用。
二、三个版本教科书中.‘分子”知识框架分析
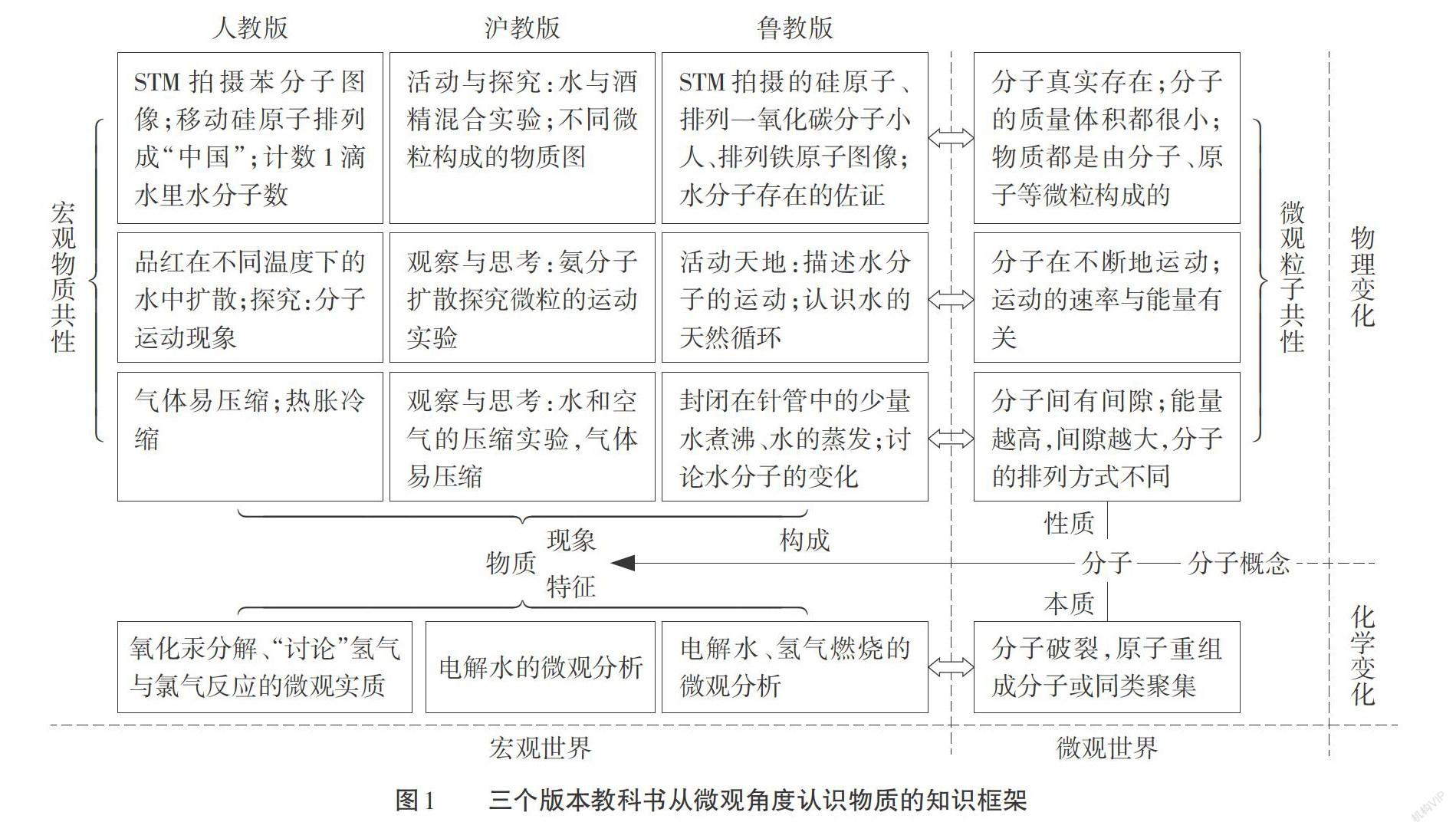
“模型”是人们对原型认识程度的一种反映,是化学学科重要的思维方法。知识具有提供核心的认识角度,形成重要的认识思路和推理路径的功能,所以才具有核心素养的发展价值,在教学中需要彰显核心概念对核心素养的发展功能[10]。义务教育化学课程标准(2011版)强调通过“品红扩散实验”“压缩空气和水”“搭建水分子、氢分子模型”“分子运动探究实验”等一系列探究活动,帮助学生初步认识辩证唯物主义的一些观点[11]。但这些探究活动,无法帮助学生依据这些现象判断微粒是分子还是原子。三个版本教科书将“分子”作为学生从微观角度认识物质性质及其变化的开始,将构成物质微观粒子的变化作为甄别物理变化和化学变化的切入点,让学生认识到不同的物质有不同的微观结构,初步搭建起从微观角度认识物质的知识框架(图1)。
三、微粒观层级构建的策略
“水的组成”从一个侧面反映了化学学习的过程,从宏观视角认识物质及其变化规律,并从微观层面解释物质及其变化本质的过程。认识分子、原子及其性质,解释日常生活中一些常见的现象,是从分子、原子的水平深入认识“纯净物和混合物、物理变化和化学变化”等的人门阶段;物质的溶解,对学生认识水溶液体系中的微粒行为,具有变革性意义,具有承上启下的作用,是形成微粒观看物质的关键时期;“质量守恒定律”“化学方程式”是学生形成以化学式、化学方程式及溶液组成等蕴含的量的关系为依据,分析构成物质的微观粒子在化学变化中“质”与“量”的关系的突破时期;金属单质与酸、可溶性盐溶液发生的“置换反应”、溶液中酸、碱、盐发生的“复分解反应”等微观本质,是学生形成微粒观的深化时期(表1)。各层级之间相互依存、螺旋式渗透,最终形成“微粒的结构影响着微粒之间相互转化的过程和方式,物质发生化学变化的过程实质上就是微粒间相互作用、相互转化的过程,微粒结构不同,作用方式、转化方式也就不同”的观念。
四、微粒观发展的实践策略
三个版本教科书都没有将“水的分解”等示意图作为模型认知层面加以利用。笔者认为教师应立足于水的微观构成,从微观视角分析问题,并建立宏观一微观之间的联系,充分体现了化学微粒观,突出了化学学科的思维特征,并启示学生学习化学既要“见微知著”,也要“见著知微”。因此,尝试利用不同的知识载体构建模型,既关注学生对知识体系的构建和高阶思维能力的发展,又注重培育学生化学学科核心素养。
1.从微观视角建构认识微粒的知识框架
“原子结构模型的演变”在培养学生“证据推理与模型认知”等素养上,具有独特的功能价值。呈现了一个不断建立模型、运用模型和修正模型的历史过程,使学生认识到模型方法对理论建构的作用、模型的发展性特征以及证据推理在其中的重要作用。因此,对于“原子的构成”的教学,可由汤姆森提出“葡萄干布丁”模型的假设为起点,引导学生像科学家那样思考问题。
卢瑟福研究放射性,找到具有一定质量的、带正电荷的α粒子作为“炮弹”并不难。金具有很好的延展性、稳定性且纯度很高,是个很好的选择。实验中,金箔的厚度只有10-4cm(1μm)。
①绝大多数α粒子能穿透金箔,不改变原来的运动方向说明了什么?
②有一小部分α粒子发生偏转,甚至有极少数的。粒子被弹了回来,说明了什么?
③描述你心目中原子及其内部是怎样的?
实验结果是卢瑟福得出原子核式模型的重要依据。这个有趣的核式模型,揭示了原子核与原子的质量、体积关系。最后,只能从电荷角度解释“偏转”:如果原子核集中了原子中的正电荷,那么电子只能在核外。从而,顺利地过渡到离子的形成和离子构成物质,使学生对构成物质的微粒有一个完整、系统的认识。
2.以水为媒介,建构原子水平上的分子模型
尝试基于水的“宏一微一符”三重表征思维,立足于水的微观构成,从微观视角分析问题,并建立宏观一微观之间的联系,充分体现化学微粒观,突出化学学科的思维特征,并启示学生学习化学既要“见微知著”,也要“见著知微”。通过观察、画模型等活动建构原子水平上的分子“模型认知”。从而,有梯度地帮助学生理解“物质一元素一微粒一化学式”四者联系的思维角度,以解构混合物与纯净物、物质与元素、物质与分子、元素与原子、分子与原子、化学反应与反应物和生成物之间的定量关系,使之形成完善的认知结构[12]。
(1)通过“水的组成”模型,建立物质的定量研究思想方法
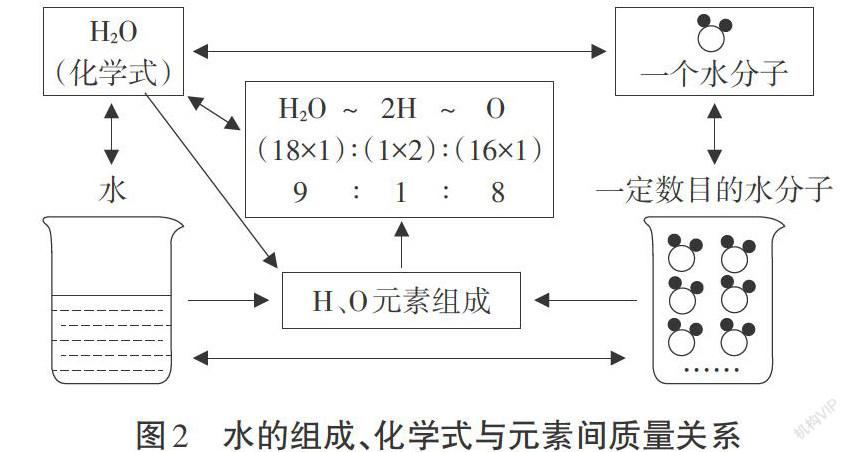
纯净物有固定的组成,可用化学式表示,组成元素的质量遵守定比定律。“水的组成与化学式、元素之间质量关系”的“模型认知”(图2),揭示了物质组成与化合价、化学式的关系;纯净物与元素、元素与元素间的定量关系,为学生建立定量研究思想方法奠定基础。
(2)通过“水的分解”模型,建构原子水平上的化学变化
从微观的视角分析水的分解(图3),发掘出分子、原子知识的生长点,强调“原子水平上的化学变化过程”。认识分子和原子在化学变化中的行为:构成物质的分子改变,变成了其他的分子;原子是构成一切物质的基本成分,不随物质种类的变化而变化,形成化学变化是有条件且伴随着能量变化的认识,引领学生探究物质的构成、组成及变化之秘,初步形成从微粒的观点看物质和物质变化的基本观念[13]。
(3)通过“水的分解”模型,揭示质量守恒定律的实质
3个版本教科书都设计了2-3个具有代表性的研究对象、实验体系验证质量守恒定律,最终再从微观分析质量守恒的原因。因此,以“水的分解”模型为例,从分子、原子水平设计驱动性问题:①参加反应的H2O与生成的H2、O2的分子数目比为多少?②计算分析参加反应的水和生成物的相对质量的变化情况?③参加反应的水和生成的氢气、氧气的质量比是多少?④若要得到16g氧气,需要电解多少水?⑤若要得到4kg氢气,又需要电解多少水?同时得到多少氧气?
使该实验的教育功能得到进一步的挖掘,既指向化学方程式的配平及原理,加深学生对化学反应中的物质、微粒变化、发生条件、微粒间定量反应关系的认识和理解,又突出学生对化学用语、化学计算的认识和理解。培养学生从化学变化中元素守恒和质量守恒的视角分析化学反应和解决化学问题的能力。
3.构建物质溶解的微观模型,发展微粒观
氯化钠在水分子的作用下,形成水合Na+和水合Cl-,并不断移动。在一定条件下,形成饱和溶液后,溶解过程并未中止,单位时间内扩散到溶剂中的溶质微粒数等于回到溶质表面的微粒数,即固体结晶与溶解之间存在动态平衡,双方速率相等。因此,将形状不规则的硫酸铜固体放入饱和的硫酸铜溶液中,溶液中的Cu2+、SO42-析出到晶体表面,晶体表面的硫酸铜又溶解到溶液中,溶解与结晶速率相等,形成动态平衡体系。因此,晶体和溶液质量虽没有改变,但晶体形状由于动态平衡完全可能发生变化。
从而,引导学生理解物质溶解的本质,形成并发展学生的微粒观、平衡观和守恒观。为进一步研究溶液中的金属与酸、某些盐溶液的反应和复分解反应问题打下认识的基础。
4.微观分析“反应类型”,深化微粒观
铁钉浸人硫酸铜溶液实验,以其反应体系有色,现象明显等特点,被3个版本教科书作为学生理解常见金属的活动性顺序、置换反应规律的重要资源。还被设计成质量守恒定律的验证实验、曾青得铁则化为铜、不能用铁制容器来配制波尔多液等问题情境。
其微观实质:Fe+Cu2+=Cu+Fe2+,实现了原子与离子相互转化(图4)。镁条与稀盐酸反应:Mg+2H+=Mg2++H2↑,实现了原子向离子、离子向原子、原子再结合成分子的转化(图5)。得出金属与酸、某些盐溶液发生置换反应的规律:金属原子失去电子给H+(位于其后的金属阳离子)变成氢气(金属单质)。
使用元素符号、化学式、化学方程式等表征复分解反应的实质,如HCl+NaOH=H2O+NaCl,说明盐酸与氢氧化钠的酸碱反应,H++OH-=H2O说明溶液中H+与OH-以1:1的数量关系形成水分子(图6)。硝酸银与稀盐酸反应实质:Ag++Cl-=AgCl↓,利用了稀盐酸的Cl-(图7)。宏观上,这2个反应都属于酸与盐的反应,但微观本质却大相径庭,H+在前者中是“主角”,在后者中则是“配角”。
微粒观指导下的“反应类型”研究,加深了学生对分子、原子和离子间相互转化关系的理解。让学生通过微观图示、解释宏观现象等具体任务探查学生对水溶液体系认识的障碍点,很好地解释了物质变化是微粒间相互作用的结果,进一步循序渐进地引导学生构建出特征离子对思维导图(图8,若缺乏从热力学层面的讨论,是容易出现科学性错误的)。既可以突破学习“反应类型”的难点,解释“CO2+2NaOH=Na2COs+H2O”为什么不属于复分解反应,又可以发展学生“宏观辨识与微观探析,,“变化观念与平衡思想”“证据推理与模型认知”等化学学科核心素养,培养系统思维能力。
五、结语
“宏一微一符”体现了化学学科最具特征的观察视角和思维方式,最终目的是希望学生通过相关的化学学习活动,能自觉利用宏微观联系的视角研究物质世界的变化,从而自觉形成的思维模型。这需要教师能关注知识间的联系,精选真实的、有意义的、有探究价值的情境设计教学任务活动,帮助学生在了解物质的多样性的基础上,从“类”的角度认识化学反应。
参考文献
[1]中华人民共和国教育部.普通高中化学课程标准(2017版)[S].北京:人民教育出版社,2018
[2][11]中华人民共和国教育部.义务教育化学课程标准(2011年版)[S].北京:北京師范天学出版社,2012
[3]于昌凤.初中化学“微粗观”建构的教学实践研究[J].化学教育,2014,35(9):23-27
[4][13]胡巢生.教科书微粗观建构方式的分析与启示[J].化学教学,2013(8):26-29
[5]程绍山.运用微粒观开发复分解反应教学价值的实践与研究[J].北学教育,2015,36(15):29-34.
[6]钱海如,赵华.初中生化学微粒观构建的实践反思[J].化.学教学,2017(5):35-40
[7]王晶,郑长龙.全日制义务教育化学九年级(上、下)[M].北京:人民教育出版社,2012
[8]王祖浩,王磊.全日制义务教育化学九年级(上、下)[M].上海:上海教育出版社,2012
[9]毕华林,卢巍.全日制义务教育化学九年级(上、下)[M].济南:山东教育出版社,2017
[10]王磊,于少华.对高中化学课程标准若干问题的理论阐释及实践解读[J].中学化学教学参考,2018(7):3-9
[12]罗月旺,李珍,杨梓生.促进初中学生定量观建构的教学设计[J].化学教学,2017(5):29-31

