FeM双金属用于甲烷催化裂解制纯氢气和碳纳米材料
钱敬侠,陈天文,刘大斌,周吕
(南京理工大学化学与化工学院,江苏 南京 210094)
近年来,对燃料能源日益增长的需求迫使人们必须寻找除化石燃料以外的可再生能源。现如今,由于大量的废弃物和COx排放,政府对环境污染物排放有着严格的规定,对污染企业有着高额的罚款。因此,开发一种可替代、环境友好型的技术来生产可再生清洁能源至关重要[1]。近几年,甲烷催化裂解(CDM)制纯氢气和副产物碳纳米材料(CNMs)的技术吸引了许多研究者[2-8]。在此吸热反应中,CDM 技术采用的是简单的一步裂解过程,如方程(1)所示[9]。

众所周知,氢气是一种清洁燃料,广泛应用于燃料电池、发动机和火箭等设备中[10]。此外,CDM的副产物CNMs可分为碳纳米管(CNTs)[11-16]、碳纳米洋葱碳(CNOs)[17-19]和碳纳米纤维(CNFs)[11,20-21]等。据报道,CNMs 具有机械强度高、耐强酸强碱、电导率高、比表面积大等优点,有望广泛应用于钢铁和碳基结构材料的制造等领域[10]。因此,CNMs 在市场上的价值可以提高CDM 的经济可行性。
甲烷由于具有较强的碳氢键(440kJ/mol)和分子结构的高对称性,是最不活跃的碳氢化合物之一。它的裂解只能在高于1200℃的条件下发生,为了降低裂解温度,金属基(Ni、Fe、Co、Pd等)[19,22-24]和碳基催化剂(活性炭、炭黑、碳纳米管等)[25-26]被用于CDM 反应中。Qian 等[10,27]通过对CDM 反应中催化剂的类型、催化剂的用量、反应器的类型、反应条件、稳定性、活性、甲烷初始和最终转化率、碳产率、氢产率和产H2成本进行分析对比。结果发现,碳基催化剂的氢产率远低于Fe 基催化剂,贵金属和Ni 基催化剂可以提高甲烷的转化率,但它们价格相对昂贵且稀有。其中,Ni基催化剂的产H2成本是Fe 基催化剂产H2成本的100 倍。因此,Fe 基催化剂用于CDM 过程是一类很有前景的催化剂。
尽管CDM 反应被很多文献报道为一类产生不含COx的纯氢气技术。但研究发现[11,28],氧化物载体(CeO2、SiO2和Al2O3) 负 载 金 属 催 化 剂 用 于CDM过程时,微量的COx会被检测到。虽然氧化物载体可以提高CDM 的催化性能,但为了消除从氧化物载体中产生的“O”,非负载的金属催化剂用于CDM反应开始被研究[29-34]。近年来,本文作者课题组研究了Fe 基催化剂用于CDM 反应[11,17,35-37],而FeM(M代表金属)双金属催化剂的组成、Fe的用量和催化剂的制备温度用于CDM 反应中的研究较少,这促使人们进一步研究FeM 双金属催化剂用于CDM反应。
本文制备了一系列的FeM(M=Mo、W、Cu)双金属催化剂,系统地研究了FeM 双金属的甲烷转化率和碳产率。进一步考察了FexMoy催化剂的不同摩尔比和焙烧温度对CDM性能的影响,CNMs的形貌也被进一步研究。
1 材料和方法
1.1 材料
Fe(NO3)3·9H2O、 H24Mo7N6O24·4H2O、 H18N2O9W和Cu(NO3)2·3H2O,AR,阿拉丁试剂(上海)有限公司;无水乙醇,AR,上海泰坦科技股份有限公司。
1.2 催化剂的制备
Fe(NO3)3·9H2O、 H24Mo7N6O24·4H2O、 H18N2O9W和Cu(NO3)2·3H2O 分别为Fe、Mo、W 和Cu 的金属前驱盐,采用熔融态的方法来制备FexMy双金属催化剂,M(M=Mo、W、Cu)为掺杂金属。例如,FexMy代表Fe 与M 金属的摩尔比是x∶y。分别取20g 的Fe(NO3)3·9H2O、17.15g 的Fe(NO3)3·9H2O 和0.5g的H24Mo7N6O24·4H2O、15.8g的Fe(NO3)3·9H2O和0.7g 的H18N2O9W、12.5g 的Fe(NO3)3·9H2O 和0.5g 的Cu(NO3)2·3H2O 于玛瑙研钵中进行研磨,直至将金属前驱盐研磨为粉末,分别将研磨好的金属前驱盐转移至不同的坩埚中,混匀;然后将不同的双金属催化剂分批于马弗炉700℃(升温速率10℃/min)的 条 件 下 焙 烧3h 来 制 备Fe、Fe15Mo1、Fe15W1和Fe15Cu1催化剂。同理,FexMoy双金属催化剂的制备过程同上,FexMoy-T代表温度T下焙烧的FexMoy双金属催化剂(本文中未特殊标明催化剂焙烧温度的,均为700℃)。
1.3 催化剂的表征
N2吸附-脱附曲线由美国麦克公司的ASAP2020 型比表面积和孔隙率分析仪测定,比表面积和吸附-脱附等温曲线是根据Brunauer-Emmett-Teller (BET) 法 和Barret-Joyner-Halenda(BJH)法计算得到,脱气温度300℃,脱气时间3h。
X 射线衍射(XRD)分析是在德国(Bruker)公司D8 Advance 型X 射线衍射仪上进行的,通过Cu靶Kα辐射,波长λ=0.15406nm,工作电压40kV,工作电流40mA,扫描范围2θ为5°~90°。
程序升温还原(H2-TPR)采用美国麦克公司的AUTO CHEM 2920型测定仪,以10℃/min的升温速率从室温程序升温至300℃干燥预处理,He气流(50mL/min)吹扫2h,冷却至50℃,通入10%H2/Ar混合气(50mL/min)0.5h 待基线稳定后,样品在50mL/min 的H2/Ar 混合还原气氛下,以10℃/min 的升温速率从室温加热到900~1000℃,样品使用量每次为50mg。
采用Thermo 公司型号为Fisher DXR 的显微拉曼光谱仪(Raman) 表征,测试波长为3000~500cm-1。
样品的元素组成及化合价态通过X射线光电子能谱仪(XPS,Thermo ESCALAB 250XI)测定。
采用美国FEI公司型号为Tecnai G2 F20的透射电镜(TEM,加速电压200kV)测定样品的微观结构。
1.4 催化剂的活性测试
甲烷催化裂解反应在固定床反应器中进行,石英管的长度为40cm,内径为2.1cm。反应温度由放置在石英管中部的热电偶控制。催化剂测试之前都未经过纯H2的预还原,催化剂被放置在以石英棉为支撑的载体上。反应尾气经冷凝除水后用气相色谱仪在线检测(热导检测器,Ar载气)。
2 结果与讨论
2.1 FeM双金属催化剂的性能
2.1.1 物理特性
表1 为Fe 和Fe15M1(M=Mo、W、Cu)样品的比表面积、孔容和孔径。从表1 可看出,与纯Fe(2.7m2/g)相比,Fe15Mo1(11.1m2/g)和Fe15W1(16.4m2/g)的比表面积增大,说明Mo 和W 金属的掺杂有利于金属颗粒的分散。Cu 金属的掺杂可能造成Fe-Cu双金属的团聚,使得Fe15Cu1的比表面积减小(0.4m2/g)。

表1 新鲜催化剂的物理特性
2.1.2 XRD
新鲜催化剂Fe 和Fe15M1(M=Mo、W、Cu)的XRD谱图如图1所示。图1中Fe2O3特征衍射峰的位置2θ主要是在24.3°、33.4°、35.8°、40.8°、43.4°、49.8°、54.5°、57.5°、62.3°、64.4°和71.9°处。这些衍射峰的位置与赤铁矿α-Fe2O3的衍射峰位置相吻合[38]。对于Fe15Mo1催化剂,在2θ为27.3°处有微弱的MoO3特征衍射峰;在22.9°处的衍射峰强度增强,代表Fe2(MoO4)3相的形成。对于Fe15W1催化剂,在2θ为18.6°处有稍强的FeWO4特征衍射峰。对于Fe15Cu1催化剂,在2θ为55.5°处有CuFe2O4相的特征衍射峰;在35.5°处有CuO 的特征衍射峰,此衍射峰与Fe2O3的衍射峰基本重合。结果表明,M 金属的掺杂改变了Fe2O3的结晶结构,从而影响Fe15M1双金属的催化性能。
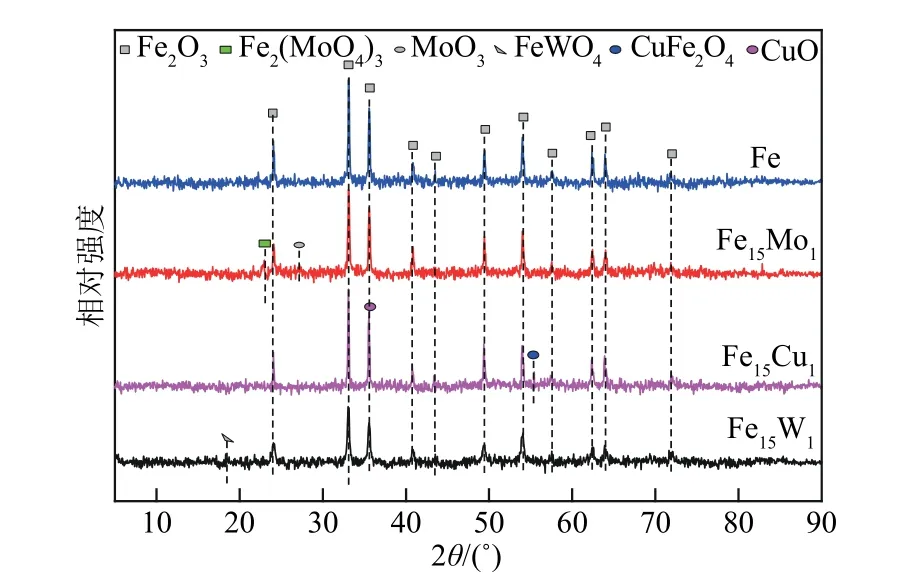
图1 新鲜催化剂的XRD图
如图2 所示,对CDM 反应后的Fe 和Fe15M1的晶体结构进行分析。在2θ为26.5°处有较强的衍射峰,代表着CDM的副产物CNMs具有石墨烯的晶体结构[29]。在2θ为44.7°处的衍射峰是Fe0/Fe3C 的晶相,此外,衍射峰在43.7°代表是Fe3C 的存在[11,39]。综上所述,反应后的催化剂均表现出Fe3C 和石墨碳的衍射峰,同时也证实了金属Fe0的存在。

图2 反应后催化剂的XRD图
2.1.3 H2-TPR
H2-TPR 的还原曲线如图3 所示,通过H2-TPR的还原曲线来研究掺杂金属M 对Fe 金属催化剂的还原特性和Fe-M 金属之间相互作用程度的影响。Fe2O3的还原过程为Fe2O3→Fe3O4→FeO→Fe0[11],分析H2-TPR 曲线发现很难区分不同相的还原峰。较低的还原温度被认为是将Fe2O3还原为Fe3O4[3Fe2O3+H2====2Fe3O4+H2O];同时,Fe3O4可能被进一步还原为FeO[Fe3O4+H2====3FeO+H2O];而部分的FeO 会部分还原为Fe0[FeO+H2====Fe0+H2O]。由图3可知,与Fe相比,Mo的掺杂使得Fe2O3的还原温度整体升高,这是由Fe2(MoO4)3相的形成造成的[40]。Cu 的加入可以有效地促进Fe2O3的还原和碳化[41],Fe15Cu1的还原温度整体降低。W的掺杂使得Fe15W1催化剂的还原温度整体升高,这是由于Fe-W之间存在更强的相互作用[42]。因而,M金属的掺杂都不同程度地改变了Fe基催化剂的氧化还原过程。

图3 新鲜催化剂的H2-TPR曲线
2.1.4 Raman光谱
CDM反应后催化剂的拉曼光谱如图4所示。在不同的催化剂中,CNMs 的拉曼光谱图中都观察到三个分辨良好的拉曼谱带。第一个拉曼光谱带位置在1337cm-1(D 带),第二个拉曼光谱带位置在1569cm-1(G 带) 和第三个拉曼光谱带位置在2683cm-1(2D 带)。1337cm-1处的D 带代表非晶态碳或石墨碳的结构缺陷[17]。然而,在图2的XRD分析中并未检测到非晶态碳,因此此处的D带是由石墨碳的缺陷造成的。1569cm-1处的G带是一种石墨层的平面内碳-碳拉伸振动[34]。2683cm-1处的2D 带来源于双原子双共振[17]。

图4 反应后催化剂的拉曼光谱图
由图4知,Fe15M1(M=Mo、W、Cu)的D带强度都显著低于Fe 的D 带强度,而G 带强度都略高于Fe 的G 带强度。金属M 掺杂到Fe 金属中使得石墨碳的结构缺陷减小。结晶度和石墨化度可以根据在不同催化剂中沉积的CNMs 的ID/IG值来进一步解释[34],CDM 反应后的Fe、Fe15Mo1、Fe15Cu1和Fe15W1催化剂的ID/IG值分别是0.95、0.81、0.62 和0.28。结果表明,M金属的掺杂使得ID/IG值降低,说明有序石墨碳的沉积效果优于缺陷碳的沉积。
2.1.5 催化剂的活性
甲烷转化率随时间的变化曲线如图5所示。在280min内,Fe15M1(M=Mo、Cu、W)的甲烷转化率均低于Fe 的甲烷转化率。Fe 的甲烷转化率最大为33%,300min之后,Fe的甲烷转化率降至5%。对于Fe15W1催化剂,虽然W的掺杂使得其比表面积增加,但Deck等[43]报道了如果金属溶碳能力非常低(在反应温度附近),则不具备催化烃类裂解的能力。因此,W作为掺杂金属不利于活性组分Fe0/Fe3C在金属W颗粒表面的富集,不利于催化活性的提高,使得Fe15W1的甲烷转化率较低(<10%)。Cu金属的掺杂使得其比表面积减小,减少了甲烷分子与活性位点Fe0/Fe3C 的接触[11],Fe15Cu1的最大甲烷转化率为11%。Mo金属的掺杂使得Fe15Mo1的比表面积增加、孔容增大、孔径减小,但FexMoy的催化性能与比表面积、孔容、孔径的相关性较小,见表2。Fe15Mo1的最大甲烷转化率为28%,在300min 内甲烷转化率下降至5%左右,说明此催化剂失活很快,稳定性较差。

图5 FeM催化剂的甲烷转化率

表2 新鲜催化剂FexMoy的物理特性
对于CDM 过程在Fe 基催化剂上反应机理的研究,已有研究者提出Fe0/Fe3C 作为催化活性位点,副产物CNMs 的沉积是在Fe0/Fe3C 上进行的,随着CNMs 沉积量的增加,导致催化剂逐渐失活[44-46]。Zhou 等[11]研究了Fe3C 的形成及其在CDM 反应过程中CNMs 沉积的作用。首先,在Fe0活性位点的表面,甲烷裂解为氢气和无定形炭;当沉积炭超过炭溶解度限制时,Fe3C通过铁原子重排形成;Fe3C作为CDM 反应的催化剂,CH4将在Fe3C 表面继续裂解,炭的继续沉积会导致Fe3C 的过饱和,从而进一步形成Fe3C1+x,而后进一步分解为Fe3C和Fe3C某个结晶区上的石墨碳。
研究者提出通过比较各催化剂最终的碳产率来评价催化性能[47],各催化剂的碳产率如图6 所示。Fe 的碳产率为4.35gC/gcat,而Fe15Mo1(2.81gC/gcat),Fe15W1(1.35gC/gcat)和Fe15Cu1(0.58gC/gcat)的碳产率均低于Fe 的碳产率。对比图5 和图6 可知,Fe、Fe15Mo1和Fe15W1的碳产率与甲烷转化率曲线相一致,而由于Fe15Cu1在高空速6L/(gcat·h)的条件下失活较快,基本没有转化率,因此,采用空速为1.8L/(gcat·h)进行CDM反应。
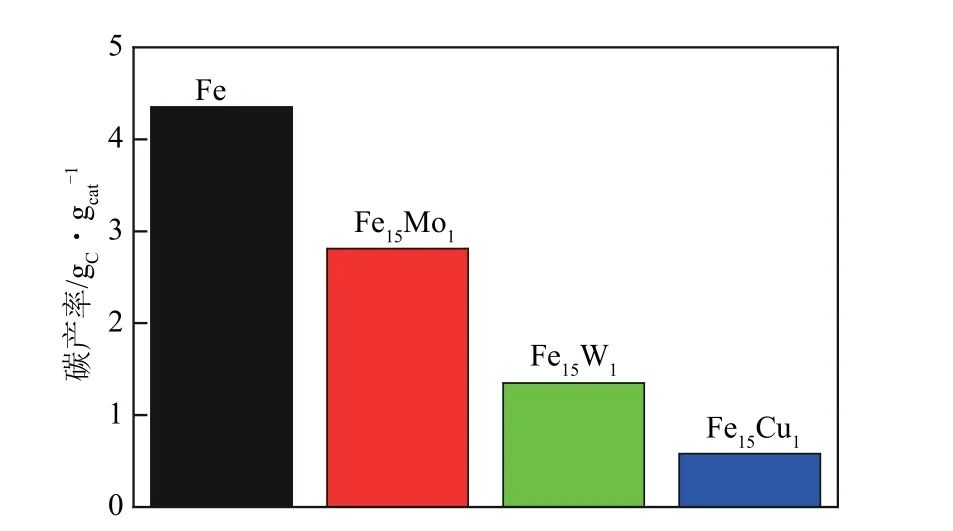
图6 FeM催化剂的碳产率
已有文献报道称Mo[48-49]作为CDM 反应活性金属(Co、Ni 和Fe)的促进剂,可提高Al2O3和MgO负载的活性金属的稳定性和分散性。因而,本文进一步探讨了无载体负载的条件下,催化剂的焙烧温度和Mo的添加量对FexMoy催化性能的影响。
2.2 FeMo双金属催化剂的性能
2.2.1 物理特性
FexMoy的比表面积、孔容和孔径如表2 所示。与Fe相比,随着Mo掺杂量的增加,比表面积和孔容先增大后减小。这是由于Mo 的少量掺杂能够促进小金属颗粒的形成[50],提高Fe2O3的分散度[51];Mo的掺杂量逐渐增加,FeMo 双金属形成Fe2(MoO4)3相(见图7),颗粒尺寸变大,比表面积和孔容减小。对比图13 和图14 发现,比表面积增加,孔容增大并未使FexMoy的催化活性提高,说明FeMo 双金属形成Fe2(MoO4)3相对催化性能的影响较大。
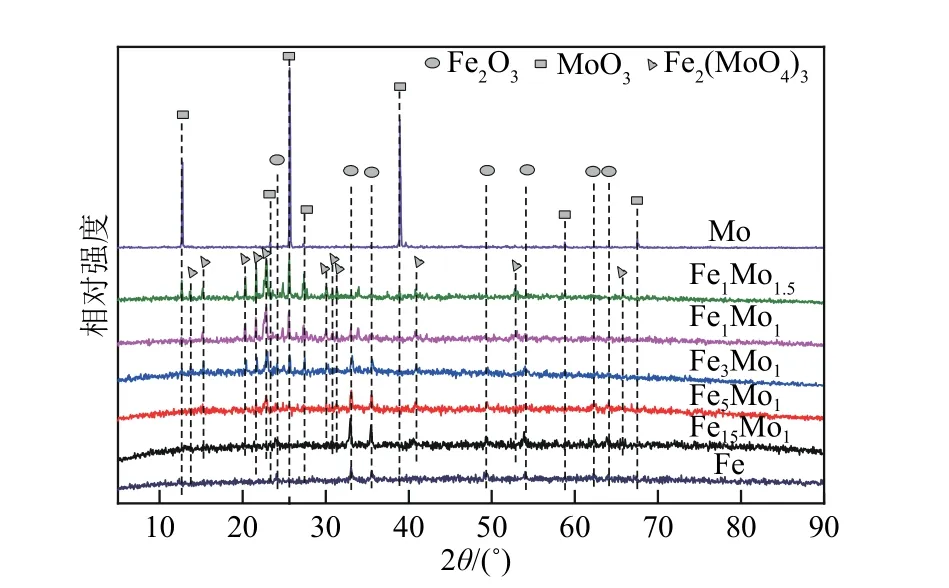
图7 新鲜催化剂FexMoy的XRD图
2.2.2 XRD
FexMoy的XRD 图谱如图7 所示,在2θ为12.7°、23.3°、25.6°、27.3°、39°、58.6°和67.5°处为MoO3的特征衍射峰。对于FexMoy催化剂,随着Mo 含量的 增 加,Fe2(MoO4)3相 在13.7°、15.4°、20.3°、21.5°、22.9°、30.1°、30.9°、31.2°、40.8°和52.9°处的衍射峰强度增强。如图8 所示,对CDM 反应后FexMoy的晶体结构进行XRD 分析。在2θ为26.5°处有较强的衍射峰,代表着CDM的副产物CNMs具有石墨烯的晶体结构[29]。在2θ为44.7°时的衍射峰是Fe0/Fe3C的晶相,此外,衍射峰在43.7°代表Fe3C的存在[11,39]。衍射峰在34.2°、37.7°、39.5°、52.3°、61.8°和69.5°处与Mo2C的衍射峰位置相吻合,代表Mo2C的存在。

图8 反应后催化剂FexMoy的XRD图
不同焙烧温度的Fe15Mo1的XRD 图谱如图9 所示,对于Fe15Mo1催化剂,随着焙烧温度的增加,样品在2θ为24.3°、33.4°、35.8°、40.8°、49.8°、54.5°、57.5°、62.3°和64.4°处衍射峰的强度在逐渐增强,说明Fe2O3的结晶度增加。

图9 不同焙烧温度的Fe15Mo1的XRD图
2.2.3 XPS
利用XPS技术对新鲜和反应后催化剂Fe1Mo1表面组分的化学状态进行研究。图10(a)是Fe1Mo1的XPS全谱图,表明催化剂是由C(参考元素)、Fe、Mo 和O 四种元素组成。Fe 2p 的高分辨XPS 能谱[图10(b)]中,711.2eV和724.3eV处两个强峰的出现归 因 于Fe2O3和Fe2(MoO4)3中Fe 2p3/2和Fe 2p1/2的Fe3+[35,52]。Fe 2p3/2峰 在719.3eV 处 有 一 个 伴 随 卫 星峰,Fe 2p1/2峰在733.0eV 处也有一个伴随卫星峰。因此,将这两个伴随卫星峰都归属于Fe3+[53]。Mo 3d的高分辨率XPS 能谱[图10(c)]中,在结合能为232.7eV 和235.8eV 处的两个峰归属于MoO3和Fe2(MoO4)3结构中Mo 3d5/2和Mo 3d3/2的Mo6+[54]。O 1s的高分辨率XPS 能谱[图10(d)]中,在529.3eV、530.3eV和530.7eV处的峰归属于晶格氧,分别代表Fe2O3、Fe2(MoO4)3和MoO3中 的 氧[55];531.7eV 处 的峰归属于表面吸附的氧[55]。这与图7 所观察到的Fe1Mo1催化剂中存在Fe2O3、Fe2(MoO4)3和MoO3的特征衍射峰相符。Fe1Mo1的XPS谱图中每种元素的质量分数分析列于表3。

图10 新鲜催化剂Fe1Mo1的XPS总谱图及Fe 2p、Mo 3d、O 1s的高分辨图谱

表3 Fe1Mo1的XPS谱图中每种元素的质量分数分析 单位:%
图11(a)是反应后催化剂Fe1Mo1的XPS 全谱图,谱图显示除了一个较低的O 1s 的峰外,只有一个较强的C 1s 的峰,并未出现Fe 和Mo 元素的峰。图11(b)为C 1s的高分辨率XPS能谱,在284.9eV处归属于CDM 反应后副产物CNMs 的峰。结果表明,CDM 反应后,石墨烯中碳的含量很高,大部分Fe1Mo1被副产物CNMs 包裹。因而,在催化剂的表面并未检测到Fe和Mo元素。

图11 反应后催化剂Fe1Mo1的XPS总谱图及C 1s的高分辨图谱
2.2.4 TEM
CDM 反应后的Fe1Mo1催化剂的TEM 如图12 所示。图12 中CNMs 的结构基本都是竹节状的CNTs[图12(a)~(c)]。CDM 的副产物CNMs 的形貌与CNMs在催化剂上的生长机理密切相关。一般情况下,在Fe 催化剂上持续的CDM 反应会使副产物CNMs 析出并在催化剂颗粒表面形成柱状网络结晶,最终生长成管状结构即CNTs。同时,在Fe1Mo1中也可以大量形成一侧为Fe3C 的特殊CNTs,称为竹节状的CNTs[11]。此外,Lu等[56]推断催化剂颗粒在一定的时间间隔从石墨鞘中“跳跃”到CNTs 管顶,解释了在管端具有催化剂颗粒的竹节状CNTs的形成。

图12 反应后催化剂Fe1Mo1碳纳米管的TEM图
2.2.5 催化活性的影响因素
如图13所示,考察了Mo的添加量对甲烷转化率的影响。随着Mo 添加量的增加,催化性能逐渐提高。当Mo 的添加量增加至n(Fe)∶n(Mo)=1∶1时,甲烷的转化率最大为22%且在350min 内下降到17%;当Mo 的添加量继续增加至n(Fe)∶n(Mo)=1∶1.5 时,甲烷的转化率最大为24%且在350min内下降到10%,由此可知催化剂的稳定性下降。综上分析,当n(Fe)∶n(Mo)=1∶1 时,催化剂的活性和稳定性为最佳。如图14所示,列出了Mo的不同添加量对碳产率的影响。随着Mo 添加量的增加,碳产率逐渐增加。当n(Fe)∶n(Mo)=1∶1 时,碳产率达到最大6gC/gcat,高于Fe的碳产率4.35gC/gcat。

图13 Mo的添加量对甲烷转化率的影响

图14 FexMoy催化剂的碳产率
Mo 不同比例的掺杂之所以会影响甲烷转化率和碳产率,是由于随着Mo掺杂量的增加,FeMo双金属形成Fe2(MoO4)3相[见图7,Fe2(MoO4)3相的形成可提高催化剂的稳定性],而当Mo的掺杂量超过一定值后[n(Fe)∶n(Mo)=1∶1],过量的Mo 形成Mo2C,见图8。部分Mo 原子取代Fe 原子,催化活性位点Fe0/Fe3C 减少(见图8),催化活性降低,碳产率减少。
此外,进一步考察了催化剂的焙烧温度(500~800℃)对催化性能的影响。对于Fe15Mo1,随着焙烧温度的升高,Fe-Mo之间的相互作用增强,Fe2O3的结晶度增加(见图9),结晶度的增加可以有效避免催化剂产生大面积的团聚现象,从而有助于提高其催化活性[57]。因此,如图15 所示,500℃(1.97gC/gcat)和600℃(2gC/gcat)焙烧的催化剂碳产率均低于700℃焙烧的催化剂碳产率(2.81gC/gcat)。对于Fe1Mo1,随着焙烧温度增加至800℃,高温导致金属烧结[42],降低了Fe1Mo1-800℃的催化活性。因而,700℃焙烧的催化剂碳产率(6gC/gcat)高于800℃焙烧的催化剂碳产率(5.7gC/gcat)。综上分析,700℃为最佳焙烧温度。

图15 焙烧温度对碳产率的影响
3 结论
(1)本文采用熔融态的方法制备了一系列的FexMy(M=Mo、Cu、W)双金属催化剂,同时,进一步考察了FexMy的催化活性和稳定性。系统地对比了Fe15M1(M=Mo、Cu、W)双金属与Fe 的CDM催化性能。结果表明,Fe15Mo1(2.81gC/gcat)、Fe15W1(1.35gC/gcat)和Fe15Cu1(0.58gC/gcat)的碳产率均低于Fe(4.35gC/gcat)的碳产率。
(2)在T=900℃、GHSV=6L/(gcat·h)、100mL/min纯甲烷的反应条件下,进一步考察了不同Mo 的掺杂量催化剂(Fe、Fe15Mo1、Fe5Mo1、Fe3Mo1、Fe1Mo1和Fe1Mo1.5)和催化剂的焙烧温度(500℃、600℃、700℃和800℃)对FexMoy双金属的CDM 催化性能的影响。结果发现,700℃焙烧的Fe1Mo1催化剂具有优异的催化活性和稳定性,Fe1Mo1的碳产率(6gC/gcat)高于Fe 的碳产率(4.35gC/gcat)。这是由于Fe1Mo1双金属形成Fe2(MoO4)3合金,进一步提高了CDM的催化活性和稳定性。
(3) TEM 结 果表明,以Fe1Mo1为催化 剂,CDM 反应后的副产物CNMs 为竹节状的CNTs。这为CDM 制纯氢气过程作为一种低成本技术应用于小型或中型的加氢站提供了重要的参考价值。同时,为副产物CNMs创造新的市场机会以寻求基于CNMs行业的诞生提供研究基础。

