磷酸铁锂正极材料改性研究进展
冯晓晗,孙 杰,,何健豪,魏义华,周成冈,孙睿敏
(1中国地质大学材料与化学学院,湖北 武汉 430070;2湖北融通高科先进材料有限公司,湖北 大冶 435100)
世界面临的能源与环境问题日益严峻,人们力求寻找出可替代传统能源的新能源[1]。锂离子电池作为二次电池,自1991 年商业化以来,迅速发展为新能源领域的主流储能器件,可望广泛应用于风力、水力、太阳能发电站系统,军事装备和航天航空等[2]。电化学储能器件的应用也改善了人类的生活方式,促进了低碳社会的建设,加速了电动汽车的发展[3]。随着新能源产业的大力发展,对电池器件的循环稳定性、高倍率性能、能量密度等电化学性能提出了更高的要求[4],商业化锂离子电池等储能器件的存储性能依旧存在改进空间。正极材料是影响锂离子电池电化学性能的重要因素之一[5]。目前,锂离子电池中含锂的正极材料主要分为以下几类:①具有三维锂离子扩散通道的尖晶石结构LiMn2O4、LiNiMnO4材料等[6];②具有二维锂离子扩散通道的层状结构LiNiO2、LiCoO2材料、三元材料及高容量富锂材料等[7];③具有一维锂离子扩散通道的聚阴离子型化合物LiFePO4、Li3V2(PO4)3、LiVPO4F 材料等[8]。在上述正极材料中,LiFePO4是最先进行商业化生产、应用最为广泛的锂离子电池正极材料。自1997年Goodenough对LiFePO4正极材料研究以来,众多研究者对LiFePO4材料的合成、应用以及改性策略开展了深入广泛的探究。
LiFePO4具有规则的橄榄石型结构,Pnma空间群,其晶格常数a=1.0329 nm,b=0.6011 nm,c=0.4699 nm。在LiFePO4的晶体结构中,O 原子呈略微扭曲的六方形紧密堆积,P占据O四面体的4c位,形成PO4四面体。Fe 和Li 分别占据O 八面体的4c和4a位,形成FeO6和LiO6八面体(图1)[4]。Li+在4a位置形成共边的直链并与b轴平行,使得Li+在充放电过程中可以自由脱嵌。PO4晶体中P—O强共价键使得该结构具有很强的热力学和动力学稳定性,充放电过程中Li+的脱嵌不会引起材料体积的急剧收缩或膨胀。LiFePO4正极材料的理论比容量为170 mA·h/g,拥有3.5 V的电压平台,充放电循环性能良好。在充电过程中,LiFePO4相转变为FePO4相,放电过程与之可逆,由FePO4相转变为LiFePO4相。尽管在充放电过程中存在明显的相分离趋势,但它仍能进行高倍率充放电。经研究表明,这主要是因为相变过程中会有亚稳相的存在,亚稳相更有利于Li+的传输[9]。

图1 以Li+一维扩散通道为视角的LiFePO4的晶体结构[4]Fig.1 Crystal structure of LiFePO4 along perspective of 1D diffusion channels of Li ions[4]
LiFePO4受其自身晶体结构限制,导电性差和离子迁移速率缓慢,这大大限制了其电化学性能的提升。由于LiFePO4本身的离子扩散速率低,低温状态下,Li+在活性电极材料内部的扩散能力下降更为明显,电荷转移阻抗增大。在温度低于零度的环境中,LiFePO4电池能量密度下降,混合动力电动汽车的全电驱动范围大幅下降,缩短了电池寿命,增加了混合动力电池的运行成本[10]。基于上述问题,本文详细介绍了LiFePO4材料目前面临的挑战,系统综述了近年来LiFePO4的最新改性策略,主要包含离子掺杂、表面改性、补锂材料的添加3个方面(图2),并总结了目前研究存在的问题以及未来发展前景,旨在为未来锂离子电池LiFePO4正极材料的进一步设计与优化提供助力。

图2 近年来LiFePO4改性策略Fig.2 LiFePO4 modification strategy in recent years
1 LiFePO4面临的挑战
LiFePO4材料充放电平台稳定、比容量高、安全性好、自放电少、成本低、对环境无污染。在LiFePO4晶格中,电子是通过过渡金属层进行传输的。但是,PO4四面体中的O 将FeO6八面体分开,每个FeO6八面体只由1个公共顶点连接,导致晶胞中无法形成连续过渡金属层网络。因此,LiFePO4材料的电子电导率低,室温下电子电导率约为10-9~10-10S/cm,远低于LiCoO2(约10-3S/cm)和LiMn2O4(约2×10-5~5×10-5S/cm)[11]。与此同时,晶胞体积的变化受限于八面体间拥有强共价键的PO4四面体结构,Li+的传输受阻,导致LiFePO4的离子扩散率较低。Li+在LiFePO4和FePO4两相晶格中的理论扩散系数较低,这些因素导致LiFePO4倍率性能较差。目前研究者主要通过碳包覆、离子掺杂和纳米化等方法来提高材料的导电性和锂离子扩散速率,进而提高材料的倍率性能[7]。
LiFePO4正极材料面临的另一个巨大挑战是材料的低温性能相对较差。低温环境下LiFePO4电池具有放电容量低、放电电压平台下降、倍率性能差和容量衰减快等特点。Ji 等[12]认为,锂离子电池在低温下的不良性能与以下因素有关:电解液黏度增大、电极材料导电性差、Li+扩散速率慢、低温下负极容易析出锂以及与电解液反应导致SEI 膜厚度增加。低温环境下,正极材料活性降低,带电离子的扩散速率变差,可以进行充放电的锂离子数量减少[13]。Yan 等[14]首先在实验室用原位X 射线衍射(in-situXRD)研究了LiFePO4在不同温度范围中充放电过程中的结构动力学,并观察到高分辨中间相的形成。实验允许在253~313 K 的温度范围内探测材料电化学反应过程中的物相结构变化,并且在相对低的温度下捕获了LiFePO4电化学过程中间相。作者进一步提出了中间相的形成机理,即由于低温下离子转移速率受限和LiFePO4/FePO4界面的超电势积累,中间相的存在可以加快磷酸铁锂在低温环境下的扩散动力学(图3)。Wu等[15]研究了在低温条件下(-10 ℃和-20 ℃)不同倍率充电循环的老化实验,利用单一变量分析法分析了LiFePO4电池的老化过程,总结了充电倍率大小对低温性能的影响。低温下正极材料中锂离子含量急剧下降,容量衰减过快,分析原因是部分锂离子并没有嵌入石墨负极晶格内部,而是在负极形成镀锂层,枝晶生长严重。

图3 (a)~(c)LiFePO4在253~313 K温度下1.4 mV/s、2.8 mV/s和4.2 mV/s不同扫描速率下的循环伏安曲线;(d)~(f)(111)、(211)、(020)、(311)和(121)晶面在1.4 mV/s、2.8 mV/s和4.2 mV/s扫速下的X射线衍射图像(XRD),相应的电流曲线绘制在右侧;(g)~(I)在1.4 mV/s、2.8 mV/s和4.2 mV/s扫速下的XRD图[14]Fig.3 (a)~(c)CV curves of LiFePO4 under different scan rates of 1.4 mV/s,2.8 mV/s,and 4.2 mV/s at temperature ranging from 253~313 K;(d)~(f)image plot of diffraction patterns for(111),(211),(020),(311),and(121)reflections during two CV cycles under different scan rates of 1.4 mV/s,2.8 mV/s,and 4.2 mV/s at a temperature of 293 K,corresponding current curves are plotted to right;LFP represent for LiFePO4;(g)~(i)selected individual diffraction patterns for two CV cycles at 1.4 mV/s,2.8 mV/s,and 4.2 mV/s[14]
2 LiFePO4改性方法
由于LiFePO4存在离子扩散速率低、导电性能差的问题,对LiFePO4的倍率性能和低温性能造成很大影响。因此,如何提高材料的离子扩散速率和导电性,从而进一步有效提高倍率性能和低温性能一直是研究人员关注的热点,对LiFePO4的改性研究也取得了丰硕的成果。本文主要总结了研究者们通过体相掺杂、包覆和正极补锂的方法提高LiFePO4电化学性能的相关研究进展。
2.1 元素掺杂改性
元素掺杂被认为是提高LiFePO4材料内部电子电导率和离子扩散率的重要方法。在Li 位、Fe 位或其他位点用少量杂离子/元素进行掺杂,有望提高大电流密度下LiFePO4材料的充放电性能。金属元素的掺杂可以增加LiFePO4的晶格缺陷,有利于提高Li+的扩散速率和颗粒的内部电导率,内在机理如下:①适量的离子掺杂扩大Li+沿b轴的一维扩散通道;②掺杂引起晶格畸变,减小Li-O键能,提高锂离子传输速率;③掺杂增加Li空位浓度,有利于Li+在材料内部的脱嵌;④掺杂降低LiFePO4和FePO4两相的带隙宽度,提高电子电导率;⑤掺杂抑制反位缺陷的形成,减少缺陷对Li+扩散的阻碍。掺杂位点的不同,掺杂元素的选择也会有差异。一般来说,两种离子的半径越接近,越容易相互取代。另外,掺杂离子的价态越高,越有利于掺杂后在晶格中形成更多的缺陷,这对促进材料的导电性和锂离子在材料中的扩散速率起到非常重要的积极作用。
2.1.1 Li位掺杂
Li 位掺杂通常采用一些半径较小的金属离子,如Zr、Cr、Nb、Mg、Na等。Chung等[16]首次报道了Li 位掺杂Ti、Al、Mg 等元素,多价态正离子的掺杂会产生正离子缺陷,Fe3+/Fe2+浓度增加,混合价态促进了P型半导体的形成,从而将磷酸铁锂的电子电导率提高到10-2S/cm,提高了约108倍。
许多研究工作报道Li位掺杂的离子可能会阻断Li+扩散通道,掺杂离子不会完全掺杂在LiFePO4的晶格中,未进入晶格的阳离子会阻断Li+在通道中的扩散,并不利于提高材料的电化学性能。但是也有研究表明Li位掺杂能够减小LiFePO4/FePO4两相混相带隙的宽度。尽管部分离子掺杂会阻断Li+在通道中的扩散,但是总体而言,适宜的Li位掺杂还是有利于LiFePO4材料电化学性能的提升。Liu等[17]利用溶剂热法合成了Li1-xNaxFePO4(x=0、0.01 和0.05)复合正极材料。Na掺杂对材料颗粒形貌影响不大。电化学数据表明,适量的Na 掺杂可以改善电化学性能。Li0.99Na0.01FePO4表现出优异的倍率性能和循环稳定性,在10 C 的电流密度下初始放电比容量为80.9 mA·h/g,循环500 圈后,其容量保持率为86.7%。这主要是由于Na 掺杂扩大了LiFePO4的晶胞参数,增强了电子电导率和锂离子扩散速率,增强了脱嵌Li+的可逆性,缓解了LiFePO4晶格结构内部的畸变,提高材料的循环性能。Darr 等[18]报道,Nb 掺杂可以导致材料晶格扭曲,进一步产生更多的Li空位,Li+传输速率增加。LiFePO4材料的循环性能和倍率性能随着Nb掺杂量的增加而提升,掺杂后的样品在10 C时拥有高达96.7 mA·h/g的放电比容量,循环200 圈后容量保持率为96.7 mA·h/g。少量Nb 掺杂可以缩短LiFePO4晶胞中的b轴长度,缩短锂离子的扩散路径,增加LiFePO4中平行于[010]方向的晶面之间的距离,使锂离子沿[010]方向一维扩散通道变宽,促进锂离子扩散。Kulka等[19]合成了Li1-3xAlxFePO4材料,中子衍射数据表明,Al很好地掺杂在LiFePO4的Li位,但是并不会阻碍Li+的传输。电化学性能测试表明,掺杂后的LiFePO4电化学性能有所改善,推测可能是Al掺杂后Li空位浓度增加引起的性能提升。
研究者们根据第一性原理并结合材料结构对大量的金属离子掺杂进行了尝试,部分离子掺杂在Li位能够导致晶格缺陷的产生,增加Li空位浓度,促进Li+在LiFePO4一维扩散通道中的传输。根据第一性原理研究发现,在Li位掺杂原子半径较小的高价金属离子,可以增加LiFePO4中的空穴迁移率,使其完成从本征半导体向非本征P 型半导体的过渡,从而实现电导率的提高,进一步提升了材料的电化学性能。但是从传统观点来看,在Li 位进行掺杂,如果掺杂元素未能完全进入材料的晶格内部,很容易阻碍锂离子的传输通道,造成倍率性能过差,比如早期文献中报道的Cr元素掺杂,对材料反而有不利影响。Li位掺杂元素的选取及掺杂含量以及元素是否能掺杂进Li位,最好通过理论计算进行预判。
2.1.2 Fe位掺杂
在Fe位掺杂金属元素,常见的掺杂元素有Mg、Mo、Co、V、Mn、Ni、Zn、Cu、Cr 等,Fe 位掺杂通常会削弱Li—O键,增加晶格体积,获得更高的离子迁移率和扩散系数,降低磷酸铁锂晶格畸变,同时Fe 位掺杂可以抑制Li/Fe 反位缺陷的产生。Li/Fe反位缺陷是指Li和Fe的混合排列。抑制Li/Fe 反位缺陷的产生,扩散通道中的Li+容易迁移而不被堵塞。因此Fe 位元素掺杂可拓宽Li+传输通道并且抑制Li/Fe 反位缺陷,这些均有助于电化学性能的提高[20]。
据报道,Mg掺杂首先占据Fe位,可有效防止Li/Fe反位缺陷的产生。Goonetilleke 等[21]用中子粉末衍射谱仪研究了非平衡条件充放电过程中Mg 掺杂LiFePO4的结构演变,发现Mg2+位于LiFePO4结构中的Fe 位点,并且不会阻碍电化学过程中Li+的脱嵌,当LiFePO4通过掺杂等价阳离子(如Zn2+、Cu2+、Mg2+、Co2+等)进行改性时,掺杂离子容易取代Fe2+而引起晶格畸变,拓宽了锂离子传输通道,从而提高了LiFePO4的电化学性能。Lee 等[22]探究了Mn掺杂对LiFePO4电化学性能的影响,少量Mn掺杂能够提高材料的电化学性能,但是掺杂量过多会产生Li/Fe 反位缺陷,甚至破坏材料结构。与纯LiFePO4相比,LiFe0.77Mn0.23PO4的平均电压和放电比容量增加,主要原因是Mn3+/2+具有氧化还原活性。Mn 掺杂样品的首圈充放电比容量和倍率性能均明显优于纯LiFePO4样品(图4)。但是在不同温度下的充放电测试发现,掺杂并没有明显提升材料的低温电化学性能。虽然掺杂Mn 元素的LiFePO4具有更好的导电性,但其结构稳定性相对较差,随着Mn 掺杂量的增加,高自旋Mn3+的形成会使正极材料的结构发生扭曲,阻碍锂离子的扩散,延缓LiFePO4的电荷转移过程。此外,随着反应的进行,Mn2+的溶解会改变正极材料的结构,降低放电容量[23]。

图4 (a)LiFePO4和(b)LiFe0.77Mn0.23PO4样品的SEM图;(c)首圈充放电曲线图;(d)倍率性能图;(e)LiFePO4 and和LiFe0.77Mn0.23PO4的阻抗图[22]Fig.4 SEM images for synthesized(a)LiFePO4 and(b)LiFe0.77Mn0.23PO4 particles;(c)first cycle charge/discharge profile,(d)cycled capacity at various charge/discharge rates,and(e)electrochemical impedance spectra for LiFePO4 and LiFe0.77Mn0.23PO4[22]
Zhang等[24]进行了Mo掺杂LiFe1-xMoxPO4/C材料的研究。XRD 结果显示,Mo 的掺杂并没有改变LiFePO4/C的橄榄石结构,但也形成了Li+空位,有助于提高Li+的扩散率。实验结果进一步表明,在Mo掺杂样品中,LiFe0.98Mo0.02PO4/C 的循环和倍率性能最高。在0.1 C电流密度下循环100圈后,其放电比容量达到143.2 mA·h/g,比纯LiFePO4/C 提高了约10 mA·h/g。当倍率达到5 C 时,LiFe0.98Mo0.02PO4/C的放电比容量仍能保持在90 mA·h/g 以上,循环100圈后容量保持率为93.2%,比未改性的LiFePO4/C容量提高了8 mA·h/g。Mo 掺杂是提高LiFePO4材料电化学性能的有效方法。Johnson 等[25]合成了LiFe0.95V0.05PO4正极材料,结合X 射线吸收光谱分析和密度泛函数理论(DFT)计算,结果显示V元素在LiFePO4结构中同时取代了部分P位和Fe位,促进了Li+空位的产生和晶体结构的变化,从而增大了Li+扩散速率。其放电比容量在同类文献中名列前茅,在1500 mA/g的电流密度下放电容量达到119 mA·h/g。Kim 等[26]利用固相反应在700 ℃下向LiFePO4中掺入Ti 元素,制备了目标产物LiTi0.08Fe0.92PO4材料。用少量Ti4+离子取代Fe2+离子,材料属于P 型半导体,其导电性增强,最终提高了材料的电化学性能。该LiTi0.08Fe0.92PO4具有较高的充放电比容量和良好的容量保持率,在0.2 C的电流密度下初始放电比容量为160 mA·h/g,50次循环后容量损失小于2%。该材料11.4 C倍率下的放电比容量为110 mA·h/g,倍率性能良好。
综上所述,在Fe 位选取合适的离子掺杂能够显著提高LiFePO4的电化学性能,比如等价离子Mg2+和多价离子V5+。等价金属离子Mg2+掺杂可有效防止Li/Fe 反位缺陷的产生同时拓宽锂离子传输通道;多价金属离子V5+掺杂在Fe 位,形成P 型半导体,能够增强材料晶格内部的导电性。但是掺杂过量会对材料有负面影响,比如Mn2+掺杂过量会产生Li/Fe 反位缺陷,姜泰勒畸变严重,Mn2+的溶解会改变正极材料结构等,阻碍锂离子传输。因此,选择合适的掺杂离子并确定最佳掺杂量尤为重要。
2.1.3 其他位置的掺杂
此外,有学者研究了O位阴离子掺杂对LiFePO4正极材料电化学性能的影响。Okada等[27]成功制备了直径约100 nm的S元素掺杂LiFePO4纳米颗粒。研究表明S 掺杂可以有效抑制Li/Fe 反位缺陷的产生。随着硫含量的增加,材料晶胞参数a和b增加了约0.2%,晶胞参数c几乎没有变化,显示Li+传输通道被拓宽。同时电化学性能测试表明,S掺杂LiFePO4的倍率性能得到显著提升,在10 C的电流密度下,初始放电比容量可达到112.7 mA·h/g。近几年Liu等[28]研究了Cl元素掺杂的LiFePO4材料。由于Cl的电负性很大,随着掺杂量的增加,Li—O键之间的距离增大,锂离子更容易脱嵌,同时P—O键之间的距离缩短,使结构更加稳定,材料中锂离子的扩散也得到了改善。0.1 C 倍率下的放电比容量为164.1 mA·h/g;10 C 倍率下的初始放电比容量为105.3 mA·h/g,循环500 圈后容量保持率为91.5%。测试表征也证明了Cl 掺杂可以有效调变LiFePO4的微观结构,提高其结构稳定性,改善材料倍率性能和循环性能(图5)。Gao 等[29]对LiFePO4-xFx/C进行了研究,报道了F元素掺杂会在一定程度上改变晶格参数,增加晶胞体积,改变原子间距,促进原生颗粒的生长。由于F 的诱导作用,磷酸盐基团的电子云重新排布,从而影响材料导电性和电化学性能。F 掺杂可以改善LiFePO4材料的固有缺点,增强电子传导速率,增大锂离子的扩散系数,提高结构稳定性。0.1 C 倍率下的放电比容量为165.7 mA·h/g,1 C倍率下的放电比容量为161.1 mA·h/g,30 C 高倍率下的放电比容量为115.7 mA·h/g(图5)。
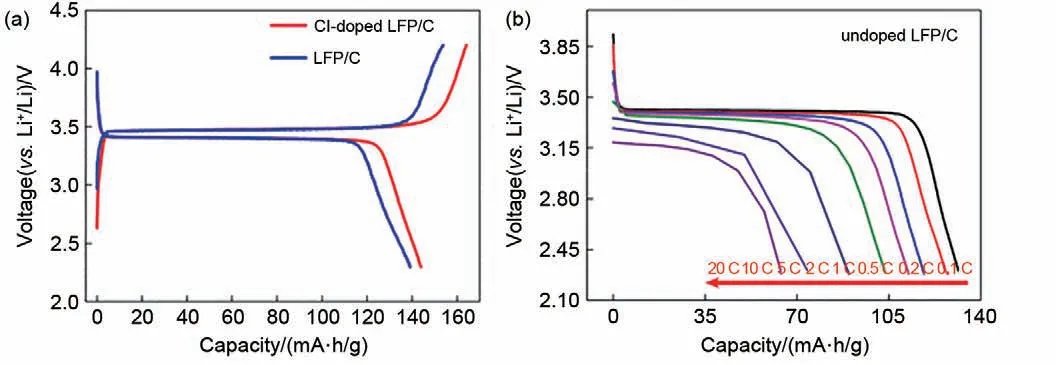

图5 (a)Cl-LFP/C和LFP/C电极材料在0.1 C时的首圈充放电曲线;(b)LFP/C;(c)Cl-LFP/C在不同电流密度下的放电曲线;(d)Cl-LFP/C正极材料和LFP/C正极材料的倍率性能;(e)Cl-LFP/C和LFP/C正极材料分别在0.1 C和10 C电流密度下的循环性能[28];(f)未掺杂和掺杂F的LiFePO4/C样品在0.1 C倍率下的初始充放电曲线;(g)LiFePO4/C和LiFePO4-xFx/C(x=0.15)样品在0.1 C倍率下的初始充/放电曲线;(h)未掺杂和掺杂F的LiFePO4/C样品的倍率和循环性能;(i)LiFePO4-xFx/C(x=0.15)样品在20 C、30 C高倍率下的循环性能[29]Fig.5 (a)First charge/discharge curves of Cl-doped LFP/C and LFP/C electrodes at 0.1 C;discharge curves of different current density:(b)LFP/C;(c)Cl-doped LFP/C;(d)rate ability of LFP/C and Cl-doped LFP/C;(e)cycling performance of Cl-doped LFP/C and LFP/C at 0.1 C and 10 C,respectively[28];(f)initial charge/discharge curves of undoped and F-doped LiFePO4/C samples at 0.1 C rate;(g)initial charge/discharge curves of LiFePO4/C and LiFePO4-xFx/C(x=0.15)samples at 0.1C rate,(h)rate and cycle performances of undoped and F-doped LiFePO4/C samples;i)cycle performances of LiFePO4-xFx/C(x=0.15)sample at high-rate 20 C,30 C[29]
非金属元素掺杂在O位往往稳定了LiFePO4的内部结构,且不会阻塞Li+传输通道,主要提高了LiFePO4材料的倍率性能。其中Cl元素掺杂能够削弱Li—O 键,此外P—O 键之间的距离缩短,使得材料结构更加稳定,掺杂效果最佳。
2.1.4 双元素掺杂
双元素掺杂LiFePO4提高材料电化学性能的研究主要以两种金属元素的掺杂为主,通常研究最多是的Li位点掺杂和Fe位点掺杂。
Tu 等[30]采用喷雾干燥法制备了Mg 和Ti共掺杂的LiFePO4(MT-LFP),显示出良好的电化学性能。MT-LFP材料是由尺寸为100 nm纳米颗粒堆积而成的微米颗粒,微米颗粒直径为2~10 μm,该材料的倍率性能良好,在0.2 C、0.5 C、1 C、3 C、5 C和8 C的倍率下,放电比容量分别为161.5、160.3、156.7、147.5、139.8和131.5 mA·h/g(图6)。

图6 (a)喷雾干燥法制备MT-LFP材料流程图;(b),(c)纯LFP的SEM的图;(d),(e)MT-LFP的SEM图;(f)LFP和MT-LFP的氮气吸脱附曲线;(g)LFP和MT-LFP样品的孔径分布曲线;(h),(i)LFP和MT-LFP在不同倍率下的充放电曲线;(j)LFP和MT-LFP在不同电流密度下的倍率性能;LFP和MT-LFP正极在(k)0.5 C、(l)1 C和(m)5 C倍率下的循环性能[30]Fig.6 (a)Schematic illustration of te synthesis process of MT-LFP materials;SEM images of the as-prepared undoped LFP(b)and(c);MT-LFP(d)and(e);Nitrogen adsorption(closed symbols)-desorption(open symbols)isotherms(f);pore diameter distribution curves(g)of as-prepared undoped LFP and MT-LFP samples;(h)charge-discharge curves of LFP and(i)MT-LFP at different rates;(j)rate capabilities of LFP and MT-LFP at various rates;cycling performance of LFP and MT-LFP cathodes at a charge/discharge rate of 0.5 C(k),1 C(l),and 5C(m)[30]
Gao 等[31]通过第一原理计算研究了Zr、Co 双元素共掺LiFePO4的机理,结果表明Zr、Co 共掺杂可以降低LiFePO4的能带间隙和Li+扩散能垒,提高Li+扩散系数。其中Li0.99Zr0.0025Fe0.99Co0.01PO4材料表现出最佳的倍率性能和循环稳定性。在0.1 C 倍率下,50 次循环后放电比容量为139.9 mA·h/g,容量保持率为85%。Yuan等[32]研究了Mn和Ni共掺杂对LiFePO4材料电化学性能的影响,掺杂改性后的材料表现出很好的电化学性能。值得一提的是,由于Mn2+(0.060 nm)比Fe2+(0.074 nm)半径小,电极材料晶胞体积随着Mn 掺杂量的增加而减小。LiNi0.02Mn0.03Fe0.95PO4/C 极化更小,表现出优异的循环稳定性,在1 C 电流密度初始放电比容量为146 mA·h/g,100圈循环后下容量保持率高达98.7%。
在改善LiFePO4电化学性能方面,阴阳离子共掺杂的改性也有少量工作。Li等[33]研究了Fe位掺杂V 元素和O 位掺杂F 元素对LiFePO4(LFP-VF)电化学性能的影响。电化学性能测试结果表明,LFP-VF具有较高的放电比容量、良好的倍率性能和循环稳定性。原因如下:一方面,F掺杂在O位,降低了Li—O 键的键能,从而为Li+传输提供了更宽的通道。另一方面,V 掺杂在Fe 位,可以通过形成Li空位实现电荷平衡。Li空位的形成可以加快离子传输速率,提高Li+的传输速率,降低Li+在传输过程中的阻力。Wang 等[34]采用高温固相法成功合成了Y 和F 元素共掺杂的LiFePO4材料。掺杂F 会引起PO43-电子云的重排,而掺杂Y会引入Li+空位,从而降低Li离子扩散阻力。此外,XRD结构精修结果表明,Y和F掺杂导致Li—O键弱化,同时也拓宽了锂离子扩散通道,从而提高了锂离子扩散速率。因此,改性后的样品在10 C高倍率下,拥有135.8 mA·h/g的超高放电比容量,5 C 倍率下的放电比容量高达148.6 mA·h/g,并且循环700圈后容量几乎无衰减。
2.1.5 多元素共掺杂
多离子共掺杂主要是在LiFePO4结构中掺入两种以上的金属元素,综合各掺杂金属离子的优点来提高电化学性能。
Liu等[35]合成了Ni、Co、Mn共掺杂的LiFePO4,材料表现出良好的结晶度。在LiFePO4的结构中,Ni、Co、Mn 都取代了Fe 位,三元素掺杂后的LiFePO4电荷转移电阻降低,电化学性能得到很大提升。Zhang等[36]研究了Mg、Zn、Mn和Al多元素掺杂的LiFePO4材料,这些元素均掺杂在Fe位。掺杂后的材料具有较高的结晶度,粒径小于100 nm。在电流密度为15、75、150、300和750 mA/g下,放电比容量分别为157、154、143、127g和118 mA·h/g,表现出优异的倍率性能。
总而言之,元素掺杂改性能够提高LiFePO4材料颗粒内部导电性并且加速锂离子的扩散,目前仍是优化材料性能的主流选择。表1总结了上述通过元素掺杂改善磷酸铁锂电化学性能的数据。总结表明,掺杂位点、掺杂元素的种类以及掺杂量对掺杂效果有很大的影响。综合考虑上述因素是LiFePO4掺杂改性过程中非常重要的一步。元素掺杂对提高磷酸铁锂的循环性能有一定的积极作用,尤其是在Fe 位和O 位发生的掺杂取代,往往可以在保持较高容量保持率的同时提高材料初始放电比容量。但是,Li位掺杂效果稍差一些,对元素种类和含量的要求也更高。这是由于掺杂离子不会完全进入LiFePO4的晶格中,未进入晶格的阳离子会阻断Li+在通道中的扩散,这就要求研究者们对掺杂机理进行深入研究和分析,选取适宜的元素进行掺杂改性。多种元素共同掺杂对LiFePO4的电化学性能具有协同作用,多种离子掺杂在LiFePO4相同位点或不同位点,可以大幅度提升LiFePO4倍率性能和循环性能。其中,以Mg 或V 为主要掺杂元素的多元素Fe 位掺杂效果最优。多元素掺杂改性的结果很可观,实验开展前通过第一性原理计算可减少多元素组合掺杂的盲目性。

表1 磷酸铁锂元素掺杂改性电化学性能概述Table 1 A sum up of electrochemical performance of LiFePO4 modified by elemental doping
2.2 材料包覆改性
要制备拥有优异电化学性能的LiFePO4,仅仅通过体相掺杂提高材料内部的导电性和锂离子扩散速率是不够的。LiFePO4的导电性极差,通过在材料表面包覆结构稳定以及性能良好的导电/导离子材料,可改善LiFePO4材料颗粒间的电子和离子传导。LiFePO4包覆改性可以控制颗粒尺寸,减小Li+迁移过程中的阻力,提高整体材料的电子电导率和离子传输速率,进一步提高材料的倍率和低温性能[37]。包覆剂类型主要有碳材料、金属或金属氧化物材料和离子导电材料等。
2.2.1 碳材料包覆
用导电物质包覆LiFePO4材料是提高其倍率和低温性能的重要措施,其中碳材料是最简单、最便宜的一种优良材料。碳包覆主要有以下作用:①碳可作为还原剂,防止LiFePO4材料中Fe2+的氧化;②碳包覆可改善LiFePO4材料间的电接触,提高材料的电导率;③碳包覆在一定程度上阻碍了颗粒间的直接接触,可有效抑制颗粒生长变大。
Liu等[38]研究表明,LiFePO4复合材料的形成与碳包覆过程中的颗粒尺寸、温度、气氛以及热力学机理有关。通过原位聚合,将有机碳源包覆在LiFePO4表面,经过高温碳化和退火工艺,得到的LiFePO4与碳的复合材料。该方法不仅可以获得完整均匀的碳层,并且包覆的碳层一致性好,厚度可控,与LiFePO4接触紧密,很好地抑制了LiFePO4颗粒的过度生长和团聚[39-40]。Wang等[41]也做了类似的工作,将聚苯并嗪同时作为LiFePO4包覆层的新型碳源和氮源,获得了氮掺杂碳包覆的LiFePO4纳米复合材料。原位生长在LiFePO4纳米颗粒上的氮掺杂碳层可以有效增强电导率并提供快速的Li+传输路径。当用作储锂正极材料时,此纳米复合材料表现出良好的倍率性能和稳定的循环性能,在2 C的电流密度下初始放电比容量为150 mA·h/g,循环150圈后,容量保持率为98.2%,10 C的电流密度下初始容量也可达到102 mA·h/g。Wang 等[42]研究了氟掺杂碳(FC)包覆对LiFePO4正极材料电化学性能的影响。通过各种表征技术对纳米复合材料的微观结构和电化学性能进行了系统研究,揭示了FC 包覆层紧紧附着在LiFePO4颗粒表面,形成了三维导电网络结构。这种良好的结构使得晶粒间电接触良好,缩短了晶粒界面间Li+扩散距离,同时促进了充放电过程中电子的快速转移。在10 C 的电流密度下,FC 包覆的LiFePO4的初始放电容量为120 mA·h/g,循环1000圈后容量保持率为95.4%。经过验证,LiFePO4@FC纳米复合材料作为储锂正极材料时,表现出非常理想的电化学性能,具有优越的倍率和循环性能。
近期,Li 等[43]采用溶剂热法,使得LiFePO4纳米颗粒在石墨烯层间生长(图7)。利用石墨烯的高导电性和多孔结构等优势,改性后的纳米LiFePO4有着优异的循环和倍率性能。0.2 C 倍率下放电比容量为160 mA·h/g,60 C 高倍率下放电比容量为107 mA·h/g,循环2000 圈以上的容量保持率为95%。Luo等[44]将LiFePO4和氧化石墨烯进行复合,然后进行还原,合成了一种石墨烯包覆的LiFePO4复合材料。石墨烯形成了LiFePO4纳米颗粒的连续导电涂层网络,促进了电子传导。复合材料获得了优异的倍率性能,在50 C 高倍率下初始容量保持率达到70%。

图7 LFP/石墨复合材料的合成和结构示意图:(a)LFP/C复合材料的合成是通过将石墨与FeCl3插层,然后在石墨层内形成LFP;(b)基于LFP/C和商业LFP正极的示意图,石墨提供的连续导电网络使LFP/石墨电极的性能更好;LFP/石墨复合材料的结构和形态:(c),(d)SEM和EDS图,(e),(f)SEM图像;(g),(h)TEM图像;(i)LFP颗粒的SAED;(j)从LFP/C复合材料中刻蚀掉LFP颗粒后的多孔石墨颗粒的SEM和(k)TEM图像[43]Fig.7 Schematic illustration of synthesis and structure of LFP/graphite composite.(a)synthesis of LFP/graphite composite by intercalating graphite with FeCl3 followed by formation of LFP within the graphite layers;(b)schematics of LFP/graphite based cathode and a commercial LFP cathode,continuous conductive network provided by graphite confers better performance on LFP/graphite electrode;structure and morphology of LFP/graphite composite:(c),(d)SEM and EDS mapping,(e),(f)SEM images,and(g),(h)TEM images of LFP/graphite composite;(i)inset in panel g is SAED of a LFP particle;(j)SEM and(k)TEM images of porous graphite particle after etching away LFP particles from LFP/graphite composite[43]
Wang 等[45]报道了一种由氮掺杂石墨烯包覆的LiFePO4纳米片复合正极材料。这种复合材料具有三维多孔结构,BET比表面积测试法测得其比表面积高达199.3 m2/g。在这种复合材料中,氮掺杂的石墨烯有着多孔结构和强导电性,为LiFePO4提供了快速电子转移通道。同时具有大比表面积的薄型LiFePO4纳米片主要暴露面为(010)面,拥有更多的活性位点,缩短了Li+的扩散距离。因此,实现了优异的高倍率性能以及长寿命循环稳定性。100 C倍率下放电比容量为78 mA·h/g,10 C 倍率下循环1000次的容量保持率为89%。
同时也有研究者将炭黑作为导电添加剂与LiFePO4材料混合,增强其导电性能。Xu等[46]已经开发了仅包含1%的多孔石墨烯(HG)和1%炭黑的二元导电添加剂。具有大量孔数量和大比表面积的HG 增强了LiFePO4的电子电导率,但不影响离子的高效传输。少量的炭黑作为HG形成导电网络的补充,可以与LiFePO4充分接触,从而在整个LiFePO4电极中实现优异的导电性。双碳包覆的LiFePO4材料在0.1 C 的电流密度下,初始放电比容量可达到160 mA·h/g,1 C电流密度下初始容量可达到140 mA·h/g,循环50圈无衰减。
碳包覆表面改性的策略在提高LiFePO4倍率和循环性能的同时,对LiFePO4材料的低温电化学性能也有一定的改善。Fan 等[47]首次采用油胺法制备了纳米结构LiFePO4@C 复合材料。油胺在控制LiFePO4@C 复合材料的粒径和形成多孔纳米结构方面起着多功能的作用。制备的材料拥有纳米结构和碳包覆层,由直径为30 nm的纳米球堆积而成的微米颗粒组成,微米颗粒尺寸为2 μm,碳包覆层厚度为2.4 nm。此LiFePO4@C 表现出优异的电化学性能。尤其是在-20 ℃低温下,1 C 倍率下能提供117 mA·h/g的容量。Wu等[48]用两种碳质材料(无定形碳和石墨化导电碳纳米管)修饰LiFePO4纳米粒子(LFP@C),以改善LiFePO4正极材料的电化学性能。双碳包覆的LiFePO4是由直径为100 nm颗粒堆积而成的微米颗粒组成,微米颗粒尺寸约为3 μm,碳包覆层厚度为2.8 nm。双碳包覆的LiFePO4表现出最佳的倍率性能、循环容量保持率和优异的低温性能。在高达120 C的倍率下循环100圈约有59%的容量保持率,在1 C 倍率下500 次循环中有98.5%的容量保持率。同时在-25 ℃下,0.1 C 倍率下初始容量为120 mA·h/g,循环100 圈,容量保持率达71.4%。这些优异的性能可能来源于无定形碳和石墨化导电碳纳米管的协同效应。无定形碳均匀涂覆在所有的LiFePO4纳米颗粒上,并在促进Li+扩散和稳定纳米颗粒的界面结构方面起主要作用,石墨化导电碳纳米管将所有的LFP@C颗粒连接起来并在整个电极中形成最佳的三维导电网络来降低内阻,进一步增强了LiFePO4的电化学性能。
在上述碳材料中,石墨烯碳纳米管由于拥有优异的电子导电性、柔韧性、稳定的力学、化学和热力学性能以及高比表面积等优点,被广泛应用于储能器件。LiFePO4材料与其复合可以提升电极的电化学性能。在电化学储能领域,对碳或石墨烯进行N、F 元素掺杂可以进一步提高碳材料导电性,最终使得复合材料电化学性能更优。
2.2.2 金属及金属氧化物
许多研究者还研究和制备了用金属或金属氧化物与碳复合改性的LiFePO4正极材料。金属材料涂层具有以下几个优点:①在LiFePO4中引入金属涂层,可以固定三维电子跃迁网络,保持材料结构完整性;②金属涂层材料可以防止LiFePO4的持续生长,控制颗粒的大小,缩短Li+的传输距离;③金属包覆材料的导电性能显著提高,振实密度也有所提高。
Chung 等[49]提出了一种简单的方法,在整个LiFePO4表面均匀地分散小部分高导电性银(质量分数约1.37%)来提高LiFePO4材料的电导率。在这种方法中,首先将硝酸银滴加到LiFePO4胶体溶液中,氧化银在LiFePO4表面原位沉淀,收集产物再通过水热和高温煅烧,制备出高致密化(>85%)的LiFePO4-Ag复合物。结果表明,包覆金属Ag后的LiFePO4正极表现出优越的电化学性能,具有较高的比容量和良好的循环稳定性,最重要的是高倍率下材料的容量得到显著提升。LiFePO4-Ag复合物在0.7 C 的电流密度下,初始比容量为155 mA·h/g,循环200 圈放电比容量无衰减,在14 C 的电流密度下,初始放电比容量可达到85 mA·h/g。
Zhu 等[50]通过改良的碳热还原法,通过简单球磨物理混合制备了LiFePO4/(C+Cu)复合材料。实验证明,在LiFePO4表面包覆C+Cu 涂层后,依然保持了LiFePO4的橄榄石型结构,材料粒径约为100~200 nm。LiFePO4/(C+Cu)复合材料在0.1 C的电流密度下表现出160.7 mA·h/g 的初始放电比容量,循环200圈后容量保持率为98%,在5 C的电流密度下初始放电比容量为105 mA·h/g,循环500圈后容量保持率可到达99%,表现出优异的循环寿命以及倍率性能。与单纯碳包覆材料相比,铜颗粒和碳材料的共同引入进一步增强了LiFePO4的电子传导性,进一步提高了其电化学性能。Lin等[51]通过简单的无电沉积(ED)工艺,获得了纳米尺寸Sn 包覆的LiFePO4/C 正极材料,复合材料的颗粒尺寸为500 nm,Sn 包覆层厚度为20 nm。与原始的LiFePO4/C相比,Sn包覆的LiFePO4/C在较宽的工作温度范围内表现出更高的容量、更好的循环稳定性。Sn 包覆的LiFePO4/C 复合材料在温度为60 ℃,电流密度为0.5 C的测试条件下,初始容量为154.3 mA·h/g,循环160 圈容量保持率为96%,未改性的LiFePO4/C初始容量为150.2 mA·h/g,循环130圈容量保持率仅为78%。在温度为-30 ℃,电流密度为0.5 C的测试条件下,Sn包覆的LiFePO4/C复合材料初始放电容量为72.5 mA·h/g,未改性的LiFePO4/C初始容量为50.4 mA·h/g。通过对电化学测试结果的分析,可以看出Sn包覆的LiFePO4/C导电颗粒间接触良好,特别是在低温下,改性后的材料拥有更低的电荷转移电阻和更高的锂离子扩散率。
金属包覆可以提高材料的导电性能,但在制备过程中容易被氧化且价格昂贵。很多研究者进一步开始研究金属氧化物的包覆作用。
Ziolkowska 等[52]采用溶胶-凝胶法成功合成了单一LiFePO4和SnO2包覆的LiFePO4材料。前体中SnO2的加入改变了材料的形貌,导致部分纳米球的形成,使平均晶粒尺寸从33 nm 增加到40 nm。SnO2包覆层降低了LiFePO4材料在充放电循环过程中的相变程度。Liu等[53]采用固相合成和溶胶-凝胶法相结合的方法制备了MoO2和碳材料共同包覆的LiFePO4正极材料。复合材料拥有较高的Li+扩散率,表观Li+扩散系数随着MoO2含量的增加而增加,并在MoO2质量分数为5%时达到最大值,为1.0×10-10cm2/s,比未改性的LiFePO4的Li+扩散系数提高了1个数量级。Liu等[54]通过原位合成法制备了WO2包覆改性的LiFePO4/C正极材料。WO2能均匀包覆在LiFePO4颗粒表面,且不改变LiFePO4的晶体结构,WO2改性后的LiFePO4/C样品表现出较好的初始放电比容量,1 C的电流密度下,初始放电比容量为130 mA·h/g,比未改性的LiFePO4正极材料提高了约20 mA·h/g。Zhang 等[55]采用溶胶-凝胶合成路线开发出具有高电导率的纳米TiN材料并将其用作电池材料的导电涂层。采用溶胶-凝胶法在LiFePO4颗粒上均匀涂覆TiN涂层。相对于未涂覆的LiFePO4而言,改性后的材料比容量更高,倍率性能更优。在0.1 C的电流密度下,TiN质量分数为10%的材料性能最佳,其放电比容量为159 mA·h/g,约为理论比容量的93%,比纯LiFePO4提高了38 mA·h/g,5 C 的电流密度下初始放电比容量可达到80 mA·h/g,比纯LiFePO4提高了40 mA·h/g。
综上所述,金属包覆层的引入可以提高材料的振实密度,提高LiFePO4的内部和颗粒间电子电导率。金属包覆层的加入也不影响正极材料的结构,使得材料容量和循环寿命得到极大改善。但金属包覆层存在氧化问题,且引入的金属一般都是贵重金属,不适合大规模生产。金属氧化物包覆策略也可以改善LiFePO4正极材料的电化学性能。其成本较低,但是金属氧化物包覆层电导率不如金属包覆层高,因此后续还需要进一步改进这些策略以及使用的包覆剂。
2.2.3 离子导电材料包覆
离子导电材料也可以用来修饰LiFePO4正极材料。碳包覆、金属及金属氧化物材料包覆主要是通过提高材料的电子电导率来改善材料的电化学性能。在充放电过程中,电荷平衡必须通过转移的电子和脱嵌的Li+之间相互补偿来保持[56]。如果Li+传输速率达不到所需要转移电子的传输速率,就会影响转移电子的传输,反之亦然。这两种情况都不利于材料电化学性能的提升[57]。离子导电材料具有较高的离子电导率和Li+储存能力,在电池充放电过程中可为电池提供额外的Li+。此外,离子导电材料的引入可以有效抑制Li/Fe反位缺陷,提高LiFePO4正极材料的电化学性能[58]。
LiFePO4正极材料中最常用的离子导电材料是具有开放三维框架的Li3V2(PO4)3[59-63],其具有较高的Li+扩散速率和工作电势。Zhang 等[61]采用溶胶-凝胶法制备了快离子导体Li3V2(PO4)3包覆的LiFePO4粉末。改良后的样品含有橄榄石LiFePO4相和单斜Li3V2(PO4)3相。一些V3+和Fe2+元素分别掺入LiFePO4和Li3V2(PO4)3的晶格中,导致晶格收缩形成晶格缺陷。与商品化的LiFePO4相比,改性后LiFePO4的锂离子扩散系数提高了一个数量级,可达到1.2×10-10cm2/s。电化学测试结果表明,改性后LiFePO4的倍率性能和循环稳定性显著提升。在5 C和10 C电流密度下,改性后的LiFePO4初始容量分别为143.78 mA·h/g和111.06 mA·h/g,在190圈循环后分别表现出134.85 mA·h/g 和104.99 mA·h/g 的放电比容量以及93.79%和94.53%的高容量保持率。Zhong 等[63]也采用溶胶-凝胶法制备了Li3V2(PO4)3包 覆 的LiFePO4。9LiFePO4-Li3V2(PO4)3/C 材 料 的电子电导率和Li+扩散系数经过实验测试得出依次为6.61×10-3S/cm 和1.88×10-10cm2/s,分别比未包覆的LiFePO4/C材料大3个和1个数量级(本实验中LiFePO4/C材料实验测试得到的电子电导率和Li+扩散系数分别为1.82×10-6S/cm和2.53×10-11cm2/s)。该复合材料在10 C 倍率下首次放电比容量为131.3 mA·h/g,循环200圈后容量保持率为95.1%。与LiFePO4/C相比,其倍率性能和循环稳定性均有显著提高。Liang 等[64]采用一锅固态反应合成了均匀的8LiFePO4-2Li3V2(PO4)3/C纳米薄片,所制备的8LiFePO4-2Li3V2(PO4)3/C纳米薄片的厚度大约为20~50 nm,并且堆叠在一起组成多孔结构材料。制备的8LiFePO4-2Li3V2(PO4)3/C 材料可以极大提高Li+扩散系数。在0.1 C电流密度下可提供161.5 mA·h/g的高容量,非常接近理论容量。即使在10 C 下,电极也可以提供118.6 mA·h/g的放电比容量。Li3PO4也是一种优良的离子导电材料[65-67]。Zhao 等[67]将LiFePO4前体直接分散在淀粉浆液中,将纳米Li3PO4涂覆在LiFePO4颗粒表面。LiFePO4颗粒表面的无定形碳可以提高电子导电性,而分散的Li3PO4颗粒涂层可以提高材料表面Li+扩散速率,进而提高大倍率下放电比容量,5 C的电流密度下的初始放电比容量可达到105 mA·h/g,比纯LiFePO4的放电比容量提高了30 mA·h/g。
具有钙钛矿结构的材料可以在晶格中提供大量的等效位点,Li+可以占据这些位点并自由移动,传输性能得到提升[57,68-69]。Shu等[69]通过氨辅助水热法首次合成了球形的LiFePO4/(C+La0.56Li0.33TiO3)复合材料。由导电子的碳和快速导Li+的La0.56Li0.33TiO3组成的包覆层有利于电子和锂离子的协同快速传输,此包覆层还可避免电解液分解产生的HF 对LiFePO4的侵蚀,从而提高电极材料电化学性能。LiFePO4/(C+La0.56Li0.33TiO3)的初始放电比容量为126.3 mA·h/g,在5 C倍率循环100圈,容量保持率高达98.3%。在30 C高倍率下,仍显示出62.3 mA·h/g的高放电比容量。Shu 等[68]制备了不同La0.56Li0.33TiO3含量(0~3%)包覆LiFePO4/C 球形复合材料。La0.56Li0.33TiO3包覆LiFePO4/C 的动力学性能优于LiFePO4/C。上述样品的初始放电比容量分别为126.3 mA·h/g,包覆改性后的材料在5 C倍率下循环100圈和10 C倍率下循环200圈,容量保持率分别高达98.3%。
综上所述,离子导体材料对LiFePO4进行包覆改性,其优良的导离子特性可以有效提高正极材料的电化学性能,同时改善了碳包覆带来的振实密度低、不具有离子传导性的缺陷,是一种磷酸铁锂材料包覆改性的十分有发展前景的方法。
材料包覆改性是LiFePO4常见的改性策略。近几年关于碳材料、金属及金属氧化物和离子导电材料包覆改性的相关研究数据如图8所示。石墨烯包覆改性的磷酸铁锂复合材料倍率性能提升最为显著,碳材料包覆在磷酸铁锂的表面形成电桥,提高材料的电子电导率,使得发生电化学反应时得失的电子能够及时传导;此外,导电物质包覆在颗粒表面,阻碍颗粒的进一步长大,抑制大倍率充放电下材料的粉化问题。金属和金属氧化物包覆在提高磷酸铁锂材料的导电性方面一般不如碳材料包覆效果好,成本相对高,在磷酸铁锂表面可起到修饰电极作用,从而减少正极材料跟电解液的副反应,减缓正极材料的循环恶化,同时还可以提高材料的振实密度。离子导电材料包覆改性,材料初始放电比容量有明显提升。这是因为其拥有较高离子电导率和Li+储存能力,在电池充放电过程中可为电池提供额外的Li+,但是这一改性策略制备工艺较为复杂,不适合商业化量产,材料最终电化学性能不如碳材料包覆效果好。

图8 不同材料包覆磷酸铁锂电化学性能概述Fig.8 Overview of electrochemical properties of LiFePO4 coated by different materials
2.3 添加补锂材料
LiFePO4电池在第1 次充电过程中,由于在负极表面形成固体电解质界面(SEI),正极材料中大约5%~20%的锂被消耗,导致首圈库仑效率低和不可逆容量损失过大。想要解决上述问题,可以在磷酸铁锂正极材料中添加补锂材料,电池在充电过程中补锂材料发生分解释放过量锂,补偿负极生成SEI 膜造成的不可逆锂损失[70]。补锂材料通常具有补锂能力强、易于合成、稳定性强和成本低廉等特点,常见的磷酸铁锂正极补锂材料有Li2O、LiF、Li3N和Li2S等。
Daiz-Lopez等[71]报道了一种Li2O∶Li2/3Mn1/3O5/6新型复合材料作为LiFePO4材料的补锂添加剂,此纳米复合材料首圈充电容量高达1157 mA·h/g。磷酸铁锂正极材料中仅添加2%的上述纳米复合物,首圈充电比容量为165 mA·h/g,增加了13%。Sun等[72]将过渡金属氧化物(MxOy,M=Fe、Co、Ni、Mn等)与Li的反应产物作为磷酸铁锂正极优良的补锂剂。通过转化反应机理:MxOy+2yLi++2ye-→xM+yLi2O,生成一系列M和Li2O的复合材料。进一步通过对材料的颗粒尺寸进行调控,发现使用N-Co/N-Li2O 纳米复合补锂材料的理论比容量远高于使用微米级M-Co/N-Li2O 和亚微米级SM-Co/N-Li2O 补锂复合材料。N-Co/N-Li2O 纳米复合补锂材料的理论比容量是磷酸铁锂正极材料的4倍以上,并且脱锂电位低于LiFePO4正极材料的电压上限,同时嵌锂电位低于LiFePO4正极材料的电压下限,这有利于实现高的预锂化效率。使用N-Co/N-Li2O 正极补锂添加剂后,磷酸铁锂/石墨全电池的初始充电比容量显著提高,可达到185 mA·h/g,远超过理论比容量(图9)。

图9 (a)N-Co/N-Li2O纳米复合材料的制备工艺示意图;(b)M-Co/N-Li2O、SM-Co/N-Li2O和N-Co/N-Li2O复合材料的初始充电电压平台分布图;(c)N-Co/N-Li2O复合材料首圈充电之后的放电电压平台变化;(d)不同含量N-Co/N-Li2O添加剂的LiFePO4半电池首圈充电容量;(e)有无N-Co/N-Li2O添加剂的LiFePO4全电池首圈充放电容量;(f)有无N-Co/N-Li2O添加剂的LiFePO4全电池的循环性能[72]Fig.9 (a)Schematic of fabrication process of N-Co/N-Li2O composites;(b)initial charge potential profiles of electrodes made with various Co/Li2O nanocomposites:M-Co/N-Li2O composite,SM-Co/N-Li2O composite and N-Co/N-Li2O composite;(c)charge/discharge potential profiles of N-Co/N-Li2O electrode after first charge process;(d)initial charge potential profiles of LiFePO4 electrodes with different amounts of N-Co/N-Li2O additive in half-cell configurations;initial charge/discharge potential profiles(e)and cycling performance(f)of LiFePO4/graphite full cells with and without N-Co/N-Li2O additive[72]
同年Sun 等[73]也提出LiF 和金属(例如,LiF/Co和LiF/Fe)组成的纳米复合材料也是有效的正极补锂材料。LiF/Co 纳米复合材料表现出1.5 V 开路电压,与现有正极材料具有良好的兼容性,并提供首圈高达516 mA·h/g 的充电比容量。当用作LiFePO4正极材料的补锂添加剂时,LiF/Co纳米复合材料提供了高锂补偿效率。添加4.8%LiF/Co添加剂的LiFePO4电极在0.1 C 倍率下可提供197 mA·h/g的初始充电比容量,对比未添加的LiFePO4电极,其首圈充电比容量增加了20.1%。Du 等[74]合成了Fe/LiF/Li2O纳米复合补锂材料,其特征在于尺寸为5 nm的Fe纳米颗粒均匀分散在Li2O和LiF基体中,实现紧密接触。Fe/LiF/Li2O纳米复合材料在首圈充电过程中,释放550 mA·h/g 的充电比容量,并且表现出比纯Li2O 材料更好的环境稳定性以及比纯LiF材料具有更低的脱锂电位和更快的反应动力学。Fe/LiF/Li2O纳米复合材料作为LiFePO4材料的补锂添加剂,表现出优异的锂补偿效果。
Li3N也可以作为磷酸铁锂正极补锂材料。Sun等[75]研究了Li3N作为正极补锂添加剂来抵消锂离子电池在首圈循环中的锂损失。虽然Li3N容量高达现有正极材料理论容量的10 倍以上,但是由于Li3N 的不稳定性以及与电极浆料混合所用溶剂之间的不相容性,导致Li3N 难以真正用作正极材料的补锂材料。Sun等利用锂金属与氮气的反应,通过退火处理制备了表面拥有钝化层的Li3N材料。由结晶相Li2O和Li2O2组成的致密表面钝化层将材料的活性成分与空气阻隔,使Li3N 颗粒在常温环境下具有良好的稳定性。
Zhan 等[76]使用Li2S 作为正极补锂材料来补偿首圈活性锂的损失,提高了锂离子电池整体的比能量。将Li2S、炭黑(KB)和聚乙烯吡咯烷酮(PVP)在无水乙醇中混合,制备出具有核壳结构的复合材料,该材料表现出1053 mA·h/g 的初始充电比容量。用核壳结构的Li2S/KB/PVP对磷酸铁锂正极材料进行包覆,表现出良好的电化学性能。在0.2 C倍率下,改性后LiFePO4(Li2S)/石墨全电池的初始放电比容量可达140 mA·h/g,比纯LiFePO4/石墨全电池的放电比容量高12 mA·h/g。
目前在电极材料中补充活性锂的途径主要分为正极补锂和负极补锂两大类。其中负极补锂流程复杂、工艺要求较高且安全性较差,这在很大程度上推动了正极补锂材料的发展。正极补锂材料一般可以直接在LiFePO4正极浆料的匀浆过程中添加,无需额外的工艺改进且成本较低,其关键点在于选择合适的正极补锂添加剂。本文综述的几种补锂添加剂均能提升LiFePO4初始充电比容量,但是并非所有的补锂添加剂都可以直接添加在浆料中来有效补偿负极SEI膜形成消耗的大量活性锂。例如常见补锂剂Li3N的不稳定性以及其与电极浆料混合所用溶剂之间的不兼容性导致其很难发挥补锂作用。应用于LiFePO4材料的补锂添加剂目前最常见的有Li2O、LiF,它们制备工艺简单,对LiFePO4材料的首圈库仑效率和放电比容量有显著提升。近年来,锂离子电池需求量越来越大,LiFePO4正极材料已经大规模商业生产,但是与之匹配的负极材料首圈库仑效率低必将导致电池在接下来的放电过程中,没有足够的锂离子回嵌至正极材料中,造成容量损失。在商业化生产中,正极补锂技术是LiFePO4改性非常有前景的发展方向,后续可以开发更多合适的正极补锂添加剂,以便解决在实际应用中正极材料首圈库仑效率和放电比容量低的问题。
3 总结和展望
经过近30年的探索,LiFePO4作为一种已经商业化应用的正极材料仍然有许多方面值得进一步深入研究。本文对LiFePO4材料的结构、性质和面临的挑战进行了深入分析,对材料的改性策略进行了总结,主要包括:体相掺杂、表面包覆和正极补锂策略。上述一系列改性策略对设计制备高比能量、高倍率和低温性能优异的LiFePO4正极材料具有重要意义。今后对LiFePO4的研究可以集中在以下几个方面开展。
(1)产业化生产改良。LiFePO4是目前较为成熟的工业化锂离子电池正极材料,已经实现产业化生产,现主要以固相烧结法为主,存在能耗大、生产出的材料倍率性能差等缺点,商业化生产方式和生产配方还有很大的提升空间。
(2)多种改性策略相结合,进一步提升LiFePO4的倍率性能,实现材料的超快充特性和优异的低温长循环性能。很多情况下,单一改性方式并不能很好地实现LiFePO4整体性能的提升。许多研究是将几种改性策略的优势相结合,制备出电化学性能更为优异的正极材料。
(3)进一步深入机理性研究。目前产业化生产LiFePO4材料时,对机理方面研究过少。通过先进的表征技术与理论计算模拟相结合,研究LiFePO4材料在充放电过程中的热力学与动力学转变过程,深入了解Li+在相界面及体相的传输机制,对LiFePO4商业化生产以及应用具有重要的指导意义。
(4)开发固态电极。将LiFePO4正极材料与固态电解质相结合,生产更为安全、可应用于柔性可穿戴电子设备的新型储能电池。
综上所述,锂离子电池正极材料LiFePO4在商业领域有着很广阔的应用和发展前景,相信经过科研者们的共同努力,LiFePO4正极材料的进一步性能提升能够最大化地满足人们生产生活的需求。

